Дигликозилированные 1, 2-диолы как псевдосоединения сиалил- lewis x и сиалил-lewis a.
Формула / Реферат
1. Соединение формулы I
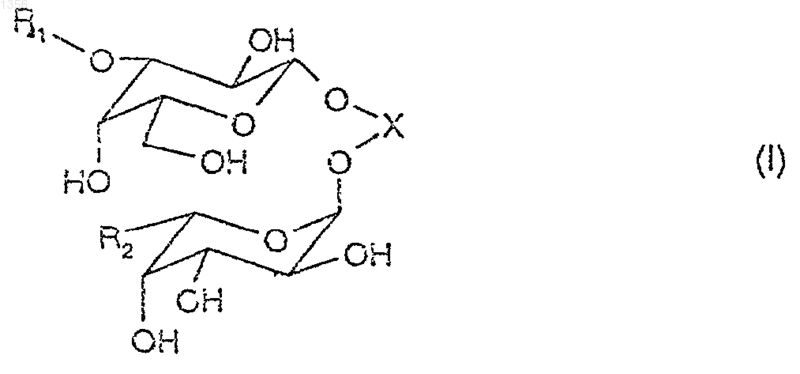
в которой
Х представляет остаток негликозидного алифатического 1,2-диола;
R1 представляет группу формулы III

R2 представляет водород, С1-С12алкил или С6арил;
R3 представляет водород или Мy;
R4 представляет С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С3-С12циклоалкенил, С2-С11гетероциклоалкил, С2-С11гетероциклоалкенил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил, С6-С10гетероаралкил, C8-С11аралкенил или С7-С10гетероаралкенил, которые незамещены или замещены одним или более заместителями, выбранными из группы, включающей ОH, галоген, C(O)ORs1, OC(O)Rs4, C(O)Rs2, нитро, NH2, циано, SO3My, ОSО3Му, NR20SO3My, С1-С12алкил, С2-С12алкенил, С1-С12алкокси, С3-С12циклоалкил, С3-С12циклоалкенил, С2-С11гетероциклоалкил, С2-С11гетероциклоалкенил, С6-С10арил, С6-С10арилокси, С5-С9гетероарил, С5-С9гетероарилокси, С7-С11аралкил, С7-С11аралкилокси, С6-С10гетероаралкил, С8-С11аралкенил, С7-С10гетероаралкенил, первичный амино, вторичный амино, сульфонил, сульфонамид, карбамид, карбамат, сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид;
Rs1 представляет водород, Мy, С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С2-С11гетероциклоалкил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил или С6-С10гетероаралкил;
Rs4 представляет водород, С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С2-С11гетероциклоалкил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил или С6-С10гетероаралкил;
Rs2 и R20 представляют водород, С1-С12алкил, С2-С12алкенил, C3-С12циклоалкил, С3-С12циклоалкенил, С2-С11гетероциклоалкил, С2-С11гетероциклоалкенил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил, C6-С10гетероаралкил, С8-С11аралкенил или С7-С10гетероаралкенил;
y равен 1 и М обозначает моновалентный металл или
у равен 1/2 и М обозначает двухвалентный металл;
причем алкил, алкенил, алкокси, циклоалкил, циклоалкенил, гетероциклоалкил, гетероциклоалкенил, арил, арилокси, гетероарил, гетероарилокси, аралкил, аралкокси, гетероаралкил, аралкенил или гетероаралкенил, в свою очередь, являются незамещенными или замещенными одним или более заместителями, выбранными из группы, состоящей из ОН, галоген, C(О)ORs1, OC(O)Rs4, C(O)Rs2, нитро, NH2, циано, SО3Му, ОSО3Му, NR20SО3Му, С1-С12алкил, С2-С12алкенил, С1-С12алкокси, С3-С12циклоалкил, С3-С12циклоалкенил, С2-С11гетероциклоалкил, С2-С11гетероциклоалкенил, С6-С10арил, C6-С10арилокси, С5-С9гетероарил, С5-С9гетероарилокси, С7-С11аралкил, С7-С11аралкилокси, С6-С10гетероаралкил, С8-С11аралкенил, С7-С10гетероаралкенил, первичный амино, вторичный амино, сульфонил, сульфонамид, карбамид, карбамат, сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид, включая их физиологически приемлемые соли указанного соединения.
2. Соединение по п.1, где Х представляет линейный или разветвленный С2-С20-алкилен, -алкенилен, С3-С12-циклоалкилен, -циклоалкенилен, С3-С11-гетероциклоалкилен или -гетероциклоалкенилен с гетероатомами, выбранными из группы, включающей -О-, -S- и -N-.
3. Соединение по п.1, где Х представляет остаток 1,2-диола, имеющего формулу
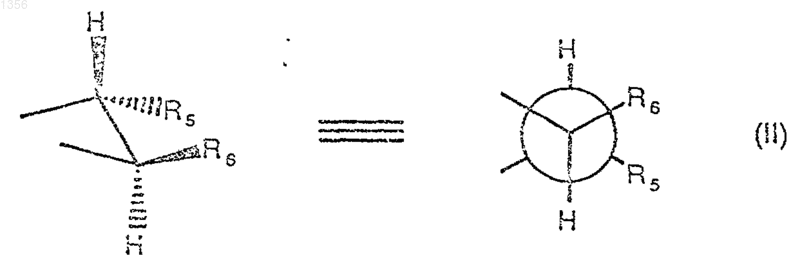
в которой
R5 и R6 независимо друг от друга представляют водород, С1-С12алкил, С3-С12циклоалкил, С2-С11гетероциклоалкил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил или С6-С10гетероаралкил; либо R5 и R6, взятые вместе с группой -СН-СН-, представляют С3-С12циклоалкилен, С3-С12циклоалкенилен, С2-С11гетероциклоалкилен и С3-С11гетероциклоалкенилен с гетероатомами, выбранными из группы, включающей -О-, -S- и -N-; где алкил, циклоалкил, гетероциклоалкил, арил, гетероарил, аралкил, гетероаралкил, циклоалкилен, циклоалкенилен, гетероциклоалкилен и гетероциклоалкенилен являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген, C(О)ORs1, OC(O)Rs4, C(O)Rs2, нитро, NH2, циано, SO3My, OSO3Му, NR20SO3My, С1-С12алкил, С2-С12алкенил, С1-С12алкокси, С3-С12циклоалкил, С3-С12циклоалкенил, С2-С11гетероциклоалкил, С2-С11гетероциклоалкенил, С6-С10арил, С6-С10арилокси, С5-С9гетероарил, С5-С9гетероарилокси, С7-С11аралкил, С7-С11арaлкилокси, С6-С10гетероаралкил, С8-С11аралкенил, С7-С10гетероаралкенил, первичный амино, вторичный амино, сульфонил, сульфонамид, карбамид, карбамат, сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид, где Rs1 представляет водород, Мy, С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С2-С11гетероциклоалкил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил или С6-С10гетероаралкил; Rs4 представляет водород, С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С2-С11гетероциклоалкил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил или С6-С10гетероаралкил; Rs2 и R20 представляют водорюф, С1-С12aлкил, С2-С12алкенил, С3-С12циклоалкил, С3-С12циклоалкенил, С2-С11гетероциклоалкил, С2-С11гетероциклоалкенил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил, С6-С10гетероаралкил, С8-С11аралкенил или С7-С10гетероаралкенил; причем алкил, алкенил, алкокси, циклоалкил, циклоалкенил, гетероциклоалкил, гетероциклоалкенил, арил, арилокси, гетероарил, гетероарилокси, аралкил, аралкокси, гетероаралкил, аралкенил или гетероаралкенил, в свою очередь, являются незамещенными или замещенными одним из вышеуказанных заместителей; у=1; а М обозначает одновалентный металл; либо у=1/2, а М обозначает двухвалентный металл.
4. Соединение по п.3, где R5 и R6
(а) являются незамещенными или замещенными С1-С12алкилом или С1-С12алкокси;
(б) вместе с группой -СН-СH- представляют 5-8-членный карбоцикл;
(в) вместе с группой -СН-СН представляют 5-8-членный гетерокарбоцикл;
(г) независимо друг от друга представляют водород, незамещенный С1-С12алкил или С1-С12алкил, который замещен заместителем, выбранным из группы, включающей -C(О)ORs1, -OC(O)Rs4, -C(O)ONa или С(O)ОК, первичный амино, вторичный амино, С3-С12циклоалкил, С1-С6алкокси, фенилокси и бензилокси; незамещенный С3-С12циклоалкил или С3-С12циклоалкил, который замещен заместителем, выбранным из группы, включающей -С(О)ОRs1, -OC(O)Rs4, -C(O)ONa или С(O)ОК, первичный амино, вторичный амино, С1-С6алкил, С1-С6алкокси, фенилокси и бензилокси; С6-С10арил, который незамещен или замещен -C(О)ORs1, -OC(O)Rs4, -C(O)ONa или С(O)ОК, первичным амино, вторичным амино, С1-С6алкилом или C1-С6алкокси; С3-С9гетероарил с 1 или 2 гетероатомами, выбранными из группы, включающей aтoмы кислорода и азота; или С7-С12аралкил, который незамещен или замещен -C(О)ORs1, -OC(O)Rs4, -C(O)ONa или С(O)ОК, первичным амино, вторичным амино, С1-С6алкилом или С1-С6алкокси;
(д) вместе с группой -СН-СН- представляют 5-12 карбоцикл или 5- или 6-членный гетерокарбоцикл с гетероатомом, выбранным из группы, включающей атомы кислорода и азота; или
(е) вместе с группой -СН-СН- представляют С3-С12циклоалкилен, С4-С12циклоалкенилен, С2-С11гетероциклоалкилен или С3-С11гетероциклоалкенилен с гетероатомами, выбранными из группы, включающей -О-, -S- и -N-; где циклоалкилен, циклоалкенилен, гетероциклоалкилен и гетероциклоалкенилен являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген, C(O)ORs1, ОС(O)Rs4, C(O)Rs2, нитро, NH2, циано, SО3My, OSO3My, NR20SO3My, С1-С12алкил, С2-С12алкенил, С1-С12алкокси, С3-С12циклоалкил, С3-С12циклоалкенил, С2-С11гетероциклоалкил, С2-С11гетероциклоалкенил, С6-С10арил, С6-С10арилокси, С5-С9гетероарил, С5-С9гетероарилокси, С7-С11аралкил, С7-С11аралкилокси, С6-С10гетероаралкил, С8-С11аралкенил, С7-С10гeтepoaралкенил, первичный амино, вторичный амино, сульфонил, сульфонамид, карбамид, карбамат, сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид, где Rs1 представляет водород, Мy, С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С2-С11гетероциклоалкил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил или С6-С10гетероаралкил; Rs4 представляет водород, С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С2-С11гетероциклоалкил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил или С6-С10гетероаралкил; a Rs2 и R20 представляют водород, С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С3-С12циклоалкенил, С2-С11гетероциклоалкил, С2-С11гетероциклоалкенил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил, C6-С10гетероаралкил, С8-С11аралкенил или С7-С10гетероаралкенил; причем алкил, алкенил, алкокси, циклоалкил, циклоалкенил, гетероциклоалкил, гетероциклоалкенил, арил, арилокси, гетероарил, гетероарилокси, аралкил, аралкокси, гетероаралкил, аралкенил или гетероаралкенил, в свою очередь, являются незамещенными или замещенными одним из вышеуказанных заместителей; у=1, а М обозначает одновалентный металл; либо y=1/2, a M обозначает двухвалентный металл.
5. Соединения по п.4, где R5 и R6, взятые вместе с группой -СН-СН-, представляют С3-С12циклоалкилен или С2-С11гетероциклоалкилен, где гетероатомом является атом азота,
где R5 и R6, взятые вместе с группой -СН-СН-, представляют С3-С12циклоалкилен или С2-С11гетероциклоалкилен, где гетероатомом является атом азота, причем указанные циклоалкилен и гетероциклоалкилен являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, C(О)ORs1, ОС(O)Rs4, C(O)Rs2, NR8R9, C1-С12алкил, R8C(O)(NH)pN(R9)-, -C(O)(NH)pNR8R9, R8S(O)2(NH)pN(R9)-, R8R40NC(O)(NH)pN(R9)-, R8OC(O)(NH)pN(R9)-, -OC(O)(NH)pNR8R9 и R10-SO2-, где R8, R9, R10 и R40 независимо друг от друга представляют водород, ОН, С1-С12алкил, С1-С12алкенил, С3-С12циклоалкил, С3-С12циклоалкенил, С2-С11гетероциклоалкил, С2-С11гетероциклоалкенил, С6-С10арил, С5-С9гетероарил, С7-С16аралкил, С8-С16аралкенил с С2-С6алкениленом и С6-С10арилом, С6-С15гетероаралкил, С6-С15гетероаралкенил, или ди-С6-С10арил-С1-С6-алкил, которые являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы , включающей ОН, галоген, C(О)ORs1, OC(O)Rs4, C(O)Rs2, нитро, NH2, циано, SO3Му, ОSО3Мy, NR20SO3My, С1-С12алкил, С2-С12алкеншы, С1-С12алкокси, С3-С12циклоалкил, С3-С12циклоалкенил, С2-С11гетероциклоалкил, С2-С11гетероциклоалкенил, С6-С10арил, С6-С10арилокси, С5-С9гетероарил, С5-С9гетероарилокси, С7-С11аралкил, С7-С11аралкилокси, С6-С10гетероаралкил, С8-С11аралкенил, С7-С10гетероаралкенил, первичный амино, вторичный амино, сульфонил, сульфонамид, карбамид, карбамат, сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид, где Rs1 представляет водород, My, С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С2-С11гетероциклоалкил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил или С6-С10гетероаралкил;
Rs4 представляет водород, С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С2-С11гетероциклоалкил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил или С6-С10гетероаралкил; Rs2 и R20 представляют водород, С1-С12алкил, С2-C12алкенил, С3-С12циклоалкил, С3-С12циклоалкенил, С2-С11гетероциклоалкил, С2-С11гетероциклоалкенил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил, С6-С10гетероаралкил, С8-С11аралкенил или С7-С10гетероаралкенил; а заместители алкил, алкенил, алкокси, циклоалкил, циклоалкенил, гетероциклоалкил, гетероциклоалкенил, арил, арилокси, гетероарил, гетероарилокси, аралкил, аралкокси, гетероаралкил, аралкенил и гетероаралкенил, в свою очередь, являются незамещенными или замещенными одним из вышеуказанных заместителей; у=1, а М обозначает одновалентный металл; либо у=1/2, а М обозначает двухвалентный металл.
6. Соединение по п.5, где R8 и R9 независимо друг от друга представляют водород, С1-С12алкил, С3-С12циклоалкил, С6-С10арил, С7-С16аралкил с 1-6 атомами в алкиленовой группе, и С6-С10арил, С8-С16аралкенил с C2-С6алкениленом и С6-С10арилом, или ди-С6-С10арил-С1-С6алкил, где R8 и R9 являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген, СООН, С(О)ОМy, С1-С12алкил, С1-С6алкокси, С6-С10арил, С6-С10арилокси, SO3My, OSO3My, NR20SO3My, NO2, амино, первичный амино, вторичный амино и CN, a R20 представляет водород, С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С3-С12циклоалкенил, С2-С11гетероциклоалкил, С2-С11гетероциклоалкенил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил, С6-С10гетероаралкил, C8-С11аралкенил или С7-С10гетероалкенил; у=1, а М обозначает одновалентный металл, либо у=1/2, а М обозначает двухвалентный металл.
7. Соединение по п.5, где R10 представляет С1-С12алкил, С3-С12циклоалкил, С6-С10арил, С7-С16аралкил с 1-6 атомами в алкиленовой группе и С6-С10арил, которые являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген, карбоксил, С(О)ОМy, С1-С12алкил, С1-С6алкокси, С6-С10арил, SО3Мy, нитро, амино, первичный амино, вторичный амино и циано; или C8-С16аралкенил с С2-С6алкениленом и С6-С10арилом, или ди-С6-С10арил-С1-С6алкил.
8. Соединение по п.5, где R5 и R6, взятые вместе с группой -СН-СН-, представляют С3-С12циклоалкилен или С2-С11гетероциклоалкилен, имеющий в качестве гетероатома азот; и где циклоалкилен и гетероциклоалкилен являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, C(O)ORs1, OC(O)Rs4, C(O)Rs2, NH2, С1-С12алкил, R8C(O)N(R9)-, -C(O)NR8R9, R8S(O)2N(R9)-, RgOC(O)N(R9)- и R10-SO2-, где R9 представляет водород, a R8 представляет С1-С12алкил, С6-С10арил или С7-С11аралкил, которые являются незамещенными или замещенными одним или несколькими С1-С12алкокси; R10 представляет C1-С12алкил, С6-С10арил или С7-С11аралкил, которые являются незамещенными или замещенными одним или несколькими С1-С12алкилами; Rs1 и Rs4 представляют С1-С12алкил, a Rs2 представляет С1-С12циклоалкенил, C3-С12циклоалкил или С6-С10арил, а заместители алкил, циклоалкенил, циклоалкил и арил, в свою очередь, могут быть незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, C(O)ORs1' и OC(O)Rs4', где Rs1' представляет Мy или C1-С12алкил, a Rs4' представляет С1-С12алкил; у=1, а М обозначает одновалентный металл, либо у=1/2, а М обозначает двухвалентный металл.
9. Соединение по п.5, где R5 и R6, взятые вместе с группой -СН-СН-, представляют циклогексилен.
10. Соединение по п.5, где R5 и R6, взятые вместе с группой -СН-СН-, представляют пиперидилен.
11. Соединение по п.10, где R5 и R6, взятые вместе с группой -СН-СН-, представляют пиперидилен; где гетероатом является незамещенным или замещенным заместителем, выбранным из группы, включающей C(O)ORs1, C(O)Rs2, C(O)NR8R9, NH2, SO3My, С1-С12алкил, С2-С12алкенил, С1-С12алкокси, С3-С12циклоалкил, С3-С12циклоалкенил, С2-С12гетероциклоалкил, С2-С11гетероциклоалкенил, С6-С10арил, С6-С10арилокси, С5-С9гетероарил, С5-С9гетероарилокси, С7-С11аралкил, С7-С11аралкилокси, C6-С10гетероаралкил, С8-С11аралкенил, С7-С10гетероаралкенил, первичный амино, вторичный амино, сульфонил, сульфонамид, сульфонгидразид; и где один или несколько атомов С на кольце являются незамещенными или замещенными одним или несколькшьш заместителями, выбранными из группы, включающей ОН, OC(O)Rs4, NH2, OSO3My, NR20SO3My, С1-С12алкокси, С6-С10арилокси, С5-С9гетероарилокси, С7-С11аралкилокси, первичный амино, вторичный амино, сульфонамид, карбамид, карбамат, сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид, где Rs1 представляет водород, Мy, С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С2-С11гетероциклоалкил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил или С6-С10гетероаралкил; Rs4 представляет водород, С1-С12алкил, С2-С12алкенил, C3-С12циклоалкил, С2-С11гетероциклоалкил, С6-С10арил, С5-С9гетероарил, C7-С11аралкил или С6-С10гетероаралкил; R8 и R9 независимо друг от друга представляют водород, ОН, С1-С12алкил, С3-С12циклоалкил, С2-С11гетероциклоалкил, С6-С10арил, С5-С9гетероарил, С7-С16аралкил, С6-С15гетероаралкил, С8-С16аралкенил с С2-С6алкениленом и С6-С10арилом, или ди-С6-С10арил-С1-С6алкил, либо R8 и R9, взятые вместе, представляют тетраметилен, пентаметилен, -(СН2)2-О-(СH2)2-, -(СН2)2-S-(СН2)2- или -(СН2)2-NR7-(СН2)2-, и R7 представляет Н, С1-С6алкил, С7-С11аралкил, C(О)Rs2, или сульфонил; Rs2 и R20 представляют водород, С1-С12алкил, С2-С12aлкенил, С3-С12циклоалкил, С3-С12циклоалкенил, С2-С11гетероциклоалкил, С2-С11гетероциклоалкенил, С6-С10арил, С5-С9гетероарил, C7-С11аралкил, С6-С10гетероаралкил, С8-С11аралкенил или С7-С10гетероаралкенил; причем алкил, алкенил, алкокси, циклоалкил, циклоалкенил, гетероциклоалкил, гетероциклоалкенил, арил, арилокси, гетероарил, гетероарилокси, аралкил, аралкокси, гетероаралкил, аралкенил и гетероаралкенил, в свою очередь, являются незамещенными или замещенными одним из вышеуказанных заместителей; y=1, a M обозначает одновалентный металл; либо у=1/2, а М обозначает двухвалентный металл.
12. Соединения по п.11, где R5 и R6, взятые вместе с группой -СН-СН-, представляют пиперидилен; где гетероатом является незамещенным или замещенным заместителем, выбранным из группы, включающей C(О)ORs1, C(O)Rs2, C(O)NR8R9 и R10-SO2-, а один или несколько атомов С на кольце являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, NH2, R8S(O)2N(R9)-, R8C(O)N(R9)- и R8OC(O)N(R9)-, где R9 представляет водород, a R8 представляет С1-С12алкил, С6-С10арил или С7-С11аралкил, где алкил, арил и аралкил являются незамещенными или замещенными одним или несколькими С1-С12aлкокси; R10 представляет С1-С12алкил, С1-С10арил или С7-С11аралкил, которые являются незамещенными или замещенными одним или несколькими С1-С6алкилами; Rs1 представляет С1-С12алкил, a Rs2 представляет C1-С12алкил, С3-С12циклоалкенил, С3-С12циклоалкил или С6-С10арил; а заместители алкил, циклоалкенил, циклоалкил и арил, в свою очередь, являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, C(О)Rs1' и OC(O)Rs4', где Rs1' представляет Мy или С1-С12алкил, a Rs4' представляет С1-С12алкил; у=1, а М обозначает одновалентный металл, либо у=1/2, а М обозначает двухвалентный металл.
13. Соединения по п.1, где Х представляет циклогексилен или пиперидилен, которые являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, состоящей из ОН, NH2, С3Н7, -C(O)C6H5, -С(O)(СH2)8С(O)ОСH3, -C(O)[CH(OH)]2C(O)ONa, С(O)-С6H8(ОН)3, -С(O)-С6Н11, -С(O)ОС3Н7, -C(O)NHC6H5, -NHS(O)2CH2C6H5, -NHC(O)OCH2C6H5, -NНС(O)С6Н3(ОСН3)2, -S(O)2-C4H9, -NHC(O)NH C6H5, -S(O)2-С6Н4СH3, -S(O)2CH2C6H5 и -S(O)2-(СН2)С10Н7.
14. Соединение по п.1, где R2 представляет С1-С6алкил.
15. Соединения по п.1, где R1 соответствует группе формулы III

в которой
R3 представляет водород или Мy; и R4 представляет С1-С12алкил, С2-С12алкенил, С3-С12циклоалкенил, С2-С11гетероциклоалкил, С2-С11гетероциклоалкенил, С6-С10арил, С6-С9гетероарил, С7-С11аралкил, С6-С10гетероаралкил, С8-С11аралкенил или С7-С10гетероаралкенил, которые являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген, C(О)ORs1, OC(O)Rs4, C(O)Rs2, нитро, NН2, циано, SO3My, ОSО3Мy, NR20SO3My, С1-С12алкил, С2-С12алкенил, С1-С12алкокси, С3-С12циклоалкил, С3-С12циклоалкенил, С2-С11гетероциклоалкил, С2-С11гетероциклоалкенил, С6-С10арил, С6-С10арилокси, С5-С9гетероарил, С5-С9гетероарилокси, С7-С11аралкил, С7-С11аралкилокси, С6-С10гетероаралкил, С8-С11аралкенил, С7-С10гетероаралкенил, первичный амино, вторичный амино, сульфонил, сульфонамид, карбамид, карбамат, сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид, где Rs1 представляет водород, My, С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С2-С11гетероциклоалкил, С6-С10арил, С5-С9гетероаршы, С7-С11аралкил или С6-С10гетероаралкил; Rs4 представляет водород, С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С2-С11гетероциклоалкил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил или С6-С10гетероаралкил; Rs2 и R20 представляют водород, С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С3-С12циклоалкенил, С2-С11гетероциклоалкил, С2-С11гетероциклоалкенил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил, С6-С10гетероаралкил, С8-С11аралкенил или С7-С10гетероаралкенил; причем алкил, алкенил, алкокси, циклоалкил, циклоалкенил, гетероциклоалкил, гетероциклоалкенил, арил, арилокси, гетероарил, гетероарилокси, аралкил, аралкокси, гетероаралкил, аралкенил или гетероаралкенил, в свою очередь, являются незамещенными или замещенными одним из вышеуказанных заместителей; у=1; а М обозначает одновалентный металл; либо y=1/2, a M обозначает двухвалентный металл.
16. Соединение по п.1, которое соответствует формуле Iа
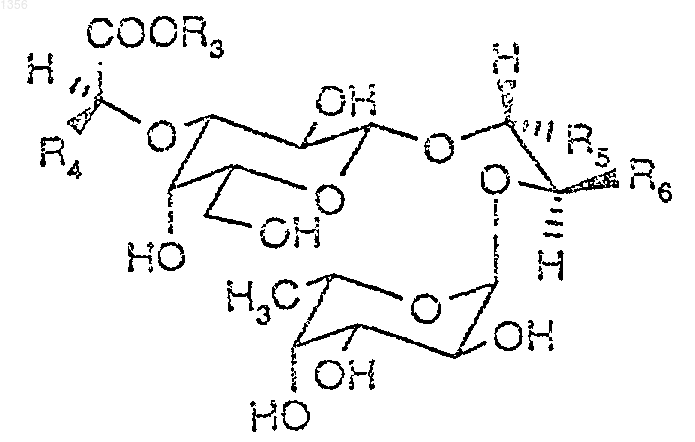
в которой
R3 представляет водород или Мy;
R4 представляет С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С3-С12циклоалкенил, С2-С11гетероциклоалкил, С2-С11гетероциклоалкенил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил, С6-С10гетероаралкил, C8-С11аралкенил или С7-С10гетероаралкенил, которые являются незамещенными или замещенными один или несколько раз;
R5 и R6 независимо друг от друга представляют водород, С1-С12алкил, С3-С12циклоалкил, С2-С11гетероциклоалкил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил или С6-С10гетероаралкил; либо R5 и R6, взятые вместе с группой -СН-СН, представляют С3-С12циклоалкилен, С4-С12циклоалкенилен, С2-С11гетероциклоалкилен и С3-С11гетероциклоалкенилен с гетероатомами, выбранными из группы, включающей -О-, -S- и -N-; где алкил, циклоалкил, гетероциклоалкил, арил, гетероарил, аралкил, гетероаралкил, циклоалкилен, циклоалкенилен, гетероциклоалкилен и гетероциклоалкенилен являются незамещенными или замещенными один или несколько раз, где заместитель выбирают из группы, включающей ОН, галоген, C(О)ORs1, OC(O)Rs4, C(O)Rs2, нитро, NH2, циано, SO3My, OSO3My, NR20SO3My, С1-С12алкил, С2-С12алкенил, С1-С12алкокси, С3-С12циклоалкил, С3-С12циклоалкенил, С2-С11гетероциклоалкил, С2-С11гетероциклоалкенил, С6-С10арил, С6-С10арилокси, С5-С9гетероарил, С5-С9гетероарилокси, С7-С11аралкил, С7-С11аралкилокси, С6-С10гетероаралкил, С8-С11аралкенил, С7-С10гетероаралкенил, первичный амино, вторичный амино, сульфонил, сульфонамид, карбамид, карбамат, сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид, где Rs1 представляет водород, Мy, С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С2-С11гетероциклоалкил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил или С6-С10гетероаралкил; Rs4 представляет водород, С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С2-С11гетероциклоалкил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил или С6-С10гетероаралкил; Rs2 и R20 представляют водород, С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С3-С12циклоалкенил, С2-С11гетероциклоалкил, С2-С11гетероциклоалкенил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил, С6-С10гетероаралкил, С8-С11аралкенил или С7-С10гетероаралкенил; причем алкил, алкенил, алкокси, циклоалкил, циклоалкенил, гетероциклоалкил, гетероциклоалкенил, арил, арилокси, гетероарил, гетероарилокси, аралкил, аралкокси, гетероаралкил, аралкенил и гетероаралкенил, в свою очередь, являются незамещенными или замещенными одним из вышеуказанных заместителей; у=1; а М обозначает одновалентный металл; либо у=1/2, а М обозначает двухвалентный металл.
17. Соединение по п.16, где R3 представляет Н, К или Na; R5 и R6, взятые вместе с группой -СН-СН-, представляют С3-С12циклоалкилен, С4-С12циклоалкенилен, С2-С11гетероциклоалкилен и С3-С11гетероциклоалкилен с гетероатомами, выбранными из группы, включающей -О-, -S- и -N-, которые являются незамещенными или замещенными один или несколько раз; где заместитель выбирают из группы, включающей ОН, галоген, C(О)ORs1, OC(O)Rs4, C(O)Rs2, нитро, NH2, циано, SO3My, ОSO3Му, NR20SO3Му, C1-С12алкил, С2-С12алкенил, С1-С12алкoкси, С3-С12циклоалкил, С3-С12циклоалкенил, С2-С11гетероциклоалкил, С2-С11гетероциклоалкенил, С6-С10арил, С6-С10арилокси, С5-С9гетероарил, С5-С9гетероарилокси, С7-С11аралкил, С7-С11аралкилокси, С6-С10гетероаралкил, С8-С11аралкенил, С7-С10гетероаралкенил, первичный амино, вторичный амино, сульфонил, сульфонамид, карбамид, карбамат, сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид, где Rs1 представляет водород, Мy, С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С2-С11гетероциклоалкил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил или С6-С10гетероаралкил; R20 и Rs4 представляет водород, С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С2-С11гетероциклоалкил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил или С6-С10гетероаралкил; Rs2 и R20 представляют водород, С1-С12алкил, С2-С12алкеншы, С3-С12циклоалкил, С3-С12циклоалкенил, С2-С11гетероциклоалкил, C2-C11гетероциклоалкенил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил, С6-С10гетероаралкил, С8-С11аралкенил или С7-С10етероаралкенил; причем алкил, алкенил, алкокси, циклоалкил, циклоалкенил, гетероциклоалкил, гетероциклоалкенил, арил, арилокси, гетероарил, гетероарилокси, аралкил, аралкокси, гетероаралкил, аралкенил и гетероаралкенил, в свою очередь, являются незамещенными или замещенными одним из вышеуказанных заместителей; и y=1; а М обозначает одновалентный металл; либо у=1/2, а М обозначает двухвалентный металл;
(a) R4 представляет остаток R12-(СН2)n или циклогексил, где n=1 или 2, a R12 представляет С1-С10алкил, С5-С8циклоалкил, С6-С10арил, или С8-С12аралкенил, которые незамещены или замещены С1-С4алкилом, С1-С4алкоксилом, F, Cl, -CN или -NO2; или R12 представляет аминогруппу NR8'R9', a R8' и R9' представляют С1-С12алкил, либо незамещенный или C1-С4-замещенный С5- или С6циклоалкил, С6-С10арил, С7-С12аралкил или C8-С12аралкенил; либо R12 представляет амидную группу -N(R9)C(О)R8-, -N(R9)S(О)R8-, -NR9C(О)NHR8- или -NR9C(О)NНR8-, где R8 представляет С6-С10арил, который незамещен или замещен С1-С4алкилом, С1-С4алкокси, F, Cl, -CN или -NO2, либо С1-С10aлкил, который незамещен или замещен F или Cl, a R9 представляет Н, С1-С10алкил, С5- или С6циклоалкил, C5- или С6циклоалкил-С1-С6алкил, фенил-С1-С6алкил или фенил-С2-С6алкенил; или
(b) R4 представляет С1-С12алкил, С3-С12циклоалкил или С7-С11аралкил, которые являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген, C(О)ORs1, OC(O)Rs4, C(O)Rs2, нитро, NH2, циано, SО3Му, OSO3Му, NR20SO3Му, С1-С12алкил, С2-С12алкенил, С1-С12алкокси, С3-С12циклоалкил, C3-С12циклоалкенил, С2-С11гетероциклоалкил, С2-С11гетероциклоалкенил, С6-С10арил, С6-С10арилокси, С5-С9гетероарил, С5-С12гетероарилокси, С7-С11аралкил, С7-С11аралкилокси, С6-С10гетероаралкил, С8-С11аралкенил, С7-С10гетероаралкенил, первичный амино, вторичный амино, сульфонил, сульфонамид, карбамид, карбамат, сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид, где Rs1 представляет водород, Мy, С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С2-С11гетероциклоалкил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил или С6-С10гетероаралкил; Rs4 представляет водород, С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С2-С11гетероциклоалкил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил или С6-С10гетероаралкил; Rs2 и R20 представляют водород, С1-С12алкил, С2-С12алкенил, С3-С12циклоалкил, С3-С12циклоалкенил, С2-С11гетероциклоал-кил, С2-С11гетероциклоалкенил, С6-С10арил, С5-С9гетероарил, С7-С11аралкил, С6-С10гетероаралкил, С8-С11аралкенил или С7-С10гетероаралкенил; причем алкил, алкенил, алкокси, циклоалкил, циклоалкенил, гетероциклоалкил, гетероциклоалкенил, арил, арилокси, гетероарил, гетероарилокси, аралкил, аралкокси, гетероаралкил, аралкенил и гетероаралкенил, в свою очередь, являются незамещенными или замещенными одним из вышеуказанных заместителей; и у=1; а М обозначает одновалентный металл; либо у=1/2, а М обозначает двухвалентный металл.
18. Соединение по п.17, где
(i) R4 представляет С6Н11, С6H11-СH2, С6H11-СH2СH2-, С6H5-СH2-, С6H5-СH2СH2- или С6H5-СН=СН-СH2-;
(ii) R4 представляет С6Н11, С6Н11-СH2-, С6Н11-СH2СH2-, С6Н5-СH2-, С6Н5-СH2СH2-, СH2-NR19-SO2R18-, СH2-NR19-C(O)R40-, СH2NНС-(O)NHR18, СH2NHR21 или -СH2N(R21)2, где R18 представляет -С6Н5, фенил, который замещен 1-3 метильными или метоксигруппами, или -NO2, или F, или Сl, или С1-С4алкил, который замещен F; R40 представляет фенил, который незамещен или замещен 1-3 метильными или метоксигруппами, или -NO2 или F или Cl; R19 представляет Н, С1-С6алкил, фенил-(CH2)z-, где z=1-3; фенил-СН=СН-СH2, -СH2-СH(СН3)2 или бензил; a R21 представляет -СH2-CR22R23R24, где R22 и R23 представляют метил, этил или фенил, a R24 представляет Н, этил или метил; или
(iii) R4 представляет С6Н11, СH2-С6H5, (СH2)2-С6Н5, метил, этил или изопропил, которые являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей NH2, циклогексил, С6-С10арил, R8C(О)N(R9)-, R8S(O)2N(R9)-, NR9C(O)NHR8- и R8'R9'N-, где R8, R9, R8' и R9' независимо друг от друга представляют водород, C1-С12алкил, C3-С12циклоалкил, C6-С10арил или C7-С11аралкил, которые являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген, С(О)ОМy, нитро, циано, SO3My, OSO3My, NR20SO3My, C1-С12алкил, C1-С12алкокси и C6-С10арил, где R20 представляет водород, C1-С12алкшы, C2-С12алкенил, С3-С12циклоалкил, C3-С12циклоалкенил, C2-С11гетероциклоалкил, C2-С11гетероциклоалкенил, C6-С10арил, C5-С9гетероарил, C7-С11аралкил, C6-С10гетероаралкил, C8-С11аралкенил или C7-С10гетероаралкенил, у=1, а М обозначает одновалентный металл, либо у=1/2, а М обозначает двухвалентный металл.
19. Соединение по п.16, где R4 представляет C6H11, CH(CH3)2, CH2-фенил, (CH2)2-фенил, CH2NHС(O)-фенил, CH2NНС(O)(CH2)3-фенил, CH2NНС(O)(CH2)3ОН, CH2NНС(O)СF3, CH2NНС(O)С6Н11, CH2NНС(O)С11Н23, CH2NНС(O)CH(C6H5)2, CH2NНС(O)NНС6Н5, CH2NНС(O)C2H4CO2Na, CH2NНС(O)С6[(1,3,4,5)ОH]4Н7, CH2NНС(O)C6H4-п-SO3Na, CH2NНС(O)C6H4Cl, CH2NНС(O)C6H4NO2, CH2NНС(O)C6H4OCH3, CH2NНС(O)C6H4(3,4)Cl2, CH2NНС(O)С6Н4СН3, CH2NНС(O)C6H4C6H5, CH2NНС(O)С6Н4СN, CH2NНС(O)С10Н7, CH2NНС(O)C6H4COONa, CH2NНС(O)(CHOH)2COONa, CH2N(CH2CH=CH-фeнил)[С(О)-фенил], СН2N[СН2СН(СН3)2][С(O)-фенил], CH2N[С(O)C6H5]СH2С6H5, CH2N-[С(O)С6Н5](СН2)3С6Н5, (СH2)С6Н11, (СН2)2C6H11, CH2NH2, CH2NHCH2CH=СН-фенил, CH2NНСH2-фенил, СH2NНСН2СH(СН3)2, СН2N(СН2-фенил)2, СН2N[СН2СH(СН3)2]2, СН2NНSO2-п-нитрофенил, CH2NHSO2-п-толил, CH2NHSО2CF3, СН2NНС(O)С6Н5 или CH2N[SO2-п-нитрофенил] [ CH2CH(CH3)2] .
Текст
1 Настоящее изобретение относится к псевдосоединениям сиалил-Lewis Х и сиалил-Lewis А, в которых натуральный тетрасахарид, остаток нейраминовой кислоты, заменен метилом вS-конфигурации, замещенным одним карбоксильным остатком и одним другим заместителем, а N-ацетилглюкозаминовый остаток заменен негликозидным остатком 1,2-диола; к способам получения этих соединений; и к использованию указанных псевдосоединений в терапевтических методах. Сложный воспалительный процесс, который имеет несколько стадий, представляет собой естественную реакцию организма на повреждение, которым, например, является также поражение инфекционными агентами. Под действием цитокинов эндотелий, который выстилает кровеносные сосуды, экспрессирует на своей поверхности адгезивные белки. Селектины Р и Е, посредством белок-углеводного взаимодействия с гликолипидами и гликопротеинами на мембране лейкоцитов, индуцируют так называемый эффект "катящихся" лейкоцитов. Эти лейкоциты замедляются в этом процессе и на их поверхности происходит активация некоторых белков (интегринов), которые обеспечивают прочную адгезию лейкоцитов к эндотелию. После этого происходит миграция лейкоцитов в поврежденную ткань. Если описанный процесс происходит регулируемым образом, то через определенный промежуток времени это повреждение ткани устраняется без каких-либо значительных неблагоприятных последствий. В противном случае, то есть в случае некоторых острых и хронических воспалительных процессов, при которых миграция лейкоцитов происходит нерегулируемым образом, эти процессы приводят к тяжелым заболеваниям организма. К таким случаям можно отнести кардиогенный шок, инфаркт миокарда, тромбоз, ревматизм, псориаз, дерматиты, острый респираторный дистресс-синдром и рак с метастазами [Dasgupta F., Rao B.N.N.,Exp. Opin. Drugs 3: 709-724 (1994)]. Было проведено уже несколько исследований в целях разработки лекарственных средств,которые могли бы в некоторых случаях воспрепятствовать развитию этих нежелательных процессов [Dasgupta F., Rao B.N.N., Exp. Opin.Drugs 3: 709-724 (1994)]. Одним из способов предупреждения взаимодействия между Р- и Еселектинами и их рецепторами на мембране лейкоцитов является предупреждение эффекта"качения" путем имитации соответствующих эпитопов. Это также приводит подавлению последующих процессов. Одним из самых малых углеводных эпитопов, служащего лигандом для Е-селектина, является соединение сиалил-Lewis Х [нейраминовая кислота-(2-3)-галактоза(1-4)-(фукоза-(1-3)-N-ацетилглюкозамин 2 В ЕР-А-0579196 в качестве соединений,конкурирующих с натуральными лигандами за связывание с Е-селектином, предложены соединения, имитирующие (sLex), в которых остаток нейраминовой кислоты заменен остатком молочной кислоты. В WO 93/10796 описаны соединения, которые вместо остатка нейраминовой кислоты содержат остаток -гидроксикислоты. В WO 93/23031 описаны псевдосоединения, в которых N-ацетилглюкозаминовый остаток (остаток GlcNAc) заменен на R,R-1,2 циклогександиокси. Однако, все эти соединения объединяет тот факт, что аффинность связывания между ними и Е-селектином лишь очень незначительно превышает афинность связывания натуральных (sLex), а иногда даже ниже аффинности природныx соединений, и является недостаточной для достижения терапевтического эффекта. Неожиданно было обнаружено, что одновременная замена остатка нейраминовой кислоты S-конфигурированным метилом, замещенным одним карбоксильным остатком и одним другим заместителем, и N-ацетилглюкозаминового остатка негликозидным остатком алифатического диола приводит к исключительно высокой аффинности связывания полученного соединения. Кроме того, эти новые соединения являются химически и структурно более простыми, имеют более низкую молекулярную массу и могут быть получены в больших количествах и более простыми методами химического синтеза. Настоящее изобретение относится к соединениям формулы I в которой Х представляет остаток негликозидного алифатического 1,2-диола;R1 представляет группу формулы IIIR3 представляет водород или My;R4 представляет С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2 С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил, С 6-С 10 гетероаралкил, C8-С 11 аралкенил или С 7-С 10 гетероаралкенил, которые незамещены или замещены одним или более заместителями,выбранными из группы, включающей ОН, галоген, C(O)ORs1, OC(O)Rs4, C(O)Rs2, нитро, NH2,циано, SO3My, ОSО 3 Му, МR20SО 3 Му, С 1-С 12 ал 3 кил, С 2-С 12 алкенил, С 1-С 12 алкокси, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил,С 6-С 10 арилокси, С 5-С 9 гетероарил, С 5-С 9 гетероарилокси, С 7-С 11 аралкил, С 7-С 11 аралкилокси, С 6 С 10 гетероаралкил, С 8-С 11 аралкенил, С 7-С 10 гетероаралкенил, первичный амино, вторичный амино, сульфонил, сульфонамид, карбамид,карбамат, сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид;Rs2 и R20 представляют водород, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил, C6-С 10 гетероаралкил, С 8 С 11 аралкенил или С 7-С 10 гетероаралкенил; у равен 1 и М обозначает моновалентный металл или у равен 1/2 и М обозначает двухвалентный металл; причем алкил, алкенил, алкокси, циклоалкил, циклоалкенил, гетероциклоалкил, гетероциклоалкенил, арил, арилокси, гетероарил, гетероарилокси, аралкил, аралкокси, гетероаралкил,аралкенил или гетероаралкенил, в свою очередь,являются незамещенными или замещенными одним или более заместителями, выбранными из группы, состоящей из ОН, галоген, C(O)ORs1,OC(O)Rs4, C(O)Rs2, нитро, NH2, циано, SО 3 Му,ОSО 3 Му, NR20SО 3 Му, С 1-С 12 алкил, С 2-С 12 алкенил, С 1-С 12 алкокси, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 6-С 10 арилокси, С 5-С 9 гетероарил, С 5-С 9 гетероарилокси, С 7 С 11 аралкил, С 7-С 11 аралкилокси, C6-С 10 гетероаралкил, С 8-С 11 аралкенил, С 7-С 10 гетероаралкенил, первичный амино, вторичный амино,сульфонил, сульфонамид, карбамид, карбамат,сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид, включая физиологически приемлемые соли указанного соединения. Предпочтительны соединения, где Х представляет линейный или разветвленный С 2-С 20 алкилен,-алкенилен,С 3-С 12-циклоалкилен,-циклоалкенилен,С 3-С 11-гетероциклоалкилен или -гетероциклоалкенилен с гетероатомами,выбранными из группы, включающей -О-, -S- и-N-. В соединениях формулы I, где Х предпочтительно представляет остаток 1,2-диола,имеющего формулуR5 и R6 независимо друг от друга представляют водород, С 1-С 12 алкил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или С 6-С 10 гетероаралкил; либо R5 и R6, взятые вместе с группой-О-, -S- и -N-; где алкил, циклоалкил, гетероциклоалкил, арил, гетероарил, аралкил, гетероаралкил, циклоалкилен, циклоалкенилен, гетероциклоалкилен и гетероциклоалкенилен являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген, C(О)ORs1,OC(О)Rs4, C(О)Rs2, нитро, NH2, циано, SО 3 Му,ОSО 3 Му, NR20SО 3 Му, С 1-С 12 алкил, С 2-С 12 алкенил, С 1-С 12 алкокси, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 6-С 10 арилокси, С 5-С 9 гетероарил, С 5-С 9 гетероарилокси, С 7 С 11 аралкил, С 7-С 11 аралкилокси, С 6-С 10 гетероаралкил, С 8-С 11 аралкенил, С 7-С 10 гетероаралкенил, первичный амино, вторичный амино, сульфонил, сульфонамид, карбамид, карбамат,сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид, где Rs1 представляет водород, Мy, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или С 6-С 10 гетероаралкил; Rs4 представляет водород, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или С 6-С 10 гетероаралкил; Rs2 и R20 представляют водород,С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил,С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил,С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил, С 6-С 10 гетероаралкил,С 8-С 11 аралкенил или С 7-С 10 гетероаралкенил; причем алкил, алкенил, алкокси, циклоалкил,циклоалкенил, гетероциклоалкил, гетероциклоалкенил, арил, арилокси, гетероарил, гетероарилокси, аралкил, аралкокси, гетероаралкил, аралкенил или гетероаралкенил, в свою очередь,являются незамещенными или замещенными одним из вышеуказанных заместителей; у=1; а М обозначает одновалентный металл; либо у=1/2, а М обозначает двухвалентный металл. При этом предпочтительны соединения, где R5 и(а) являются незамещенными или замещенными С 1-С 12 алкилом или С 1-С 12 алкокси;(г) независимо друг от друга представляют водород, незамещенный С 1-С 12 алкил или С 1-С 12 алкил, который замещен заместителем, выбранным из группы, включающей -C(O)ORs1,-OC(O)Rs4, -C(O)ONa или С(O)ОК, первичный амино, вторичный амино, С 3-С 12 циклоалкил, С 1 С 6 алкокси, фенилокси и бензилокси; незамещенный С 3-С 12 циклоалкил или С 3-С 12 циклоалкил, который замещен заместителем, выбранным из группы, включающей -C(O)ORs1,-OC(O)Rs4, -C(O)ONa или С(O)ОК, первичный амино, вторичный амино, С 1-С 6 алкил, С 1-С 6 алкокси, фенилокси и бензилокси; С 6-С 10 арил,который незамещен или замещен -C(O)ORs1,-OC(O)Rs4, -C(O)ONa или С(O)ОК, первичным амино, вторичным амино, С 1-С 6 алкилом или С 1 С 6 алкокси; С 3-С 9 гетероарил с 1 или 2 гетероатомами, выбранными из группы, включающей атомы кислорода и азота; или С 7-С 12 аралкил,который незамещен или замещен -C(O)ORs1,-OC(O)Rs4, -C(O)ONa или С(O)ОК, первичным амино, вторичным амино, С 1-С 6 алкилом или С 1 С 6 алкокси;(д) вместе с группой -СН-СН- представляют 5-12 карбоцикл или 5- или 6-членный гетерокарбоцикл с гетероатомом, выбранным из группы, включающей атомы кислорода и азота; или(е) вместе с группой -СН-СН- представляют С 3-С 12 циклоалкилен, С 4-С 12 циклоалкенилен,С 2-С 11 гетероциклоалкилен или С 3-С 11 гетероциклоалкенилен с гетероатомами, выбранными из группы, включающей -О-, -S- и -N-; где циклоалкилен, циклоалкенилен, гетероциклоалкилен и гетероциклоалкенилен являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген, C(O)ORs1,OC(O)Rs4, C(O)Rs2, нитро, NH2, циано, SO3My,OSО 3 Му,NR20SО 3 Му,C1-С 12 алкил,С 2 С 12 алкенил,С 1-С 12 алкокси,С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил,C6-С 10 арилокси, С 5-С 9 гетероарил, С 5-С 9 гетероарилокси, С 7-С 11 аралкил, С 7-С 11 аралкилокси, С 6 С 10 гетероаралкил, С 8-С 11 аралкенил, С 7-С 10 гетероаралкенил, первичный амино, вторичный амино, сульфонил, сульфонамид, карбамид,карбамат, сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид, где Rs1 представляет водород, Мy, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил,С 7-С 11 аралкил или С 6-С 10 гетероаралкил; 6 представляют водород, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил,С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил, C6-С 10 гетероаралкил, С 8-С 11 аралкенил или С 7-С 10 гетероаралкенил; причем алкил, алкенил,алкокси, циклоалкил, циклоалкенил, гетероциклоалкил, гетероциклоалкенил, арил, арилокси,гетероарил, гетероарилокси, аралкил, аралкокси,гетероаралкил, аралкенил или гетероаралкенил,в свою очередь, являются незамещенными или замещенными одним из вышеуказанных заместителей; у=1, а М обозначает одновалентный металл; либо у=1/2, а М обозначает двухвалентный металл. Предпочтительными являются соединения,где R5 и R6, взятые вместе с группой -СН-СН-,представляют С 3-С 12 циклоалкилен или С 2-С 11 гетероциклоалкилен, где гетероатомом является атом азота, где R5 и R6, взятые вместе с группой-СН-СН-, представляют С 3-С 12 циклоалкилен или С 2-С 11 гетероциклоалкилен, где гетероатомом является атом азота, причем указанные циклоалкилен и гетероциклоалкилен являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, C(O)ORs1, ОС(O)Rs4,С(O)Rs2, NR8R9, С 1-С 12 алкил, R8C(O)(NH)pN(R9)-,-C(O)(NH)pNR8R9,R8S(O)2(NH)рN(R9)-,R8R40NC(O)-(NH)pN(R9)-, R8OC(O)(NH)pN(R9)-,-OC(O)(NH)pNR8R9, и R10-SO2-, где R8, R9, R10 иR40 независимо друг от друга представляют водород, ОН, С 1-С 12 алкил, С 1-С 12 алкенил, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 16 аралкил, С 8-С 16 аралкенил с С 2-С 6 алкениленом и С 6-С 10 арилом,С 6-С 15 гетероаралкил,С 6-С 15 гетероаралкенил,или ди-С 6-С 10 арил-С 1-С 6-алкил, которые являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген, C(O)ORs1,OC(O)Rs4, C(O)Rs2, нитро, NH2, циано, SО 3 Му,ОSО 3 Му, NR20SО 3 Му, С 1-С 12 алкил, С 2-С 12 алкенил, С 1-С 12 алкокси, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 6-С 10 арилокси, С 5-С 9 гетероарил, С 5-С 9 гетероарилокси, С 7 С 11 аралкил, С 7-С 11 аралкилокси, С 6-С 10 гетероаралкил, С 8-С 11 аралкенил, С 7-С 10 гетероаралкенил, первичный амино, вторичный амино,сульфонил, сульфонамид, карбамид, карбамат,сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид, где Rs1 представляет водород, My, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или С 6-С 10 гетероаралкил; Rs4 представляет водород, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или С 6-С 10 гетероаралкил; Rs2 и R20 представляют водород, 7 С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил,С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил,С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил, С 6-С 10 гетероаралкил,С 8-С 11 аралкенил или С 7-С 10 гетероаралкенил; а заместители алкил, алкенил, алкокси, циклоалкил, циклоалкенил, гетероциклоалкил, гетероциклоалкенил, арил, арилокси, гетероарил, гетероарилокси, аралкил, аралкокси, гетероаралкил,аралкенил и гетероаралкенил, в свою очередь,являются незамещенными или замещенными одним из вышеуказанных заместителей; у=1, а М обозначает одновалентный металл; либо у=1/2, а М обозначает двухвалентный металл. В указанной выше группе предпочтительными являются соединения, где R8 и R9 независимо друг от друга представляют водород, С 1 С 12 алкил, С 3-С 12 циклоалкил, С 6-С 10 арил, С 7-С 16 аралкил с 1-6 атомами в алкиленовой группе, и С 6-С 10 арил, С 8-С 16 аралкенил с С 2-С 6 алкениленом и С 6-С 10 арилом, или ди-С 6-С 10 арил-С 1-С 6 алкил, где R8 и R9 являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген, СООН, С(O)ОМy, С 1-С 12 алкил, С 1-С 6 алкокси, C6-С 10 арил, С 6-С 10 арилокси, SO3My, OSO3 Мy, МR20SО 3 Мy, NO2, амино,первичный амино, вторичный амино, и CN, а R20 представляет водород, С 1-С 12 алкил, С 2-С 12 алкеС 3-С 12 циклоалкенил,С 3-С 12 циклоалкил,нил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7 С 11 аралкил, С 6-С 10 гетероаралкил, С 8-С 11 аралкенил или С 7-С 10 гетероалкенил; у=1, а М обозначает одновалентный металл, либо у =1/2, а М обозначает двухвалентный металл. В указанной группе предпочтительными также являются соединения, где R10 представляет С 1-С 12 алкил, С 3-С 12 циклоалкил, С 6-С 10 арил,С 7-С 16 аралкил с 1-6 атомами в алкиленовой группе, и С 6-С 10 арил, которые являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген, карбоксил,С(O)ОМy, C1-С 12 алкил, С 1-С 6 алкокси, С 6 С 10 арил, SО 3 Мy, нитро, амино, первичный амино, вторичный амино и циано; или С 8 С 16 аралкенил с С 2-С 6 алкениленом и С 6 С 10 арилом, или ди-С 6-С 10 арил-С 1-С 6 алкил. Кроме того, предпочтительными являются соединения, где R5 и R6, взятые вместе с группой -СН-СН-, представляют С 3-С 12 циклоалкилен или С 2-С 11 гетероциклоалкилен, имеющий в качестве гетероатома азот; и где циклоалкилен и гетероциклоалкилен являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, C(O)ORs1, OC(O)Rs4, C(O)Rs2, NH2,R8C(-O)N(R9)-,-C(O)NR8R9,С 1-С 12 алкил,R8S(O)2N(R9)-, R8OC(O)N(R9)- и R10-SO2-, где R9 представляет водород, a R8 представляет С 1-С 12 8 алкил, С 6-С 10 арил или С 7-С 11 аралкил, которые являются незамещенными или замещенными одним или несколькими С 1-С 12 алкокси; R10 представляет С 1-С 12 алкил, С 6-С 10 арил или С 7-С 11 аралкил, которые являются незамещенными или замещенными одним или несколькими С 1-С 12 алкилами; Rs1 и Rs4 представляют С 1-С 12 алкил, aRs2 представляет С 1-С 12 циклоалкенил, С 3-С 12 циклоалкил или С 6-С 10 арил, а заместители алкил, циклоалкенил, циклоалкил и арил, в свою очередь, могут быть незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН,С(O)ОRs1' и ОС(O)Rs4', где Rs1' представляет Мy или С 1-С 12 алкил, a Rs4' представляет С 1 С 12 алкил; у=1, а М обозначает одновалентный металл, либо у=1/2, а М обозначает двухвалентный металл. Особенно предпочтительны соединения,где R5 и R6, взятые вместе с группой -СН-СН-,представляют циклогексилен. Еще более предпочтительными соединениями являются соединения, где R5 и R6, взятые вместе с группой -СН-СН-, представляют пиперидилен. При этом предпочтительны соединения,где R5 и R6, взятые вместе с группой -СН-СН-,представляют пиперидилен; где гетероатом является незамещенным или замещенным заместителем, выбранным из группы, включающейC(O)ORs1, C(O)Rs2, C(O)NR8R9, NH2, SO3My, С 1 С 12 алкил, С 2-С 12 алкенил, С 1-С 12 алкокси, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 12 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 6-С 10 арилокси, С 5-С 9 гетероарил, С 5-С 9 гетероарилокси, С 7-С 11 аралкил, С 7-С 11 аралкилокси, C6-С 10 гетероаралкил, С 8-С 11 аралкенил,С 7-С 10 гетероаралкенил, первичный амино, вторичный амино, сульфонил, сульфонамид, сульфонгидразид; и где один или несколько атомов С на кольце являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН,OC(O)Rs4, NH2, ОSО 3 Му, NR20SО 3 Му, С 1-С 12 алкокси, С 6-С 10 арилокси, С 5-С 9 гетероарилокси, С 7 С 11 аралкилокси, первичный амино, вторичный амино, сульфонамид, карбамид, карбамат, сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид, где Rs1 представляет водород, My, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или С 6-С 10 гетероаралкил; Rs4 представляет водород, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или С 6-С 10 гетероаралкил; R8 и R9 независимо друг от друга представляют водород, ОН, С 1-С 12 алкил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 16 аралкил, С 6-С 15 гетероаралкил, С 8-С 16 аралкенил с С 2-С 6 алкениленом и С 6-С 10 арилом, или ди-С 6-С 10 арил-С 1-С 6 9 алкил, либо R8 и R9, взятые вместе, представляют тетраметилен, пентаметилен, -(СН 2)2-О(СН 2)2-, -(СН 2)2-S-(СН 2)2- или -(СН 2)2-NR7(СН 2)2-, и R7 представляет Н, C1-С 6 алкил, С 7-С 11 аралкил, C(O)Rs2, или сульфонил; Rs2 и R20 представляют водород,С 1-С 12 алкил,С 2 С 12 алкенил, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7 С 11 аралкил, С 6-С 10 гетероаралкил, С 8-С 11 аралкенил или С 7-С 10 гетероаралкенил; причем алкил,алкенил, алкокси, циклоалкил, циклоалкенил,гетероциклоалкил, гетероциклоалкенил, арил,арилокси, гетероарил, гетероарилокси, аралкил,аралкокси, гетероаралкил, аралкенил и гетероаралкенил, в свою очередь, являются незамещенными или замещенными одним из вышеуказанных заместителей; у=1, а М обозначает одновалентный металл; либо у=1/2, а М обозначает двухвалентный металл. Более предпочтительны соединения, где R5 и R6, взятые вместе с группой -СН-СН-, представляют пиперидилен; где гетероатом является незамещенным или замещенным заместителем,выбранным из группы, включающей C(O)ORs1,C(O)Rs2, C(O)NR8R9 и R10-SO2-, а один или несколько атомов С на кольце являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, NH2, R8S(O)2N(R9)-,R8C(O)N(R9)- и R8OC(O)N(R9)-, где R9 представляет водород, a R8 представляет С 1-С 12 алкил, С 6-С 10 арил или С 7-С 11 аралкил, где алкил,арил и аралкил являются незамещенными или замещенными одним или несколькими С 1-С 12 алкокси; R10 представляет С 1-С 12 алкил, С 1-С 10 арил или С 7-С 11 аралкил, которые являются незамещенными или замещенными одним или несколькими С 1-С 6 алкилами; Rs1 представляет С 1-С 12 алкил, a Rs2 представляет С 1-С 12 алкил, С 3 С 12 циклоалкенил, С 3-С 12 циклоалкил или С 6-С 10 арил; а заместители алкил, циклоалкенил, циклоалкил и арил, в свою очередь, являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, C(O)Rs1' и ОС(O)Rs4',где Rs1' представляет Мy или С 1-С 12 алкил, a Rs4' представляет С 1-С 12 алкил; у=1, а М обозначает одновалентный металл, либо у=1/2, а М обозначает двухвалентный металл. Особенно предпочтительными являются также соединения, где Х представляет циклогексилен или пиперидилен, которые являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, состоящей из ОН, NH2, С 3 Н 7,-C(O)C6H5,-С(O)(CH2)8 С(О)OСН 3,-C(O)[CH(OH)]2C(O)ONa,C(O)-C6H8(OH)3,-С(O)-С 6 Н 11,-С(O)OС 3 Н 7,-C(O)NHC6H5,-NHC(O)OCH2C6H5,-NHS(O)2CH2C6H5,-NНС(O)С 6 Н 3(ОСН 3)2,-S(O)2-C4H9, 001356-NHC(O)NHС 6H5,-S(O)2-C6H4CH3,-S(O)2CH2C6H5, и -S(O)2-(CH2)C10H7. К предпочтительным относятся и соединения, где R2 представляет C1-С 6 алкил, а также соединения, где R1 соответствует группе формулы IIIR3 представляет водород или Мy; иR4 представляет С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил,С 6-С 9 гетероарил, С 7-С 11 аралкил, С 6-С 10 гетероаралкил, С 8-С 11 аралкенил или С 7-С 10 гетероаралкенил, которые являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген, C(O)ORs1, OC(O)Rs4,C(O)Rs2, нитро, NH2, циано, SO3My, OSO3My,NR20SO3My, С 1-С 12 алкил, С 2-С 12 алкенил, С 1-С 12 алкокси, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 6-С 10 арилокси, С 5 С 9 гетероарил, С 5-С 9 гетероарилокси, С 7-С 11 аралкил, С 7-С 11 аралкилокси, С 6-С 10 гетероаралкил,С 8-С 11 аралкенил, С 7-С 10 гетероаралкенил, первичный амино, вторичный амино, сульфонил,сульфонамид, карбамид, карбамат, сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид, где Rs1 представляет водород, My, С 1-С 12 алкил, С 2-С 12 алкенил,С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6 С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или С 6-С 10 гетероаралкил; Rs4 представляет водород,С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил,С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или C6-С 10 гетероаралкил;Rs2 и R20 представляют водород, С 1-С 12 алкил,С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил; С 5-С 9 гетероарил,С 7-С 11 аралкил, С 6-С 10 гетероаралкил, С 8-С 11 аралкенил или С 7-С 10 гетероаралкенил; причем алкил, алкенил, алкокси, циклоалкил, циклоалкенил, гетероциклоалкил, гетероциклоалкенил,арил, арилокси, гетероарил, гетероарилокси,аралкил, аралкокси, гетероаралкил, аралкенил или гетероаралкенил, в свою очередь, являются незамещенными или замещенными одним из вышеуказанных заместителей; у=1; а М обозначает одновалентный металл; либо у=1/2, а М обозначает двухвалентный металл. В особенно предпочтительном варианте изобретение относится к соединению, которое соответствует формуле IаR3 представляет водород или Мy;R4 представляет С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2 С 11 гетероциклоалкил,С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил, С 6-С 10 гетероаралкил, C8-С 11 аралкенил или С 7-С 10 гетероаралкенил, которые являются незамещенными или замещенными один или несколько раз;R5 и R6 независимо друг от друга представляют водород, С 1-С 12 алкил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или С 6-С 10 гетероаралкил; либо R5 и R6, взятые вместе с группой-N-; где алкил, циклоалкил, гетероциклоалкил,арил, гетероарил, аралкил, гетероаралкил, циклоалкилен, циклоалкенилен, гетероциклоалкилен и гетероциклоалкенилен являются незамещенными или замещенными один или несколько раз, где заместитель выбирают из группы,включающей ОН, галоген, C(O)ORs1, OC(O)Rs4,С(O)Rs2, нитро, NH2, циано, SО 3 Му, ОSО 3 Му,NR20SО 3 Му, С 1-С 12 алкил, С 2-С 12 алкенил, С 1-С 12 алкокси, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 6-С 10 арилокси, С 5-С 9 гетероарил, С 5-С 9 гетероарилокси, С 7-С 11 аралкил, С 7-С 11 аралкилокси, С 6-С 10 гетероаралкил,С 8-С 11 аралкенил, С 7-С 10 гетероаралкенил, первичный амино, вторичный амино, сульфонил,сульфонамид, карбамид, карбамат, сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид, где Rs1 представляет водород, Мy, С 1-С 12 алкил, С 2-С 12 алкенил, С 3 С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6 С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или C6 С 10 гетероаралкил; Rs4 представляет водород, С 1 С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 2 С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или С 6-С 10 гетероаралкил; 12 аралкокси, гетероаралкил, аралкенил и гетероаралкенил, в свою очередь, являются незамещенными или замещенными одним из вышеуказанных заместителей; у=1; а М обозначает одновалентный металл; либо у=1/2, а М обозначает двухвалентный металл. Предпочтительно соединение формулы Iа,где R3 представляет Н, К или Na;R5 и R6, взятые вместе с группой -СН-СН-,представляют С 3-С 12 циклоалкилен, С 4-С 12 циклоалкенилен, С 2-С 11 гетероциклоалкилен и С 3-С 11 гетероциклоалкилен с гетероатомами, выбранными из группы, включающей -О-, -S- и -N-,которые являются незамещенными или замещенными один или несколько раз; где заместитель выбирают из группы,включающей ОН, галоген, C(O)ORs1, OC(O)Rs4,С(O)Rs2, нитро, NH2, циано, SО 3 Му, ОSО 3 Му,NR20SО 3 Му, C1-С 12 алкил, С 2-С 12 алкенил, С 1-С 12 алкокси, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, C6-С 10 арилокси, С 5-С 9 гетероарил, С 5-С 9 гетероарилокси, С 7-С 11 аралкил, С 7-С 11 аралкилокси, С 6-С 10 гетероаралкил,С 8-С 11 аралкенил, С 7-С 10 гетероаралкенил, первичный амино, вторичный амино, сульфонил,сульфонамид, карбамид, карбамат, сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид, где Rs1 представляет водород, Мy, С 1-С 12 алкил, С 2-С 12 алкенил,С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6 С 10 арил, C5-С 9 гетероарил, С 7-С 11 аралкил или С 6 С 10 гетероаралкил; Rs4 представляет водород, С 1 С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 2 С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или C6-С 10 гетероаралкил;Rs2 и R20 представляют водород, С 1-С 12 алкил,С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 5-С 9 гетероарил,С 7-С 11 аралкил, C6-С 10 гетероаралкил, С 8-С 11 аралкенил или С 7-С 10 гетероаралкенил; причем алкил, алкенил, алкокси, циклоалкил, циклоалкенил, гетероциклоалкил, гетероциклоалкенил,арил, арилокси, гетероарил, гетероарилокси,аралкил, аралкокси, гетероаралкил, аралкенил и гетероаралкенил, в свою очередь, являются незамещенными или замещенными одним из вышеуказанных заместителей; и у=1; а М обозначает одновалентный металл; либо у=1/2, а М обозначает двухвалентный металл;(a) R4 представляет остаток R12-(СН 2)n или циклогексил, где n=1 или 2, a R12 представляет С 1-С 10 алкил, С 5-С 8 циклоалкил, С 6-С 10 арил, или С 8-С 12 аралкенил, которые незамещены или замещены С 1-С 4 алкилом, С 1-С 4 алкоксилом, F, Cl,-CN или -NO2; или R12 представляет аминогруппу NR8'R9', a R8' и R9' представляют С 1-С 12 алкил,либо незамещенный или С 1-С 4-алкилзамещенный C5- или С 6 циклоалкил, С 6-С 10 арил, С 7 С 12 аралкил или С 8-С 12 аралкенил; либо R12 представляет амидную группу -N(R9)C(O)R8, 13-NR9C(O)NHR8, где R8 представляет С 6-С 10 арил,который незамещен или замещен С 1-С 4 алкилом,С 1-С 4 алкокси, F, Cl, -CN или -NO2, либо С 1-С 10 алкил, который незамещен или замещен F или(b) R4 представляет С 1-С 12 алкил, С 3-С 12 циклоалкил или С 7-С 11 аралкил, которые являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген, C(O)ORs1,OC(O)Rs4, C(O)Rs2, нитро, NH2, циано, SО 3 Му,OSO3My, NR20SО 3 Му, C1-С 12 алкил, С 2-С 12 алкенил, С 1-С 12 алкокси, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 6-С 10 арилокси, С 5-С 9 гетероарил, С 5-С 9 гетероарилокси, С 7 С 11 аралкил, С 7-С 11 аралкилокси, С 6-С 10 гетероаралкил, С 8-С 11 аралкенил, С 7-С 10 гетероаралкенил, первичный амино, вторичный амино,сульфонил, сульфонамид, карбамид, карбамат,сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид, где Rs1 представляет водород, Мy, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или С 6-С 10 гетероаралкил; Rs4 представляет водород, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или С 6-С 10 гетероаралкил; Rs2 и R20 представляют водород,С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил,С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил,С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил, C6-С 10 гетероаралкил,С 8-С 11 аралкенил или С 7-С 10 гетероаралкенил; причем алкил, алкенил, алкокси, циклоалкил,циклоалкенил, гетероциклоалкил, гетероциклоалкенил, арил, арилокси, гетероарил, гетероарилокси, аралкил, аралкокси, гетероаралкил, аралкенил и гетероаралкенил, в свою очередь, являются незамещенными или замещенными одним из вышеуказанных заместителей; и у=1; а М обозначает одновалентный металл; либо у=1/2, а М обозначает двухвалентный металл. При этом наиболее предпочтительными являются соединения, где(ii) R4 представляет С 6 Н 11, С 6 Н 11-СH2-,С 6 Н 5-СH2-,С 6 Н 5-СH2 СН 2-,С 6 Н 11-CH2 СH2-,-CH2-NR19-SO2R18,-CH2-NR19-C(O)R40,-CH2NHC(O)NHR18, CH2NHR21 или -СН 2N(R21)2,где R18 представляет -C6H5, фенил, который замещен 1-3 метальными или метокси-группами,или -NO2 или F или Сl, или С 1-С 4 алкил, который замещен F; R40 представляет фенил, который незамещен или замещен 1-3 метальными или метокси-группами, или -NO2 или F или Сl;(iii) R4 представляет C6H11, CH2-C6H5,(СН 2)2-С 6 Н 5, метил, этил или изопропил, которые являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей NH2, циклогексил, С 6-С 10 арил, R8C(O)N(R9)-, R8S(O)2N(R9)-,-NR9C(O)NHR8 и R8'R9'N-, где R8, R9, R8' и R9' независимо друг от друга представляют водород, С 1-С 12 алкил, С 3-С 12 циклоалкил, С 6-С 10 арил,или С 7-С 11 аралкил, которые являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген, С(О)ОМy,нитро, циано, SО 3 Му, ОSО 3 Му, NR20SO3My, С 1 С 12 алкил, С 1-С 12 алкокси и C6-С 10 арил, где R20 представляет водород, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2 С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил, С 6-С 10 гетероаралкил, С 8-С 11 аралкенил или С 7-С 10 гетероаралкенил, у=1, а М обозначает одновалентный металл, либо у=1/2, а М обозначает двухвалентный металл. Другим предпочтительным соединением формулы Iа является соединение, где R4 представляет C6H11, СH(CH3)2, СН 2-фенил, (СН 2)2 фенил, СН 2NHС(О)-фенил, СН 2NНС(O)(СН 2)3 фенил, CH2NHC(O)(СН 2)3 ОН, СН 2NНС(O)СF3,СН 2NНС(O)С 6 Н 11,СН 2NНС(О)С 11 Н 23,СН 2NНС(O)CH(C6H5)2,СН 2NНС(O)NHC6H5,СН 2NНС(O)C2H4CO2Na,СН 2NНС(O)C6[(1,3,4,5)OH]4H7,СН 2NНС(O)C6H4-п-SO3Na, СН 2NНС(O)С 6 Н 4 Сl,СН 2NНС(O)С 6 Н 4NO2,СН 2NНС(O)С 6 Н 4OСН 3,СН 2NНС(O)С 6 Н 4(3,4)Сl2, СН 2NНС(O)С 6 Н 4 СН 3,СН 2NНС(O)С 6 Н 4 СN,СН 2NНС(O)С 6 Н 4 С 6 Н 5,СН 2NНС(O)С 10 Н 7,СН 2NНС(O)C6H4COONa,СН 2NНС(O)(CHOH)2COONa,СН 2N(СН 2 СН=СН-фенил)[С(O)-фенил],CH2N[CH2CH(CH3)2][С(О)-фенил],CH2N[C(O)C6H5]CH2C6H5,(CH2)C6H11,CH2N-[С(O)С 6 Н 5](СН 2)3 С 6 Н 5,(СН 2)2 С 6 Н 11,CH2NH2,СН 2NНСН 2 СН=СНфенил, CH2NHCH2-фенил, СН 2NНСН 2 СН(СН 3)2,СН 2N(СН 2-фенил)2,СН 2N[СН 2 СН(СН 3)2]2,СН 2NНSO2-п-нитрофенил, СН 2NНSO2-п-толил,СН 2NНSO2 СF3, СН 2NНС(O)C6H5 или CH2N[SO2 п-нитрофенил][СН 2 СН(СН 3)2]. Предпочтительными алифатическими остатками Х являются линейные или разветвленные C2-C20-, предпочтительно C2-C12-, а особенно предпочтительно С 2-С 6-алкилен и -алкенилен, С 3-С 12-, предпочтительно С 3-C8-, а особенно предпочтительно С 3-С 7-циклоалкилен и циклоалкенилен, и С 3-С 11-, предпочтительно С 3-С 7-, а особенно предпочтительно С 3-С 5-гетероцикло 15 алкилен и гетероциклоалкенилен с гетероатомами, выбранными из группы атомов -О-, -S- и-N-. Остаток X может содержать заместители,такие, как ОН, галоген, C(O)ORs1, OC(O)Rs4,C(O)Rs2, нитро, NH2, циано, SО 3 Му, OSO3 Му,NR20SO3 Му, С 1-С 12 алкил, С 2-С 12 алкенил, С 1-С 12 алкокси, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 6-С 10 арилокси, С 5 С 9 гетероарил, С 5-С 9 гетероарилокси, С 7-С 11 аралкил,C7-С 11 аралкилокси,С 6-С 10 гетероаралкил, С 8-С 11 аралкенил, С 7-С 10 гетероаралкенил, первичный амино, вторичный амино, сульфонил, сульфонамид, карбамид, карбамат,сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид, где Rs1 представляет водород, Мy, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10 арил, C5-С 9 гетероарил, С 7-С 11 аралкил или С 6-С 10 гетероаралкил; Rs4 представляет водород, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или C6-С 10 гетероаралкил; Rs2 и R20 представляют водород,С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил,С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил,С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил, C6-С 10 гетероаралкил,С 8-С 11 аралкенил или С 7-С 10 гетероаралкенил; причем алкил, алкенил, алкокси, циклоалкил,циклоалкенил, гетероциклоалкил, гетероциклоалкенил, арил, арилокси, гетероарил, гетероарилокси, аралкил, аралкокси, гетероаралкил, аралкенил или гетероаралкенил, в свою очередь,являются незамещенными или замещенными одним из вышеуказанных заместителей; у=1; а М обозначает одновалентный металл; либо у=1/2, а М обозначает двухвалентный металл. Следует отметить, что в контексте настоящего изобретения термин "металл" означает щелочной металл, например, литий (Li), натрий(Ag). Термин "физиологически приемлемые соли" означает, в частности, соли щелочных металлов и щелочно-земельных металлов, например, соли натрия, калия, магния и кальция. При этом предпочтительными являются ионы натрия и калия и их соли. Термин "галоген" означает фтор, хлор,бром и йод. Предпочтительными является фтор,хлор и бром, а особенно предпочтительными фтор и хлор. Алкил может быть линейным или разветвленным, предпочтительно разветвленным один раз или два раза в -положении. Конкретными примерами алкила, который содержит предпочтительно 1-12 атомов углерода, могут служить метил, этил и изомеры пропила, бутила, пенти 001356 16 ла, гексила, гептила, октила, нонила, децила,ундецила и додецила. Предпочтительными алкильными группами являются метил, этил, н- и изопропил, н-, изо- и трет.-бутил. Примерами алкенила являются аллил, бут 1-ен-3-ил или 4-ил, пент-3-или 4-ен-1-ил или 2 ил, гекс-3- или 4- или 5-ен-1-ил или -2-ил и (С 1 С 4 алкил)СН=СН-СН 2-. Циклоалкил и циклоалкенил могут содержать предпочтительно 5-8, а особенно предпочтительно 5 или 6 атомов углерода на кольце. Примерами циклоалкила являются циклопропил, циклобутил, циклопентил, циклогексил,циклопентил, циклогептил, циклооктил, циклононил, циклодецил, циклоундецил и циклододецил. Особенно предпочтительной циклоалкильной группой является циклогексил. Примерами циклоалкенила являются циклопропенил, циклобутенил, циклопентенил, циклогексенил, циклогептенил, циклооктенил, циклононенил, циклодеценил, циклоундеценил и циклододеценил. Особенно предпочтительной циклоалкенильной группой является циклогексенил. Примерами алкилена являются этилен, 1,2 пропилен, 1,2- или 2,3-бутилен, 1,2- или 2,3 пентилен, 1,2-, 2,3- или 3,4-гексилен. Примерами циклоалкилена являются 1,2-циклопропилен,1,2-циклобутилен,1,2-циклопентилен,1,2 циклогексилен, 1,2-циклогептилен и 1,2 циклооктилен. Примерами гетероциклоалкилена являются пирролидинилен, пиперидинилен,тетрагидрофуранилен, ди- и тетрагидропиранилен. Примерами гетероциклоалкила являются группы, происходящие от пирролидина, имидазолидина, оксазолидина, пиразолидина, пиперидина, пиперазина и морфолина. Примерами гетероциклоалкенила являются группы, происходящие от 2- и 3-пирролина, оксазолина, 2- и 4 имидазолина и 2- и 3-пиразолина. В соответствии с настоящим изобретением, арил или гетероарил представляют собой 5 или 6-членное кольцо или бицикл, состоящий из двух конденсированных 6- или 5-членных колец, или из одного 6-членного и одного 5 членного кольца, и в случае такого гетероарила,один или несколько атомов углерода могут быть независимо друг от друга заменены другим атомом, выбранным из группы, включающей атомы кислорода, азота и серы. Примерами могут служить группы, происходящие от бензола,нафталина, индена, фурана, пиррола, пиразола,имидазола, изоксазола, оксазола, фуразана, тиадиазола, тиофена, тиазола, оксадиазола, триазола, индола, индазола, пурина, бензимидазола,бензоксазола, бензотиазола, пирана, пиридина,пиридазина, триазина, пиримидина, пиразина,изохинолина, циннолина, фталазина, хинолина,хиназолина, птеридина, бензотриазина или хиноксалина. Предпочтительным арилом является нафтил и фенил. Особенно предпочтительным является фенил. Предпочтительным гетероари 17 лом является фуранил, пиридинил и пиримидинил. Аралкил предпочтительно имеет 7-12 атомов углерода и может представлять собой фенил-СnН 2n-, где n равно целому числу от 1 до 6. В качестве примеров могут служить бензил,фенилэтил или фенилпропил. Предпочтительными являются бензил и 2-фенилэтил. Аралкенилом является предпочтительно незамещенный фенил-СН=СН-СН 2- (циннамил), или циннамил является замещенным на фениле заместителем,выбранным из группы, включающей ОН, галоген, СООН, С(O)ОМy, С 1-С 12 алкил, С 1 С 6-С 10 арил,SО 3 Му,ОSО 3 Мy,С 6 алкокси,NR20SO3 Мy, где R20 представляет С 1-С 12 алкил,С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 6-С 10 арилокси,С 5-С 9 гетероарил, C7-С 11 аралкил, С 6-С 10 гетероаралкил, С 8-С 11 аралкенил, С 7-С 10 гетероаралкенил, и NO2, С 1-С 12 первичный амино, С 2-С 20 вторичный амино, амино и CN. Гетероаралкилом и гетероаралкенилом являются предпочтительно C4-С 5 гетероарилметил и С 4-С 5 гетероарилэтенил с 1 или 2 гетероатомами, выбранными из группы, включающей атомы О и N, а гетероарил может содержать вышеупомянутые гетероарильные остатки. Алкокси может быть линейным или разветвленным, предпочтительно разветвленным один раз или дважды в -положении. Конкретными примерами алкокси, который предпочтительно содержит 1-12 атомов углерода, могут служить метокси, этокси, и изомеры пропокси,бутокси, пентокси, гексокси, гептокси, октокси,нонокси, дексокси, ундекскси и додексокси. Предпочтительными алкоксигруппами являются метокси и этокси . Примерами арилокси и аралкокси являются фенокси и бензилокси. Предпочтительным гетероарилокси являются фуранилокси, пиридинилокси и пиримидинилокси. Первичный амино предпочтительно содержит 1-12, а более предпочтительно 1-6 атомов С. Конкретными примерами могут служить метил-, этил-, гидроксиэтил-, н- или изопропил,н-, изо- или трет.-бутил-, пентил-, гексил-, циклопентил-, циклогексил-, фенил-, метилфенил-,бензил- и метилбензиламино. Вторичный амино предпочтительно содержит 2-14, а особенно предпочтительно 2-8 атомов С. Конкретными примерами могут служить диметил-, диэтил-,метилэтил-, ди-н-пропил-, диизопропил, ди-нбутил-, дифенил-, дибензиламино, морфолино,пиперидино и пирролидино.NH2, первичный амино, вторичный амино,карбамид, карбамат, карбгидразид, сульфонамид, сульфогидразид и аминокарбониламид репрезентативно выбирают из вышеуказанных групп, включающих R8C(O)(NH)pN(R9)-,R8OC(O)(NH)pN(R9)-,-C(O)(NH)pNR8R9,R8R40NC(O)(NH)pN(R9)-, 001356-NR40S(O)2NR8R9, где R8, R9 и R40 независимо друг от друга представляют водород, ОН, С 1-С 12 алкил, С 1-С 12 алкенил, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 16 аралкил, C8-С 16 аралкенил с С 2-С 6 алкениленом и С 6-С 10 арилом, С 6-С 15 гетероаралкил, С 6-С 15 гетероаралкенил, или ди-С 6-С 10 арил-С 1-С 6-алкил, либо R8'R9'N, где R8' и R9' независимо друг от друга представляют водород,ОН, SO3My, OSO3 Мy, C1-С 12 алкил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5 С 9 гетероарил, С 7-С 11 аралкил, С 6-С 10 гетероаралкил, С 8-С 16 аралкенил с С 2-С 6 алкениленом и С 6-С 10 арилом, или ди-С 6-С 10 арил-С 1-С 6-алкил,которые являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН,галоген, C(O)ORs1, OC(O)Rs4, C(O)Rs2, нитро,NH2, циано, SO3My, ОSО 3 Му, NR20SO3My, С 1 С 12 алкил, С 2-С 12 алкенил, С 1-С 12 алкокси, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 6-С 10 арилокси, С 5-С 9 гетероарил, С 5-С 9 гетероарилокси, С 7-С 11 аралкил, С 7-С 11 аралкилокси, С 6-С 10 гетероаралкил, С 8-С 11 аралкенил,С 7-С 10 гетероаралкенил, первичный амино, вторичный амино, сульфонил, сульфонамид, карбамид, карбамат, сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид, где Rs1 представляет водород, Мy,С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил,С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или C6-С 10 гетероаралкил;Rs4 представляет водород, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или С 6-С 10 гетероаралкил; a Rs2 представляют водород, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил, С 6-С 10 гетероаралкил, С 8-С 11 аралкенил или С 7-С 10 гетероаралкенил; причем алкил, алкенил, алкокси,циклоалкил, циклоалкенил, гетероциклоалкил,гетероциклоалкенил, арил, арилокси, гетероарил, гетероарилокси, аралкил, аралкокси, гетероаралкил, аралкенил или гетероаралкенил, в свою очередь, являются незамещенными или замещенными одним из вышеуказанных заместителей; р=0 или 1, у=1, а М обозначает одновалентный металл; либо у=1/2, а М обозначает двухвалентный металл; либо R8 и R9 или R8' иR10 обозначает С 1-С 12 алкил, С 3-С 12 циклоалкил,С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или С 6-С 10 гетероаралкил,которые являются незамещенными или замещенными одним или несколькими заместителями, где указанные заместители выбирают из группы, включающей ОН, галоген, C(O)ORs1,OC(O)Rs4, C(O)Rs2, нитро, NН 2, циано, SО 3 Му,ОSО 3 Му, NR20SO3My, С 1-С 12 алкил, С 2-С 12 алкенил, С 1-С 12 алкокси, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 6-С 10 арилокси, С 5-С 9 гетероарил, C5-С 9 гетероарилокси, С 7 С 11 аралкил, С 7-С 11 аралкилокси, С 6-С 10 гетероаралкил, С 8-С 11 аралкенил, С 7-С 10 гетероаралкенил, первичный амино, вторичный амино, сульфонил, сульфонамид, карбамид, карбамат,сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид, где Rs1 представляет водород, My, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или С 6-С 10 гетероаралкил; Rs4 представляет водород, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или С 6-С 10 гетероаралкил; a Rs2 и R20 представляют водород, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил,С 5-С 9 гетероарил, С 7-С 11 аралкил, С 6-С 10 гетероаралкил, С 8-С 11 аралкенил или С 7-С 10 гетероаралкенил; причем алкил, алкенил, алкокси, циклоалкил, циклоалкенил, гетероциклоалкил, гетероциклоалкенил, арил, арилокси, гетероарил,гетероарилокси, аралкил, аралкокси, гетероаралкил, аралкенил или гетероаралкенил, в свою очередь, являются незамещенными или замещенными одним из вышеуказанных заместителей; у=1, а М обозначает одновалентный металл; либо у=1/2, а М обозначает двухвалентный металл.R10 представляет, в частности, С 1-С 12 алкил,С 3-С 12 циклоалкил, С 6-С 10 арил, С 7-С 16 аралкил с 1-6 атомами в алкиленовой группе, и С 6 С 10 арил, C8-С 16 аралкенил с С 2-С 6 алкениленом и С 6-С 10 арилом, или ди-С 6-С 10 арил-С 1-С 6 алкил,например, дифенилметил или 2,2-дифенилэтил,которые являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН,галоген, СООН, С(O)ОМу, С 1-С 12 алкил, С 1 С 6 алкокси,С 6-С 10 арил,SO3My,ОSО 3 Му,NR20SО 3 Му, NO2, амино, первичный амино, вторичный амино и CN; где R20 представляет водород, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, 001356R10 представляет С 1-С 12 алкил, С 3-С 12 циклоалкил, С 6-С 10 арил, С 7-С 16 аралкил с 1-6 атомами в алкиленовой группе, и С 6-С 10 арил, которые являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген,карбоксил, С(O)ОМ , С 1-С 12 алкил, С 1-С 6 алкокси, С 6-С 10 арил, SО 3 Мy, нитро, амино, первичный амино, вторичный амино и циано; или C8 С 16 аралкенил с С 2-С 6 алкениленом и С 6 С 10 арилом, или ди-С 6-С 10 арил-C1-С 6 алкил, например, дифенилметил или 2,2-дифенилэтил. Предпочтительной подгруппой соединений являются соединения, в которых R5 и R6,взятые вместе с группой -СН-СН-, представляют пиперидилен, который является незамещенным или замещенным одним или несколькими заместителями, выбранным из группы, включающей ОН, C(O)ORs1, ОС(O)Rs4, C(O)Rs2, NH2,С 1-С 12 алкил,R8C(O)N(R9)-,-C(O)NR8R9,R8S(O)2N(R9);N(R9)-, -OC(O)NR8R9 и R10-SO2-, где R9 представляет водород, R8 представляет С 1-С 12 алкил,С 6-С 10 арил или С 7-С 11 аралкил, которые являются незамещенными или замещенными одним или несколькими С 1-С 12 алкокси; R10 представляет С 1-С 12 алкил, С 6-С 10 арил или С 7-С 11 аралкил,которые являются незамещенными или замещенными одним или несколькими С 1 С 6 алкилами; R40 предствляет водород, С 1-С 12 алкил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 10 гетероарил, С 7-С 11 аралкил или С 6-С 10 гетероаралкил; Rs1 и Rs4 представляют С 1-С 12 алкил, и Rs2 представляет С 1-С 12 алкил, С 3-С 12 циклоалкенил, С 3-С 12 циклоалкил или С 6-С 10 арил; а заместители алкил, циклоалкенил, циклоалкил и арил, в свою очередь,являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, C(O)Rs1' и OC(O)Rs4', где Rs1' представляет Мy или С 1 С 12 алкил, a Rs4' представляет С 1-С 12 алкил; у=1, а М обозначает одновалентный металл; либо у=1/2, а М обозначает двухвалентный металл. Предпочтительными соединениями формулы I являются соединения, в которых R1 соответствует группе формулы III, где R3 представляет водород или My, a R4 представляет(а) незамещенный С 1-С 12 алкил; С 1-С 12 алкил, который замещен одним или несколькими заместителями, выбранными из группы, включающей -NН 2, первичный амино, вторичный амино, С 1-С 12 сульфонил, карбамид, карбамат,карбгидразид, сульфонамид, сульфонгидразид,аминокарбониламидо, С 3-С 12 циклоалкил, С 1 С 6 алкокси, фенилокси и бензилокси; незаме 21 щенный С 3-С 12 циклоалкил; С 3-С 12 циклоалкил,который замещен одним или несколькими заместителями, выбранными из группы, включающей С 3-С 12 циклоалкил, С 1-С 6 алкил, С 1 С 6 алкокси, С 1-С 12 сульфонил, фенилокси и бензилокси; С 6-С 10 арил; С 3-С 9 гетероарил с 1 или 2 гетероатомами, выбранными из атомов кислорода и азота; С 7-С 16 аралкил с С 1-С 8 алкилом и С 6-С 10 арилом; С 4-С 16 гетероаралкил с С 1 С 6 алкилом и С 3-С 10 гетероарилом, имеющим 1 или 2 гетероатома, выбранных из атомов кислорода и азота, и всего 3-5 атомов углерода; С 6 С 10 арил, С 3-С 9 гетероарил с 1 или 2 гетероатомами, выбранными из атомов кислорода и азота; С 7-С 16 аралкил с С 1-С 6 алкилом и С 6-С 10 арилом; С 3-С 16 гетероаралкил с С 1-С 6 алкилом и С 4-С 10 гетероарилом, имеющим 1 или 2 гетероатома,выбранных из атомов кислорода и азота, и всего 3-5 атомов углерода, которые замещены одним или несколькими заместителями, выбранными из группы включающей ОН, галоген, С 1-С 12 сульфонил, карбоксил, С(O)ОМy, С 1-С 12 алкил,C1-С 6 алкокси, С 6-С 10 арил, SO3My, OSO3My,NR20SO3My, где R20 представляет водород, С 1 С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 3 С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2 С 11 гетероциклоалкенил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил, С 6-С 10 гетероаралкил, С 8 С 11 аралкенил или С 7-С 10 гетероаралкенил, и нитро, NH2, первичный амино, вторичный амино,карбамид, карбамат, сульфонамид и циано, где у=1, а М обозначает одновалентный металл,либо у=1/2, а М обозначает двухвалентный металл, либо(б) С 1-С 12 алкил или С 7-С 11 аралкил, которые являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген,C(O)ORs1, OC(O)Rs4, C(O)Rs2, нитро, NH2, циано, SО 3 Му, OSO3My, NR20SО 3 Му, С 1-С 12 алкил,С 2-С 12 алкенил, С 1-С 12 алкокси, С 3-С 12 циклоалС 2-С 11 гетероциккил, С 3-С 12 циклоалкенил,лоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил,С 6-С 10 арилокси, С 5-С 9 гетероарил, С 5-С 9 гетероарилокси,С 7-С 11 аралкил,С 7-С 11 аралкилокси, С 6-С 10 гетероаралкил, С 8-С 11 аралкенил, С 7 С 10 гетероаралкенил, первичный амино, вторичный амино, сульфонил, сульфонамид, карбамид,карбамат, сульфонгидразид, карбгидразид, карбоксигидроксамовую кислоту и аминокарбониламид, где Rs1 представляет водород, Мy, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил,С 7-С 11 аралкил или C6-С 10 гетероаралкил; Rs4 представляет водород, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил,С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или С 6-С 10 гетероаралкил; Rs2 и R20 представляют водород, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил, С 6-С 10 22 гетероаралкил, С 8-С 11 аралкенил или С 7-С 10 гетероаралкенил; причем алкил, алкенил, алкокси, циклоалкил, циклоалкенил, гетероциклоалкил, гетероциклоалкенил, арил, арилокси, гетероарил, гетероарилокси, аралкил, аралкокси, гетероаралкил,аралкенил и гетероаралкенил, в свою очередь,являются незамещенными или замещенными одним из вышеуказанных заместителей; у=1, а М обозначает одновалентный металл; либо у=1/2, а М обозначает двухвалентный металл.R3 в формуле III является предпочтительно водородом, К или Na. Предпочтительной является группа (а), в которойR4 представляет алкил, предпочтительно метил, этил, н- или изопропил, изо- или трет.бутил. В случае замещенного алкила, алкиленовой группой предпочтительно является этилен, а особенно предпочтительно метилен. Особенно предпочтительной циклоалкильной группой является циклогексил. Предпочтительными арилом и аралкилом являются нафтил и фенил,наиболее предпочтительно фенил и фенилСnН 2n-, где n равно целому числу от 1 до 6, а особенно предпочтительно бензил и 2 фенилэтил. Если R4 представляет гетероарил, то предпочтительным является С 4-С 5 гетероарил с одним или двумя гетероатомами, выбранными из группы, включающей О и N. Предпочтительными являются фуранил, пиридинил и пиримидил. Если R4 представляет гетероаралкил, то предпочтительным является С 4-С 5 гетероарилметил, который имеет один или два гетероатома, выбранные из группы, включающей О и N, а в качестве гетероарила может содержать вышеупомянутые гетероарильные группы. Другими предпочтительными соединениями являются соединения, в которых R4 в формуле III представляет С 3-С 12 циклоалкил, особенно предпочтительно циклогексил, С 1-С 4 алкил, в частности, метил или этил, замещенный С 3 С 12 циклоалкилом или С 1-С 4 алкилом, а в частности, циклогексилом или метилом; С 6-С 10 арил, а особенно предпочтительно фенил, либо R4 представляет С 7-С 12 аралкил с С 1-С 6 алкилом и С 6-С 10 арилом. В этой серии особенно предпочтительными группами R4 являются бензил, нафтилметил, 2-фенилэтил, 3-фенилпропил, циклогексилметил, 2-циклогексилэтил, циклогексил и изопропил. Карбамидо, карбгидразидо, сульфонамидо,сульфонгидразидо, амино-карбониламид и карбамат, присутствующие в качестве заместителей для R4, предпочтительно представляют группу формулR8NHC(O)N(R9)-,R8OC(O)-N(R9)-,R8C(O)(NH)pN(R9)- и R8S(O)2(NH)pN(R9)-, где R8 предпочтительно представляет Н, С 1-С 12 алкил,C5- или С 6 циклоалкил, С 5- или С 6 циклоалкилметил или -этил, C5- или С 6 гетероциклоалкил,С 5- или С 6 гетероциклоалкилметил или -этил,фенил, нафтил, бензил, 2-фенилэтил, дифенил 23 метил, которые являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, -NH2, С 1-С 8 пepвичный амино, С 2-С 14 вторичный амино, NО 2, CN, -F, -Cl, -С(O)ОН,-C(O)ONa, -SО 3 Н, -OSO3Na, NR20SO3Na, где R20 представляет водород, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2 С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил, С 6-С 10 гетероаралкил, С 8-С 11 аралкенил или С 7-С 10 гетероаралкенил, и SО 3Nа, С 1-С 4 алкил,С 1-С 4 алкокси и фенил; a R9 представляет Н, С 1 С 10 алкил, фенил, нафтил, бензил, 2-фенилэтил или фенил-СН=СН-СН 2-, и р=0 или 1. В группе (а) особенно предпочтительным карбамидозамещенным алкильным заместителем для R4 является R8C(O)NR9-(CH2)n-, где n=1 или 2,R8 представляет водород, С 1-С 12 алкил, С 3 С 12 циклоалкил, С 6-С 10 арил или С 7-С 16 аралкил с С 1-С 6 алкилом и С 6-С 10 арилом, где алкил, циклоалкил, арил и аралкил являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген, карбоксил, С(O)ОМу, С 1 С 12 алкил, С 1-С 6 алкокси, С 6-С 10 арил, SО 3 Му,ОSО 3 Му, NR20SO3My, C(O)ORs1, ОС(O)Rs4, нитро, амино и циано; или С 8-С 16 аралкенил с С 2-С 8 алкенилом и С 6-С 10 арилом, или ди-С 6-С 10 арилС 1-С 6 алкил; a R9 представляет Н, линейный или разветвленный С 1-С 10 алкил, C5- или С 6 циклоалкил, С 5- или С 6 циклоалкилметил- или -этил, фенил, нафтил или бензил, 2-фенилэтил или фенил-СН=СН-СН 2-; у=1, а М обозначает щелочной металл, либо у=1/2, а М обозначает щелочно-земельный металл, R20 представляет водород,С 1-С 12 алкил,С 2-С 12 алкенил,С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, C6-С 10 арил,С 5-С 9 гетероарил, С 7-С 11 аралкил, С 6-С 10 гетероаралкил, C8-С 11 аралкенил или С 7-С 10 гетероаралкенил; Rs1 представляет водород, Мy, C1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10aрил, С 5-С 9 гетероарил,С 7-С 11 аралкил или С 6-С 10 гетероаралкил, a Rs4 представляет водород, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил,С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил, С 6 С 10 гетероаралкил. Особенно предпочтительным сульфонамидозамещенным алкильным заместителем для R4 является R8-SO2NR9-(CH2)n-, гдеR8, R9 и n являются такими, как они были определены выше для карбамидо. Особенно предпочтительным аминокарбониламино- или карбаматозамещенным алкильным заместителем для R4 является R9NН-С(O)-NН-(CH2)n или R9OC(O)-NH-(СН 2)n, где R9 является таким, как он определен выше для карбамидо, и, кроме того,R9 представляет фенил, а n является таким, как он определен выше в случае карбамидо. Особенно предпочтительным карбгидразидозаме 001356 24 щенным алкильным заместителем для R4 является R8 С(O)-NНNR9-(CН 2)n, где R8, R9 и n являются такими, как они были определены выше в случае карбамидо. Особенно предпочтительным сульфонгидразидозамещенным алкильным заместителем для R4 является R8-SO2-NHNR9(CH2)n, где R8, R9 и n являются такими, как они были определены выше в связи с карбамидо. Еще более предпочтительными являются соединения, в которых R4 в формуле III представляет амидR8S(O2)N(R9)(CH2)n-, где R8 и R9 независимо друг от друга представляют водород, незамещенный С 1-С 12 алкил, который замещен одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген, карбоксил, C(O)ONa, C1-С 12 алкил, C1-С 6 алкокси, C6 С 10 арил, -SO3H, OSO3Na, NR20SО 3Nа, SO3Nа,нитро и циано; незамещенный C3-С 12 циклоалкил; C3-С 12 циклоалкил, замещенный одним или несколькими ОН; незамещенный C6-С 10 арил,незамещенный C7-С 12 аралкил с C1-С 6 алкилом иC1-С 6 алкилом и C6-С 10 арилом, который замещен одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген,карбоксил, C(O)ONa, -С(O)К, C1-С 12 алкил, C1 С 6 алкокси,C6-С 10 арил,OSO3Na,SО 3Nа,NR20SO3Na, C(O)ORs1, С(O)ОRs4, нитро, амино и циано; R20 представляет водород, C1-С 12 алкил,C2-С 12 алкенил, C3-С 12 циклоалкил, С 3-С 12 циклоалкенил, C2-С 11 гетероциклоалкил, C2-С 11 гетероциклоалкенил, C6-С 10 арил, С 5-С 9-гетероарил,C7-С 11 аралкил, C6-С 10 гетероаралкил, C8-С 11 аралкенил или C7-С 10 гетероаралкенил; RS1 представляет водород, Мy, С 1-С 12 алкил, C2-С 12 алкенил, C3-С 12 циклоалкил, C2-С 11 гетероциклоалкил,C6-С 10aрил, С 5-С 9-гетероарил, C7-С 11 аралкил илиC6-С 10 гетероаралкил, a Rs4 представляет водород, C1-С 12 алкил, C2-С 12 алкенил, C3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, C6-С 10 арил, С 5 С 9 гетероарил, C7-С 11 аралкил или С 6-С 10 гетероаралкил; n=2 или 1. Особенно предпочтительными являются соединения, в которых R4 в формуле III представляет амидR8S(O2)N(R9)(СН 2)n-, где R8 представляет незамещенный С 1-С 12 алкил; С 1-С 8 алкил, который замещен одним или несколькими заместителями, выбранными из группы, включающей ОН,галоген, C(O)ONa, и С 6-С 10 арил; незамещенный С 3-С 12 циклоалкил; С 3-С 8 циклоалкил, замещенный одним или несколькими ОН; незамещенный C6-С 10 арил, или С 7-С 12 аралкил с С 1-С 6 алкилом; С 6-С 10 арил, С 7-С 12 аралкил с С 1-С 6 алкилом и С 6-С 10 арилом, или С 8-С 16 аралкенил с С 2-С 6 алкенилом и C6-С 10 арилом, который замещен одним или несколькими заместителями, выбранными из группы, включающей галоген,С(O)ОН, C(O)ONa, С 1-С 12 алкил, С 1-С 6 алкокси,-SО 3 Н, SO3Nа, OSO3Na, NR20SO3Na, где R20 представляет водород,С 1-С 12 алкил,С 2 25 С 12 алкенил, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 5-С 9-гетероарил, С 7 С 11 аралкил, С 6-С 10 гетероаралкил, С 8-С 11 аралкенил или С 7-С 10 гетероаралкенил; нитро и циано;C6-С 10aрилом; а n=2, а предпочтительно 1. Особенно предпочтительными также являются соединения, в которых R4 в формуле III представляет амид R8C(O)N(R9)(CH2)n-, где R8 представляет незамещенный С 1-С 12 алкил; С 1-С 8 алкил, который замещен одним или несколькими заместителями, выбранными из группы,включающей циклогексил, ОН, галоген,С(O)ОН, C(O)ONa, и фенил; незамещенный С 3 С 12 циклоалкил; С 3-С 12 циклоалкил, который замещен одним или несколькими ОН; незамещенный С 6-С 10 арил; С 6-С 10 арил, который замещен одним или несколькими заместителями, выбранными из группы, включающей галоген,C(O)ONa, -С(O)ОН, С 1-С 6 алкил, С 1-С 6 алкокси,фенил, -SO3 Н, SO3Na, ОSО 3Na, NНSО 3Nа, нитро и циано; или С 7-С 16 аралкил с С 1-С 6 алкилом и С 6-С 10 арилом, a R9 представляет водород; незамещенный С 1-С 6 алкил, незамещенный С 7 С 16 аралкил с С 1-С 6 алкилом и С 6-С 16 арилом; или С 8-С 16 аралкенил с С 2-С 6 алкенилом и С 6-С 10 арилом; а n=2, а предпочтительно 1. Еще более предпочтительными являются соединения, в которых R4 в формуле III представляет амид R8C(O)N(R9)(CH2)n-, где R8 представляет незамещенный С 1-С 12 алкил; С 1-С 4 алкил, который замещен одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген, С(O)ОН, C(O)ONa, и фенил; незамещенный С 3-С 12 циклоалкил, в частности, С 6 Н 11; С 3-С 12 циклоалкил, который замещен одним или несколькими ОН; незамещенный С 6-С 10 арил, в частностиC6H5 или С 10 Н 7; С 6-С 10 арил, который замещен одним или несколькими заместителями, выбранными из группы, включающей галоген,-С(O)ОН, C(O)ONa, С 1-С 6aлкил, С 1-С 6 алкокси,фенил, -SO3H, SO3Nа, ОSО 3Nа, NHSO3Na, нитро и циано, в частности, C6H4Cl, С 6 Н 4(3,4)Сl2,С 6 Н 4 СООNа, С 6H4CН 3, С 6 Н 4SO3Nа или C6H4CN; или незамещенный С 7-С 16 аралкил с С 1-С 6 алкилом и С 6-С 10 арилом, в частности, (СН 2)2 С 6 Н 5; aR9 представляет водород, С 1-С 4 алкил, фенилСН 2-, фенил-СН 2 СН 2, фенил-(СH2)3- или фенилСН=СН-СН 2; а n равно 2 или 1, предпочтительно 1. Особенно предпочтительными являются соединения, в которых R4 в формуле III представляет амид R8C(O)N(R9)(CH2)n-, где R8 представляет незамещенный или замещенный С 1 С 12 алкил, циклогексил, нафтил, бифенил, фенил,бензил, фенилэтил или дифенилметил, а R9 представляет С 1-С 4 алкил, фенил-С 1-С 6 алкил, в 26 частности, СН 2 С 6 Н 5, (СН 2)2 С 6 Н 5 или (CH2)3C6H5; или фенил-С 2-С 6-алкенил, в частности, C6H5CH=CH-CH2; и n=2, а предпочтительно 1. Особенно предпочтительными являются соединения, в которых R4 в формуле III представляет амид R8C(O)N(R9)(CH2)n-, где R8 представляет С 1-С 12 алкил, который является незамещенным или замещенным одним или несколькими атомами галогена (например, Сl, а особено F), в частности, СF3; или С 6-С 10 арил, особенно фенил или нафтил, который замещен одним или несколькими заместителями, такими как С 1-С 4 алкил (например, метил или этил), С 1-С 4 алкокси (например,метокси или этокси), галоген, -CN или NO2; a R9 представляет водород или изобутил; и n=2, а предпочтительно 1. Еще более предпочтительными являются соединения, в которых R4 в формуле III представляет амид R8 С(O)N(R9)(СН 2)n-, где R8 представляет С 1-С 12 алкил или С 6-С 10 арил, особенно С 1-С 6 алкил, который незамещен или замещен галогеном, -CN, -NO2, С 1-С 4 алкилом или С 1 С 4 алкокси, или С 5- или С 6 циклоалкил, С 6 С 10 арил, такой как фенил или нафтил, или С 7 С 12 аралкил, такой как бензил, фенилэтил, фенилпропил или фенилпропенил; и n = 2, а предпочтительно 1. Кроме того, особенно предпочтительными являются соединения, в которых R4 в формуле II представляет аминоалкил, предпочтительноR8'R9'N(CH2)n-, где R8' и R9' независимо друг от друга представляют водород; незамещенный C1 С 12 алкил; С 1-С 12 алкил, который замещен одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген, C(O)ORs1,C(O)ORs4, C(O)-NR11R12, С 1-С 12 алкил, С 1 С 6 алкокси, С 6-С 10 арил, -SO3 Н, SO3Na, ОSО 3Nа,NR20SО 3Nа, нитро, амино и циано; незамещенный С 3-С 12 циклоалкил; С 3-С 12 циклоалкил, который замещен одним или несколькими ОН; С 6 С 10 арил; С 7-С 16 аралкил с С 1-С 6 алкилом и С 6 С 10 арилом; или C8-С 16 аралкенил с С 2 С 6 алкенилом и С 6-С 10 арилом, где арил и арил в аралкиле и аралкениле являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген, C(O)ORs1, С(O)ОRs4,C(O)ONa, -C(O)OK, -C(O)-NR11R12, С 1-С 12 алкил,С 1-С 6 алкокси, С 6-С 10 арил, -SO3 Н, SO3Na,OSO3Na, NR20SO3Na, нитро, амино и циано; гдеn=2, а предпочтительно 1; Rs1 представляет водород, К или Na, С 1-С 12 алкил, С 2-С 12 алкенил,С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6 С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или С 6 С 10 гетероаралкил, Rs4 представляет водород, С 1 С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 2 С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или С 6-С 10 гетероаралкил; R11 представляет Н, С 1-С 4 алкил, С 2-С 4 гидроксиалкил, фенил или бензил; R12 независимо от R11 имеет те же значения, либо R11 и R12, взятыеIII представляет аминоалкил R8'R9'NCH2-, где R8' и R9' независимо друг от друга представляют водород; С 1-С 8 алкил, циклопентил, циклогексил, С 5-или С 6-циклоалкилметил, фенил-С 1-С 4 алкил, в частности, -СН 2 С 6 Н 5-, или фенил-С 2-С 4 алкенил, в частности, -СН 2 СН=СНС 6 Н 5. Кроме того, особенно предпочтительными являются соединения, в которых R4 в формулеIII представляет аминоалкил R8'R9'NCH2-, где R8' и R9' независимо друг от друга представляют водород; С 1-С 6 алкил, фенил-C1-, или С 2-алкил, в частности, СН 2 С 6 Н 5. Предпочтительными соединениями группы (b) являются соединения, в которых R4 представляет С 7-С 11 аралкил, в частности, СН 2-С 6 Н 5 и (СН 2)2-С 6 Н 5-, С 3-С 12 циклоалкил или С 1-С 12 алкил, который является незамещенным или замещенным одним или несколькими заместителями, выбранными из группы, включающейNH2, С 3-С 12 циклоалкил, первичный амино, вторичный амино, сульфонамид, карбамид и аминокарбониламино. Особенно предпочтительными заместителями для С 1-С 12 алкила являютсяR8 и R9 независимо друг от друга представляют водород, С 1-С 12 алкил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил,С 7-С 11 аралкил или С 6-С 10 гетероарил, a R8' и R9' независимо друг от друга представляют водород, ОН, С 1-С 12 алкил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил,С 7-С 11 аралкил или С 6-С 10 гетероалкил, которые являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, галоген,C(O)ORs1, OC(O)Rs4, C(O)Rs2, нитро, NH2, циано, SО 3 Му, ОSО 3 Му, NR20SО 3 Му, С 1-С 12 алкил,С 2-С 12 алкенил, С 1-С 12 алкокси, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил,С 6-С 10 арилокси, С 5-С 9 гетероарил, С 5-С 9 гетероарилокси, С 7-С 11 аралкил, С 7-С 11 аралкилокси, С 6 С 10 гетероаралкил, С 8-С 11 аралкенил, C7-С 10 гетероаралкенил, первичный амино, вторичный амино, сульфонил, сульфонамид, карбамид,карбамат, сульфонгидразид, карбгидразид, карбогидроксамовую кислоту и аминокарбониламид, где Rs1 представляет водород, My, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил, С 6-С 10 арил, С 5-С 9 гетероарил,С 7-С 11 аралкил или C6-С 10 гетероаралкил; Rs4 28 представляет водород, С 1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 2-С 11 гетероциклоалкил,С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11 аралкил или С 6-С 10 гетероаралкил; Rs2 и R20 представляют водород, C1-С 12 алкил, С 2-С 12 алкенил, С 3-С 12 циклоалкил, С 3-С 12 циклоалкенил, С 2-С 11 гетероциклоалкил, С 2-С 11 гетероциклоалкенил, С 6-С 10 арил, С 5-С 9 гетероарил, С 7-С 11aралкил, С 6-С 10 гетероаралкил, С 8-С 11 аралкенил или С 7-С 10 гетероаралкенил; причем алкил, алкенил, алкокси,циклоалкил, циклоалкенил, гетероциклоалкил,гетероциклоалкенил, арил, арилокси, гетероарил, гетероарилокси, аралкил, аралкокси, гетероаралкил, аралкенил и гетероаралкенил, в свою очередь, являются незамещенными или замещенными одним из вышеуказанных заместителей; у=1; а М обозначает одновалентный металл; либо у=1/2, а М обозначает двухвалентный металл; либо R8' и R9' вместе представляют тетраметилен, пентаметилен, -(CH2)2-O-(CH2)2-,-(CH2)2-S-(CH2)2- или -(CH2)2-NR7-(CH2)2-, a R7 представляет Н, С 1-С 6 алкил, С 7-С 11 аралкил,C(O)Rs2 или сульфонил. Особенно предпочтительными соединениями этой группы являются соединения, в которых R4 представляет -СH2-С 6 Н 5, -(CH2)2-C6H5,циклогексил, метил, этил или изопропил, которые являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей NH2, циклогексил, С 6-С 10 арил, R8C(O)N(R9)-, R8S(O)2N(R9)-,R8NHC(O)N(R9)- и R8'R9'N-, где R8, R9, R8' и R9' независимо друг от друга представляют водород, С 1-С 12 алкил, С 3-С 12 циклоалкил, С 6-С 10 арил или С 7-С 11 аралкил, которые являются незамещенными или замещенными заместителями,выбранными из группы, включающей ОН, галоген, С(О)ОМy, нитро, циано, SО 3 Мy, ОSО 3 Мy,NR20SO3 Мy, С 1-С 12 алкил, С 1-С 12 алкокси и С 6 С 10 арил, где у=1, а М обозначает одновалентный металл, либо у=1/2, а М обозначает двухвалентный металл. Особенно предпочтительными являются соединения, в которых R8, R9, R8' и R9' независимо друг от друга представляют водород, С 1-С 12 алкил, циклогексил, фенил, нафтил или С 7-С 11 аралкил, которые являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, F, Cl, C(O)ONa, нитро, циано, SO3Nа, С 1-С 6 алкил, метокси и фенил. В предпочтительной группе соединений формулы I, R1 представляет группу формулы III,где R4 представляет С 6 Н 11, СН(СН 3)2, СН 2 СН 2NНС(O)-фенил,фенил,(СН 2)2-фенил,СН 2NНС(O)(СH2)3-фенил,СН 2NНС(O)(СH2)3 ОН,СН 2NНС(O)СF3,СН 2NНС(O)С 6 Н 11,СН 2NНС(O)С 11 Н 23,СН 2NНС(O)CH(C6H5)2,СН 2NНС(O)NHC6H5,СН 2NНС(O)C2H4CO2Na,СН 2NНС(O)С 6[(1,3,4,5)ОН]4 Н 7,СН 2NНС(O)C6H4-p-SO3Na, СН 2NНС(O)С 6 Н 4 Сl,СН 2NНС(O)C6H4NO2,СН 2NНС(O)C6H4OCH3, 29 СН 2NНС(O)С 6 Н 4(3,4)Сl2, СН 2NНС(O)С 6H4 СН 3,СН 2NНС(O)С 6 Н 4 СN,СН 2NНС(O)С 6 Н 4 С 6 Н 5,СН 2NНС(O)C10H7,СН 2NНС(O)С 6 Н 4 СООNа,СН 2NНС(O)(CHOH)2COONa,CH2N(CH2CH=СН-фенил)[С(О)-фенил],СН 2N[СН 2 СН(СН 3)2][С(O)-фенил],CH2N[C(O)C6H5]CH2C6H5,(СН 2)С 6 Н 11,CH2N-[С(O)С 6 Н 5](СН 2)3 С 6 Н 5,(CH2)2 С 6 Н 11,CH2NH2,CH2NHCH2CH=CHфeнил, CН 2NНСH2-фенил, СН 2NHСН 2 СН(СH3)2,CH2N(CH2-фeнил)2,СН 2N[СН 2 СН(СН 3)2]2,CH2NHSO2-п-нитpoфeнил, СН 2NНSO2-п-толил,CH2NHSO2CF3, CH2NHC(O)C6H5 или CH2N[SO2 п-нитрофенил][СН 2 СH(СH3)2]. Если R2 является алкилом, то он может содержать предпочтительно от 1 до 6 атомов углерода, а более предпочтительно от 1 до 4 атомов углерода. Особенно предпочтительными являются метил и этил. В случае, если заместителем для R2 является галоген, то им может быть предпочтительно F, Cl и Вr; в случае -С(O)Му, предпочтительным является -C(O)ONa или -С(O)ОК; в случае алкила, предпочтительным является C1-C6-, a особенно предпочтительно C1-C4-алкил, такой как метил, этил, н- или изопропил и н-, изо- или трет.-бутил; в случае алкокси, то предпочтительно C1-C4 алкокси, например, метокси и этокси; вслучае арила, предпочтительно фенил или нафтил; в случае -SО 3 Мy, предпочтительно-SO3Na или -SO3 К; в случае первичного амина,предпочтительно C1-C12 первичный амино, такой как метил-, этил-, н- или изопропил, н-, изо- или трет.-бутил, фенил, гексил, циклогексил, фенил или бензиламино; в случае вторичного амино,предпочтительно C2-C20 вторичный амино, такой как диметил-, диэтил-, метилэтил-, ди-н-пропил-,ди-изопропил-, ди-н-бутил-, дифенил-, дибензиламино, морфолино, тиоморфолино, пиперидино и пирролидино; -SO2-NR8R9; и C(O)-NR8R9,где R8 и R9, взятые вместе с атомом N, образуют морфолино, тиоморфолино, пирролидино или пиперидино. Если R8 и R9 представляют алкил, то этот алкил предпочтительно содержит 1-6, а особенно предпочтительно 1-4 атомов углерода, и может быть, например, метилом, этилом, н- или изопропилом, либо н-, изо- или трет.-бутилом. Если R8 и R9 представляют гидроксиалкил, то этот гидроксиалкил содержит предпочтительно 1-6, а особенно предпочтительно 1-4 атомов углерода, и может быть, например, гидроксиметилом или 2-гидроксиэтилом. Если R8 и R9 представляют циклоалкил, то таким циклоалкилом является предпочтительно циклопентил или циклогексил. Заместителями для R8 и R9, представляющих фенил и бензил, являются предпочтительно F, Cl, метил, этил, метокси и этокси. Предпочтительной подгруппой соединений формулы I являются соединения, в которых 30 в частности, метил или этил, или C1-C6 алкил,особенно предпочтительно C1-C4 алкил, в частности, метил или этил, который замещен С(O)ОН-, -C(O)ONa, -C(O)OK, -ОН, -C(O)NR8R9 или -SO2-NR8R9, где R8 представляет водород, C1-C4 алкил, C2-C4 гидроксиалкил, фенил или бензил, a R9 независимо имеет те же значения, что и R8; либо R8 и R9, взятые вместе, представляют тетраметилен, пентаметилен или-СН 2 СН 2-О-СН 2 СН 2-. Особенно предпочтительными являются соединения, в которых R2 представляет водород, метил, этил, НО(O)ССН 2 СН 2-,NaOC(O)CH2CH2-, R8R9NC(O)CH2CH2-, a R8 иR9 независимо друг от друга представляют водород, C1-C6 алкил, C2-C4 гидроксиалкил, фенил,бензил, либо, взятые вместе, они представляют морфолино. Особенно предпочтительными являются соединения, в которых R8, R9, R8' и R9' независимо друг от друга представляют водород, C1C12 алкил, циклогексил, фенил, нафтил или C7C11 аралкил, которые являются незамещенными или замещенными одним или несколькими заместителями, выбранными из группы, включающей ОН, F, Cl, C(O)ONa, нитро, циано,SО 3Nа, C1-C5 алкил, метокси и фенил. Кроме того, настоящее изобретение относится к способу получения соединений формулы I, который предусматривает этерификацию группы 3-ОН в соединении формулы V где R2 и X имеют вышеуказанные значения, R12 представляет защитную группу, a R12' и R12" независимо друг от друга представляют водород или защитную группу, посредством реакции с соединением формулы VIR1 - R13 (VI) где R1 имеет вышеуказанные значения, а R13 является уходящей группой, и с последующим удалением защитных групп. Уходящими группами могут быть атомы галогена, такие как хлор, бром и йод, и остатки соответствующих сульфоновых кислот, например, трифторметансульфонат, алифатических,циклоалифатических или ароматических сульфоновых кислот, которые могут быть незамещенными или замещенными C1-C4 алкилом, C1C4 алкокси, нитро, циано или галогеном (хлором,бромом). Некоторыми примерами таких кислот могут служить метансульфоновая кислота, моно-, ди- или трифторметансульфоновая кислота,или п-нитробензолсульфоновая кислота. Особенно предпочтительно использовать CF3-SO2O- (также называемая трифлат). Уходящую группу предпочтительно выбирают из группы, 31 включающей галоген и незамещенный и галогенированный R-SO2-, где R представляет C1-C12 алкил, в частности, C1-C6 алкил, C5-C6 циклоалкил, фенил, бензил, C1-C12 алкилфенил, в частности, C1-C4 алкилфенил или C1-С 12 алкилбензил, в частности, C1-C4 алкилбензил, например, метан,этан, пропан, бутан, бензол, бензил и пметилбензилсульфонил. Предпочтительными уходящими группами являются Сl, Вr, I,-О-SО 2 СF3 (трифлат) и п-нитробензолсульфонил, при этом особенно предпочтительной уходящей группой является -OSO2 СF3. Некоторые соединения формулы VI являются известными, либо они могут быть получены известными способами, описанными Degerbeck et al. [Degerbeck F., Fransson В., Grehn L.,Ragnarsson U., J. Chem. Soc. Perkin Trans. 1: 1114 (1993)] и Dureault et al. [Durealt A.,Tranchepain I., Depezay J.C., Synthesis 491-493(1987)]. Оптически чистые соединения могут быть получены с использованием оптически чистых исходных соединений (например, аминокислот, -гидроксикислот), либо методами хроматографического разделения, например, с использованием хиральных твердых фаз. Соединения формулы V являются новыми соединениями, которые рассматриваются в настоящем изобретении. Они могут быть получены известными методами гликозилирования с использованием известных фукозильных и галактозильных доноров и диодов формулы НОХ-ОН. При этом предпочтительным является постадийное введение галактозы и фукозы или наоборот. Для получения соединений формулы V сначала синтезируют блоки псевдотрисахаридов. Синтез псевдотрисахаридов осуществляют либо путем гликозидного присоединения активированной и защищенной галактозы к полученному блоку фукоза-O-Х-ОН, или путем гликозидного присоединения соответствующим образом защищенной и активированной фукозы к полученному блоку галактоза-O-Х-ОН. Реакция гликозилирования является широко известной и описана в специальной литературе. В псевдотрисахарид может быть затем введена группа R1. После этого полученные соединения формулы I могут быть модифицированы. Такой модификацией может быть галогенирование ароматических соединений с образованием циклоалифатических групп, и в то же самое время, например, может быть осуществлено гидрогенолитическое удаление защитных групп. Кроме того, может быть осуществлено ацилирование и/или алкилирование и/или сульфирование аминогруппы. Получение вторичных и третичных аминов может быть осуществлено путем восстановительного аминирования. При этом предпочтительно, чтобы группа 3-ОН галактозного остатка была активирована путем этерификации. Для этой цели особенно подходящими являются оксиды диалкилолова, 001356 32 алкоксиды диалкилолова и оксиды бис(триалкил)олова. В качестве некоторых конкретных примеров могут служить оксид дибутилолова, дибутилолово(O-метил)2 и (трибутилолово)2 О. Активирующие агенты предпочтительно использовать в стехиометрических количествах. В этом случае реакцию осуществляют в две стадии, а именно, а) активация и b) реакция взаимодействия с соединениями формулы VI. Реакция активации может быть проведена при температурах 40-200 С, а предпочтительно при 60-120 С. Соединения формулы V и формулы VI могут быть использованы в эквимолярных количествах. Однако, было установлено, что соединение формулы VI целесообразно использовать в избыточных количествах, которое, например, до 10 раз, а предпочтительно 5 раз, превышают количество соединения формулы V. Кроме того, обе стадии реакции предпочтительно проводить в присутствии инертного растворителя или смеси растворителей. Реакционноспособные протонные растворители, такие как алканолы, а также амиды кислот являются неподходящими для использования в стадии b). Могут быть использованы неполярные апротонные и полярные апротонные или полярные протонные растворители. Указанными растворителями могут быть алифатические или ароматические углеводороды, такие как пентан, гексан, циклогексан, метилциклогексан, бензол,толуол или ксилол; галогенированные углеводороды, такие как метиленхлорид, хлороформ,тетрахлорметан, 1,2-дихлорэтан, 1,1,2-трихлорэтан, 1,1,2,2-тетрахлорэтан и хлорбензал; линейные или циклические простые эфиры, такие как диэтиловый эфир, диметиловый или диэтиловый эфир этиленгликоля, тетрагидрофуран и диоксан; N,N-диалкилированные карбоксамиды,такие как диметилформамид, N-алкилированные лактамы, такие как N-метилпирролидон; кетоны, такие как ацетон и метилизобутилкетон; сложные эфиры карбоновых кислот, такие как метил- или этилацетат; или алканолы, такие как метанол, этанол, пропанол, бутанол и моноэтиловый простой эфир этиленгликоля. Особенно предпочтительными растворителями являются метанол, этанол, бензол и толуол. Защитные группы и методы, используемые для дериватизации гидроксильных групп, в основном, известны специалистам в области химии cахаров и нуклеотидов и описаны, например, Beaucage S.L., Lyer R., Tetrahedron 48: 2223-2311 (1992). Примерами таких защитных групп являются бензил, метилбензил, диметилбензил, метоксибензил, диметоксибензил, бромбензил, 2,4-дихлорбензил; дифенилметил, ди(метилфенил)метил, ди(диметилфенил)метил,ди(метоксифенил)метил, ди(диметоксифенил) метил, трифенилметил, трис-4,4',4"-трет.-бутилфенилметил, ди-п-анизилфенилметил, три(ме 33 тилфенил)метил, три(диметилфенил)метил, метоксифенил(дифенил)метил, ди(метоксифенил) фенилметил, три(метоксифенил)метил, три(диметоксифенил)метил; трифенилсилил, алкилдифенилсилил, диалкилфенилсилил и триалкилсилил с 1-20, предпочтительно 1-12, а особенно предпочтительно 1-8, атомами углерода в алкильных группах, например, триэтилсилил, трин-пропилсилил, изопропилдиметилсилил, трет.бутилдиметилсилил, трет.-бутилдифенилсилил,н-октилдиметилсилил (1,1,2,2-тетраметилэтил) диметилсилил; C2-C12-, особенно C2-C6 ацил,такой как ацетил, пропаноил, бутаноил, пентаноил, гексаноил, бензоил, метилбензоил, метоксибензоил, хлорбензоил и бромбензоил. Защитные группы могут быть одинаковыми или различными. Предпочтительные защитные группы выбирают из группы, включающей линейный и разветвленный C1-C8 алкил, в частности, C1-C4 алкил, например, метил, этил, н- и изопропил,н-, изо- и трет.-бутил;C7-C12 аралкил, например, бензил; триалкилсилил с 3-20 атомами углерода, в частности,с 3-12 атомами углерода, например, триэтилсилил, три-н-пропилсилил, триизопропилсилил,изопропилдиметилсилил, трет.-бутил -диметилсилил, трет.-бутилдифенилсилил, н-октилдиметилсилил (1,1,2,2-тетраметилэтил)диметилсилил; замещенные метилиденовые группы,которые могут быть получены путем образования ацеталя или кеталя из смежных гидроксильных групп cахаров или производных cахаров посредством их взаимодействия с альдегидами и кетонами, которые предпочтительно содержат 2-12 или 3-12 атомов углерода, например, C1C12 алкилиден,предпочтительноC1C6 алкилиден, в частности, C1-C4 алкилиден, такой как этилиден, 1,1- и 2,2-пропилиден, 1,1- и 2,2-бутилиден, бензилиден; незамещенный и галогенированный C2-C12 ацил, в частности, C2C8 ацил, такой как ацетил, пропаноил, бутаноил,пентаноил, гексаноил, пивалоил и бензоил. Синтез предпочтительно осуществляют с использованием защитных групп для R12' и R12",которые вместе образуют алкилиденовую группу, предпочтительно с 1-12, а более предпочтительно с 1-8 атомами углерода. При этом особенно предпочтительными защитными группами являются такие группы, при которых R12' иR12", взятые вместе, представляют алкилиденовую группу, в частности, с 1-12 атомами углерода, где алкилиденовая группа образует ацеталь или кеталь с атомами кислорода. Эти защитные группы могут быть элиминированы в нейтральных или слабокислых условиях. Особенно подходящими защитными группами являются ацил, бензил, замещенный бензил, бензилоксиметил, алкил и силил. Особенно предпочтительно, если R12' и R12", взятые вместе,представляют алкилиден, например, алкил- или алкокси-замещенный бензилиден. Однако R12' иR12" могут быть также водородом, либо одна изR12' и R12" может быть защитной группой, такой как бензил, а другая может быть водородом. Примерами защитных карбоксилатных групп являются алкокси- и аралкоксикарбонильные группы, предпочтительно -СО 2 Вn,-СО 2 СН 3. Реакцию элиминирования защитных групп предпочтительно осуществляют при температуре от 0 до 50 С, а в частности, при комнатной температуре. Получение соединений формулы I более подробно описано в примерах. Альтернативный способ синтеза предусматривает гликозидное связывание защищенного гидроксиэфира фукозы формулы VII где R2 и Х являются такими, как они были определены выше, a R12 является защитной группой,путем реакции с защищенной галактозой формулы VIII где R1 и R12 являются такими, как они были определены выше, Z представляет О или S, a R является уходящей группой, с последующим удалением защитных групп из полученного соединения. Реакционные условия могут быть аналогичны условиям, используемым для осуществления способа, описанного выше. Уходящей группой R может быть, например, -С(=NН)-ССl3 или 4-пентенил. Соединения формулы VII могут быть получены просто путем гликозидного связывания соответствующим образом защищенной фукозы с соединением формулы НО-Х-ОН,которое может быть монозащищенным, если это необходимо. Соединения формулы VIII могут быть получены путем этерификации соединений формулы R1OH галактозой, которая может быть защищена, если это необходимо. Соединения настоящего изобретения обладают противовоспалительными свойствами, а поэтому могут быть использованы в качестве лекарственных средств. В частности, они могут применяться для лечения таких заболеваний,как кардиогенный шок, инфаркт миокарда,тромбоз, ревматизм, псориаз, дерматиты, острый респираторный дистресс-синдром и рак с метастазами. Кроме того, настоящее изобретение относится к соединениям, описанным в настоящем изобретении и предназначенным для использования в терапевтическом методе для лечения заболеваний теплокровных животных,включая человека. Доза введения такого соеди 35 нения теплокровному животному весом примерно 70 кг может составлять, например, 0,011000 мг в день. Соединения настоящего изобретения предпочтительно вводить парентерально,например, внутривенно или внутрибрюшинно, в форме фармацевтических композиций. Кроме того, настоящее изобретение относится к фармацевтической композиции, содержащей эффективное количество соединения настоящего изобретения, взятого отдельно или в сочетании с другими активными веществами,фармацевтический носитель, предпочтительно в значимых количествах, и, если необходимо,фармацевтические добавки. Фармакологически активные соединения настоящего изобретения могут быть использованы в форме композиций, которые могут быть введены парентерально или в виде растворов для вливания. Такими растворами являются предпочтительно изотонические водные растворы или суспензии, которые могут быть приготовлены непосредственно перед использованием, например, из лиофилизованных композиций,содержащих активное соединение, взятое отдельно или вместе с носителем, например, маннитом. Фармацевтические композиции могут быть стерилизованы и/или содержать добавки,например, консерванты, стабилизаторы, смачивающие агенты и/или эмульгаторы, стабилизаторы, соли для регуляции осмотического давления и/или буферы. Фармацевтические композиции, которые, если это необходимо, могут содержать другие фармакологически активные вещества, такие как антибиотики, могут быть приготовлены способами, известными per se,например, путем обычного растворения или лиофилизации и могут содержать около 0,190%, в частности, от около 0,5% до около 30%,например, 1-5% активного вещества (активных веществ). Настоящее изобретение проиллюстрировано в нижеследующих примерах. В этих примерах были использованы следующие сокращения и обозначения:Bz - бензоил; Вn - бензил; DMTST - трифлат диметил(метилтио)сульфония; FAB - массспектроскопия путем бомбардировки быстрыми атомами; OTf -трифлат; Ph - фенил; SE - C2H2S;HRP - пероксидаза хрена; BSA - альбумин коровьей сыворотки; РАА - полиакриламид; SA стрептавидин. Несвязанная связь в формулах означает метил. Перед использованием молекулярные сита активировали при 300 С в условиях высокого вакуума в течение 12 ч. Эти сита были использованы в порошкообразной форме. А: Получение исходных соединений. Пример А 1: Получение соединенияА 1 Бензилхлорид (660 мл, 5,72 ммоль) добавляли при комнатной температуре к смеси R-3 азидо-2-гидроксипропионовой кислоты 28[Dureault A., Tranchepain I., Depezay H.C., Synthesis 491-493 (1987)], триэтиламина (850 мл, 6,1 ммоль) и ДМФ (7,0 мл). Смесь размешивали в течение 16 ч, а затем добавляли еще 850 мкл(6,1 ммоль) триэтиламина и 660 мкл (5,72 ммоль) бензилхлорида. Реакционную смесь размешивали в течение 2 дней, а затем концентрировали в высоком вакууме. Остаток растворяли в воде и смесь несколько раз экстрагировали этилацетатом. Объединенные органические фазы промывали насыщенным раствором NaCl,осушали (Nа 2SO4), фильтровали и концентрировали в вакууме. Неочищенный продукт (1 г) очищали с помощью флеш-хроматографии на силикагеле (этилацетат/гексан = 1:4), в результате чего получали бензил-R-3-азидо-2 гидроксипропионат 29 (0,717 г, 85%) в виде маслообразного продукта. 1 Н-ЯМР (250 МГц,CDCl3)7,36 (м, 5 Н), 5,25 (с, 2 Н), 4,39 (кв, J=4,2 Гц, 1 Н), 3,65 (дд, J=3,3, 12,9 Гц, 1 Н), 3,51 (дд,J=4,3, 12,9 Гц, 1 Н), 3,20 (д, J=4,0 Гц, 1 Н).-20 С к раствору спирта 29 (0,85 г, 3,84 ммоль) и 2,6-ди-трет.-бутилпиридина (1,12 мл, 4,99 ммоль) в безводном CH2Cl2 (11,0 мл). Бесцветный прозрачный раствор нагревали до 0 С в течение 40 мин и перемешивали при этой температуре еще 2 ч. Полученную смесь разбавляли СН 2 Сl2 (40 мл) и при интенсивном перемешивании добавляли 1 М водный раствор KH2PO4 (30 мл). Органическую фазу отделяли, а водную фазу дважды экстрагировали метиленхлоридом. Объединенные органические фазы промывали водой (30 мл), осушали (Na2SO4), фильтровали и концентрировали в вакууме. Маслянистый остаток (2,3 г) очищали с помощью флешхроматографии на короткой колонке с силикагелем (этилацетат/гексан = 1:7), в результате чего получали бензил-R-азидо-2-трифторметансульфонилоксипропионат А 1 (1,16 г, 85%) в виде желтоватого маслообразного вещества. 1 НЯМР (250 МГц, CDCl3)7,38 (шир.с., 5 Н), 5,32 Бензил (R)-4-фенил-2-трифторметансульфонилоксибутират (А 2). Раствор (R)-2-фенил-2-гидрокси-4-фенилмасляной кислоты 26 (0,2 г, 1,11 ммоль) в МеОН/Н 2 О (9:1, 1,3 мл) доводили до рН 8 путем добавления 20% раствора Cs2CO3. Полученный раствор концентрировали в вакууме и подвергали азеотропной перегонке сначала с этанолом, а затем с гексаном, после чего осушали в высоком вакууме для удаления остаточной воды. Остаток смешивали с N,N-диметилформамидом (1,3 мл) и бензилбромидом (132 мкл, 1,11 ммоль), и смесь перемешивали при комнатной температуре в течение 75 мин. Затем добавляли еще 20 мкл (0,168 ммоль) бензилбромида и полученную смесь размешивали еще 50 мин. Суспензию белого цвета разбавляли CH2Cl2 (5 мл), фильтровали через HyfloSuperCel и концентрировали в вакууме. Полученный продукт очищали с помощью флеш-хроматографии на силикагеле(элюент:этилацетат/гексан 4:1) и получали бензил (R)-2-гидрокси-2-фенилбутират 27 (0,21 г,70%). Этот продукт (0,3 г, 1,11 ммоль) растворяли в СН 2 Сl2 (4,5 мл), добавляли 2,6-ди-трет.бутилпиридин (323 мкл, 1,44 ммоль), и полученную смесь охлаждали до -20 С. Затем по каплям добавляли в течение 3 мин трифторметансульфоновый ангидрид (222 мкл, 1,27 ммоль), и раствор нагревали до 0 С в течение 45 мин. После выдерживания в течение 75 мин при 0 С смесь разбавляли CH2Cl2 (20 мл) и промывали 1-молярным водным раствором КН 2 РO4 (15 мл). Водную фазу экстрагировали СН 2 Сl2 (2 х 10 мл), а объединенные органические фазы промывали водой (10 мл), осушали (Na2SO4), фильтровали и концентрировали в вакууме. Остаток подвергали грубой очистке путем фильтрации на колонке с силикагелем(элюент:этилацетат/гексан 1:9), в результате чего получали сырой трифлат А 2 (0,311 г, 70%) в виде маслообразного продукта. Этот продукт непосредственно использовали в следующей стадии (получение В 1.18). 1 Н-ЯМР (250 МГц,CDCl3)7,50-7,17 (м, 10 Н), 5,31 (с, 2 Н), 5,28T.J.C., J. Med. Chem. 38: 1538-1546 (1995)] и акцептора 2 (3,44 г, 6,46 ммоль) осушали в течение 1 ч в условиях высокого вакуума. Затем в атмосфере азота добавляли активированные 4A молекулярные сита (20 г) и DMTST (4,17 г,16,14 ммоль), а затем CH2Cl2 (70 мл). Желтоватую суспензию осушали при комнатной температуре и через 3 ч добавляли 5 мл суспензии,состоящей из DMTST (5,84 г, 22,61 ммоль), 4 молекулярных сит (4,0 г) и СН 2 Сl2 (35 мл). Затем через 30, 45 и 90 мин, соответственно, добавляли 5-миллилитровые порции этой суспензии DMTST. Затем коричневую реакционную смесь перемешивали в течение 15 ч и фильтровали через HyfloSuperCel (фильтр), промывая СН 2 Сl2 (300 мл), фильтрат экстрагировали путем встряхивания сначала 10% водным раствором NаНСО 3, а затем насыщенным растворомNaCl, a органическую фазу осушали (Na2SO4),фильтровали и концентрировали в вакуумном роторном испарителе. Оставшуюся коричневую пену очищали двумя стадиями колоночной хроматографии на силикагеле (элюент для 1 стадии хроматогрфии: этилацетат/гексан = 1:4; элюент для 2 стадии хроматографии: этилацетат/толуол= 1:9), в результате чего получали чистый продукт 3 в виде бесцветного твердого вещества(4,28 г, 60%), который непосредственно использовали в последующей стадии. 39 Раствор тетрабензоата 3 (3,38 г, 3,04 ммоль) и метоксида натрия (0,165 г, 3,05 ммоль) в безводном метаноле (32 мл) перемешивали при комнатной температуре в течение 3 ч. Полученную смесь нейтрализовали путем добавления сильно кислотного ионообменника (Amberlyst 15), а затем фильтровали через Hyflo Super Cel, промывая СH2 Сl2. Фильтрат концентрировали в вакууме и остаточное желтое маслянистое вещество очищали с помощью флешхроматографии на силикагеле (элюент: СН 2 Сl2/ метанол = 19:1), в результате чего получали чистый тетрол 4 (1,95 г, 92%). Раствор тетрола 4 (1,0 г, 1,44 ммоль), диметилацеталя бензальдегида (430 мл, 2,86 ммоль) и камфорсульфоновой кислоты (0,1 г,0,43 ммоль) в ацетонитриле (20 мл) перемешивали при комнатной температуре. Через 4 ч добавляли еще 0,15 г (0,65 ммоль) камфорсульфоновой кислоты и полученную смесь перемешивали еще 6 ч при комнатной температуре, а затем нагревали при 35 С в течение 6 ч. После добавления еще 0,06 г (0,26 ммоль) камфорсульфоновой кислоты раствор перемешивали при комнатной температуре в течение 6 ч. Реакционную смесь фильтровали через Hyflo SuperCel, промывая при этом этилацетатом. Фильтрат экстрагировали путем встряхивания сначала насыщенным водным раствором NаНСО 3, а затем насыщенным раствором хлорида натрия,после чего органическую фазу осушали(Na2SO4), фильтровали и концентрировали в вакууме, в результате чего получали 1,5 г неочищенного продукта. Неочищенный продукт очищали с помощью флеш-хроматографии на силикагеле (CH2Cl2/MeOH = 39:1), в результате чего получали нужный бензилиденацеталь 5(0,475 г), и смесь менее полярных побочных продуктов (0,4 г). Последний продукт один раз обрабатывали в реакционных условиях, как описано выше, и очищали, в результате чего получали еще 0,08 г бензилиденацеталя 5. Полный выход соединения 5 составил 0,555 г (49%): 1 Н-ЯМР (500 МГц, CDCl3)7,53-7,51 (м, 2 Н),7,38-7,19 (м, 18 Н), 5,62 (с, 1 Н), 4,83 (д, J=3,8 Гц,1 Н), 4,77 (д, J=12,1 Гц, 1 Н), 4,71 (д, J=11,5 Гц,1 Н), 4,70 (м,1 Н), 4,66 (д, J=12,0 Гц, 1H), 4,62 (д,J=11,5 Гц, 1 Н), 4,51 (д, J=11,1 Гц, 1H), 4,36-4,31 Смесь диола 5 (0,098 г, 0,125 ммоль), оксида ди-н-бутилолова (0,062 г, 0,25 ммоль) и метанола (5 мл) нагревали с обратным холодильником в атмосфере аргона в течение 2 ч. Реакционную смесь концентрировали в вакууме и к остатку добавляли пентан, после чего снова концентрировали. После добавления сухого CsF(осушенного в условиях высокого вакуума при 300 С, 0,068 г, 0,45 ммоль) в атмосфере аргона,смесь снова осушали в условиях высокого вакуума (30 мин). После добавления безводного 1,2-диметоксиэтана (1,5 мл) к смеси добавляли раствор бензил-R-3-фенил-2-трифторметансульфонилоксипропионата [Degerbeck F., Fransson В., Grehn L., Ragnarsson U., J. Chem. Soc. PerkinTrans.1: 11-14 (1993)] (0,24 г, 0,62 ммоль) в сухом 1,2-диметоксиэтане (1,5 мл). Полученную смесь интенсивно перемешивали при комнатной температуре в течение 4 ч, а затем при температуре 40 С в течение 2 ч. После добавления 1 М водного раствора КН 2 РO4 смесь разбавляли водой и 3 раза экстрагировали этилацетатом. Объединенные органические фазы экстрагировали путем встряхивания сначала разбавленным водным раствором KF, а затем насыщенным раствором хлорида натрия. Органическую фазу осушали (Na2SO4), фильтровали и концентрировали в вакуумном роторном испарителе, в результате чего получали неочищенный продукт. Продукт очищали с помощью флеш-хроматографии на силикагеле (элюирование в градиенте этилацетата/толуола (1:4)100% этилацетата),в результате чего получали эфир 6 (0,045 г,35%) и менее полярный предшественник 5 41 Диоксан (2,5 мл), воду (1,2 мл) и ледяную уксусную кислоту (0,1 мл) добавляли к смеси Рd(ОН)2/С (катализатор Pearlman, 20% содержание Pd, 0,03 г) и защищенного соединения 6(0,03 г, 0,029 ммоль). Содержимое колбы откачивали и несколько раз продували аргоном. После продувки водородом черную реакционную смесь гидрировали при слегка пониженном давлении водорода при комнатной температуре в течение 13 ч, а затем фильтровали через целлюлозный фильтр (размер пор 45 мкм). Фильтрат концентрировали в вакууме и остаток растворяли в воде, а затем снова концентрировали несколько раз для удаления избытка уксусной кислоты. Раствор этого остатка в воде пропускали через ионообменную колонку Dowex 50 (формаNa+, диаметр колонки 0,9 см, длина 3,5 см),промывая при этом деионизированной водой. Прозрачный фильтрат концентрировали и очищали с помощью обращенно-фазовой хроматографии (силикагель RP18, диаметр колонки 1,4 см, длина 7,0 см, элюирование в градиенте 40% МеОН/Н 2 О - 45% МеОН/Н 2 О - 50% МеОН/Н 2 О),в результате чего получали целевую молекулу В 1.1 (0,015 г, 78%) в виде бесцветного твердого вещества: 1 Н-ЯМР (500 МГц, CDCl3)7,38-7,30 Смесь тетрола 4 (0,038 г, 0,055 ммоль) и оксида ди-н-бутилолова (0,029 г, 0,117 ммоль) в сухом метаноле (2,0 мл) нагревали с обратным холодильником в атмосфере аргона. Через 2,25 ч прозрачный бесцветный раствор концентрировали в вакууме, а остаток смешивали с бензолом и концентрировали несколько раз для удаления избытка метанола. После осушки в течение 30 мин в условиях высокого вакуума остаток смешивали в атмосфере аргона с CsF (осушенном в высоком вакууме при 300 С, 0,03 г,0,197 ммоль) и безводным 1,2-диметокси 001356 42 этаном (0,4 мл). Смесь охлаждали до 0 С и с помощью шприца добавляли раствор бензил-R3-фенил-2-трифторметансульфонилоксипропионата [Degerbeck F., Fransson В., Grehn L., Ragnarsson U., J. Chem. Soc. Perkin Trans.1: 11-14(1993)] (0,085 г, 0,219 ммоль) в безводном 1,2 диметоксиэтане (0,4 мл). Затем реакционную смесь нагревали до комнатной температуры и перемешивали в течение 1 ч, после чего перемешивали при 40 С в течение 2 ч. После добавления 1 М водного раствора КН 2 РO4 смесь разбавляли водой и 3 раза экстрагировали CH2Cl2. Объединенные органические фазы промывали водным раствором KF, а затем осушали(Na2SO4), фильтровали и концентрировали в вакууме. Остаток очищали с помощью флешхроматографии на силикагеле в две стадии (первая стадия: 2% МеОН/СНСl3; вторая стадия: 45% этилацетат/толуол), в результате чего получали эфир 8 в виде маслообразного веществаPd), а затем добавляли ледяную уксусную кислоту (0,1 мл). Содержимое колбы откачивали и несколько раз продували аргоном. Эту процедуру повторяли с использованием водорода. Полученную смесь гидрировали при слегка повышенном давлении водорода и при энергичном перемешивании до тех пор, пока тонкослойная хроматография (силикагелевые пластины; нВuОH:Н 2 О: ацетон:ледяная уксусная кислота:NH4OH, 70:60: 50:18:1,5) не указывала на отсутствие предшественника и его промежуточных соединений (около 3,5 ч). Полученную черную суспензию дважды фильтровали через целлюлозный фильтр (размер пор 45 мкм), а затем фильтрат концентрировали в вакууме. Остаток растворяли в воде и раствор пропускали через ионообменную колонку (DOWEX 50, формаRP18, диаметр колонки 1,4 см, длина 7,0 см,элюирование в градиенте 40% МеОН/Н 2 О - 45% МеОН/Н 2 О - 50% МеОН/Н 2 О), в результате чего получали целевую молекулу В 1.1 (0,015 г, 78%) в виде бесцветного твердого продукта. Пример В 2. Получение соединенияВ 1.2. Ароматическое соединение В 1.1 (0,152 г,0,256 ммоль) и 5% Rh/Аl2 О 3 (0,2 г) растворяли в воде (5,5 мл), диоксане (3,5 мл) и уксусной кислоте (1,0 мл). Воздух заменяли путем многократного откачивания сначала на аргон, а затем на водород. Черную суспензию гидрировали при слегка повышенном давлении водорода при энергичном перемешивании в течение 2 дней, а затем фильтровали через целлюлозный фильтр(размер пор 45 мкм). Прозрачный бесцветный раствор концентрировали в вакууме, а остаток растворяли в воде и концентрировали несколько раз для удаления избытка уксусной кислоты. Раствор неочищенного продукта в воде фильтровали через ионообменную колонку Dowex 50(форма Na+, длина 9 см, диаметр 1,3 см), а затем колонку промывали водой. Фильтрат концентрировали в вакууме, а затем остаток (0,16 г) очищали путем гель-фильтрации на Bio-Gel P2(размер частиц 65 мкм, диаметр колонки 2,5 см,длина 100 см, элюент: вода; скорость потока 0,55 мл/мин.; детекция при 215 нм), после чего подвергали обращенно-фазовой хроматографииMeOH/H2O), в результате чего получали целевую молекулу В 1.2 (0,11 г, 73%) в виде белых твердых хлопьев (после лиофилизации). 1 НЯМР (500 МГц, D2O)4,93 (д, J=3,8 Гц, 1 Н),4,58 (кв, J=6,4 Гц, 1 Н), 4,43 (д, J=7,5 Гц, 1H),3,91 (дд, J=3,5, 9,0 Гц, 1 Н), 3,88-3,83 (м, 2 Н),3,75 (д, J=3,3 Гц, 1 Н), 3,73-3,64 (м, 4 Н), 3,573,53 (м, 1 Н), 3,49 (дд, J=7,3, 9,0 Гц, 1 Н), 3,503,43 (м, 1 Н), 3,33 (дд, J=3,2, 9,2 Гц, 1H), 2,101,99 (м, 2 Н), 1,73 (шир.д., J=12,0 Гц, 1 Н), 1,691,44 (м, 9 Н), 1,29-1,07 (м, 7 Н), 1,14 (д, J=6,5 Гц,3 Н), 0,96-0,80 (м, 2 Н); МС (FАВ, THG) 623 44 Суспензию, содержащую бензилиденацеталь 9 (0,5 г, 1,60 ммоль) (ЕР 671406), цианборогидрид натрия (0,9 г, 14,3 ммоль), активированные 4 молекулярные сита (1,0 г) и сухой тетрагидрофуран (30 мл), охлаждали до 0 С в атмосфере азота. рН смеси доводили до 1 путем осторожного добавления насыщенного раствора газообразного хлористого водорода в безводном диэтиловом эфире. Суспензию перемешивали при 0 С, а рН поддерживали при 1 путем осторожного добавления раствора НСl в эфире. Через 10 ч добавляли холодный насыщенный водный раствор бикарбоната натрия (30 мл). Органическую фазу отделяли, а водную фазу дважды экстрагировали этилацетатом (70 мл - каждый раз). Объединенные органические фазы осушали (Nа 2SO4), фильтровали и концентрировали в вакууме, в результате чего получали 1,3 г неочищенного продукта. Этот продукт очищали с помощью флеш-хроматографии на силикагеле(хлороформ/изопропанол = 19:1) и получали нужный 6-бензиловый эфир 10 (0,3 г, 60%) и некоторое количество менее полярного побочного продукта (0,045 г): 1 Н-ЯМР (250 МГц,CDCl3)7,47-7,33 (м, 5 Н), 4,64 (с, 2 Н), 4,37 (д,J=9,3 Гц, 1 Н), 4,13 (шир.д., J=3,0 Гц, 1 Н), 3,893,69 (м, 4 Н), 3,64 (дд, J=3,1, 9,0 Гц, 1H), 2,892,70 (м, 2 Н), 1,38 (т, J=7,3 Гц, 3 Н).(3,0 мл) при 0 С. Реакционную смесь перемешивали при 0 С в течение 3,5 ч, а затем добавляли 1 М водный раствор KH2PO4, и смесь 3 раза экстрагировали метиленхлоридом. Объединенные органические фазы промывали водой, осушали (Na2SO4), фильтровали и концентрировали в вакууме с получением 1,0 г неочищенного продукта. Продукт очищали с помощью флешхроматографии на силикагеле (гексан/ этилацетат = 4:1), в результате чего получали трибензоат 11 в виде желтоватых кристаллов (0,517 г,88%). 1 Н-ЯМР (250 МГц, CDCl3)8,09 (д, J=7,5 Гц, 2 Н), 8,02 (д, J=7,5 Гц, 2 Н), 7,85 (д, J=7,5 Гц,2 Н), 7,68 (т, J=7,4 Гц, 1 Н), 7,63-7,39 (м, 7 Н),7,38-7,23 (м, 6 Н), 6,06 (д, J=3,3 Гц, 1 Н), 5,85 (т,J=10,0 Гц, 1 Н), 5,66 (дд, J=3,5, 10,0 Гц, 1 Н), 4,88 45 Сухой метиленхлорид (CH2Cl2) (8,0 мл) добавляли к смеси тиогликозида 11 (0,377 г,0,60 ммоль), гликозильного акцептора 2 (0,32 г,0,60 ммоль) (ЕР 671409) и активированных 4 молекулярных сит (2,5 г) в атмосфере аргона. Во второй круглодонной колбе была получена суспензия из DMTST (0,39 г, 1,51 ммоль) и активированных 4 молекулярных сит (0,8 г) в безводном метиленхлориде (5,0 мл). Обе суспензии перемешивали при комнатной температуре в течение 3,5 ч. К смеси гликозильного донора/акцептора в течение 1 ч тремя порциями добавляли 1 мл суспензии DMTST. Желтоватую реакционную смесь перемешивали при комнатной температуре в течение еще 1,5 ч, а затем фильтровали через Hyflo Super Cel, промываяCH2Cl2. Фильтрат экстрагировали при встряхивании водным раствором NаНСО 3, а затем водой. Водные фазы снова экстрагировали СН 2 Сl2,а объединенные органические фазы осушали(Na2SO4), фильтровали и концентрировали в вакууме, в результате чего получали 0,67 г неочищенного продукта. Продукт очищали 2 раза с помощью флеш-хроматографии на силикагеле Раствор трибензоата 12 (3,42 г, 3,12 ммоль) и метоксида натрия (0,169 г, 3,12 ммоль) в метаноле (65 мл) перемешивали при комнатной температуре в течение 6 ч. Затем основание нейтрализовали путем добавления кислотного ионообменника (Amberlist 15) и суспензию фильтровали через Hyflo Super Cel. Затем фильтрат концентрировали в вакууме и остаточное желтое маслообразное веществo (3,35 г) очищали с помощью флеш-хроматографии на силикагеле(CH2Cl2/MeOH, 19:1), в результате чего получали триол 13 (2,15 г, 88%) в виде бесцветной пены: 1 Н-ЯМР (500 МГц, CDCl3)7,41-7,24 (м,20 Н), 4,99 (д, J=3,6 Гц, 1 Н), 4,95 (д, J=11,2 Гц,1H), 4,83 (д, J=11,2 Гц, 1 Н), 4,77 (д, J=11,3 Гц,1H), 4,69 (д, J=11,3 Гц, 1H), 4,68 (д, J=11,5 Гц,1H), 4,61 (д, J=11,5 Гц, 1H), 4,53 (с, 2 Н), 4,34 (д,J=7,0 Гц, 1H), 4,33 (м, 1H), 4,04 (дд, J=3,7, 10,1 Гц, 1H), 4,02 (м, 1H), 3,97 (дд, J=2,9, 10,0 Гц,1H), 3,81-3,77 (м, 1H), 3.77 (дд, J=6,0, 9,4 Гц,1H), 3,70 (дд, J=5,0, 9,6 Гц, 1H), 3,65 (д, J=2,0 Гц, 1H), 3,63-3,54 (м, 4 Н), 2,95 (шир.с, 1H), 2,60 Смесь триола 13 (0,515 г, 0,656 ммоль) и оксида ди-н-бутилолова (0,245 г, 0,984 ммоль) в безводном метаноле (15 мл) нагревали с обратным холодильником в атмосфере азота в течение 2 ч. Прозрачный раствор концентрировали в вакууме, растворяли в бензоле и 3 раза концентрировали для удаления избытка метанола. Остаток осушали в условиях высокого вакуума, а затем в атмосфере аргона добавляли безводныйCsF (осушенный в высоком вакууме при 300 С,0,5 г, 3,29 ммоль), после чего добавляли безводный 1,2-диметоксиэтан (4,0 мл) и раствор бензил-R-3-азидо-2-трифторметансульфонилоксипропионата А 1 (1,16 г, 3,28 ммоль) в безводном 1,2-диметоксиэтане (8,0 мл). Реакционную смесь перемешивали при комнатной температуре в течение 6 ч, а затем добавляли 1 М водный раствор КН 2 РО 4 (60 мл). Полученную смесь 3 раза экстрагировали этилацетатом, а объединенные органические фазы промывали сначала водным раствором бикарбоната натрия, а затем раствором хлорида натрия, после чего осушали(сначала элюировали продукт смесью толуола/этилацетата (4:1), а затем элюировали предшественник смесью CH2Cl2/MeOH, 19:1), в результате чего получали эфир 14 (0,488 г, 75%) в виде бесцветной пены и предшественник 13Pt/BaSO4 (0,35 г, содержание Pt: 5%) добавляли к раствору азида 14 (0,11 г, 0,111 ммоль) в этилацетате (12 мл). Содержимое колбы откачивали и несколько раз продували аргоном. После продувки колбы водородом смесь гидрировали при атмосферном давлении, интенсивно перемешивая при этом. Через 2,5 ч гидрирование прекращали и суспензию фильтровали через целлюлозный фильтр (размер пор 45 мкм), а затем фильтрат концентрировали в вакууме. Остаток (0,115 г) очищали с помощью флеш-хроматографии на силикагеле (элюент: СН 2 Сl2/МеОн = 19:1), в результате чего получали не только нужный амин 16 (0,055 г, 51%), но также и менее полярный предшественник 14(0,042 г, 38%). Полученный амин 16 является нестабильным и может быть использован непосредственно в последующих экспериментах.(i) Получение бензамидного промежуточного соединения 17. Диизопропилэтиламин (3,5 мл, 0,02 ммоль) и гексафторфосфат бензотриазол-1 илокситрипирролидинфосфония (РуВОР) (0,012 г, 0,0271 ммоль) добавляли при 0 С к раствору производного -аминокислоты 16 (0,013 г,0,0135 ммоль) и бензойной кислоты (0,0033 г,0,027 ммоль) в сухом ТГФ (0,5 мл). Реакционную смесь перемешивали в течение 45 мин, а затем добавляли насыщенный водный раствор бикарбоната натрия. Затем смесь 3 раза экстрагировали метиленхлоридом, а объединенные органические фазы промывали сначала 1 М водным раствором КН 2 РО 4 (рН доводили до 1-2 путем добавления 1 М водного НСl), а затем водным раствором NаНСО 3, после чего осушали(Na2SO4), фильтровали и концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии на силикагеле (элюирование в градиенте 35% этилацетата/толуола - 40% этилацетата/толуола), в результате чего получали бензамид 17 (0,0098 г, 68%).(ii) Деблокирование соединения 17. Диоксан (1,5 мл), воду (0,7 мл) и ледяную уксусную кислоту (0,1 мл) добавляли к смеси Рd(ОН)2/С (катализатор Pearlman, содержание(0,0097 г, 0,0091 ммоль). Колбу откачивали и несколько раз продували аргоном. Затем колбу продували водородом и черную смесь гидрировали при слегка повышенном давлении в течение 14 ч, интенсивно перемешивая при этом. Полученную смесь фильтровали через целлюлозный фильтр (размер пор 45 мкм) и фильтрат концентрировали в вакууме. Остаток растворяли в воде и несколько раз концентрировали для удаления избытка уксусной кислоты. Затем рас 001356 48 твор неочищенного продукта в небольшом количестве воды пропускали через ионообменную колонку (Dowex 50, форма Na+, диаметр колонки 0,9 см, длина 3,5 см), промывая деионизированной водой. После концентрирования фильтрата в вакууме остаток (0,007 г) очищали путем гель-фильтрации на Bio-Gel P2 (размер частиц 65 мкм, диаметр колонки 2,5 см, длина 35 см,элюент: вода; скорость потока 0,59 мл/мин, детекция при 230 нм), а затем подвергали обращенно-фазовой хроматографии (силикагельMerck RP18, элюирование в градиенте 37% МеОН/Н 2 О - 45% МеОН/Н 2 О), в результате чего получали целевую молекулу В 1.3 (3,3 мг, 58%) в виде белых твердых хлопьев (после лиофилизации). 1 Н-ЯМР (500 МГц, D2O)7,74 (д, J=7,5 Гц, 2 Н), 7,57 (т, J=7,2 Гц, 1 Н), 7,48 (т, J=7,6 Гц,2 Н), 4,92 (д, J=4,0 Гц, 1 Н), 4,57 (кв, J=6,7 Гц,1 Н), 4,44 (д, J=7,8 Гц, 1 Н), 4,17 (дд, J=3,9, 8,1 Гц, 1 Н), 3,94 (д, J=3,0 Гц, 1H), 3,86 (д, J=3,5 Гц,1 Н), 3,84 (т, J=4,0 Гц, 1 Н), 3,74 (д, J=3,5 Гц, 1 Н),3,75-3,65 (м,4 Н), 3,60-3,52 (м, 3 Н), 3,49-3,44(a) Получение амидного промежуточного соединения 19. Диизопропилкарбодиимид (20 мл, 0,129 ммоль) добавляли при комнатной температуре к раствору амина 16 (0,032 г, 0,033 ммоль), дигидрокоричной кислоты (0,015 г, 0,1 ммоль) и 1-гидроксибензотриазола (0,025 г,0,185 ммоль) в безводном ТГФ (1,0 мл). Реакционную смесь перемешивали в течение 30 мин, а затем концентрировали в вакууме. Остаток (0,09 г) очищали с помощью флеш-хроматогрфии на силикагеле в две стадии (элюент для первой стадии хроматографии: метиленхлорид/метанол= 39:1; элюент для второй стадии хроматографии: метиленхлорид/изопропанол = 39:1), в результате чего получали чистый амид 19 (0,031 г,86%).(b) Деблокирование 19. Диоксан (2,0 мл),воду (1,0 мл) и ледяную уксусную кислоту (0,5 мл) добавляли к смеси Pd(OH)2/C (катализаторPearlman, 20% содержание Pd, 0,035 г) и бензилового эфира 19 (0,031 г, 0,0283 ммоль). Колбу откачивали и несколько раз продували аргоном. Затем колбу продували водородом и черную смесь гидрировали при слегка повышенном давлении водорода в течение 18 ч при интенсивном перемешивании. Полученную смесь фильтровали через целлюлозный фильтр (размер пор 45 мкм), и фильтрат концентрировали в вакууме. Образовавшийся остаток смешивали с 49 толуолом (около 2 мл) и несколько раз концентрировали для удаления избыточного количества уксусной кислоты. Раствор неочищенного продукта (0,021 г) в небольшом количестве воды пропускали через ионообменную колонку(Dowex 50, форма Na +, диаметр колонки 0,9 см,длина 3,5 см), промывая деионизированной водой. После концентрирования фильтрата в вакууме остаток (0,02 г) очищали с помощью обращенно-фазовой хроматографии на силикагелеMerck RP18 (диаметр колонки 1,2 см, длина 6 см, элюент: 60% МеОН/Н 2 О), а затем подвергали гель-фильтрации на Bio-Gel P2 (размер частиц 65 мкм, диаметр колонки 2,5 см, длина 35 см, элюент: вода, скорость потока 0,5 мл/мин,детекция при 215 нм), в результате чего получали целевую молекулу В 1.4 (0,014 г, 74%) в виде бесцветных твердых хлопьев (после лиофилизации). 1 Н-ЯМР (500 МГц, D2 О)7,32 (м,2 Н), 7,24(а) Получение амидного промежуточного соединения 21. Диизопропилкарбодиимид (16 мл, 0,103 ммоль) добавляли при комнатной температуре,перемешивая, к раствору амина 16 (0,026 г,0,027 ммоль), 4-гидроксибутирата натрия (0,010 г, 0,079 ммоль) и 1-гидроксибензотриазола(1,0 мл) и ДМФ (0,2 мл). Через 4 ч добавляли еще 0,2 мл ДМФ (диметилформамида) и смесь перемешивали в течение 13 ч. После отгонки летучих веществ (включая ДМФ) в высоком вакууме остаток (0,09 г) очищали с помощью флеш-хроматографии на силикагеле (СН 2 Сl2/ МеОН = 29:1), в результате чего получали амид 21 (0,02 г, 71%).(b) Деблокирование 21. Диоксан (2,0 мл),воду (1,0 мл) и ледяную уксусную кислоту (0,5 мл) добавляли к смеси Рd(ОН)2/С (катализаторPearlman, содержание Pd 20%, 0,04 г) и бензилового эфира 21 (0,036 г, 0,034 ммоль). Содержимое колбы откачивали и несколько раз продували аргоном. Затем колбу продували водородом и черную смесь гидрировали при слегка повышенном давлении водорода в течение 18 ч, интенсивно перемешивая при этом. Полученную 50 смесь фильтровали через целлюлозный фильтр(около 2 мл) и несколько раз концентрировали для удаления избытка уксусной кислоты. Раствор неочищенного продукта (0,022 г) в небольшом количестве воды пропускали через ионообменную колонку (Dowex 50, форма Na+,диаметр колонки 0,9 см, длина 3,5 см), промывая при этом деионизированной водой. После концентрирования фильтрата в вакууме остаток(0,02 г) очищали с помощью гель-фильтрации на Bio-Gel P2 (размер частиц 65 мкм, диаметр колонки 2,5 см, длина 35 см, элюент: вода; скорость потока 0,5 мл/мин, детекция при 215 нм),а затем подвергали обращенно-фазовой хроматографии (силикагель Merck RP18, диаметр колонки 1,2 см, длина 6 см, элюент:МеОН/Н 2 О,1:4), в результате чего получали целевую молекулу В 1.5 (0,015 г, 70%) в виде бесцветных твердых хлопьев (после лиофилизации). 1HЯМР (500 МГц, D2O)4,93 (д, J=3,9 Гц, 1 Н),4,59 (кв, J=6,7 Гц, 1 Н), 4,47 (д, J=7,5 Гц, 1 Н),4,04 (дд, J=3,8, 7,3 Гц, 1 Н), 3,92 (д, J=3,2 Гц,1 Н), 3,86 (дд, J=3,4, 10,2 Гц, 1H), 3,75 (д, J=3,5 Гц, 1 Н), 3,74-3,65 (м,4 Н), 3,62 (дд, J=3,9, 14,0 Гц, 1H), 3,59-3,51 (м,2 Н), 3,55 (т, J=6,3 Гц, 2 Н),3,50-3,44 (м,1 Н), 3,43 (дд, J=3,5, 9,8 Гц, 1H), 3,38 Диоксан (2,0 мл), воду (1,0 мл) и ледяную уксусную кислоту (0,5 мл) добавляли к смесиPd(OH)2/C (катализатор Pearlman, 20% содержание Pd, 0,03 г) и азида 14 (0,03 г, 0,03 ммоль). Содержимое колбы откачивали и несколько раз продували аргоном. После продувки колбы водородом черную смесь гидрировали при слегка повышенном давлении водорода в течение 16 ч,интенсивно перемешивая при этом. Полученную смесь фильтровали через целлюлозный фильтр (размер пор 45 мкм) и фильтрат концентрировали в вакууме. Остаток очищали с помощью гель-фильтрации на Bio-Gel P2 (размер частиц 65 мкм, диаметр колонки 2,5 см, длина 35 см, элюент: вода; скорость потока 0,5 мл/мин, детекция при 215 нм), а затем подвергали обращенно-фазовой хроматографии (силикагель Merck RP18, диаметр колонки 1,2 см, длина 7 см, элюент: 25% МеОН/Н 2 О), и получали целевую молекулу В 1.6 (0,011 г, 70%) в виде бесцветного хлопьевидного твердого продукта (по 51 сле лиофилизации). 1 Н-ЯМР (500 МГц, D2O)4,93 (д, J=3,9 Гц, 1 Н), 4,58 (кв, J=6,7 Гц, 1H),4,48 (д, J=7,9 Гц, 1H), 4,22 (дд, J=3,7, 8,4 Гц,1 Н), 3,99 (д, J=3,1 Гц, 1H), 3,86 (дд, J=3,3, 9,9 Гц, 1H), 3,75 (д, J=3,3 Гц, 1H), 3,74-3,65 (м, 4 Н),3,61-3,55 (м, 2 Н), 3,50 (дд, J=3,0, 9,3 Гц, 1H),3,48 (м,1 Н), 3,35 (дд, J=3,7, 12,9 Гц, 1H), 3,16 Амин В 1.6 (0,09 г, 0,176 ммоль) растворяли в безводном метаноле (1,5 мл) и СН 2 Сl2 (1,8 мл), а затем добавляли активированные 3 молекулярные сита (около 0,2 г), циннамальдегид(24 мкл, 0,19 ммоль) и уксусную кислоту (9 мкл). Желтоватую суспензию перемешивали в течение 2 мин, а затем добавляли NaBH3(CN)(0,018 г, 0,286 ммоль). Через 1,5 ч смесь фильтровали через целлюлозный фильтр (размер пор 45 мкм), и фильтр промывали смесью метанола/метиленхлорида (1:1), а затем фильтрат концентрировали в вакууме. Стекловидный остаток растворяли в воде (5 мл), и раствор подкисляли(до рН примерно 1-2) 1 М соляной кислотой (0,7 мл). Мутный раствор снова фильтровали через целлюлозный фильтр (размер пор 45 мкм), а затем фильтрат доводили до рН = 7 путем добавления 1 М раствора гидроксида натрия (около 1 мл) и концентрировали. Остаток очищали с помощью гель-фильтрации на Bio-Gel P2 (размер частиц 65 мкм, диаметр колонки 2,5 см,длина 100 см, элюент:вода, скорость потока 0,6 мл/мин, детекция при 215 нм), а затем подвергали обращенно-фазовой хроматографии на силикагеле (силикагель Merck RP18, элюирование в градиенте 50% МеОН/Н 2 О - 70% MeOH/H2O), в результате чего получали целевую молекулу В 1.7 (0,003 г, 27%) в виде белых твердых хлопьев (после лиофилизации). 1 Н-ЯМР (500 МГц,D2O)7,48 (д, J=8,0 Гц, 2 Н), 7,41-7,31 (м, 3 Н),6,83 (д, J=15,4, 7,0 Гц, 1 Н), 6,26 (дт, J=15,4, 7,0 Гц, 1 Н), 4,92 (д, J=3,8 Гц, 1 Н), 4,56 (кв, J=6,3 Гц,1 Н), 4,43 (д, J=7,6 Гц, 1 Н), 4,31 (дд, J=3,5, 8,2 Гц, 1 Н), 3,98 (д, J=3,0 Гц, 1 Н), 3,88-3,81 (м, 2 Н),3,84 (д, J=6,0 Гц, 1 Н), 3,76-3,63 (м, 5 Н), 3,603,51 (м, 2 Н), 3,49 (дд, J=3,0, 10,4 Гц, 1 Н), 3,493,41 (м, 1 Н), 3,41 (дд, J=3,5, 13,2 Гц, 1 Н), 3,26 Раствор аминокислоты В 1.7 (0,01 г, 0,0159 ммоль) в 1 М водном растворе NaHCO3 (0,1 мл) охлаждали до 0 С, интенсивно перемешивая при этом, а затем добавляли 1 М раствор бензоилхлорида в бензоле (16,0 мкл). Через 40 мин добавляли 8,0 мкл раствора бензоилхлорида,через 130 мин добавляли еще 3,0 мкл, а через 3,5 ч еще 1,0 мкл. Через 4 ч реакционную смесь разводили водой и экстрагировали метиленхлоридом для удаления избытка реактива. Водную фазу концентрировали в вакууме, а остаток очищали с помощью гель-фильтрации на BioGel P2 (размер частиц 65 мкм, диаметр колонки 2,5 см, длина 35 см, элюент: вода; скорость потока 0,49 мл/мин, детекция при 215 нм), а затем подвергали обращенно-фазовой хроматографии(силикагель Merck RP18, элюирование в градиенте 60% МеОН/Н 2 О - 70% МеОН/Н 2 О), в результате чего получали целевую молекулу В 1.8(7,9 мг, 66%) в виде белых твердых хлопьев (после лиофилизации). 1 Н-ЯМР (500 МГц, D2O) : смесь (1,4:1) ротамеров, характерные сигналы: 7,52-7,24 (м, 10 Н, 2 хРh), 6,71 (д, J=15,5 Гц,0,42 Н, PhCH=CH), 6,42 (дт, J=15,5, 6,1 Гц,0,42 Н, PhCH=CH), 6,39 (д, J=15,5 Гц, 0,58H,PhCH=CH), 6,13 (дт, J=15,5, 5,6 Гц, 0,58H,PhCH=CH), 4,92 (д, J=4,0 Гц, 1H, Fuc-1H), 1,16 Метиленхлоридный раствор только что подвергнутого дистилляции бензальдегида(0,083 г в 1,0 мл СН 2 Сl2, 0,1 мл, 0,078 ммоль),активированные 3 молекулярные сита (0,1 г) и ледяную уксусную кислоту (5 мкл, 0,087 ммоль) добавляли к раствору аминокислоты В 1.6 (0,04 г, 0,078 ммоль) в МеОН/СН 2 Сl2 (1:1, 1,0 мл). Суспензию перемешивали при комнатной температуре и через 2 мин добавляли NaBH3(CN)(0,008 г, 0,129 ммоль). Через 2,5 ч добавляли еще 15 мкл раствора бензальдегида и смесь перемешивали в течение еще 1 ч. Реакционную смесь разбавляли водой, подкисляли разбавленной уксусной кислотой, фильтровали через целлюлозный фильтр (размер пор 45 мкм), а затем 53 фильтрат доводили до рН=8-9 путем добавления 1 М водного раствора бикарбоната натрия, после чего концентрировали. Остаток очищали с помощью гель-фильтрации на Bio-Gel P2 (размер частиц 65 мкм, диаметр колонки 2,5 см, длина 35 см, элюент; вода; скорость потока 0,5 мл/мин, детекция при 215 нм), а затем подвергали обращенно-фазовой хроматографии (силикагель Merck RP18, элюирование в градиенте 35% МеОН/Н 2 О - 60% МеОН/Н 2 О), в результате чего получали монобензиламин В 1.9 (0,020 г, 41%) и дибензиламин В 1.10 (0,005 г, 9%). Монобензиламин В 1.9: 1 Н-ЯМР (500 МГц, D2O)7,45 (с,5 Н), 4,93 (д, J=4,0 Гц, 1 Н), 4,57 (кв, J=6,7 Гц,1H), 4,45 (д, J=7,6 Гц, 1 Н), 4,33 (дд, J=3,8, 8,8 Гц, 1H), 4,28 (д, J=13,3 Гц, 1H), 4,24 (д, J=13,3 Гц, 1H), 3,99 (д, J=3,1 Гц, 1H), 3,85 (дд, J=3,5,10,2 Гц, 1H), 3,74-3,65 (м, 5 Н), 3,59-3,54 (м, 2 Н),3,49 (дд, J=3,2, 9,7 Гц, 1H), 3,48-3,44 (м, 1 Н),3,42 (дд, J=3,7, 13,2 Гц, 1H), 3,26 (дд, J=8,9, 13,2 Гц, 1H), 2,04 (м, 2 Н), 1,65 (шир.с, 2 Н), 1,28-1,14(м, 4 Н), 1,12 (д, J=6,7 Гц, 3 Н); МС (FAB, THG) 624 (M+Na), 602 (М+Н). Дибензиламин В 1.10: 1 Н-ЯМР (500 МГц,D2O) : сигналы 6 Нпо отношению к N являются очень широкими в условиях комнатной температуры (д 4,10-3,60, 4 Н и 3,12-2,67, 2 Н):7,38 (с,10 Н), 4,93 (д, J=4,0 Гц, 1 Н), 4,60 (кв,J=6,6 Гц, 1H), 4,43 (д, J=8,0 Гц, 1H), 4,23 (дд,J=3,6, 8,5 Гц, 1 Н), 3,88-3,83 (м, 2 Н), 3,75-3,63 (м,5 Н), 3,56 (дд, J=8,0, 9,3 Гц, 1H), 3,53-3,44 (м,2 Н), 3,32 (дд, J=3,0, 9,5 Гц, 1H), 2,13-1,98 (м,2 Н), 1,66 (шир.с, 2 Н), 1,31-1,10 (м, 4 Н), 1,14 (д,J=6,6 Гц, 3 Н); МС (FAB, THG) 714 (M+Na), 692 1 М метиленхлоридный раствор изобутиральдегида (0,156 мл), активированные 3 молекулярные сита (0,2 г) и ледяную уксусную кислоту (10 мкл, 0,17 ммоль) добавляли к раствору аминокислоты В 1.6 (0,08 г, 0,156 ммоль) в метаноле/метиленхлориде (1:1, 2,0 мл). Полученную суспензию перемешивали при комнатной температуре и через 1 мин добавлялиNaBH3(CN) (0,016 г, 0,258 ммоль). Через 60 мин реакционную смесь разбавляли водой и фильтровали через целлюлозный фильтр (размер пор 45 мкм), а затем фильтрат доводили до рН=8-9 путем добавления 1 М водного раствора бикарбоната натрия и концентрировали. Остаток очищали с помощью гель-фильтрации на BioGel P2 (размер частиц 65 мкм, диаметр колонки 2,5 см, длина 35 см, элюент: вода; скорость потока 0,5 мл/мин, детекция при 215 нм), а затем подвергали обращенно-фазовой хроматографии 1 М раствор бензоилхлорида в толуоле (41 мкл) добавляли при комнатной температуре к раствору аминокислоты В 1.11 (0,020 г, 0,0339 ммоль) в 1 М водном растворе NaHCO3 (100 мкл). Полученную смесь интенсивно перемешивали и через 1 ч добавляли дополнительное количество бензоилхлорида (41 мкл 1 М раствора). После завершения реакции летучие компоненты удаляли в высоком вакууме и остаток очищали с помощью гель-фильтрации на Bio-Gel P2 (размер частиц 65 мкм, диаметр колонки 2,5 см,длина 35 см, элюент: вода; скорость потока 0,5 мл/мин, детекция при 215 нм), а затем подвергали обращенно-фазовой хроматографии (силикагель Merck RP18, элюент: 45% метанол/вода),после чего лиофилизовали и получали бензамид В 1.13 в виде хлопьевидного порошка (0,014 г,59%). 1 Н-ЯМР (500 МГц, D2O), смесь ротамеров 1 М раствор пара-нитробензолсульфонилхлорида в толуоле (43 мкл) при интенсивном перемешивании добавляли к раствору аминокислоты В 1.6 (0,02 г, 0,039 ммоль) в 1 М водном растворе NаНСО 3 (0,2 мл). Реакционную смесь перемешивали при комнатной температуре в течение 16 ч, а затем концентрировали в вакууме. Остаток растворяли в воде (0,3 мл) и очищали с помощью гель-фильтрации на Bio-Gel P2(размер частиц 65 мкм, диаметр колонки 2,5 см,длина 35 см, элюент: вода; скорость потока 0,5 мл/мин, детекция при 215 нм). Затем 0,025 г неочищенного продукта очищали с помощью обращенно-фазовой хроматографии в две стадии (силикагель Merck RP18, элюент для 1 стадии хроматографии: 50% метанол/вода, элюент для 2 стадии хроматографии: 40% метанол/вода), после чего лиофилизовали и получали целевое соединение в виде хлопьевидного порошка (0,0105 г, 39%). 1 Н-ЯМР (400 МГц,D2O)8,39 (м, 2 Н), 8,07 (м, 2 Н), 4,93 (д, J=4,0 Гц, 1 Н), 4,56 (кв, J=6,6 Гц, 1H), 4,43 (д, J=7,9 Гц,1 Н), 3,96 (дд, J=3,5, 7,1 Гц, 1 Н), 3,88-3,83 (м,2 Н), 3,76-3,64 (м, 5 Н), 3,54-3,44 (м, 3 Н), 3,38 (дд,J=3,5, 13,7 Гц, 1H), 3,33 (дд, J=3,2, 9,6 Гц, 1H),3,19 (дд, J=7,3, 13,7 Гц, 1 Н), 2,05 (шир.т, J=13,4 Гц, 2 Н), 1,66 (шир.с, 2 Н), 1,30-1,12 (м, 4 Н), 1,14 1 М раствора п-толуолсульфонилхлорида в толуоле (22 мкл) при температуре 0 С и при интенсивном перемешивании добавляли к раствору аминокислоты В 1.6 (0,01 г, 0,02 ммоль) в 1 М водном растворе NaHCO3 (0,1 мл). Реакционную смесь перемешивали при температуре 0 С в течение 90 мин, после чего добавляли дополнительное количество п-толуолсульфо 001356 56 нилхлорида (10 мкл 1 М раствора). Затем реакционную смесь нагревали до комнатной температуры, перемешивали в течение 18 ч и концентрировали в вакууме. Остаток растворяли в воде и очищали посредством гель-фильтрации наBio-Gel Р 2 (размер частиц 65 мкм, диаметр колонки 2,5 см, длина 35 см, элюент: вода; скорость потока 0,5 мл/мин, детекция при 215 нм),а затем подвергали обращенно-фазовой хроматографии (силикагель Merck RP18, элюент: 45% МеОН/Н 2 О) и лиофилизовали, в результате чего получали целевое соединение в виде хлопьевидного порошка (0,004 г, 30%). 1 Н-ЯМР (400 МГц, D2O)7,69 (д, J=8,2 Гц, 2 Н), 7,37 (д, J=8,1 Гц, 2 Н), 4,88 (д, J=3,9 Гц, 1H), 4,52 (кв, J=6,6 Гц,1H), 4,35 (д, J=7,9 Гц, 1H), 3,85-3,78 (м, 2 Н), 3,74 Пентафторфенилтрифторацетат (4,5 мл,0,026 ммоль) добавляли при комнатной температуре, перемешивая, к раствору, содержащему производное изосерина 16 (0,025 г, 0,026 ммоль) и триэтиламин (0,7 мл, 0,005 ммоль) в ДМФ(100 мл). Через 15 мин добавляли еще 2,5 мл(0,015 ммоль) пентафторфенилтрифторацетaта,а через 30 мин добавляли еще 2,8 мл (0,02 ммоль) триэтиламина и 4,5 мл (0,026 ммоль) пентафторфенилтрифторацетата. Через 20 мин снова добавляли некоторое количество пентафторфенилтрифторацетата. Полученную смесь перемешивали в течение 45 мин, а затем добавляли 0,2 мл насыщенного водного раствораNаНСО 3 и смесь разбавляли водой и несколько раз экстрагировали этилацетатом. Объединенные органические фазы осушали (Na2SO4),фильтровали и концентрировали в вакууме. Неочищенный продукт (0,04 г) очищали с помощью флеш-хроматографии на силикагеле (элюент: этилацетат/толуол = 1:3) и получали трифторацетамид 24 (0,022 г, 83%). Деблокирование соединения 24. Диоксан(1,4 мл), воду (0,7 мл) и ледяную уксусную кислоту (0,35 мл) добавляли к смеси Pd(OH)2/C(катализатор Pearlman, 20% содержание Pd, 0,02 г) и бензилового эфира 24 (0,021 г, 0,021 ммоль). Содержимое колбы откачивали и несколько раз продували аргоном. После продувки водородом черную смесь гидрировали при слегка повышенном давлении в течение 3,5 ч. Реакционную смесь фильтровали через целлюлозный фильтр (размер пор 45 мкм) и фильтрат концентрировали в вакууме. Раствор остатка в 57 небольшом количестве воды пропускали через ионообменную колонку (Dowex 50, форма Na +,диаметр колонки 0,9 см, длина 3,5 см), промывая деионизированной водой. После концентрирования фильтрата в вакууме остаток очищали посредством гель-фильтрации на Bio-Gel P2- 40% МеОН/Н 2 О), в результате чего получали целевую молекулу В 1.16 (0,0085 г, 68%) в виде хлопьевидного твердого бесцветного вещества(а) Получение амида 26. Диизопропилкарбодиимид (17 мл, 0,11 ммоль) добавляли при комнатной температуре при перемешивании к смеси амина 16 (0,027 г, 0,028 ммоль), циклогексанкарбоновой кислоты (0,011 г, 0,086 ммоль), 1-гидроксибензотриазола (0,021 г, 0,155 ммоль) и безводного тетрагидрофурана (0,9 мл). После выдерживания в течение 20 мин добавляли безводный ДМФ (0,4 мл) и смесь перемешивали еще 1 ч. Реакционную смесь концентрировали в вакууме и оставшееся количество ДМФ удаляли в условиях высокого вакуума. Остаток очищали с помощью флеш-хроматографии на силикагеле (СН 2 Сl2/изопропанол = 39:1), в результате чего получали амид 26 (0,024 г, 80%).(b) Деблокирование соединения 26. Диоксан (2,0 мл), воду (1,0 мл) и ледяную уксусную кислоту (0,5 мл) добавляли к смеси Рd(OH)2/С(катализатор Pearlman, 20% содержание Pd, 0,03 г) и бензилового эфира 26 (0,024 г, 0,022 ммоль). Колбу откачивали, а затем несколько раз продували аргоном. После продувки водородом черную смесь гидрировали при слегка пониженном давлении в течение 18 ч. Реакционную смесь фильтровали через целлюлозный фильтр (размер пор 45 мкм) и фильтрат концентрировали в вакууме. Раствор остатка в небольшом количестве воды пропускали через ионообменную колонку (Dowex 50, форма Na+, диаметр колонки 0,9 см, длина 3,5 см), промывая 58 деионизированной водой. Фильтрат концентрировали в вакууме и остаток очищали посредством гель-фильтрации на Bio-Gel P2 (размер частиц 65 мкм, диаметр колонки 2,5 см, длина 35 см, элюент: вода; скорость потока 0,5 мл/мин,детекция при 215 нм), а затем подвергали обращенно-фазовой хроматографии (силикагельMerck RP18, диаметр колонки 1,2 см, длина 6 см, элюент: МеОН/Н 2 О = 3:2), в результате чего получали целевую молекулу В 1.17 (0,008 г,56%) в виде хлопьевидного бесцветного твердого продукта (после лиофилизации). 1 Н-ЯМР Раствор триола 13 (0,129 г, 0,17 ммоль) в безводном метаноле (4,0 мл) и оксиде ди-нбутилолова (0,064 г, 0,258 ммоль) кипятили с обратным холодильником в атмосфере аргона в течение 2 ч. Прозрачный раствор концентрировали в вакууме, а остаток смешивали с пентаном(2 мл), снова концентрировали, а затем осушали в условиях высокого вакуума в течение 30 мин для удаления остатков метанола. После этого остаток смешивали в атмосфере аргона с безводным CsF (0,131 г, 0,86 ммоль) и безводным 1,2-диметоксиэтаном (0,5 мл), а затем добавляли раствор бензил-(R)-4-фенил-2-трифторметансульфонилоксибутирата (А 2) (0,3 г, 0,861 ммоль) в безводном 1,2-диметоксиэтане (1,0 мл). Реакционную смесь перемешивали при комнатной температуре в течение 75 мин, а затем добавляли 1 М водный раствор КН 2 РO4, и смесь разбавляли водой и экстрагировали этилацетатом (разделение фазы осуществляли путем добавления небольшого количества водного раствора KF). Органические экстракты объединяли, осушали сульфатом натрия, фильтровали и концентрировали в вакууме, в результате чего получали неочищенный продукт в виде маслянистого вещества (39 г). Это вещество очищали с помощью флеш-хроматографии на силикагеле(элюент: толуол/этилацетат = 5:1) и получали чистый эфир 30 (0,143 г, 81%). 1 Н-ЯМР (250 МГц, CDCl3)7,35-7,05 (м, 30 Н), 5,13 (д, J=12,1 Гц, 1H), 5,03 (д, J=12,1 Гц, 1 Н), 4,88 (д, J=11,4 Бензиловый эфир 30 (0,14 г, 0,135 ммоль) растворяли в диоксане (4 мл) и воде (2 мл), а затем добавляли ледяную уксусную кислоту (1 мл) и 20% Рd(ОН)2/С (0,14 г). Воздух в реакционном сосуде сначала заменяли на аргон, а затем содержимое откачивали и несколько раз продували аргоном, после чего сосуд продували водородом. Черную реакционную смесь гидрировали при слегка повышенном давлении водорода в течение 90 мин, а затем фильтровали через целлюлозный фильтр (размер пор 45 мкм),промывая при этом водой. После концентрирования фильтрата остаток растворяли в толуоле и несколько раз концентрировали для удаления остатков уксусной кислоты. Неочищенный продукт (0,095 г) растворяли в небольшом количестве воды и фильтровали через ионообменную колонку Dowex 50 (Na+). Фильтрат осушали путем вымораживания, а затем остаток (0,085 г) очищали с помощью обращенно-фазовой хроматографии (силикагель Merck RP18, элюент: 40% МеОH/Н 2 О), а затем с помощью гельфильтрации на Bio-Gel P2 (размер частиц 65 мкм, диаметр колонки 2,5 см, длина 35 см, элюент: вода; скорость потока 0,5 мл/мин, детекция при 215 нм). После лиофилизации получали целевое соединения В 1.18 в виде хлопьевидного порошка (0,045 г, 55%). 1 Н-ЯМР (500 МГц, D2O)7,35-7,27 (м,4 Н), 7,22 (тт, J=1,5, 7,0 Гц, 1H),4,93 (д, J=4,0 Гц, 1 Н), 4,60 (кв, J=6,7 Гц, 1H),4,47 (д, J=7,8 Гц, 1H), 3,89-3,82 (м, 3 Н), 3,76 (д,J=3,5 Гц, 1H), 3,74-3,63 (м, 4 Н), 3,59-3,52 (м,2 Н), 3,51-3,45 (м, 1 Н), 3,37 (дд, J=3,5, 9,8 Гц,1H), 2,80-2,68 (м,2 Н), 2,12-1,99 (м,ЗН), 1,98-1,89 60 Ароматическое соединение В 1.18 (0,02 г,0,033 ммоль) растворяли в воде (1,8 мл) и диоксане (1,2 мл), а затем добавляли ледяную уксусную кислоту (0,3 мл) и 5% Rh/Аl2 О 3 (0,04 г). Воздух в реакционном сосуде заменяли на водород путем откачивания, а затем сосуд несколько раз продували водородом и смесь гидрировали при слегка повышенном давлении водорода в течение 1,5 дней, интенсивно перемешивая при этом. После фильтрования через целлюлозный фильтр (размер пор 45 мкм) и промывки водой фильтрат концентрировали, а остаток растворяли в толуоле и несколько раз концентрировали для удаления остатков уксусной кислоты. Неочищенный продукт очищали посредством гель-фильтрации на Bio-Gel P2(размер частиц 65 мкм, диаметр колонки 2,5 см,длина 35 см, элюент: вода; скорость потока 0,5 мл/мин, детекция при 215 нм), а затем снова гидрировали при аналогичных условиях в течение 2 дней. Реакционную смесь фильтровали через целлюлозный фильтр (размер пор 45 мкм) и промывали водой, а затем фильтрат концентрировали. Остаток растворяли в толуоле и несколько раз концентрировали. Неочищенный продукт очищали посредством гель-фильтрации на Bio-Gel P2 (размер частиц 65 мкм, диаметр колонки 2,5 см, длина 35 см, элюент: вода; скорость потока 0,5 мл/мин, детекция при 215 нм),а затем подвергали обращенно-фазовой хроматографии (силикагель Merck RP18, элюент: 50% МеОН/Н 2 О) и лиофилизовали, в результате чего получали целевое соединение В 1.19 в виде хлопьевидного порошка (0,01 г, 50%). 1 Н-ЯМР Раствор п-нитробензолсульфонилхлорида в толуоле (1 М 150 мкл) добавляли к раствору аминокислоты В 1.11 (0,0035 г, 0,0617 ммоль) в 1 М водном растворе NаНСО 3 (315 мкл). Полученную смесь интенсивно перемешивали при комнатной температуре и через 17 ч добавляли еще 120 мкл п-нитробензолсульфонилхлоридного раствора. Реакционную смесь перемешивали еще 24 ч, а затем разбавляли водой и дважды промывали этилацетатом. Водную фазу концентрировали в вакууме до объема 0,5 мл, и этот раствор очищали с помощью гельфильтрации на Bio-Gel P2 (размер частиц 65
МПК / Метки
МПК: A61P 7/02, C07H 15/207, A61K 31/70
Метки: lewis, сиалил, дигликозилированные, псевдосоединения, 2-диолы, сиалил-lewis
Код ссылки
<a href="https://eas.patents.su/30-1356-diglikozilirovannye-1-2-dioly-kak-psevdosoedineniya-sialil-lewis-x-i-sialil-lewis-a.html" rel="bookmark" title="База патентов Евразийского Союза">Дигликозилированные 1, 2-диолы как псевдосоединения сиалил- lewis x и сиалил-lewis a.</a>
Предыдущий патент: Способ диагностики энергетического состояния организма человека
Следующий патент: Производные 8-замещенного-1,3,8-триазаспиро [4.5]декан-4-она.
Случайный патент: Готовый к употреблению напиток зеленого чая и способ его получения





























