Двухканальное устройство для иммунологических анализов
Формула / Реферат
1. Устройство для тестов, предназначенное для определения наличия лиганда в жидкой пробе, содержащее:
a) первую полоску из сорбирующего материала, расположенную в первом местоположении, которая предназначена для приема раствора и определяет первый путь миграции;
b) вторую полоску из сорбирующего материала, иную, чем упомянутая первая полоска из сорбирующего материала, расположенную во втором местоположении, которая предназначена для приема жидкой пробы и определяет второй путь миграции, отличный от упомянутого первого пути миграции; и
c) участок проведения теста, расположенный по меньшей мере на или в одной из упомянутых полосок: упомянутой первой полоски из сорбирующего материала и упомянутой второй полоски из сорбирующего материала, причем упомянутая область проведения теста имеет иммобилизированное лигандсвязующее средство, а упомянутые первая и вторая полоски из сорбирующего материала соприкасаются друг с другом в области проведения теста.
2. Устройство для тестов по п.1, дополнительно содержащее:
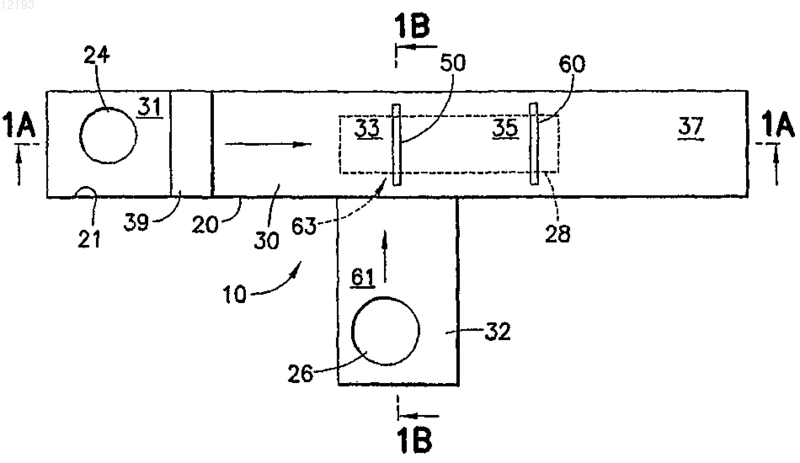
d) корпус, определяющий первое отверстие, расположенное рядом с упомянутым первым местоположением, второе отверстие, расположенное рядом с упомянутым вторым местоположением, и окно, расположенное рядом с упомянутой областью проведения теста, через которое видна упомянутая область проведения теста.
3. Устройство для тестов по п.1, в котором упомянутая первая полоска из сорбирующего материала служит носителем конъюгата.
4. Устройство для тестов по п.3, в котором упомянутым лигандсвязующим средством является антиген или антитело к упомянутому лиганду, а упомянутый конъюгат содержит антиген или антитело к лиганду и маркер, связанный с антигеном или антителом.
5. Устройство для тестов по п.4, в котором упомянутым маркером является окрашенный маркер, видимый в видимой области спектра.
6. Устройство для тестов по п.2, в котором упомянутая по меньшей мере одна из упомянутых первой и второй полосок из сорбирующего материала содержит контрольную область, а упомянутый корпус определяет окно для просмотра упомянутой контрольной области.
7. Устройство для тестов по п.1, в котором упомянутая первая полоска из сорбирующего материала и упомянутая вторая полоска из сорбирующего материала расположены таким образом, что имеют конфигурацию в виде буквы Т.
8. Устройство для тестов по п.1, в котором упомянутая первая полоска из сорбирующего материала и упомянутая вторая полоска из сорбирующего материала расположены таким образом, что имеют конфигурацию в виде знака +.
9. Устройство для тестов по п.1, в котором упомянутая первая полоска из сорбирующего материала имеет поры первого размера, а упомянутая вторая полоска из сорбирующего материала имеет поры второго размера.
10. Устройство для тестов по п.9, в котором упомянутые поры второго размера являются большими по величине, чем упомянутые поры первого размера.
11. Устройство для тестов по п.10, в котором упомянутые поры первого размера имеют величину от 3 до 20 мкм, а упомянутые поры второго размера имеют величину от 20 до 40 мкм.
12. Устройство для тестов по п.2, в котором упомянутая по меньшей мере одна из упомянутых первой и второй полосок из сорбирующего материала содержит контрольную область, и либо упомянутое окно имеет такой размер, что позволяет видеть упомянутую контрольную область, либо упомянутый корпус снабжен вторым окном, позволяющим видеть упомянутую контрольную область.
13. Устройство для тестов по п.1, дополнительно содержащее буферный раствор.
14. Устройство для тестов по п.1, дополнительно содержащее раствор, который содержит подсистему из буферного раствора и конъюгата, содержащую антиген или антитело к лиганду и маркер, связанный с антигеном или антителом.
15. Устройство для тестов по п.1, в котором упомянутая область проведения теста, содержащая иммобилизированное лигандсвязующее средство, содержит антиген ВИЧ (вируса иммунодефицита человека) или антитело к ВИЧ.
16. Устройство для тестов по п.1, в котором упомянутая область проведения теста, содержащая иммобилизированное лигандсвязующее средство, содержит одно из следующих веществ: антигены, антитела, аптамеры, нуклеиновые кислоты или ферменты по меньшей мере для одного из следующих тестов: на беременность, на ВИЧ, на туберкулез (ТБ), на прион, на наркотики по анализу мочи, на хламидии, на маркеры болезней сердца, на маркеры рака, на болезнь Чагаса (американский трипаносомоз), на зубные бактерии (SM/LC), на стрептококк группы А, на грипп А, на грипп В, на аденовирус/ротавирус, на парвовирус собак (CPV), на вирус иммунодефицита кошек (FIV), на вирус лейкемии кошек (FeLV) и на сердечного червя.
17. Устройство для тестов по п.1, в котором упомянутая первая полоска из сорбирующего материала содержит первую мембрану и первую подложку и упомянутая вторая полоска из сорбирующего материала содержит вторую мембрану и вторую подложку, а упомянутая первая полоска из сорбирующего материала и упомянутая вторая полоска из сорбирующего материала расположены таким образом, что упомянутая первая мембрана находится в контакте с упомянутой второй мембраной.
18. Устройство для тестов по п.17, дополнительно содержащее первую липкую пластину подложки, расположенную под упомянутой первой полоской из сорбирующего материала или поверх нее.
19. Устройство для тестов по п.18, дополнительно содержащее вторую липкую пластину подложки, расположенную под упомянутой второй полоской из сорбирующего материала или поверх нее.
20. Устройство для тестов по п.1, в котором упомянутая первая полоска из сорбирующего материала и упомянутая вторая полоска из сорбирующего материала содержат одну мембрану, являющуюся единой для обеих полосок: упомянутой первой полоски из сорбирующего материала и упомянутой второй полоски из сорбирующего материала.
21. Устройство для тестов по п.1, в котором упомянутое устройство для тестов предназначено для определения наличия множества различных лигандов в жидкой пробе, и упомянутая область проведения теста имеет множество отдельных иммобилизированных лигандсвязующих средств для раздельного связывания с соответствующими лигандами из упомянутого множества различных лигандов.
22. Устройство для тестов по п.21, в котором упомянутое множество отдельных иммобилизированных лигандсвязующих средств содержит антиген туберкулеза и по меньшей мере один антиген ВИЧ.
23. Устройство для тестов по п.21, в котором упомянутое множество отдельных иммобилизированных лигандсвязующих средств содержит антитела р24 и по меньшей мере один из антигенов ВИЧ1 и ВИЧ2.
24. Устройство для тестов по п.21, в котором упомянутая первая полоска из сорбирующего материала является носителем множества различных конъюгатов, содержащих антигены и/или антитела к множеству различных лигандов и маркеры, связанные с антигенами и/или с антителами.
25. Устройство для тестов по п.1, в котором упомянутое иммобилизированное лигандсвязующее средство расположено по меньшей мере на четырех линиях, содержащих различные соответствующие антигены ВИЧ или антитела к ВИЧ.
26. Устройство для тестов по п.25, в котором упомянутые различные антигены ВИЧ или антитела к ВИЧ содержат по меньшей мере четыре из следующих: р24, gp41, gp120, gp160 и gp36.
27. Устройство для тестов по п.1, в котором по меньшей мере часть упомянутой области проведения теста окрашена видимым цветным красителем.
28. Устройство для тестов, предназначенное для определения наличия лиганда в жидкой пробе, содержащее:
a) первую полоску из сорбирующего материала, расположенную в первом местоположении, которая предназначена для приема раствора и определяет первый путь миграции;
b) вторую полоску из сорбирующего материала, иную, чем упомянутая первая полоска из сорбирующего материала, расположенную во втором местоположении, которая предназначена для приема жидкой пробы и определяет второй путь миграции, отличный от упомянутого первого пути миграции, причем упомянутая вторая полоска из сорбирующего материала содержит конъюгат из антитела, связанного с временным связующим веществом, а упомянутое антитело, выбрано таъшь образом, чтобы связываться с лигандом при его наличии в пробе; и
с) участок проведения теста, расположенный по меньшей мере на или в одной из упомянутых полосок: упомянутой первой полоски из сорбирующего материала и упомянутой второй полоски из сорбирующего материала, причем упомянутая область проведения теста содержит иммобилизированное связующее вещество, при этом упомянутое временное связующее вещество и упомянутое иммобилизированное связующее вещество выбраны таким образом, что способны избирательно хорошо связываться друг с другом, а упомянутые первая и вторая полоски из сорбирующего материала соприкасаются друг с другом в области проведения теста.
29. Устройство для тестов по п.28, в котором упомянутая первая полоска из сорбирующего материала служит носителем конъюгата, содержащего маркер, связанный со вторым антителом, выбранным таким образом, что оно связывается с лигандом при его наличии в пробе.
30. Устройство для тестов по п.29, в котором упомянутым лигандом является антиген р24, упомянутым конъюгатом из антитела, связанного с временным связующим веществом, является моноклональное антитело р24, связанное с биотином, а упомянутым иммобилизированным связующим веществом является стрептавидин.
31. Устройство для тестов по п.29, в котором упомянутым лигандом является антиген р24, упомянутым конъюгатом из антитела, связанного с временным связующим веществом, является моноклональное антитело р24, связанное с биотином, упомянутым иммобилизированным связующим веществом является стрептавидин, а упомянутым конъюгатом, содержащим маркер, связанный со вторым антителом, является конъюгат окрашенного латекса с моноклональным антителом.
32. Устройство для тестов по п.1, в котором упомянутая первая полоска из сорбирующего материала и упомянутая вторая полоска из сорбирующего материала расположены таким образом, что имеют непараллельную конфигурацию.
33. Устройство для тестов по п.1, содержащее видимый растворимый индикатор.
34. Устройство для тестов, предназначенное для определения наличия лиганда в жидкой пробе, содержащее:
а) первую полоску из сорбирующего материала, расположенную в первом местоположении, которая предназначена для приема раствора и определяет первый путь миграции;
b) вторую полоску из сорбирующего материала, иную, чем упомянутая первая полоска из сорбирующего материала, расположенную во втором местоположении, которая предназначена для приема жидкой пробы и определяет второй путь миграции, отличный от упомянутого первого пути миграции; и
c) область проведения теста, расположенную по меньшей мере на или в одной из упомянутых первых и вторых полосок из сорбирующего материала, причем упомянутая область проведения теста содержит иммобилизированное лигандсвязующее средство, осажденное по меньшей мере на или в одной из упомянутых первой и второй полосок из сорбирующего материала, а упомянутые первая и вторая полоски из сорбирующего материала находятся в непосредственном контакте друг с другом в области проведения теста.
35. Устройство для тестов, предназначенное для определения наличия лиганда в жидкой пробе, содержащее:
a) первый участок материала, определяющий первое местоположение, который предназначен для приема раствора и определяет первый путь миграции;
b) второй участок материала, определяющий второе местоположение, который предназначен для приема раствора и определяет второй путь миграции, не являющийся параллельным упомянутому первому пути миграции; и
c) область проведения теста, расположенную по меньшей мере на или в одном из упомянутых участков материала, которыми являются упомянутый первый участок материала и упомянутый второй участок материала, причем упомянутая область проведения теста имеет иммобилизированное лигандсвязующее средство, осажденное по меньшей мере на или в одном из упомянутых участков материала, которыми являются упомянутый первый участок материала и упомянутый второй участок материала, а упомянутые первый и второй участки материала находятся в контакте друг с другом в области проведения теста.
36. Устройство для тестов по п.35, в котором упомянутые первый и второй пути миграции пересекаются в упомянутой области проведения теста.
37. Способ проведения теста пробы на наличие лиганда, содержащий следующие операции:
а) изготавливают устройство для тестов, содержащее первую полоску из сорбирующего материала, расположенную в первом местоположении, которая предназначена для приема раствора и определяет первый путь миграции, вторую полоску из сорбирующего материала, расположенную во втором местоположении, которая предназначена для приема жидкой пробы и определяет второй путь миграции, отличный от упомянутого первого пути миграции, и область проведения теста, расположенную по меньшей мере на или в одной из упомянутых полосок: упомянутой первой полоски из сорбирующего материала и упомянутой второй полоски из сорбирующего материала, причем упомянутая область проведения теста имеет иммобилизированное лигандсвязующее средство, а упомянутые первая и вторая полоски из сорбирующего материала соприкасаются друг с другом в месте расположения области проведения теста;
b) вводят пробу в упомянутое второе местоположение;
c) после упомянутого ввода пробы вводят раствор в первое местоположение и
d) производят осмотр упомянутой области проведения теста для определения показания, свидетельствующего о наличии или об отсутствии лиганда в пробе.
38. Способ по п.37, в котором
упомянутое устройство для тестов имеет корпус, определяющий первое отверстие, расположенное рядом с упомянутым первым местоположением, второе отверстие, расположенное рядом с упомянутым вторым местоположением, и окно, расположенное рядом с упомянутой областью проведения теста, через которое видна упомянутая область проведения теста, а
введение пробы осуществляют через упомянутое второе отверстие в упомянутое второе местоположение,
введение раствора осуществляют через упомянутое первое отверстие в упомянутое первое местоположение, при этом
производят осмотр через упомянутое окно.
39. Способ проведения теста пробы на наличие лиганда с использованием устройства по п.33, включающий следующие этапы:
a) вводят пробу в устройство для тестов по п.1;
b) осматривают область проведения теста, наблюдая исчезновение видимого индикатора;
c) после исчезновения видимого индикатора в устройство для тестов вводят раствор и
d) производят осмотр области проведения теста для определения показания, свидетельствующего о наличии или об отсутствии лиганда в пробе.
40. Способ по п.39, включающий в себя осмотр области проведения теста с целью установления, захвачен ли коньюгат, имеющий маркер, областью проведения теста.
41. Способ по п.40, в котором упомянутое устройство для проведения тестов снабжено первой сорбирующей полоской для приёма раствора и формирования первого пути миграции для раствора и для коньюгата, имеющего маркер, вторым сорбирующим материалом, имеющим второе место расположения для получения образца и формирования второго пути миграции, отличного от первого пути, где область проведения теста расположена на или в первой сорбирующей полоске и/или второй сорбирующей полоске, при этом первая и вторая сорбирующие полоски соприкасаются в месте проведения теста.
42. Способ по п.41, в котором второй путь миграции расположен в стороне от второго расположения, по крайней мере, до области проведения теста так, что продвижение жидкой пробы во второе место расположения требует времени, в течение которого жидкий образец распространяется в области проведения теста, не смачивая при этом моментально область проведения теста по мере продвижения.
Текст
012193 Предпосылки создания изобретения 1. Область техники, к которой относится изобретение Это изобретение относится, в широком его толковании, к устройствам для иммунологических анализов и к способам их использования. В частности, это изобретение относится к индикаторным полоскам для экспресс-тестов методом хроматографии для обнаружения лиганда в жидкости организма. 2. Уровень техники До настоящего времени использовалось множество типов анализов, основанных на связывании лиганда с рецептором, для обнаружения наличия различных веществ, часто именуемых в целом лигандами,в жидкостях организма, например в крови, моче или слюне. Эти анализы включают в себя реакции антигена с антителом, синтетические конъюгаты, содержащие радиоактивные, ферментативные, флуоресцентные метки или визуально различимые метки из золя полистирола или металла, и специально разработанные камеры для реакций. Во всех этих анализах имеется рецептор, например антитело, которое является специфическим для выбранного лиганда или антигена, и средство для обнаружения наличия, а в некоторых случаях и количества продукта реакции лиганд-рецептор. Некоторые тесты предназначены для количественного определения, но во многих обстоятельствах требуется всего лишь качественное указание, является ли результат положительным/отрицательным. Примерами таких качественных анализов являются, в том числе, определение группы крови, большинство типов анализов мочи, тесты на беременность и тесты на синдром приобретнного иммунодефицита (СПИД). Для этих тестов предпочтительно наличие визуально различимого индикатора, такого как, например, наличие агглютинации или изменение цвета. Даже качественные анализы должны быть очень чувствительными вследствие того, что часто имеет место малая концентрация интересующего лиганда в анализируемой жидкости. Ложные положительные результаты также могут быть ненадежными, в частности, при агглютинации и иных способах быстрого анализа, таких как, например, анализы на основе тест-полосок (dipstick) и изменения цвета. Вследствие наличия этих проблем были разработаны так называемые средства "сэндвич-анализа" и иные чувствительные средства обнаружения, в которых использованы золи металлов или окрашенные частицы иных типов. В способе "сэндвич-анализа" вещество-мишень, определяемое при анализе, которым является, например, антиген, "зажимают" между меченым антителом и антителом, иммобилизированным на твердой подложке. Результат анализа считывают путем наблюдения наличия комплекса "связанный антиген меченое антитело" и/или его количества. При "конкурентном" иммунологическом анализе антитело, связанное с твердой поверхностью, вводят в контакт с пробой, содержащей неизвестное количество анализируемого антигена, и с меченым антигеном того же самого типа. Затем определяют количество меченого антигена, связанного с твердой поверхностью, для получения косвенного показателя количества анализируемого антигена в пробе. Поскольку эти и иные способы анализа могут обеспечивать обнаружение как антител, так и антигенов, то их обычно именуют иммунохимическими анализами, основанными на связывании лиганда с рецептором, или просто иммунологическими анализами. Устройства для твердофазных иммунологических анализов, вне зависимости от того, основаны ли они на способе сэндвич-анализа или на способе конкурентного анализа, обеспечивают обнаружение вещества, определяемого при анализе, в жидкой биологической пробе, например в крови, моче или слюне,с высокой чувствительностью. Устройства для твердофазных иммунологических анализов содержат твердую подложку, с которой связан один из элементов пары лиганд-рецептор, которым обычно является антитело, антиген или гаптен. Широко распространенными видами твердых подложек, которые использовались на начальном этапе, являлись пластинки, трубки или гранулы полистирола, которые являются хорошо известными из области техники радиоиммунологического анализа и иммуноферментного анализа. В прошедшем десятилетии в качестве твердых подложек использовался ряд пористых материалов,которыми являются, например, нейлон, нитроцеллюлоза, ацетат целлюлозы, стекловолокна и иные пористые полимеры. Уже было описано несколько автономных комплектов для иммунологического анализа, в которых в качестве твердофазных носителей иммунохимических компонентов, например антигенов, гаптенов или антител, использованы пористые материалы. Эти комплекты обычно выполнены в виде тест-полосок, в виде устройств проточного или миграционного типа. В более широко распространенных видах анализов на тест-полосках, типичным примером которых являются комплекты для анализов на беременность и на овуляцию в домашних условиях, иммунохимические компоненты, которыми являются, например, антитела, связаны с твердой фазой. Устройство, используемое для анализа, "опускают" для инкубации в пробу, подозреваемую на содержание вещества,определяемого при анализе, которым является неизвестный антиген. Затем добавляют меченое ферментом антитело, либо в течение, либо после инкубационного периода. Затем устройство промывают и вводят во второй раствор, содержащий подложку для фермента. При наличии ферментной метки она взаимодействует с подложкой, вызывая образование окрашенных продуктов реакции, которые либо осаждаются на твердой фазе в виде осадка, либо создают видимое изменение цвета раствора на подложке.-1 012193 Были разработаны устройства для иммунологических анализов проточного типа, устраняющие необходимость в операции длительной инкубации и трудоемкой операции мытья, которые присущи анализам при помощи тест-полосок. В патенте США 4632901, выданном Валкирсу и др. (Valkirs et al.), раскрыто устройство, содержащее антитело (специфичное для анализируемого антигена-мишени), которое является связанным с пористой мембраной или с пористым фильтром, в который добавляют жидкую пробу. По мере протекания жидкости через мембрану вещество-мишень, определяемое при анализе, связывается с антителом. После добавления пробы добавляют меченые антитела. Визуальное обнаружение меченого антитела обеспечивает указание наличия в пробе анализируемого антигена-мишени. В европейском патенте ЕР-А-0299359, выданном Корому и др. (Korom et al.), раскрыт видоизмененный вариант проточного устройства, в котором меченое антитело включено в состав мембраны, которая действует в качестве системы подачи реагента. Необходимость наличия множества операций добавления и промывки в устройствах для иммунологических анализов на основе тест-полосок и в устройствах проточного типа увеличивает вероятность получения ошибочных результатов анализа персоналом с минимальным уровнем подготовки и пользователями в домашних условиях. В анализах миграционного типа мембрана пропитана реагентами, необходимыми для проведения анализа. Имеется зона обнаружения вещества, определяемого при анализе, в которой происходит связывание меченого вещества, определяемого при анализе, и считывают индикаторы анализа. См., например,патент США 4366241, выданный Тому и др. (Tom et al.), и патент США 4596275, выданный Зуку и др. (Zuk et al.). Однако чувствительность анализов миграционного типа часто является сниженной вследствие наличия или формирования в пробе нежелательных твердых компонентов, которые препятствуют прохождению меченого вещества, определяемого при анализе, в зону обнаружения. Чувствительность анализа также является сниженной в тех случаях, когда в устройства анализа миграционного типа залито слишком большое количество жидкой пробы. Устройства для анализов миграционного типа обычно содержат находящиеся в них реагенты, которые были присоединены к окрашенным меткам (то есть конъюгатам), позволяя, тем самым, производить визуальное обнаружение результатов анализа без добавления дополнительных веществ. См., например,патент США 4770853, выданный Бернстайну (Bernstein). Такими метками являются, в том числе, частицы золя золота, которые, например, описаны в патенте США 4313734, выданном Леверингу (Leuvering), частицы золя красителя, которые, например, описаны в патенте США 4,373,932, выданном Грибнау и др. (Gribnau et al.), окрашенный латекс, который, например, описан в международной заявке на патентWO 88/08534, выданной Мэго и др. (May et al.), и красители, инкапсулированные в липосомах,которые описаны в патенте США 4703017, выданном Кэмпбеллу и др. (Campbell et al.). Эти окрашенные метки обычно имеют ограничения с точки зрения подходящих способов иммобилизации. Кроме того, они требуют наличия относительно большого количества молекул лиганда и могут включать в себя дорогостоящие реагенты, что, тем самым, увеличивает их стоимость. Таким образом, по-прежнему остается потребность в чрезвычайно надежных, но недорогих устройствах экспресс-анализа. Также попрежнему остается потребность в создании очень чувствительного способа анализа, в котором может быть использован малый объем пробы и который обеспечивает при этом получение точных результатов. Сущность изобретения Следовательно, задачей настоящего изобретения является создание устройства для иммунологических экспресс-анализов. Другой задачей настоящего изобретения является создание таких устройств для иммунологических анализов, которые являются простыми в использовании и обеспечивают точные результаты. Еще одной задачей настоящего изобретения является создание таких устройств для иммунологических анализов, которые не требуют миграции веществ, определяемых при анализе, вдоль того же самого пути, что и путь конъюгата, являющегося носителем буферных растворов. Также задачей настоящего изобретения является создание таких устройств для иммунологических экспресс-анализов, которые являются простыми по своей конструкции. Дополнительной задачей настоящего изобретения является создание таких устройств для иммунологических анализов, в которых может быть использована как система с сухим конъюгатом, так и система с жидким конъюгатом. Другой задачей настоящего изобретения является создание высокочувствительного устройства для иммунологических анализов, которое обеспечивает получение точных результатов при использовании проб малого объема. Еще одной задачей настоящего изобретения является создание таких высокочувствительных устройств для иммунологических анализов, которые являются пригодными для различных типов жидкостей организма. В соответствии с этими задачами, подробное обсуждение которых приведено ниже, предложены системы устройства для иммунологических анализов как с сухим, так и с жидким конъюгатом. Системы из настоящего изобретения содержат ячейки для тестов с первым сорбирующим материалом, расположенным в первом местоположении, которое предназначено для приема буферного раствора (в случае-2 012193 системы с сухим конъюгатом) или раствора конъюгата (в случае системы с жидким конъюгатом), при этом первый сорбирующий материал определяет первый горизонтальный путь протекания жидкости, со вторым сорбирующим материалом, расположенным во втором местоположении, которое предназначено для приема пробы, при этом второй сорбирующий материал определяет второй горизонтальный путь протекания жидкости, отличающийся от первого пути протекания жидкости, и линию проведения теста или область проведения теста с иммобилизированными антигенами или антителами или с другими лигандосвязующими молекулами, такими как, например, аптамеры, нуклеиновые кислоты и т.д., расположенную в зоне проведения теста в месте пересечения первого и второго сорбирующих материалов. Следует понимать, что в данном описании термин "отличающийся" при его использовании совместно со словами "путь протекания жидкости" или "путь миграции" означает "не сообщающийся никаким иным образом, как через зону проведения теста". Когда ячейка для тестов из настоящего изобретения выполнена в корпусе, то корпус снабжен первым отверстием, расположенным рядом с первым местоположением, и вторым отверстием, расположенным рядом со вторым местоположением. Корпус снабжен имеющимся в нем смотровым окном, расположенным над линией проведения теста. В предпочтительном варианте осуществления настоящего изобретения первый сорбирующий материал и второй сорбирующий материал представляют собой отдельные элементы, которые наложены друг на друга, и линия проведения теста является напечатанной на одном или на обоих сорбирующих материалах в месте их пересечения. В альтернативном варианте, хотя и не являющемся предпочтительным,первый и второй сорбирующие материалы могут быть выполнены в виде единого цельного элемента. Системы из настоящего изобретения в предпочтительном варианте также содержат контрольную линию или область, которую можно увидеть из смотрового окна. Согласно одной группе вариантов осуществления настоящего изобретения сорбирующие материалы из настоящего изобретения (и корпус, в котором находятся эти материалы) выполнены имеющими Тобразную форму, где первое местоположение, предназначенное для приема буферного раствора или буферного раствора с конъюгатом, расположено вблизи одного из концов верхней поперечины Т-образной структуры, второе местоположение, предназначенное для приема пробы, расположено вблизи конца ножки Т-образной структуры, а сорбирующие материалы являются наложенными друг на друга в месте их пересечения. Согласно другой группе вариантов осуществления настоящего изобретения сорбирующие материалы из настоящего изобретения (и корпус, в котором находятся эти материалы) выполнены в форме знака "+", где первое местоположение, предназначенное для приема буферного раствора или буферного раствора с конъюгатом, расположено вблизи от одного из концов первой поперечины, второе местоположение, предназначенное для приема пробы, расположено вблизи от конца одного из концов второй поперечины, а сорбирующие материалы являются наложенными друг на друга в месте их пересечения. Конечно же, сорбирующие материалы могут быть расположены в виде иных конфигураций, и корпус может быть выполнен имеющим иные формы, например прямоугольную, квадратную, неправильную форму и т.д., вне зависимости от схемы расположения сорбирующих материалов. В одном из вариантов осуществления настоящего изобретения значения толщины и длины первого и второго сорбирующих материалов и сами эти материалы выбраны таким образом, чтобы обеспечить согласование того момента времени, когда жидкая проба и жидкий буферный раствор достигают области проведения теста. В системе с сухим конъюгатом согласно настоящему изобретению предусмотрено наличие сухого конъюгата между первым отверстием и областью проведения теста. Конъюгат удерживается на сорбирующем материале или внутри него, поэтому, когда в первое отверстие добавляют буферный раствор, то сорбирующий материал обеспечивает капиллярное протекание буферного раствора к конъюгату, который затем переносится буферным раствором в область проведения теста. В системе с жидким конъюгатом согласно настоящему изобретению предусмотрено наличие жидкостной подсистемы "буферный раствор-конъюгат", и она применена для первого отверстия. Затем сорбирующий материал обеспечивает капиллярное протекание подсистемы "буферный раствор-конъюгат" в область проведения теста. Согласно одному из способов из настоящего изобретения, в нем предложена система, которая содержит ячейку для тестов, имеющую первый сорбирующий материал, расположенный в первом местоположении, который предназначен для приема буферного раствора (в случае системы с сухим конъюгатом) или раствора конъюгата (в случае системы с жидким конъюгатом), при этом, первый сорбирующий материал определяет первый горизонтальный путь протекания жидкости, второй сорбирующий материал, расположенный во втором местоположении, который предназначен для приема пробы, при этом, второй сорбирующий материал определяет второй горизонтальный путь протекания жидкости, отличающийся от первого пути протекания жидкости, и линию проведения теста или область проведения теста с иммобилизированными антигенами или антителами или иными лигандосвязующими молекулами, такими как, например, аптамеры, нуклеиновые кислоты и т.д., расположенную в зоне проведения теста в месте пересечения первого и второго сорбирующих материалов. При желании, также предусмотрено наличие корпуса, имеющего первое отверстие для приема буферного раствора или раствора конъюгата, второе отверстие для приема пробы и смотровое окно, расположенное над линией проведения теста. Пред-3 012193 ставляющую интерес пробу подают во второе отверстие или местоположение. По истечении желательного промежутка времени в первое отверстие или местоположение добавляют жидкость, например, буферный раствор. Если сорбирующий материал удерживает конъюгат (то есть в системе с сухим конъюгатом), то жидкостью предпочтительно является просто буферный раствор. Если же сорбирующий материал не удерживает конъюгат (то есть в системе с жидким конъюгатом), то жидкостью предпочтительно является жидкостная подсистема "буферный раствор-конъюгат". В любом случае, по истечении достаточного количества времени для обеспечения возможности миграции конъюгата в область проведения теста (и в контрольную область при ее наличии) производят осмотр области проведения теста (и контрольной области при ее наличии) для определения того, является ли проба "положительной" или нет. Понятно, что система из настоящего изобретения может быть использована применительно к пробам различных типов, таким как, например, кровь, моча, слюна и кал, и может быть использована для тестов на наличие любого лиганда. В тех случаях, когда должны быть предоставлены кровь, слюна или кал, то перед их добавлением через второе отверстие кровь, слюна или кал могут быть разбавлены буферным раствором или смешаны с ним. В альтернативном варианте в некоторых случаях проба может быть добавлена через отверстие, а затем через то же самое отверстие может быть добавлен разбавитель. Ячейка для тестов из настоящего изобретения имеет преимущество по сравнению с аналогичными устройствами из известного уровню техники потому, что в ячейке для тестов из настоящего изобретения преодолены проблемы агрегации/агглютинации между конъюгатом и тем веществом в пробе, которое определяют при анализе, что представляет собой существенную проблему при традиционном хроматографическом иммунологическом анализе для аналитов относительно большого размера, таких как, например, бактерии. В частности, при традиционных хроматографических иммунологических анализах миграция комплекса бактерии с конъюгированным антителом к линии проведения теста затруднена, и он имеет тенденцию оставаться на дне индикаторной полоски или в подкладке. В этом изобретении не происходит связывание вещества, определяемого при анализе, с конъюгатом с образованием комплекса до тех пор, пока проба не достигнет области проведения теста, поскольку вещество, определяемое при анализе, подают в область проведения теста по его собственному пути, в то время как конъюгат мигрирует сам по себе. В результате, система из настоящего изобретения является чрезвычайно чувствительной и точной. Дополнительные задачи и преимущества настоящего изобретения станут очевидными для специалистов в данной области техники из приведенного ниже подробного описания при его рассмотрении совместно с сопроводительными чертежами. Краткое описание чертежей На фиг. 1 на виде сверху показан схематичный чертеж первого варианта осуществления настоящего изобретения; на фиг. 1 А - вид в разрезе вдоль линии 1 А-1 А из фиг. 1; на фиг. 1 В - вид в разрезе вдоль линии 1 В-1 В из фиг. 1; на фиг. 2 на виде сверху - схематичный чертеж второго варианта осуществления настоящего изобретения; на фиг. 2 А - вид в разрезе вдоль линии 2 А-2 А из фиг. 2; на фиг. 3 на виде в разрезе - третий вариант осуществления настоящего изобретения; на фиг. 4 на виде сверху - схематичный чертеж четвертого варианта осуществления настоящего изобретения; на фиг. 5 на виде сверху - схематичный чертеж пятого варианта осуществления настоящего изобретения; на фиг. 6 на виде сверху - схематичный чертеж шестого варианта осуществления настоящего изобретения; на фиг. 7 на виде сверху - схематичный чертеж седьмого варианта осуществления настоящего изобретения; на фиг. 8 на виде сверху - схематичный чертеж восьмого варианта осуществления настоящего изобретения; на фиг. 9 на виде сверху - схематичный чертеж девятого варианта осуществления настоящего изобретения; на фиг. 10 на виде сверху - схематичный чертеж варианта реализации настоящего изобретения без использования корпуса; на фиг. 11 - таблица, на которой показаны сравнительные данные о чувствительности устройства для тестов из настоящего изобретения по сравнению с типичным устройством для тестов на туберкулез(ТБ) из известного уровня техники; на фиг. 12 - две таблицы и пояснение, в таблицах показаны сравнительные данные о чувствительности устройства для тестов из настоящего изобретения по сравнению с типичными устройствами для тестов на ВИЧ 1 (HIV1) и ВИЧ 2 (HIV2) из известного уровня техники; на фиг. 13 А-13G - схемы, составленные из фотографий/инструктивной информации, на которых показано изделие, представляющее собой кассету для тестов на ВИЧ 1/2 согласно настоящему изобретению,-4 012193 при этом на фиг. 13 А-13 С показана процедура использования изделия для проведения тестов, а на фиг. 13D-13G показаны различные возможные результаты; на фиг. 14 А-14G - схемы, составленные из фотографий/инструктивной информации, на которых показано изделие, представляющее собой тест-полоску для тестов на ВИЧ 1/2 согласно настоящему изобретению, при этом на фиг. 14 А-14 С процедура использования изделия для проведения тестов, а на фиг. 14D-14G показаны различные возможные результаты; на фиг. 15 А-15G - схемы, составленные из фотографий/инструктивной информации, на которых показано изделие, представляющее собой кассету для массового обследования/подтверждающих тестов на ВИЧ 1/2 согласно настоящему изобретению, при этом на фиг. 15 А-15 С показана процедура использования изделия для массового обследования/тестов, а на фиг. 15D-15G показаны различные возможные результаты; на фиг. 16 А-16 Е - фотографии результатов тестов, полученные на реальных тест-полосках для тестов на ВИЧ 1/2 согласно настоящему изобретению. Подробное описание предпочтительных вариантов осуществления изобретения Теперь перейдем к рассмотрению фиг. 1, 1 А и 1 В. В устройстве для иммунологических анализов имеется ячейка 10 для тестов, содержащая корпус 20 Т-образной формы, имеющий верхнюю стенку 21,определяющий первое отверстие 24 и второе отверстие 26, и окно 28; и первый и второй сорбирующие или абсорбирующие материалы 30, 32, определяющие перпендикулярные горизонтальные пути протекания жидкости в корпусе. Первый сорбирующий материал 30 содержит по меньшей мере две зоны, а в предпочтительном варианте - три или четыре зоны, и может быть выполнен из множества материалов. Первая зона 31 (иногда именуемая зоной фильтра) расположена у первого отверстия 24 и продолжается до второй зоны 33 (иногда именуемой зоной проведения теста), которая расположена в месте пересечения поперечин "Т". Первая зона 31 предпочтительно содержит фильтр 31 а, подкладку 31b, на которой или в которой осажден и иммобилизирован конъюгат 39, имеющий желательные антигены или антитела с присоединенными окрашенными маркерами, и первый участок тонкой мембраны или сорбирующего или абсорбирующего материала 30, обычно выполненный из нитроцеллюлозы с пластмассовой подложкой (на чертеже не показана). Первая зона 31 приспособлена для приема буферного раствора, вызывая вхождение буферного раствора в контакт с конъюгатом, обеспечивая, тем самым, мобилизацию конъюгата и капиллярное протекание буферного раствора, являющегося носителем конъюгата, во вторую зону 33. Вторая зона 33 (для проведения теста) содержит второй участок тонкой мембраны 30, на котором предпочтительно напечатана линия 50 проведения теста, содержащая иммобилизированные антигены или антитела (в зависимости от того, предназначена ли ячейка для тестов для проведения тестов на наличие антител или антигенов) на мембране, что является известным уровнем техники. Линия 50 проведения теста может быть видна через окно 28 из прозрачной пластмассы, имеющееся в корпусе. Также может быть напечатана необязательная третья зона 35 (иногда именуемая контрольной зоной), которая содержит третий участок тонкой мембраны 30, с контрольной линией 60, обычно содержащей антитела к конъюгированным антигенам (или в некоторых случаях антитела, которые будут связываться с конъюгированными антителами, или даже антигены, которые будут связываться с конъюгированными антителами), что является известным уровнем техники. При наличии третьей зоны 35 окно 28 продолжается над контрольной линией 60. При желании может быть предусмотрено наличие необязательной четвертой зоны 37 (иногда именуемой зоной резервуара), служащей в качестве резервуара для капиллярного растекания, что также является известным уровнем техники. Четвертая зона 37 содержит относительно более толстую гигроскопичную бумагу 31d. В предпочтительном варианте все зоны покрыты лежащей поверх них тонкой, предпочтительно прозрачной пластмассовой пленкой или пластиной 38 а с клеем, который удерживает сорбирующие материалы на месте. Пластина 38 может быть вырезана таким образом, что имеет отверстие в месте расположения отверстия 24 для того, чтобы не препятствовать доступу жидкости в отверстие 24. Второй сорбирующий материал 32 также может быть выполнен из множества материалов и предпочтительно содержит две зоны 61, 63. Первая зона 61 (иногда именуемая зоной фильтра) содержит фильтр или подкладку 62 и первый участок тонкой мембраны или сорбирующего или абсорбирующего материала 32, обычно выполненный из нитроцеллюлозы с подложкой (на чертеже не показана). Первая зона 61 расположена у второго отверстия 26 и продолжается до второй зоны 63. Вторая зона 63 содержит второй участок тонкой мембраны 32, который находится в контакте со второй зоной 33 первого сорбирующего материала 30. Как видно на фиг. 1 А и 1 В, первый сорбирующий материал 30 является наложенным на второй сорбирующий материал 32 таким образом, что мембраны находятся в контакте друг с другом (в отличие от подложек, имеющих контакт с мембранами или друг с другом), и поэтому линия 50 проведения теста фактически расположена между мембранами. Следовательно, линия 50 проведения теста может быть напечатана на второй зоне 63 второго сорбирующего материала 32 вместо ее печати на второй зоне 33 первого сорбирующего материала 30 или в дополнение к этому. При желании может быть использована тонкая пластмассовая пленка или пластина 38b с клеем, который удерживает второй сорбирующий материал на месте. В тех случаях, когда в качестве первой и второй мембран использованы полоски из нитроцеллюло-5 012193 зы стандартного типа с подложкой, желательно, чтобы мембраны имели поры различного размера. Например, и как более подробно изложено ниже, если мембрана 31 (для миграция конъюгата) имеет размер пор, равный 3, а мембрана 32 (для миграции пробы) имеет размер пор, равный 15, то проба, поданная на мембрану 32, будет стремиться мигрировать и оставаться в мембране 32 для пробы и не будет стремиться мигрировать в мембрану 31 для конъюгата. Устройство для иммунологического анализа из фиг. 1 предпочтительно используют следующим образом. Сначала во второе отверстие или в отверстие 26 подают пробу (на чертеже не показана), которая, возможно, содержит антитела (или антигены), и обеспечивают возможность ее миграции через второй сорбирующий материал 32 в его вторую зону 63, которая находится в контакте со второй зоной 33 первого сорбирующего материала 30. Возможно, но не обязательно, после подачи пробы в отверстие 26,в это отверстие 26 может быть добавлена жидкость, например буферный раствор, количество которой предпочтительно является измеренным, для содействия миграции пробы. Вне зависимости от того, добавлена жидкость или нет, проба достигает линии 50 проведения теста, которая напечатана наверху второй зоны 33 первого сорбирующего материала или внедрена в нее. По истечении желательного промежутка времени, в течение которого антитела (или антигены) в пробе (при их наличии) уже имели бы возможность связаться с антигенами (или с антителами), иммобилизированными на линии 50 проведения теста, в первое отверстие 24 добавляют жидкость, например, буферный раствор (на чертеже не показан),количество которой предпочтительно является измеренным. По истечении другого промежутка времени,который является достаточным для того, чтобы обеспечить возможность миграции конъюгата в область 50 проведения теста (и в контрольную область 60 при ее наличии), производят осмотр области 50 проведения теста (и контрольной области 60 при ее наличии) через окно 28 для определения того, является ли проба положительной или нет. Как правило, "положительный" результат теста, указывающий на наличие антитела (или антигена) в пробе, получают тогда, когда в обеих областях: в области 50 проведения теста и в контрольной области 60, видны цветные линии. "Отрицательный" результат теста, указывающий на отсутствие антитела (или антигена) в пробе, получают тогда, когда цветная линия видна только лишь в контрольной области 60. Способ из настоящего изобретения может быть ускорен путем создания корпуса с нумерацией и/или с надписями для указания того, что отверстие 26 предназначено для приема пробы (и возможно, но не обязательно, некоторого количества буферного раствора), и его следует использовать первым по порядку, и что отверстие 24 предназначено для приема буферного раствора, и его следует использовать вторым по порядку. Для специалистов в данной области техники понятно, что устройство 10 для иммунологического анализа функционирует следующим образом. Поскольку линия 50 проведения теста снабжена антигенами (или антителами), иммобилизированными на мембране, то в том случае, если проба теста содержит антитела к антигенам (или антигены к антителам), то эти антитела (или антигены) будут связываться с антигенами (или с антителами) на линии проведения теста. После этого, когда вызвана миграция конъюгата 39, содержащего антиген к антителу (или антитело к антигену), связанный с окрашенным маркером,к линии проведения теста, то в том случае, если тестируемая проба содержит антитела (или антигены),которые теперь удерживаются на линии 50 проведения теста, то антиген (или антитело) из конъюгата связывается с антителами (или с антигенами), и окрашенный маркер вызывает появление цветной линии в области 50 проведения теста. Если же тестируемая проба не содержит антител (или антигенов), то в конъюгате отсутствуют антитела (антигены), образующие связи на линии 50 проведения теста, и в области 50 проведения теста цветная линия не появится. С другой стороны, поскольку контрольная линия 60 снабжена антителами (или антигенами), то антигены (или антитела) конъюгата будут всегда связываться с антителами (или антигенами) на контрольной линии 60, вызывая, тем самым, появление цветной линии в контрольной области 60, если конъюгат достигает контрольной области 60. Таким образом, если в ячейку для тестов подано достаточное количество буферного раствора, то в контрольной области 60 всегда должна появляться цветная линия, обеспечивая, тем самым, контроль проведения теста. На фиг. 2 и 2 А показан второй вариант осуществления настоящего изобретения. На фиг. 1, 1 А, 1 В, 2 и 2 А для аналогичных элементов использованы одинаковые номера позиций. Таким образом, понятно,что основное различие между вторым вариантом осуществления изобретения, показанным на фиг. 2 и 2 А, и первым вариантом осуществления изобретения, показанным на фиг. 1, 1 А и 1 В, состоит в том, что второй сорбирующий материал 32 а ячейки 10 а для тестов выполнен имеющим форму ключа (предпочтительно путем штамповки). При наличии конфигурации в форме ключа зона 61 а имеет такую форму, что она сужается к второй узкой зоне 63 а. В результате, зона 63 а соприкасается со второй зоной 33 первого сорбирующего материала 30 почти исключительно в месте расположения линии 50 проведения теста. Для специалистов в данной области техники понятно, что ячейка 10 а для иммунологических тестов из фиг. 2 может быть использована тем же самым образом, как и ячейка 10 для тестов из фиг. 1, и что она функционирует, по существу, точно так же. На фиг. 3 показан третий вариант осуществления настоящего изобретения. На фиг. 1, 1 А, 1 В и 3 для аналогичных элементов использованы одинаковые номера позиций. Таким образом, понятно, что основное различие между ячейкой 10b для тестов из третьего варианта осуществления изобретения, показан-6 012193 ной на фиг. 3, и ячейкой 10 для тестов из первого варианта осуществления изобретения, показанной на фиг. 1, 1 А и 1 В, состоит в том, что на вторую полоску 32 из нитроцеллюлозы в том месте, где первая полоска 30 из нитроцеллюлозы соприкасается со второй полоской (за исключением узкой зоны в области 50 проведения теста и рядом с ней), наложен очень тонкий слой непористого материала 99, например пластмассы. В результате наличия материала 99 полоски 30 и 32 соприкасаются друг с другом почти исключительно в месте расположения линии 50 проведения теста. Для специалистов в данной области техники понятно, что ячейка 10b для иммунологических тестов из фиг. 3 может быть использована тем же самым образом, как и ячейка 10 для тестов из фиг. 1, и что она функционирует, по существу, точно так же. На фиг. 4 показан четвертый вариант осуществления устройства для иммунологических анализов,снабженного ячейкой 10' для тестов (немного видоизмененной по сравнению с ячейкой 10 для тестов из фиг. 1), которая содержит Т-образный корпус 20', имеющий верхнюю стенку 21', определяющую первое и второе отверстия 24', 26', и окно 28'; и первый и второй сорбирующие или абсорбирующие материалы 30', 32', определяющие перпендикулярные горизонтальные пути протекания жидкости в корпусе. Первый сорбирующий материал 30' содержит по меньшей мере две зоны, а в предпочтительном варианте - три или четыре зоны, и может быть выполнен из множества материалов. Первая зона 31' (иногда именуемая зоной фильтра) расположена у первого отверстия 24' и продолжается до второй зоны 33' (иногда именуемой зоной проведения теста), которая расположена в месте пересечения Т. Первая зона 31' предпочтительно содержит фильтр, подкладку, на которой или в которой осажден и иммобилизирован конъюгат 39', имеющий желательные антигены или антитела с присоединенными окрашенными маркерами, и тонкую мембрану, обычно выполненную из нитроцеллюлозы (которая продолжается до второй зоны и до необязательных третьей и четвертой зон) с подложкой. Первая зона 31' приспособлена для приема буферного раствора, вызывая вхождение буферного раствора в контакт с конъюгатом, обеспечивая, тем самым, мобилизацию конъюгата и капиллярное протекание буферного раствора, являющегося носителем конъюгата, во вторую зону 33'. Вторая зона 33' имеет напечатанную на ней линию 50' проведения теста,которая, как описано ниже, расположена под вторым сорбирующим материалом 32'. Необязательная третья зона 35' (иногда именуемая контрольной зоной) может быть снабжена контрольной линией 60', обычно содержащей антитела к конъюгированным антигенам (или в некоторых случаях антитела, которые будут связываться с конъюгированными антителами, или даже антигены, которые будут связываться с конъюгированными антителами), что является известным уровнем техники. При наличии третьей зоны 35' окно 28' продолжается над контрольной линией 60'. При желании может быть предусмотрено наличие необязательной четвертой зоны 37' (иногда именуемой зоной резервуара),служащей в качестве резервуара для капиллярного растекания, что также является известным уровнем техники. Четвертая зона 37' содержит относительно более толстую гигроскопичную бумагу. В предпочтительном варианте под всеми четырьмя зонами имеется подложка из тонкой пластмассовой пленки с клеем, который удерживает сорбирующие материалы на месте. Второй сорбирующий материал 32' также может быть выполнен из множества материалов и предпочтительно содержит две зоны 61', 63'. Первая зона 61' (иногда именуемая зоной фильтра) расположена у второго отверстия 26' и продолжается до второй зоны 63', которая находится в контакте со второй зоной 33' первого сорбирующего материала 30'. При желании, во второй зоне 63' второго сорбирующего материала 32' может быть напечатана линия 50' проведения теста, имеющая иммобилизированные антигены или антитела (в зависимости от того, предназначена ли ячейка для тестов для проведения тестов на наличие антител или антигенов), что является известным уровнем техники. Вне зависимости от того,снабжена ли вторая зона 63' или вторая зона 33' или обе из них линией 50' проведения теста, линия 50' проведения теста может быть видна через окно 28' из прозрачной пластмассы, имеющееся в корпусе. Как предложено посредством линий на фиг. 4 (по сравнению с фиг. 1), второй сорбирующий материал 32' лежит поверх первого сорбирующего материала 30' таким образом, что тонкие мембраны обоих материалов находятся в контакте друг с другом, по меньшей мере, в месте расположения линии проведения теста. Второй сорбирующий материал 32' может быть выполнен имеющим такую же форму, как на фиг. 1,поэтому имеется стандартная полоска из нитроцеллюлозы с подложкой. В альтернативном варианте материал 32' может быть выполнен имеющим такую же форму, как на фиг. 2, вследствие чего он соприкасается с первым сорбирующим материалом почти исключительно в месте расположения линии 50' проведения теста. В качестве другого альтернативного варианта материал 32' выполнен имеющим такую же форму, как на фиг. 1, и может быть предусмотрено наличие тонкой непористой мембраны, как на фиг. 3,вследствие чего материалы 30' и 32' соприкасаются друг с другом почти исключительно в месте расположения линии 50' проведения теста. Для специалистов в данной области техники понятно, что ячейка 10' для иммунологических тестов из фиг. 4 может быть использована тем же самым образом, как и ячейка 10 для тестов из фиг. 1, и что она функционирует, по существу, точно так же. На фиг. 5 показана ячейка 10" для тестов из устройства для иммунологических анализов, содержащая Т-образный корпус 20", имеющий верхнюю стенку 21", определяющую первое и второе отверстия 24", 26", и окно 28"; и сорбирующий или абсорбирующий материал 30" Т-образной формы, определяю-7 012193 щий перпендикулярные пути протекания жидкости в корпусе. Сорбирующий материал 30" Т-образной формы содержит по меньшей мере три зоны, а в предпочтительном варианте - четыре или пять зон, и может быть выполнен из множества материалов. Первая зона 31" (иногда именуемая зоной фильтра) расположена у первого отверстия 24" и продолжается до второй зоны 33" (иногда именуемой зоной проведения теста), которая расположена в месте пересечения Т. Первая зона 31" предпочтительно содержит фильтр, подкладку, на которой или в которой осажден и иммобилизирован конъюгат 39", имеющий желательные антигены или антитела с присоединенными окрашенными маркерами, и тонкую мембрану,обычно выполненную из нитроцеллюлозы, и подложку для нее. Первая зона 31" приспособлена для приема буферного раствора, вызывая вхождение буферного раствора в контакт с конъюгатом, обеспечивая, тем самым, мобилизацию конъюгата и капиллярное протекание буферного раствора, являющегося носителем конъюгата, во вторую зону 33". На второй зоне 33" (для проведения теста) предпочтительно напечатана линия 50" проведения теста, содержащая иммобилизированные антигены или антитела (в зависимости от того, предназначена ли ячейка для тестов для проведения тестов на наличие антител или антигенов) на мембране, что является известным уровнем техники. Линия 50" проведения теста может быть видна через окно 28" из прозрачной пластмассы, имеющееся в корпусе. Третья зона 61" (иногда также именуемая зоной фильтра), расположенная у второго отверстия 26", является перпендикулярной полоске, определенной первой и второй зонами, и продолжается до второй зоны 33". Также может быть напечатана необязательная четвертая зона 35" (иногда именуемая контрольной зоной) с контрольной линией 60", обычно содержащая антитела к конъюгированным антигенам (или в некоторых случаях антитела, которые будут связываться с конъюгированными антителами, или даже антигены, которые будут связываться с конъюгированными антителами), что является известным уровнем техники. При наличии четвертой зоны 35" окно 28" продолжается над контрольной линией 60". При желании может быть предусмотрено наличие необязательной пятой зоны 37" (иногда именуемой зоной резервуара), служащей в качестве резервуара для капиллярного растекания, что также является известным уровнем техники. Пятая зона 37" содержит относительно более толстую гигроскопичную бумагу. В предпочтительном варианте под всеми зонами лежит тонкая пластмассовая пленка с клеем, который удерживает сорбирующие материалы на месте. Вариант осуществления изобретения из фиг. 5 отличается от вариантов осуществления изобретения, показанных на фиг. 1-4 только тем, что вместо использования двух отдельных полосок материала,наложенных одна на другую в зоне проведения теста, используется одиночная мембрана Т-образной формы, которая определяет первую горизонтальную полоску с зонами 31", 33" и предпочтительно 35" и 37", и вторую (цельную) полоску с зоной 61", которая соприкасается с первой полоской в зоне 33" проведения теста. Несмотря на то, что вариант осуществления изобретения из фиг. 5 не позволяет специально приспосабливать горизонтальные пути протекания жидкости посредством материалов с порами различных размеров, сохранены два различных пути миграции, поскольку первая и третья зоны не сообщаются друг с другом никаким иным образом, как через вторую зону (для проведения теста). На фиг. 6 показана ячейка 110 для тестов из устройства для иммунологических анализов, содержащая корпус 120, выполненный в форме знака +, который имеет верхнюю стенку 121, определяющую первое и второе отверстия 124, 126, и окно 128; и первый и второй сорбирующие или абсорбирующие материалы 130, 132, определяющие перпендикулярные пути протекания жидкости в корпусе. Первый сорбирующий материал 130 содержит по меньшей мере две зоны, а предпочтительно - три или четыре зоны, и может быть выполнен из множества материалов. Первая зона 131 (иногда именуемая зоной фильтра) расположена у первого отверстия 124 и продолжается до второй зоны 133 (иногда именуемой зоной проведения теста), которая расположена в месте пересечения поперечин знака +. Первая зона 131 предпочтительно содержит фильтр, подкладку на которой или в которой осажден и иммобилизирован конъюгат 139, имеющий желательные антигены или антитела с присоединенными окрашенными маркерами, и тонкую мембрану, обычно выполненную из нитроцеллюлозы. Первая зона 131 приспособлена для приема буферного раствора, вызывая вхождение буферного раствора в контакт с конъюгатом, обеспечивая, тем самым, мобилизацию конъюгата и капиллярное протекание буферного раствора, являющегося носителем конъюгата, во вторую зону 133. Во второй зоне 133 (для проведения теста) предпочтительно напечатана линия 150 проведения теста, содержащая иммобилизированные антигены или антитела (в зависимости от того, предназначена ли ячейка для тестов для проведения тестов на наличие антител или антигенов) на мембране, что является известным уровнем техники. Линия 150 проведения теста может быть видна через окно 128 из прозрачной пластмассы, имеющееся в корпусе. Также может быть напечатана необязательная третья зона 135 (иногда именуемая контрольной зоной) с контрольной линией 160, обычно содержащая антитела к конъюгированным антигенам (или в некоторых случаях антитела,которые будут связываться с конъюгированными антителами, или даже антигены, которые будут связываться с конъюгированными антителами), что является известным уровнем техники. При наличии третьей зоны 135 окно 128 продолжается над контрольной линией 160. При желании может быть предусмотрено наличие необязательной четвертой зоны 137 (иногда именуемой зоной резервуара), служащей в качестве резервуара для капиллярного растекания, что также является известным уровнем техники. Четвертая зона 137 содержит относительно более толстую гигроскопичную бумагу. В предпочтительном-8 012193 варианте зоны покрыты лежащей поверх них (таким же образом, как и на фиг. 1 А) тонкой пластмассовой пленкой с клеем, который удерживает сорбирующие материалы на месте. Второй сорбирующий материал 132 также может быть выполнен из множества материалов и предпочтительно содержит по меньшей мере три зоны 161, 163, 165. Первая зона 161 (иногда именуемая зоной фильтра) расположена у второго отверстия 126 и продолжается до второй зоны 163, которая находится в контакте со второй зоной 133 первого сорбирующего материала 130. При желании линия 150 проведения теста может быть напечатана на второй зоне 163 сорбирующего материала 132 вместо ее печати на второй зоне 133 материала 130 или в дополнение к этому. Как показано пунктирной линией на фиг. 6, первый сорбирующий материал 130 лежит поверх второго сорбирующий материалом 132 (как в варианте осуществления изобретения из фиг. 1). В альтернативном варианте второй сорбирующий материал 132 может быть выполнен таким образом, что он лежит поверх первого сорбирующего материала 130 (как в варианте осуществления изобретения из фиг. 4), и в этом случае пленки с клеем, при их использовании, и другие элементы должны быть размещены надлежащим образом. При желании может быть предусмотрено наличие необязательной третьей зоны 165 (иногда именуемой зоной резервуара),служащей в качестве резервуара для капиллярного растекания. Четвертая зона 137 содержит относительно более толстую гигроскопичную бумагу. При желании может быть использована тонкая пластмассовая пленка с клеем, который удерживает второй сорбирующий материал на месте. На фиг. 7 показан седьмой вариант осуществления настоящего изобретения. На фиг. 1, 1 А, 1 В и 7 для аналогичных элементов использованы одинаковые номера позиций. Таким образом, понятно, что основное различие между седьмым вариантом осуществления изобретения, показанным на фиг. 7, и первым вариантом осуществления изобретения, показанным на фиг. 1, 1 А и 1 В, состоит в том, что напечатаны две линии 50 А и 50 В проведения теста, расположенные в зоне 33 первого сорбирующего материала 30 и/или в зоне 63 второго сорбирующего материала 32. Эти две линии 50 А и 50 В проведения теста предпочтительно содержат различные иммобилизированные антигены или антитела. Например, одна из линий (например, линия 50 А) может содержать пептиды ВИЧ 1 и/или рекомбинантные антигены, такие как, например, gp41/gp120, в то время как другая линия (например, линия 50 В) может содержать пептиды ВИЧ 2 и/или рекомбинантные антигены, например, gp36. В качестве другого примера, одна из линий может содержать пептиды ВИЧ 1, ВИЧ 2 или ВИЧ 1/2 и/или рекомбинантные антигены, в то время как другая линия содержит антигены туберкулеза. Как описано ниже, в тех случаях, когда линии проведения теста содержат иммобилизированные антитела или антигены, которые не будут связываться с одиночным конъюгатом (например, с протеином А), может оказаться желательным использование множества различных конъюгатов, содержащих желательные антигены или антитела с присоединенными окрашенными маркерами. Для специалистов в данной области техники понятно, что ячейка 10 с для иммунологических тестов из фиг. 7 может быть использована тем же самым образом, как и ячейка 10 для тестов из фиг. 1, и что она функционирует, по существу, точно так же, за исключением того, что "положительный" результат теста, указывающий факт наличия первого антитела (или антигена) в пробе, подвергаемой тестированию, получают тогда, когда цветные линии видны на линии 50 А проведения теста и в контрольной области 60; "положительный" результат теста, указывающий факт наличия второго антитела (или антигена) в пробе, подвергаемой тестированию, получают тогда, когда цветные линии видны на линии 50 В проведения теста и в контрольной области 60; и "положительный" результат теста, указывающий факт наличия обоих антител: первого и второго антител (или антигенов), в пробе, подвергаемой тестированию, получают тогда, когда цветные линии видны на линиях 50 А и 50 В проведения теста в контрольной области 60. "Отрицательный" результат теста, указывающий факт отсутствия антитела (или антигена) в пробе, получают тогда, когда цветная линия видна только в контрольной области 60 (и ни на одной из линий 50 А и 50 В проведения теста). Недостоверный результат теста получают тогда, когда цветная линия в контрольной области отсутствует. На фиг. 8 показан восьмой вариант осуществления настоящего изобретения. На фиг. 1, 1 А, 1 В и 8 для аналогичных элементов использованы одинаковые номера позиций. Таким образом, понятно, что основное различие между восьмымвариантом осуществления изобретения, показанным на фиг. 8, и первым вариантом осуществления изобретения, показанным на фиг. 1, 1 А и 1 В, состоит в том, что напечатаны три линии 50 А, 50 В, 50C проведения теста, расположенные в зоне 33 первого сорбирующего материала 30 и/или в зоне 63 второго сорбирующего материала 32, и что использованы два различных латексных конъюгата 39 А, 39 В. Эти три линии 50 А, 50 В и 50 С проведения теста предпочтительно содержат различные иммобилизированные антигены или антитела. Например, одна из линий (например, линия 50 А) может содержать моноклональные антитела р 24, вторая линия (например, линия 50 В) может содержать пептиды ВИЧ 1 и/или рекомбинантные антигены, такие как, например, gp41/gp120, в то время как третья линия (например, линия 50 С) может содержать пептиды ВИЧ 2 и/или рекомбинантные антигены, такие как, например, gp36. В этом случае предусмотрено наличие двух конъюгатов 39 А, 39 В, причем конъюгатом 39 А является латексный конъюгат с протеином А, который будет связываться с антителами к ВИЧ 1 и ВИЧ 2 при их наличии, но не будет связываться с антигеном р 24, а конъюгатом 39 В является латекс, конъюгированный с моноклональным антителом к р 24, который будет связываться с антигеном р 24 в пробе при его наличии, но не будет связываться с пептидами ВИЧ 1 и ВИЧ 2 и/или с рекомбинант-9 012193 ными антигенами. Как показано на фиг. 8, конъюгаты 39 А и 39 В расположены в различных местах пути миграции (например, в двух участках одной подкладки, или на двух соединенных между собой подкладках). Однако понятно, что конъюгаты 39 А и 39 В могут быть поданы в одно и то же место в виде смеси. Для специалистов в данной области техники понятно, что ячейка 10d для иммунологических тестов из фиг. 8 может быть использована тем же самым образом, как и ячейка 10 для тестов из фиг. 1, и что она функционирует, по существу, точно так же, за исключением того, что "положительный" результат теста на ВИЧ указывает наличие видимого цвета на одной или на большем количестве линий 50 А, 50 В, 50 С и на контрольной линии 60, "отрицательный" результат теста указывает наличие видимого цвета только лишь на контрольной линии 60, а "недостоверный" результат теста указывает отсутствие появления цвета на контрольной линии 60. На фиг. 9 показан девятый вариант осуществления настоящего изобретения. На фиг. 1, 1 А, 1 В и 9 для аналогичных элементов использованы одинаковые номера позиций. Таким образом, понятно, что основное различие между девятым вариантом осуществления изобретения, показанным на фиг. 9, и первым вариантом осуществления изобретения, показанным на фиг. 1, 1 А и 1 В, состоит в том, что второй сорбирующий материал 32'" содержит первую зону 61'" (иногда именуемую зоной фильтра), имеющую фильтр или подкладку 62'", на которой имеется конъюгат 39'" антитела, связанный с временным связующим веществом (без маркера), а зона проведения теста имеет линию 50 проведения теста с иммобилизированным связующим веществом. Временное связующее вещество и иммобилизированное связующее вещество выбраны таким образом, что являются способными чрезвычайно хорошо избирательно связываться друг с другом. Таким образом, временным связующим веществом может являться, например, биотин, а иммобилизированным связующим веществом может являться стрептавидином. Следовательно,конъюгатом 39'" на пути миграции пробы может являться антитело, например, моноклональное антитело р 24, которое связано с биотином. Аналогичным образом, конъюгатом 39 на пути миграции буферного раствора предпочтительно является латексный маркерный конъюгат с антителом (например, с моноклональным антителом), который будет связываться с интересующим антигеном. В ячейке 10 е для тестов из фиг. 9, которая предназначена для обнаружения наличия вируса р 24,пробу сначала добавляют во второй сорбирующий материал 32'". Когда проба достигает конъюгата 39'""моноклональное антитело р 24 - биотин", то антиген (вирус) р 24, при его наличии в пробе, связывается с конъюгатом "моноклональное антитело р 24 - биотин" и будет мигрировать в область 63'" проведения теста на полоске 32'", где биотин захватывается стрептавидином на линии 50 проведения теста, расположенной на полоске 32'" и/или на полоске 31. Таким образом, на линии 50 проведения теста будет иметься комплекс из стрептавидина, связанного с биотином, который связывается с моноклональным антителом р 24, которое, в свою очередь, связывается с антигеном р 24. Затем добавляют буферный раствор на первый сорбирующий материал 31. Буферный раствор переносит конъюгат 39 "латексный маркер - моноклональное антитело" в область 33 проведения теста, где моноклональное антитело конъюгата 39 связывается с антигеном р 24, удерживаемым в уже имеющемся комплексе, обеспечивая, тем самым, появление цветной линии вследствие наличия маркера. Если антиген в пробе не присутствует, то конъюгат 39'""биотин - моноклональное антитело р 24" будет по-прежнему оставаться со стрептавидином, причем комплекс из стрептавидина, биотина и моноклонального антитела р 24 будет оставаться на линии проведения теста. Однако когда конъюгат 39 "латексный маркер - моноклональное антитело" доходит до области проведения теста, то какой-либо антиген, с которым может связываться моноклональное антитело,отсутствует. Следовательно, маркерный конъюгат 39 не будет удерживаться на линии 50 проведения теста, и будет зарегистрирован "отрицательный" результат теста. Специалистам в данной области техники понятно, что система из фиг. 9 обеспечивает большое преимущество по сравнению с традиционными системами с растеканием в боковом направлении из известного уровня техники вследствие высокой аффинности временного связующего вещества (например, биотина) и иммобилизированного связующего вещества (например, стрептавидина), что приводит к чрезвычайно высокой чувствительности теста. На фиг. 10 показан комплект 200 для иммунологических тестов, содержащий скальпель 201, упаковку 202 с буферным раствором, петлю 203, спиртовой протирочный тампон 204, лейкопластырь 205 и устройство для тестов или ячейку 210 для тестов. Ячейка 210 для тестов является аналогичной ячейкам для тестов из других вариантов осуществления изобретения с определенными исключениями, например,вместо корпуса предусмотрена картонная подложка 215, и различные участки сорбирующих материалов снабжены расположенными поверх них бумажными защитными покрытиями 217 а, 217b, 217 с. Предпочтительно предусмотрено наличие обозначений в виде стрелок, указывающих, в каком направлении следует потянуть бумажные защитные покрытия 217 а, 217b для их удаления с сорбирующих материалов. В частности, ячейка 210 для тестов содержит первый и второй сорбирующие или абсорбирующие материалы 230, 232, определяющие перпендикулярные горизонтальные пути протекания жидкости. Первый сорбирующий материал 230 содержит по меньшей мере две зоны, а предпочтительно - три или четыре зоны,и может быть выполнен из множества материалов. Первая зона 231 (иногда именуемая зоной фильтра) расположена на одном конце первого сорбирующего материала и продолжается до второй зоны 233(иногда именуемой зоной проведения теста), которая расположена в месте пересечения поперечин Т. Первая зона 231 предпочтительно содержит фильтр, подкладку на которой или в которой осажден и иммобилизирован конъюгат 239, имеющий желательные антигены или антитела с присоединенными окрашенными маркерами, и первый участок тонкой мембраны или сорбирующего или абсорбирующего материала 230, обычно выполненный из нитроцеллюлозы с пластмассовой подложкой (на чертеже не показана). Первая зона 231 приспособлена для приема буферного раствора, вызывая вхождение буферного раствора в контакт с конъюгатом, обеспечивая, тем самым, мобилизацию конъюгата и капиллярное протекание буферного раствора, являющегося носителем конъюгата, во вторую зону 233. По меньшей мере часть первой зоны обычно закрыта бумажным защитным покрытием 217 а. Вторая зона 233 (для проведения теста) содержит второй участок тонкой мембраны 230, на котором предпочтительно напечатана одна или большее количество линий 250 проведения теста (на чертеже показана одна такая линия), содержащих иммобилизированные антигены или антитела (например, пептиды gp41/gp120 и gp36 для обнаружения ВИЧ 1/2) на мембране, что является известным уровнем техники. Сорбирующий материал на линии 250 проведения теста может быть открытым или может быть закрыт прозрачной пластмассовой крышкой(на чертеже не показана). Также может быть напечатана необязательная третья зона 235 (иногда именуемая контрольной зоной), которая содержит третий участок тонкой мембраны 230 с контрольной линией 260, обычно содержащей антитела к конъюгированным антигенам (или в некоторых случаях антитела,которые будут связываться с конъюгированными антителами, или даже антигены, которые будут связываться с конъюгированными антителами), что является известным уровнем техники. Третья зона может быть, аналогичным образом, оставлена открытой, или она может быть закрыта прозрачной пластмассовой крышкой. При желании может быть предусмотрено наличие необязательной четвертой зоны 237(иногда именуемой зоной резервуара), служащей в качестве резервуара для капиллярного растекания,что также является известным уровнем техники. Четвертая зона 237 содержит относительно более толстую гигроскопичную бумагу и может быть закрыта крышкой 217b. В предпочтительном варианте под зонами 231, 235 и 237 лежит тонкая липкая полоска (на чертеже не показана), которая удерживает сорбирующие материалы на месте. Липкая полоска положена поверх картона 215. Второй сорбирующий материал 232 также может быть выполнен из множества материалов и предпочтительно содержит две зоны 261, 263. Первая зона 261 (иногда именуемая зоной фильтра) содержит фильтр или подкладку 262 и первый участок тонкой мембраны или сорбирующего или абсорбирующего материала 232, обычно выполненный из нитроцеллюлозы с подложкой (на чертеже не показана). Первая зона 261 продолжается до второй зоны 263. По меньшей мере часть первой зоны обычно закрыта бумажным защитным покрытием 217 с. Вторая зона 263 содержит второй участок тонкой мембраны 232, который находится в контакте со второй зоной 233 первого сорбирующего материала 230. Второй сорбирующий материал 232 лежит под первым сорбирующим материалом 230 таким образом, что мембраны находятся в контакте друг с другом, и поэтому линия 250 проведения теста фактически расположена между мембранами. Следовательно, линия 250 проведения теста может быть напечатана на второй зоне 263 второго сорбирующий материала 232 вместо ее печати на второй зоне 233 первого сорбирующий материала 230 или в дополнение к этому. В предпочтительном варианте под зонами 261 и 263 лежит тонкая липкая полоска (на чертеже не показана), которая удерживает второй сорбирующий материал на месте. Липкая полоска положена поверх картона 215. Понятно, что устройство 210 для тестов из фиг. 10 может быть видоизменено, при этом предполагают, что оно может иметь любую из конфигураций согласно вышеописанным вариантам осуществления изобретения. Пользователь использует комплект для тестов из фиг. 10 следующим образом: он открывает блистерную упаковку (на чертеже не показана), содержащую все элементы комплекта, удаляет бумажное защитное покрытие (при его наличии) с устройства 210 для тестов, открывая упаковку со спиртовым протирочным тампоном и протирает его/ее палец спиртовым протирочным тампоном 204, берет ланцет 201 и прокалывает его/ее протертый палец для извлечения крови. Затем, предпочтительно используя петлю 203, пользователь собирает каплю крови (например, объемом 5 мкл) и помещает каплю крови на незакрытый участок зоны 261 второго сорбирующего материала 232. Затем пользователь может открыть упаковку с лейкопластырем и наклеить лейкопластырь 205 на проколотый палец. Затем пользователь открывает упаковку 202 с буферным раствором и выдавливает одну каплю (например, объемом 30 мкл) буферного раствора на то же самое место, что и кровь, в зоне 261. После ожидания в течение желательного промежутка времени (равного, например, 5 мин) для того, чтобы кровь мигрировала в зону 263 проведения теста, пользователь добавляет до двух капель (например, 60 мкл) буферного раствора в первую зону 231 из первого сорбирующего материала 230. После ожидания в течение желательного промежутка времени (равного, например, 7 мин) после того, как в зону 231 был добавлен буферный раствор, производят осмотр линии 250 проведения теста и контрольной линии 260. "Положительный" результат теста указывает появление цвета на обеих линиях: на линии 250 проведения теста и на контрольной линии 260."Отрицательный" результат теста указывает появление цвета на контрольной линии 260 и отсутствие цвета на линии 250 проведения теста. Если на контрольной линии 260 цвет не появляется, то результаты теста являются недостоверными.- 11012193 Согласно другим вариантам осуществления настоящего изобретения, вместо создания в ячейке для тестов сухого осадка конъюгата, содержащего желательные антигены или антитела с присоединенными окрашенными маркерами, ячейка для тестов вообще не содержит сухого конъюгата. Вместо этого используется (влажная) подсистема "буферный раствор - конъюгат", и подкладка с конъюгатом (обозначенная на фиг. 1 А номером позиции 31b) не требуется, поэтому тонкая полоска из нитроцеллюлозы или иного сорбирующего материала может быть непосредственно соединена с фильтром (обозначенным на фиг. 1 А номером позиции 31 а). Таким образом, после того как проба была введена во второе отверстие в корпусе и была обеспечена возможность ее миграции в область проведения теста, в первое отверстие в корпусе вводят подсистему "буферный раствор - конъюгат" и аналогичным образом обеспечивают возможность ее миграции в область проведения теста. Согласно другим вариантам осуществления настоящего изобретения, вместо смотрового окна,имеющегося на верхней поверхности корпуса, окно создано на нижней поверхности корпуса. Для специалистов в данной области техники понятно, что варианты осуществления настоящего изобретения могут быть реализованы с использованием множества различных материалов. Например,сорбирующий материал (сорбирующие материалы), который обычно содержит очень тонкую, инертную пленку, полоску, лист или мембрану, может быть сформирован из нитроцеллюлозы, фильтровальной бумаги, диоксида кремния или, например, из микропористых или микрозернистый тканых или нетканых материалов, или из их комбинации. Множество типов пригодных материалов и их комбинаций описано в патенте США 4960691, выданном Гордону и др. (Gordon et al.) и в патенте США 4956275, выданному Зуку и др. (Zuk et al.), оба из которых тем самым включены сюда в полном объеме путем ссылки. Как описано выше, нитроцеллюлоза или другие сорбирующие материалы часто снабжены тонкой непористой инертной пластмассовой подложкой. Таким образом, согласно еще одним дополнительным вариантам осуществления настоящего изобретения, значения толщины и длины первого и второго сорбирующих материалов и сами эти материалы выбраны таким образом, чтобы обеспечить согласование того момента времени, когда жидкая проба и жидкий буферный раствор (или подсистема "буферный раствор - конъюгат") достигают области проведения теста. За счет обеспечения отдельных путей миграции для пробы/вещества, определяемого при анализе, и для буферного раствора или подсистемы "буферный раствор - конъюгат", материалы также могут быть выбраны таким образом, чтобы повысить чувствительность системы. Аналогичным образом, понятно, что сорбирующему материалу может быть придана любая из множества форм и что он может иметь любые из множества размеров, что является известным в данной области техники. Таким образом, для содействия ускорению капиллярного растекания сорбирующий материал может быть выполнен в форме ключа с полоской, имеющей меньшую ширину в первом отверстии,в которое поступает буферный раствор, и в области проведения теста и контрольной области, и более значительную ширину в зоне резервуара. Такое устройство продемонстрировано в патенте США 5989921, выданном Чарльтону и др. (Charlton et al.), который тем самым включен сюда в полном объеме путем ссылки. Как правило, в любом случае индикаторная полоска является существенно большей по длине, чем по ширине, и существенно большей по ширине, чем по толщине. На самом деле, по меньшей мере, в некоторых вариантах осуществления настоящего изобретения полоска в зоне проведения теста должна быть тонкой, как бумага, (например, иметь толщину, равную 0,1 мм) и достаточно прозрачной для того, чтобы линия для проведения теста и контрольная линия могли быть легко видимыми через индикаторную полоску. Кроме того, корпус и сорбирующий материал могут быть встроены в открытую платформу, обеспечивающую растекание в боковом направлении, в которой полимер, полученный способом литья под давлением, снабжен микроскопическими направляющими стойками, которые обеспечивают возможность точного контроля потока путем изменения высоты, диаметра, формы направляющих стоек и/или расстояния между ними. В такой платформе используют, по существу, одинаковый материал для корпуса и для сорбирующего материала, обеспечивающего капиллярное растекание, который продается фирмой"Amic AB", г. Упсала, Швеция. См., например, Интернет-сайт www.amic.se. Поскольку полимер, полученный способом литья под давлением, как правило, может быть прозрачным, то весь корпус можно считать "окном", через которое могут быть видны линии/участки для проведения теста и контрольные линии/участки. Также понятно, что в зависимости от типа создаваемого теста (например, на беременность, на ВИЧ,на туберкулез (ТБ), на прион, на наркотики по анализу мочи, на маркеры болезней сердца, на маркеры рака, на болезнь Чагаса (американский трипаносомоз), на хламидии, на зубные бактерии (SM/LC), на грипп А, на грипп В, на аденовирус, на ротавирус, на стрептококк группы А, на другие бактерии или вирусы и т.д., и даже и для применений в ветеринарии, таких как, например, тест на парвовирус собак(CPV), на вирус иммунодефицита кошек (FIV), на вирус лейкемии кошек (FeLV) и на сердечного червя),интересующее антитело (или антиген) будет различным, и, следовательно, антиген (или антитело), используемый в индикаторной полоске, должен быть подобран соответствующим образом. Также соответствующим образом должен быть подобран антиген или антитело в конъюгате. В некоторых случаях (например, при тестах на ВИЧ) в индикаторной полоске может быть использован антиген, идентичный ан- 12012193 тигену в конъюгате, так как связывающий участок антитела к ВИЧ связывается с антигеном ВИЧ в области проведения теста и, тем не менее, обеспечивает наличие дополнительных связывающих участков для связывания с антигеном-конъюгатом, в то время как в других случаях могут потребоваться различные антигены. По аналогии с этим, понятно, что в зависимости от типа создаваемого теста контрольная область, при ее наличии, также должна быть специально приспособлена соответствующим образом. Таким образом, например, в тесте на обнаружение антител к ВИЧ, в котором лигандом, идентифицируемым в зоне проведения теста, являются антитела к ВИЧ 1 и/или ВИЧ 2, антигеном в зоне проведения теста может являться смесь пептидов ВИЧ 1 (например, gp41/gp120) и ВИЧ 2 (gp36) и/или рекомбинантных антигенов. Конъюгатом может являться окрашенный латекс или коллоидное золото, конъюгированное с протеином А, с протеином A/G, с антителами к иммуноглобулинам IgG/IgM человека, с пептидами или с рекомбинантными антигенами. Для специалистов в данной области техники также понятно, что маркер конъюгата может иметь множество разновидностей, в том числе, различные типы золей металлов, окрашенный латекс, любой из различных ферментов и т.д. Несмотря на то, что предпочтительный вариант осуществления настоящего изобретения обеспечивает сигнал обнаружения, легко видимый для невооруженного глаза, понятно, что настоящее изобретение охватывает собой и другие маркеры, которые могут быть обнаружены при помощи ультрафиолетового излучения или иными способами, например, способом флюороскопии. Таким образом, понятно, что может быть создана система, в которой используют ячейки для тестов из настоящего изобретения, считываемые автоматическим считывающим устройством, таким как, например,флюороскопическое или цифровое считывающее устройство. Настоящее изобретение обеспечивает улучшенную чувствительность, не включая в себя специфичность анализа. Основными причинами улучшенной чувствительности являются улучшенная миграция пробы в зону проведения теста вследствие различного пути миграции и эффективное связывание вещества, определяемого при анализе, со связывающим участком в зоне проведения теста до реакции конъюгированного маркера с комплексом в зоне проведения теста. Например, в случае теста на ВИЧ специфические для ВИЧ антитела в пробах сыворотки крови, нанесенные на вторую полоску сорбента, будет мигрировать в зону проведения теста и будут связываться с линией (линиями) проведения теста на ВИЧ. Никакой иной иммуноглобулин G (IgG) в крови не будет связываться с антигенами ВИЧ, иммобилизированными в зоне проведения теста. При добавлении буферного раствора на первую полоску сорбента для того, чтобы вызвать миграцию конъюгата протеина А с латексом или с золотом в зону проведения теста,конъюгат протеина А будет связываться с FC-участком антител ВИЧ, которые уже являются захваченными пептидами ВИЧ на линии проведения теста. Поскольку связывание между протеином А и FCучастком антитела к ВИЧ является очень сильным, то необходимо наличие всего лишь небольшого количества антител к ВИЧ для их регистрации. Это является отличием от традиционных систем для тестов на ВИЧ с растеканием в боковом направлении, в которых весь иммуноглобулин IgG человека (содержащий антитела к ВИЧ) в пробе крови является связанным с протеином А перед миграцией к линии проведения теста, поскольку протеин А неспецифически связывает весь IgG. Таким образом, весь комплекс"протеин А, IgG, золото/латекс" будет мигрировать к линии проведения теста, которая содержит антигены ВИЧ. Только затем антитела к ВИЧ, протеин А, конъюгат золо/латекс связываются с антигенами ВИЧ. Однако вследствие наличия в пробах большого количества неродственного иммуноглобулина IgG и малого количества антител к ВИЧ имеется риск того, что с протеином А будет связываться недостаточное количество антител к ВИЧ, и что цветная линия не будет видна. Повышенная чувствительность, обеспечиваемая настоящим изобретением, была протестирована путем сравнения результатов иммунологических анализов на туберкулез (ТБ) согласно настоящему изобретению ("Новое поколение"), что, по существу, показано на фиг. 10, с результатами, полученными стандартными средствами (ТВ Stat-Pak II) для иммунологических экспресс-анализов на туберкулез (ТВ). Было создано шестнадцать проб, по две пробы для каждого из восьми различных уровней содержания антител (32, 8, 2, 1, 1/2, 1/4, 1/8 ед./мл, и контрольная проба 0 ед./мл). Результаты сравнительного тестирования показаны на фиг. 11, при этом результаты иммунологических анализов согласно настоящему изобретению продемонстрировали, по меньшей мере, восьмикратное повышение чувствительности относительно стандартных тестов из известного уровня техники (то есть при иммунологическом анализе согласно настоящему изобретению положительный результат был зарегистрирован при концентрации 1/4 ед./мл, а при иммунологическом анализе из известного уровня техники сомнительный результат был зарегистрирован при концентрации 2 ед./мл). Кроме того, двадцать тестов отрицательных проб не дали каких-либо ложных положительных результатов. Повышенная чувствительность согласно настоящему изобретению была также протестирована путем сравнении результатов иммунологических анализов на ВИЧ 1 и ВИЧ 2 согласно настоящему изобретению ("тест на ВИЧ нового поколения"), которые, по существу, показаны на фиг. 10, с результатами,полученными стандартными средствами (HIV Stat-Pak) для иммунологических экспресс-анализов на ВИЧ. Были созданы пробы с различными уровнями разбавления (1:64, 1:128, 1:256, 1:512, 1:1024, 1:2048,1:4096; 1:8192 для ВИЧ 1 и 1:4, 1:8, 1:16, 1:32, 1:64, 1:128, 1:256, 1:512, 1:1024, 1:2048 для ВИЧ 2). Результаты сравнительного тестирования показаны на фиг. 12, при этом результаты иммунологических анали- 13012193 зов согласно настоящему изобретению свидетельствуют приблизительно о четырехкратном увеличении чувствительности по сравнению со стандартными тестами из известного уровеня техники (то есть для ВИЧ 1 при иммунологическом анализе согласно настоящему изобретению положительный результат с самой высокой чувствительностью зарегистрирован при разбавлении 1:4096, а при иммунологическом анализе из известного уровня техники положительный результат с самой высокой чувствительностью зарегистрирован при разбавлении 1:1024; и для ВИЧ 2 при иммунологическом анализе согласно настоящему изобретению положительный результат с самой высокой чувствительностью зарегистрирован при разбавлении 1:512, а при иммунологическом анализе из известного уровня техники положительный результат с самой высокой чувствительностью зарегистрирован при разбавлении 1:128). Кроме того, сто двадцать тестов с отрицательными пробами при тестах на ВИЧ нового поколения продемонстрировали,что процент ложных положительных результатов составляет менее 1%. Полагают, что устройства для иммунологического анализа на основе индикаторной полоски согласно настоящему изобретению могут обеспечить уменьшение времени, затрачиваемого на анализ, по сравнению с устройствами из известного уровня техники. В частности, известно, что в обычных хроматографических тестах на полосках кровь, кал или слюна будут мигрировать очень медленно. Однако поскольку в устройствах для иммунологического анализа с индикаторной полоской согласно настоящему изобретению обеспечен отдельный путь миграции для пробы, то используемый сорбирующий материал может быть выбран специально для представляющего интерес теста для того, чтобы обеспечить возможность быстрой миграции, не беспокоясь при этом о миграции конъюгата, и, следовательно, время анализа может быть очень быстрым по сравнению с известным уровнем техники. Например, первый сорбирующий материал 30, 30', 30", 130, 230 может быть выполнен из материала, имеющего относительно малые поры (например, менее 20 мкм, а в наиболее предпочтительном варианте 3-15 мкм, но эти значения не являются ограничивающим признаком), в то время как второй сорбирующий материал 32, 32', 32", 132,232 может быть выполнен из материала, имеющего относительно большие поры (например, более чем 20 мкм, а в наиболее предпочтительном варианте 25-40 мкм, но эти значения не являются ограничивающим признаком). Таким образом, проба с веществом, определяемым при анализе, будет способна более легко мигрировать вниз по ее пути, в то время как линия высокочувствительной индикаторной полоски создана на первом сорбирующем материале с относительно малыми порами. Кроме того, как упомянуто выше,путем обеспечения большего размера пор во втором сорбирующем материале, чем размер пор в первом сорбирующем материале, миграция пробы из второго сорбирующего материала в первый сорбирующий материал является желательным образом ограниченной. Примерами полосок сорбирующего материала (мембран), имеющих относительно малые поры, являются, в том числе, следующие: MDI-08 (8 мкм), MDI-10 (10 мкм), MDI-15 (15 мкм), производимые фирмой "Advanced Microdevice of Ambala", Индия, и SP (3 мкм), FP (5 мкм) и RP (8 мкм), производимые фирмой "Whatman, Inc.", г. Флорал Парк, штат Нью-Джерси, США. Примером полоски сорбирующего материала, имеющего относительно большие поры, является полоска Р 40 (30 мкм), производимая фирмой "SchleicherSchuell Bioscience, Inc." г. Кин, штат Нью-Гемпшир, США. Кроме того, все же полагают, что миграция конъюгированных частиц в отсутствии пробы обеспечивает более однородную и согласованную миграцию, приводя к улучшению фонового клиренса. Другое преимущество устройств для иммунологического анализа на основе индикаторной полоски согласно настоящему изобретению состоит в том, что в них преодолены проблемы агрегации/агглютинации между маркерным конъюгатом и веществом в пробе, определяемым при анализе, что представляет собой главную проблему для аналитов большого размера (например, бактерий) при традиционных хроматографических иммунологических анализах. На известном уровне техники миграция большого комплекса бактерий с конъюгированными антителами к линии проведения теста затруднена. В результате, комплекс стремится оставаться на дне индикаторной полоски или в подкладке. В настоящем изобретении бактерии, имеющиеся в пробе, поступают (после фильтрации) непосредственно в область проведения теста, и иммобилизируются в ней, в то время как маркерный конъюгат свободно мигрирует без пробы в область проведения теста. Когда маркерный конъюгат достигает области проведения теста,то бактерии, уже захваченные иммобилизированным антителом в области проведения теста, связываются с конъюгатом. Таким образом, система из настоящего изобретения является чрезвычайно чувствительной и точной. Еще одним преимуществом настоящего изобретения является способность обеспечивать тесты на множество инфекционных заболеваний с высокой чувствительностью и без каких-либо компромиссов относительно специфичности, обусловленной перекрестной реактивностью или уменьшением чувствительности, для множества веществ, определяемых при анализе в том случае, когда они напечатаны в виде отдельных линий в зоне проведения теста. В частности при традиционных анализах с растеканием в боковом направлении проба и конъюгат мигрируют вместе. Если устройства из известного уровня техники снабжены множеством линий проведения теста, то каждая линия может удерживать вещество, определяемое при анализе, или вступать в перекрестную реакцию с веществом, определяемым при анализе, поэтому видимый результат на последующих линиях становится все более и более слабым. В отличие от этого, в настоящем изобретении пробы, содержащие несколько веществ, определяемых при анализе,- 14012193 мигрируют в зону проведения теста без конъюгата и одновременно доходят до нескольких линий. Таким образом, вещества, определяемые при анализе, могут в равной степени связываться с несколькими линиями, поэтому может поддерживаться одинаковый уровень чувствительности. Затем вводят конъюгат по иному пути миграции, и он может связываться с комплексами, уже иммобилизированными на линиях. Например, для одновременного обнаружения антител к ВИЧ и туберкулезу (ТБ) в пробе пациента, антигены ВИЧ и антигены туберкулеза (ТБ) являются иммобилизированными в виде отдельных линий в зоне проведения теста, и пробу подают на одну полоску для миграции и для связывания в зоне проведения теста. Затем на другую полоску добавляют буферный раствор, обеспечивая для золота или латекса протеина А возможность миграции и связывания с комплексом антиген-антитело ВИЧ и с комплексом антиген-антитело туберкулеза (ТБ). Вследствие высокой чувствительности теста, при наличии туберкулеза(ТБ) он будет зарегистрирован. Это является важным потому, что у больных, зараженных одновременно ВИЧ и туберкулезом (ТБ), титр антител для туберкулеза (ТБ) имеет тенденцию быть низким. Согласно другому объекту настоящего изобретения, в котором обеспечены тесты для множества инфекционных заболеваний (например, ВИЧ и туберкулез), могут использоваться частицы латекса различного цвета для конъюгирования с различными антигенами или антителами, имеющимися в подкладке с конъюгатом или в буферном растворе. В результате, в зоне проведения теста будут появляться линии различного цвета, причем один цвет (например, красный) соответствует первому заболеванию (например, ВИЧ), а второй цвет (например, синий) соответствует второму заболеванию (например, туберкулезу). Для специалистов в данной области техники понятно, что время ожидания между подачей пробы на одну из полосок из сорбирующего материала и подачей буферного раствора на другую полоску из сорбирующего материала может изменяться в зависимости от вязкости пробы и от различных свойств полоски из сорбирующего материала, на которую поступает проба, в том числе, например, от размера пор и от длины полоски. Поэтому устройство для тестов обычно содержит инструкции, уведомляющие пользователя о необходимости ожидания в течение заранее заданного промежутка времени (например, 5 мин) после добавления пробы (и необязательного буферный раствор) на одну полоску перед добавлением буферного раствора на другую полоску. Для получения оптимальных результатов в наибольшем проценте случаев время ожидания выбрано существенно более длительным, чем реально необходимое. Таким образом, согласно другому объекту настоящего изобретения, для уменьшения времени ожидания область проведения теста в любом из вышеописанных вариантов осуществления настоящего изобретения снабжена видимым пищевым красителем или иным растворимым в воде красителем. Когда в устройство для тестов подана проба и необязательный буферный раствор, то после миграции пробы в область проведения теста краситель в области проведения теста становится разбавленным и исчезает для невооруженного глаза, посредством чего обеспечивают видимый индикатор того, что на другую полоску может быть надлежащим образом добавлен буферный раствор, не влияющий на эффективность теста. В устройстве для тестов, снабженном видимым красителем в области проведения теста, пользователю дают инструкции, чтобы он добавлял буферный раствор после того, как исчезнет цвет в области проведения теста. Таким образом, согласно одному из способов из настоящего изобретения, устройство для тестов, предназначенное для определения наличия лиганда в жидкой пробе, снабжено областью проведения теста, содержащей иммобилизированный лигандосвязующий механизм и видимый растворимый индикатор. В устройство для тестов подают пробу и рассматривают область проведения теста, наблюдая исчезновение видимого индикатора. После этого в устройство для тестов подают раствор (буферный раствор). Затем, по истечении некоторого времени может быть произведен осмотр области проведения теста для определения показания о наличии или об отсутствии этого лиганда в пробе. На фиг. 13 А-13G показаны схемы, составленные из фотографий/инструктивной информации, на которых показано изделие, представляющее собой кассету для тестов на ВИЧ 1/2 согласно настоящему изобретению, в которых использован видимый краситель в области проведения теста. Изделие, представляющее собой кассету для тестов, сконструировано, по существу, в соответствии с любым из вышеописанных вариантов осуществления изобретения и снабжено пластмассовым корпусом кассеты с четырьмя отверстиями или окнами. Первое из этих четырех отверстий промаркировано как S+B и предназначено для приема пробы, подвергаемой тесту, плюс буферного раствора. Второе из этих четырех отверстий промаркировано как В и предназначено для приема дополнительного буферного раствора. Третье из этих четырех отверстий промаркировано цифрами 1, 2, 3, 4, и 5, и в нем имеются линии проведения теста,соответствующие пяти различными антигенам или пептидам ВИЧ (которыми предпочтительно являются,соответственно, р 24, gp41, gp120, gp160 и gp36). В четвертом отверстии, промаркированном как С, имеется контрольная линия. Линии проведения теста, появляющиеся в третьем отверстии, снабжены цветным красителем (например, синего цвета) для того, чтобы они были видимыми. Контрольная линия, появляющаяся в четвертом отверстии, также снабжена цветным красителем (например, зеленного цвета) для того, чтобы она была видимой. Устройство, показанное на фиг. 13 А, используют следующим образом: добавляют в предпочтительном варианте приблизительно 10 мкл (микролитров) сыворотки или крови в лунку для пробы, промаркированную как S+B. Затем, как видно на фиг. 13 В, добавляют в предпочтительном варианте прибли- 15012193 зительно 30 мкл буферного раствора в ту же самую лунку для пробы. Миграция пробы (обычно при помощи буферного раствора) в зону проведения теста вызывает рассеяние красителя на линиях проведения теста и на контрольной линии. Исчезновение красителя с линий подтверждает тот факт, что проба достигла области проведения теста. В этот момент времени, и как показано на фиг. 13 С, добавляют в предпочтительном варианте приблизительно 90 мкл буферного раствора в отверстие, промаркированное как В, для того, чтобы вызвать миграцию маркера конъюгата в область проведения теста. По истечении некоторого промежутка времени может быть произведено считывание результатов. Четыре примера результатов показаны на фиг. 13D-13G. На фиг. 13D видна только лишь контрольная линия С, что указывает достоверный результат, а именно отрицательный результат теста пробы на антитела ВИЧ 1 и ВИЧ 2. На фиг. 13 Е видна контрольная линия и линии 1, 2, 3 и 4, что указывает достоверный результат, а именно положительный результат теста пробы на наличие четырех различных антител типа ВИЧ 1, но отрицательный результат теста пробы на антитела типа ВИЧ 2. На фиг. 13F видна контрольная линия и линия 5,что указывает достоверный результат, а именно положительный результат теста пробы на антитела типа ВИЧ 2, но отрицательный результат теста пробы на наличие четырех различных антител типа ВИЧ 1. На фиг. 13G видна контрольная линия и все линии 1-5, что указывает достоверный результат, а именно положительный результат теста пробы на наличие четырех различных антител типа ВИЧ 1 и на наличие антител типа ВИЧ 2. Следует отметить, что если контрольная линия С не видна, то результаты теста не интерпретируют как являющийся достоверным. Также следует отметить, что возможна ситуация, когда положительный результат могут указывать только одна, две или три линии из линий 1-4, что можно увидеть со ссылкой на фиг. 15A-15D, поскольку проба не обязательно должна содержать все четыре различных антитела типа ВИЧ 1 или ни одного из них. На фиг. 14 А-14G показаны схемы, составленные из фотографий/инструктивной информации, на которых показано изделие, представляющее собой тест-полоску для тестов на ВИЧ 1/2 согласно настоящему изобретению. Фиг. 14 А-14G полностью соответствуют рассмотренным выше фиг. 13A-13G, за исключением того, что изделие для тестов, показанное на фиг. 14 А-14G, не содержит пластмассовую кассету с окнами, а представляет собой изделие, выполненное в виде тест-полоски на картоне. На фиг. 15 А-15G показаны схемы, составленные из фотографий/инструктивной информации, на которых показано изделие, представляющее собой кассету для подтверждающих тестов на ВИЧ 1/2 согласно настоящему изобретению, в которой использован видимый краситель в области проведения теста. Изделие для подтверждающих тестов является, по существу, тем же самым, что и изделие, показанное на чертежах фиг. 13 А -фиг. 13G, и сконструировано, по существу, в соответствии с любым из вышеописанных вариантов осуществления изобретения, за исключением того, что изделие, показанное на фиг. 15 А 15G снабжено пластмассовым корпусом кассеты с пятью отверстиями или окнами вместо четырех, которые имеет изделие, показанное на фиг. 13 А-13G. Первое из этих пяти отверстий промаркировано какS+B и предназначено для приема тестируемой пробы плюс буферного раствора. Второе из этих пяти отверстий промаркировано как В и предназначено для приема дополнительного буферного раствора. Третье из этих пяти отверстий промаркировано как Т и соответствует линии проведения теста, имеющей все антигены или пептиды ВИЧ, содержащиеся в четвертом окне. Четвертое из этих пяти отверстий промаркировано цифрами 1, 2, 3, 4 и 5 и снабжено линиями проведения теста, соответствующими пяти различными антигенам или пептидами ВИЧ (которыми предпочтительном являются, соответственно, р 24,gp41, gp120, gp160 и gp36). Пятое отверстие, промаркированное как С, снабжено контрольной линией. Линии проведения теста, появляющиеся во втором и в третьем отверстиях, снабжены цветным красителем (например, синего цвета) для того, чтобы они были видимыми. Контрольная линия, появляющаяся в четвертом отверстии, также снабжена цветным красителем (например, зеленного цвета) для того, чтобы она была видимой. Изделие для массового обследования/подтверждающих тестов, показанное на фиг. 15 А-15G, используется тем же самым образом, как и изделие, показанное на фиг. 13 А-13G. Различие между изделиями состоит в том, что третье окно Т обеспечивает цифровой результат для массового обследования; то есть ответ "да" или "нет" относительно содержания антител к ВИЧ в пробе. В частности, поскольку линия Т проведения теста содержит комбинацию всех антигенов или пептидов, имеющихся на линиях 1-5 проведения теста, то она будет заметной в том случае, если будет наблюдаться любая из других линий 15 проведения теста. Линии 1-5 проведения теста обеспечивают детализацию установленного результата; то есть какое именно антитело или антитела ВИЧ 1 зарегистрировано/зарегистрированы и было ли зарегистрировано антитело ВИЧ 2. На фиг. 16 А-16 Е показаны фотографии результатов реальных тестов, полученные на тест-полосках для тестов на ВИЧ 1/2 согласно настоящему изобретению. Как видно на фиг. 16 А, видна контрольная линия и одна линия (gp36), что указывает достоверный результат теста пробы, дающей положительный результат теста на антитела типа ВИЧ 2. На фиг. 16 В показано, что видимыми являются следующие линии: контрольная линия и первая и пятая линии проведения теста, что указывает достоверный результат теста пробы, дающей положительный результат теста на антитела ВИЧ 1, связывающиеся с антигеном р 24, и на антитела типа ВИЧ 2 (которые связываются с антигеном gp36), и отрицательный результат теста на другие антитела ВИЧ 1. На фиг. 16 С показано, что видимыми являются контрольная линия и вторая- 16012193 линия проведения теста, что указывает достоверный результат теста пробы, дающей положительный результат теста на антитела ВИЧ 1, связывающиеся с антигеном gp41, и отрицательный результат теста на другие антитела ВИЧ 1 и антитела типа ВИЧ 2. На фиг. 16D показано, что видимыми являются следующие линии: контрольная линия и первая, вторая и четвертая линии проведения теста, что указывает достоверный результат теста пробы, дающей положительный результат теста на антитела ВИЧ 1, связывающиеся с антигенами gp24, gp41 и gp160, и отрицательный результат теста на другие антитела ВИЧ 1 и антитела типа ВИЧ 2. На фиг. 16 Е показано, что видимыми являются следующие линии: контрольная линия и линии проведения теста с первой по пятую, что указывает достоверный результат теста пробы,дающей положительный результат теста на все тестируемые антитела ВИЧ 1 и антитела ВИЧ 2. Пример 1. Тест на ВИЧ. Подготовка полоски 1, предназначенной для приема пробы и буферного раствора. Индикаторная полоска для сбора и транспортировки пробы была подготовлена следующим образом. Мембрана из нитроцеллюлозы (525 мм) с размером пор 20-30 мкм (произведенная фирмой "Whatman Inc.", США) была ламинирована на пластиковую карточку. Подкладка для пробы из целлюлозной бумаги (произведенной фирмой "SS", Германия) была обработана забуференным фосфатом физиологическим раствором (PBS),8.4 и NP40 и прикреплена к мембране из нитроцеллюлозы. Та же самая процедура была использована для изготовления множества индикаторных полосок 1. Подготовка полоски 2, предназначенной для приема только буферного раствора и имеющей зону конъюгата и линии проведения теста и контрольную линию. Индикаторная полоска для обнаружения антител к ВИЧ 1 и ВИЧ 2 была подготовлена следующим образом. Синтетические пептиды ВИЧ 1 gp41,gp120 и синтетический пептид ВИЧ 2 gp36 были обработаны биотином, а затем смешаны с авидином(произведенным фирмой "Zymed, Inc.", США). Эта смесь была отфильтрована через фильтр с размером пор 0,2 мкм и иммобилизирована в концентрации 0,25-0,50 мг/мл на мембрану из нитроцеллюлозы с размером пор 10-15 мкм (произведенную фирмой "MDI Ltd.", г. Амбелла, Индия) для использования в качестве линии проведения теста с применением печатающего устройства ISO-Flow (произведенного фирмой "Imagine Technology, Inc.", США). Протеин А (произведенный фирмой "Zymed, Inc.", США) в концентрации 0,25 мг/мл, предназначенный для использования в качестве контрольной линии, был иммобилизирован тем же самым способом. Мембрана была высушена в течение 1 ч при температуре 37 С. Затем мембрана была ламинирована на мембранную подложку (произведенную фирмой "GL, Inc.",США). Подкладка для конъюгата была подготовлена с использованием пористой полиэфирной матрицы(произведенной фирмой "Alstrom, Inc." США). На подкладку был распылен протеин А (произведенный фирмой "Zymed Inc.", США), который был конъюгирован с пурпурными частицами коллоидного золота размером приблизительно 40 нм и OD 60, повторно суспензированный с буферным раствором конъюгата(50 мМ PBS, сахароза, бычий сывороточный альбумин (BSA), VPA, Tween 20) и высушенный при температуре 37 С в течение 1 ч. Индикаторная полоска (размером 7,262 мм) была подготовлена путем присоединения подкладки с конъюгированным золотом, подкладки для пробы (произведенной фирмой "SSInc.", Германия) и подкладки для стока (произведенной фирмой "SS Inc.", Германия) к мембране из нитроцеллюлозы, присоединенной к ламинированной карте. Та же самая процедура была использована для изготовления множества индикаторных полосок 2. Монтаж полоски 1 и полоски 2 в кассете. Полоска 2 (размером 7,262 мм) была помещена в нижнюю часть кассеты таким образом, что ее ламинированная карта находится на дне, а подкладка для конъюгата, подкладка для пробы, линии проведения теста и контрольная линия обращены лицевой стороной вверх. Затем, полоска 1 была помещена в нижнюю часть кассеты. Полоска 1 была размещена таким образом, что она соприкасалась с полоской 2 в месте расположения области проведения теста с мембраной нитроцеллюлозы полоски 1, соприкасаясь с мембраной из нитроцеллюлозы полоски 2. Затем на нижнюю часть кассеты была установлена верхняя часть кассеты, имеющая отдельные отверстия для пробы и буферного раствора и окно, расположенное над местом расположения области проведения теста и контрольной области. Та же самая процедура была использована для изготовления множества сборочных единиц (именуемых ниже как сборочные единицы для тестов на ВИЧ 1/2 типа Chembio DPP(DPP - платформа с двумя путями. Процедура теста. Через отверстие для пробы было добавлено 5 мкл сыворотки/крови, и к ней была немедленно добавлена 1 капля (40-50 мкл) буферного раствора (PBS, рН 8,5-9,5, сыворотка цыплят,EDTA, Tween 20) через то же самое отверстие. После ожидания в течение 1-2 мин до тех пор, пока проба не достигнет зоны проведения теста и не исчезнут цветные линии (контроль качества), три или четыре капли (приблизительно 130-150 мкл) того же самого буферного раствора было добавлено через отверстие для буферного раствора. Через 15 мин было произведено считывание результатов теста. Появление двух розовых линий (тестовой и контрольной) указывает наличие положительного результат. Появление одной полоски (контрольной) указывает наличие отрицательного результата. Отсутствие появления полосок указывало бы наличие недостоверного результата. Результаты теста. Было проведено тестирование серийно выпускаемой панели (PRZ-204), предназначенной для смешанных анализов на ВИЧ 1 и ВИЧ 2, которая произведена фирмой "BBI Inc.", США, на- 17012193 сборочных единицах, подготовленных и собранных описанным выше способом, со следующими результатами. Во всех пробах правильный результат был обнаружен посредством тестов Chembio DPP ВИЧ 1/2 иELIA 1/2 фирмы "Abbott". Результат для пробы 15 не был определен посредством обоих тестов "Western Blot", результаты которых были интерпретированы с использованием критериев, выработанных Ассоциацией руководителей лабораторий органов здравоохранения штатов и территорий/Центром по контролю за заболеваемостью, США (ASTPHLD/CDC) (журнал "Еженедельный отчет о заболеваемости и смертности" (MMWR), т. 38, выпуск S-7, 1989 г.), но являлся положительным при тестах Chembio DPP ВИЧ 1/2 и ELIA 1/2 фирмы "Abbott". Пример 2. Микобактериальный туберкулез (ТБ). Для обнаружения антител к туберкулезу (ТБ) были подготовлены устройства для тестов, такие же как и в примере 1, но только с видоизмененной полоской 2. Полоска 2 была видоизменена путем получения смеси рекомбинантных антигенов (F10, Е 6, Р 10, 14, 16) туберкулеза (ТБ) с концентрацией 1,0 мг/мл вместо пептидов ВИЧ и путем иммобилизации рекомбинантных антигенов туберкулеза (ТБ) с плотностью 0,5 мкл/см на линии проведения теста на мембране для создания первой линии (Т 1) проведения теста. В области проведения теста также была иммобилизирована вторая линия (Т 2) проведения теста из антигена туберкулеза (ТБ) липоарабинманнана (Lipoarabinmannan, LAM) с концентрацией 0,05 мг/мл и иммобилизированного с плотностью 0,5 мкл/см. В качестве контрольной линии был иммобилизирован протеин А, разбавленный PBS 7.4 с концентрацией 0,25 мг/мл. На подкладку для конъюгата был нанесен протеин A/G (произведенный фирмой "Pierce", США) и антитела к иммуноглобулину IgM человека (произведенные фирмой "Sigma", США), конъюгированные с пурпурными частицами коллоидного золота размером, приблизительно, 40 нм. Процедура теста. Процедура теста для теста на туберкулез (ТБ) была той же самой, что и в примере 1, за исключением того, что объем пробы составлял 10 мкл сыворотки. Результаты теста. Была произведена оценка, в общей сложности, 300 коммерческих проб на туберкулез (ТБ) (произведенные фирмой "Zeptometrix Inc.", США) посредством теста DPP на туберкулез. Все положительные пробы имели положительный результат на культуре, но некоторые из проб были отрицательными по мазку и одновременно зараженными ВИЧ. На этих эндемических пробах были достигнуты значения общей чувствительности и специфичности, равные, соответственно, 75 и 90%. Пример 3. Тест-полоска для подтверждающих тестов на ВИЧ. Устройства для тестов в виде подтверждающих индикаторных полосок для обнаружения антител ВИЧ 1 и ВИЧ 2 были подготовлены так же, как и в примере 1. Однако полоска 1 и полоска 2 были прикреплены с использованием клея (произведенного фирмой "GL Inc.", США) на ламинированной карте без какого-либо пластмассового корпуса (то есть в виде "тест-полоски" ("dipstick". В качестве пяти различных линий в области проведения теста были иммобилизированы пять различных антигенов ВИЧ 1 (р 24, gp41, gp120, gp160) и ВИЧ 2 (gp36) (с концентрацией 0,25-0,50 мг/мл). Этими антигенами являлись рекомбинантные синтетические пептиды и нативные антигены. В качестве контрольной линии был иммобилизирован протеин А, разбавленный PBS 7.4 до концентрации 0,25 мг/мл. На подкладку для конъюгата был распылен протеин А (произведенный фирмой "Zymed", США), конъюгированный с пур- 18012193 пурными частицами коллоидного золота размером приблизительно 40 нм, и был использован в качестве системы обнаружения. Процедура теста. Процедура теста была той же самой, что и в примере 1, за исключением того, что использовались значения объема пробы, равные 10 мкл сыворотки. Результаты теста. При этом анализе была произведена оценка коммерческих проб панели ВИЧ(произведенных фирмами "BBI Inc.", США, "Zeptometrix Inc.", США и "Teragenix Inc.", США). Результаты показали, что подтверждающий тест DPP на ВИЧ обеспечил правильно обнаружение проб ВИЧ 1 и ВИЧ 2 и имел 100%-ную корреляцию с тестами методом вестерн-блоттинга (Western Blot) и EIA. Пример 4. Тест на ВИЧ. Были подготовлены устройства для тестов, по существу, идентичные устройствам для тестов из примера 1, а отличие состояло в том, что в каждом тесте полоска 1 была выполнена более длинной,поэтому полоска 1 и полоска 2 имели конфигурацию не в форме буквы Т, а в форме знака +. Результаты были такими же, как и в примере 1. Пример 5. Тест на ВИЧ. Были подготовлены устройства для тестов, по существу, такие же, как и в примере 1, за исключением того, что линия проведения теста и контрольная линия были нанесены на полоску 1 вместо полоски 2. Результаты были такими же, как и в примере 1. Пример 6. Тест на ВИЧ. Были подготовлены устройства для тестов, по существу, такие же, как и в примере 1, за исключением того, что в области проведения теста на линии проведения теста было иммобилизировано поликлональное антитело к антигену ВИЧ p24 и что моноклональное антитело к антигену ВИЧ p24 было конъюгировано с коллоидным золотом. Результаты показали, что в пробах сыворотки может быть зарегистрирован уровень содержания антигена p24 порядка пикограмма. Пример 7. Бактерии лептоспиры (Leptospira). Были подготовлены устройства для тестов, по существу, такие же, как и в примере 1, за исключением того, что в области проведения теста в качестве линии проведения теста были смешаны и иммобилизированы четыре рекомбинантных антигена lij (А, В, С, D). В качестве конъюгата на подкладку для конъюгата был нанесен протеин A/G (произведенный фирмой "Проникают", США), и антитела к иммуноглобулину IgM человека (произведенные фирмой "Сигма", США), конъюгированные с пурпурными частицами коллоидного золота размером приблизительно 40 нм. При тестировании более чем 300 эндемических проб из Бразилии и Таиланда была получена полная чувствительность, равная приблизительно 70% для проб острой фазы, и равная приблизительно 90% для проб фазы выздоровления, и специфичность, равная приблизительно 95%. Здесь были описаны и проиллюстрированы несколько вариантов осуществления иммунологических анализов и способов их использования. Несмотря на то, что выше было приведено описание конкретных вариантов осуществления настоящего изобретения, подразумевают, что изобретение не ограничено ими,так как подразумевают, что изобретение имеет настолько широкий объем патентных притязаний, насколько позволяет ему уровень техники, и что описание следует толковать аналогичным образом. Следовательно, несмотря на то, что в описании рассмотрено связывание лиганда с использованием реакций антиген/антитело, также могут быть использованы иные лигандсвязующие механизмы например связывание с аптамером, связывание с нуклеиновой кислотой, ферментативное связывание и т.д К тому же,несмотря на то, что ячейки для тестов описаны как имеющие одну линию для тестирования на наличие одного лиганда, две линии для тестирования на наличие двух лигандов, три линии для тестирования на наличие трех лигандов и пять линий проведения теста для тестирования на наличие пяти лигандов, понятно, что для тестирования на наличие различных количеств лигандов могут быть использованы различные количества линий. В таком случае может быть использован один корпус с одним отверстием для пробы, или в альтернативном варианте при желании может быть использовано множество отверстий. В случае использования множества отверстий может использоваться множество полосок для одной или большего количества предоставленных проб. В предпочтительном варианте множество полосок соприкасается с одиночной полоской (например, они являются наложенными на нее или подложенными под нее), обеспечивающей путь миграции для конъюгата. Также может существовать возможность создания одиночного отверстия, которое расположено над двумя соседними полосками, приспособленными для миграции пробы, или ведет к ним. Кроме того, несмотря на то, что ячейки для тестов описаны имеющими отверстия в верхней стенке корпуса, предназначенные для приема пробы и буферного раствора или подсистемы "буферный раствор - конъюгат", понятно, что одно или оба отверстия могут быть созданы в торцевой стенке или в боковой стенке корпуса. Аналогичным образом, несмотря на то, что сорбирующий материал был описан как предпочтительно содержащий тонкую пластмассовую подложку, понятно, что может быть предусмотрено наличие пластмассовой подложки только в определенных местах, или она вообще может отсутствовать. В тех случаях, когда предусмотрено наличие только лишь частичных подложек или когда подложки отсутствуют, область проведения теста и контрольная область могут быть расположены на любой стороне или на обеих сторонах сорбирующего материала. Помимо этого, несмотря на то, что индикаторная полоска и контрольная полоска показаны имеющими прямоугольную конфи- 19012193 гурацию (то есть в виде линий), понятно, что область проведения теста и контрольная область могут быть выполнены имеющими иную конфигурацию, например, в виде кругов, квадратов, овалов, пунктирной линии и т.д. Фактически, область проведения теста и контрольная область могут иметь отличающуюся друг от друга конфигурацию. К тому же, несмотря на то, что изобретение было описано как использование корпуса Т-образной формы и как использование сорбирующих материалов, являющихся перпендикулярными друг другу, понятно, что корпус может быть выполнен имеющим различные формы(например, прямоугольную, в форме пистолета), обеспечивая при этом перпендикулярность сорбирующих материалов относительно друг друга. Кроме того, при желании, сорбирующие материалы не обязательно должны быть перпендикулярными друг другу при условии обеспечения различных путей миграции для вещества, определяемого при анализе, пробы и для подсистемы "буферный раствор - конъюгат". Таким образом, например, может быть создано устройство Y-образной формы. Фактически, возможно даже создать прямоугольную компоновку, в которой, например, область для пробы и сорбирующий материал расположены выше (или ниже) линии для проведения теста, контрольной линии и резервуара и отделены от них стенкой в корпусе, а линия для проведения теста и контрольная линия являются видимыми из окна на другой стороне корпуса. Для специалистов в данной области техники также понятно, что корпус может быть видоизменен дополнительными способами таким образом, чтобы он содержал отдельные окна для каждой линии проведения теста. К тому же, несмотря на то, что изобретение было описано таким образом, что в нем используют буферный раствор, который добавляют к пути миграции конъюгата и, возможно, но не обязательно, к пути миграции пробы, понятно, что может быть выбран один или большее количество желательных буферных растворов, которые могут быть добавлены к путям миграции в зависимости от проводимого теста или проводимых тестов. Таким образом, часто используют такие буферные растворы, как,например, фосфатные буферные растворы или буферные растворы ТРИС (трис-гидроксиметиламинометан). Однако подразумевают, что настоящее изобретение охватывает собой использование любого разбавителя, в том числе воды. Кроме того, при необходимости разбавитель может быть добавлен к пробе и смешан с ней перед добавлением пробы на сорбирующий материал, или же сначала может быть введена проба, а после этого может быть добавлен разбавитель. Аналогичным образом, может быть использован любой разбавитель, способный вызывать миграцию конъюгата, и он может быть заранее смешан с конъюгатом в системе с жидким конъюгатом, или им может быть снабжен путь миграции конъюгата в системе с сухим конъюгатом. Следовательно, для специалистов в данной области техники понятно, что могут быть выполнены и другие модификации предложенного изобретения, не выходя за пределы его сущности и объема патентных притязаний, определяемых формулой изобретения. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Устройство для тестов, предназначенное для определения наличия лиганда в жидкой пробе, содержащее:a) первую полоску из сорбирующего материала, расположенную в первом местоположении, которая предназначена для приема раствора и определяет первый путь миграции;b) вторую полоску из сорбирующего материала, иную, чем упомянутая первая полоска из сорбирующего материала, расположенную во втором местоположении, которая предназначена для приема жидкой пробы и определяет второй путь миграции, отличный от упомянутого первого пути миграции; иc) участок проведения теста, расположенный по меньшей мере на или в одной из упомянутых полосок: упомянутой первой полоски из сорбирующего материала и упомянутой второй полоски из сорбирующего материала, причем упомянутая область проведения теста имеет иммобилизированное лигандсвязующее средство, а упомянутые первая и вторая полоски из сорбирующего материала соприкасаются друг с другом в области проведения теста. 2. Устройство для тестов по п.1, дополнительно содержащее:d) корпус, определяющий первое отверстие, расположенное рядом с упомянутым первым местоположением, второе отверстие, расположенное рядом с упомянутым вторым местоположением, и окно,расположенное рядом с упомянутой областью проведения теста, через которое видна упомянутая область проведения теста. 3. Устройство для тестов по п.1, в котором упомянутая первая полоска из сорбирующего материала служит носителем конъюгата. 4. Устройство для тестов по п.3, в котором упомянутым лигандсвязующим средством является антиген или антитело к упомянутому лиганду, а упомянутый конъюгат содержит антиген или антитело к лиганду и маркер, связанный с антигеном или антителом. 5. Устройство для тестов по п.4, в котором упомянутым маркером является окрашенный маркер,видимый в видимой области спектра. 6. Устройство для тестов по п.2, в котором упомянутая по меньшей мере одна из упомянутых первой и второй полосок из сорбирующего материала содержит контрольную область, а упомянутый корпус определяет окно для просмотра упомянутой контрольной области.- 20012193 7. Устройство для тестов по п.1, в котором упомянутая первая полоска из сорбирующего материала и упомянутая вторая полоска из сорбирующего материала расположены таким образом, что имеют конфигурацию в виде буквы Т. 8. Устройство для тестов по п.1, в котором упомянутая первая полоска из сорбирующего материала и упомянутая вторая полоска из сорбирующего материала расположены таким образом, что имеют конфигурацию в виде знака +. 9. Устройство для тестов по п.1, в котором упомянутая первая полоска из сорбирующего материала имеет поры первого размера, а упомянутая вторая полоска из сорбирующего материала имеет поры второго размера. 10. Устройство для тестов по п.9, в котором упомянутые поры второго размера являются большими по величине, чем упомянутые поры первого размера. 11. Устройство для тестов по п.10, в котором упомянутые поры первого размера имеют величину от 3 до 20 мкм, а упомянутые поры второго размера имеют величину от 20 до 40 мкм. 12. Устройство для тестов по п.2, в котором упомянутая по меньшей мере одна из упомянутых первой и второй полосок из сорбирующего материала содержит контрольную область, и либо упомянутое окно имеет такой размер, что позволяет видеть упомянутую контрольную область, либо упомянутый корпус снабжен вторым окном, позволяющим видеть упомянутую контрольную область. 13. Устройство для тестов по п.1, дополнительно содержащее буферный раствор. 14. Устройство для тестов по п.1, дополнительно содержащее раствор, который содержит подсистему из буферного раствора и конъюгата, содержащую антиген или антитело к лиганду и маркер, связанный с антигеном или антителом. 15. Устройство для тестов по п.1, в котором упомянутая область проведения теста, содержащая иммобилизированное лигандсвязующее средство, содержит антиген ВИЧ (вируса иммунодефицита человека) или антитело к ВИЧ. 16. Устройство для тестов по п.1, в котором упомянутая область проведения теста, содержащая иммобилизированное лигандсвязующее средство, содержит одно из следующих веществ: антигены, антитела, аптамеры, нуклеиновые кислоты или ферменты по меньшей мере для одного из следующих тестов: на беременность, на ВИЧ, на туберкулез (ТБ), на прион, на наркотики по анализу мочи, на хламидии, на маркеры болезней сердца, на маркеры рака, на болезнь Чагаса (американский трипаносомоз), на зубные бактерии (SM/LC), на стрептококк группы А, на грипп А, на грипп В, на аденовирус/ротавирус, на парвовирус собак (CPV), на вирус иммунодефицита кошек (FIV), на вирус лейкемии кошек (FeLV) и на сердечного червя. 17. Устройство для тестов по п.1, в котором упомянутая первая полоска из сорбирующего материала содержит первую мембрану и первую подложку и упомянутая вторая полоска из сорбирующего материала содержит вторую мембрану и вторую подложку, а упомянутая первая полоска из сорбирующего материала и упомянутая вторая полоска из сорбирующего материала расположены таким образом, что упомянутая первая мембрана находится в контакте с упомянутой второй мембраной. 18. Устройство для тестов по п.17, дополнительно содержащее первую липкую пластину подложки,расположенную под упомянутой первой полоской из сорбирующего материала или поверх нее. 19. Устройство для тестов по п.18, дополнительно содержащее вторую липкую пластину подложки,расположенную под упомянутой второй полоской из сорбирующего материала или поверх нее. 20. Устройство для тестов по п.1, в котором упомянутая первая полоска из сорбирующего материала и упомянутая вторая полоска из сорбирующего материала содержат одну мембрану, являющуюся единой для обеих полосок: упомянутой первой полоски из сорбирующего материала и упомянутой второй полоски из сорбирующего материала. 21. Устройство для тестов по п.1, в котором упомянутое устройство для тестов предназначено для определения наличия множества различных лигандов в жидкой пробе, и упомянутая область проведения теста имеет множество отдельных иммобилизированных лигандсвязующих средств для раздельного связывания с соответствующими лигандами из упомянутого множества различных лигандов. 22. Устройство для тестов по п.21, в котором упомянутое множество отдельных иммобилизированных лигандсвязующих средств содержит антиген туберкулеза и по меньшей мере один антиген ВИЧ. 23. Устройство для тестов по п.21, в котором упомянутое множество отдельных иммобилизированных лигандсвязующих средств содержит антитела р 24 и по меньшей мере один из антигенов ВИЧ 1 и ВИЧ 2. 24. Устройство для тестов по п.21, в котором упомянутая первая полоска из сорбирующего материала является носителем множества различных конъюгатов, содержащих антигены и/или антитела к множеству различных лигандов и маркеры, связанные с антигенами и/или с антителами. 25. Устройство для тестов по п.1, в котором упомянутое иммобилизированное лигандсвязующее средство расположено по меньшей мере на четырех линиях, содержащих различные соответствующие антигены ВИЧ или антитела к ВИЧ. 26. Устройство для тестов по п.25, в котором упомянутые различные антигены ВИЧ или антитела к ВИЧ содержат по меньшей мере четыре из следующих: р 24, gp41, gp120, gp160 и gp36.- 21012193 27. Устройство для тестов по п.1, в котором по меньшей мере часть упомянутой области проведения теста окрашена видимым цветным красителем. 28. Устройство для тестов, предназначенное для определения наличия лиганда в жидкой пробе, содержащее:a) первую полоску из сорбирующего материала, расположенную в первом местоположении, которая предназначена для приема раствора и определяет первый путь миграции;b) вторую полоску из сорбирующего материала, иную, чем упомянутая первая полоска из сорбирующего материала, расположенную во втором местоположении, которая предназначена для приема жидкой пробы и определяет второй путь миграции, отличный от упомянутого первого пути миграции,причем упомянутая вторая полоска из сорбирующего материала содержит конъюгат из антитела, связанного с временным связующим веществом, а упомянутое антитело выбрано таким образом, чтобы связываться с лигандом при его наличии в пробе; и с) участок проведения теста, расположенный по меньшей мере на или в одной из упомянутых полосок: упомянутой первой полоски из сорбирующего материала и упомянутой второй полоски из сорбирующего материала, причем упомянутая область проведения теста содержит иммобилизированное связующее вещество, при этом упомянутое временное связующее вещество и упомянутое иммобилизированное связующее вещество выбраны таким образом, что способны избирательно хорошо связываться друг с другом, а упомянутые первая и вторая полоски из сорбирующего материала соприкасаются друг с другом в области проведения теста. 29. Устройство для тестов по п.28, в котором упомянутая первая полоска из сорбирующего материала служит носителем конъюгата, содержащего маркер, связанный со вторым антителом, выбранным таким образом, что оно связывается с лигандом при его наличии в пробе. 30. Устройство для тестов по п.29, в котором упомянутым лигандом является антиген р 24, упомянутым конъюгатом из антитела, связанного с временным связующим веществом, является моноклональное антитело р 24, связанное с биотином, а упомянутым иммобилизированным связующим веществом является стрептавидин. 31. Устройство для тестов по п.29, в котором упомянутым лигандом является антиген р 24, упомянутым конъюгатом из антитела, связанного с временным связующим веществом, является моноклональное антитело р 24, связанное с биотином, упомянутым иммобилизированным связующим веществом является стрептавидин, а упомянутым конъюгатом, содержащим маркер, связанный со вторым антителом,является конъюгат окрашенного латекса с моноклональным антителом. 32. Устройство для тестов по п.1, в котором упомянутая первая полоска из сорбирующего материала и упомянутая вторая полоска из сорбирующего материала расположены таким образом, что имеют непараллельную конфигурацию. 33. Устройство для тестов по п.1, содержащее видимый растворимый индикатор. 34. Устройство для тестов, предназначенное для определения наличия лиганда в жидкой пробе, содержащее: а) первую полоску из сорбирующего материала, расположенную в первом местоположении, которая предназначена для приема раствора и определяет первый путь миграции;b) вторую полоску из сорбирующего материала, иную, чем упомянутая первая полоска из сорбирующего материала, расположенную во втором местоположении, которая предназначена для приема жидкой пробы и определяет второй путь миграции, отличный от упомянутого первого пути миграции; иc) область проведения теста, расположенную по меньшей мере на или в одной из упомянутых первых и вторых полосок из сорбирующего материала, причем упомянутая область проведения теста содержит иммобилизированное лигандсвязующее средство, осажденное по меньшей мере на или в одной из упомянутых первой и второй полосок из сорбирующего материала, а упомянутые первая и вторая полоски из сорбирующего материала находятся в непосредственном контакте друг с другом в области проведения теста. 35. Устройство для тестов, предназначенное для определения наличия лиганда в жидкой пробе, содержащее:a) первый участок материала, определяющий первое местоположение, который предназначен для приема раствора и определяет первый путь миграции;b) второй участок материала, определяющий второе местоположение, который предназначен для приема раствора и определяет второй путь миграции, не являющийся параллельным упомянутому первому пути миграции; иc) область проведения теста, расположенную по меньшей мере на или в одном из упомянутых участков материала, которыми являются упомянутый первый участок материала и упомянутый второй участок материала, причем упомянутая область проведения теста имеет иммобилизированное лигандсвязующее средство, осажденное по меньшей мере на или в одном из упомянутых участков материала, которыми являются упомянутый первый участок материала и упомянутый второй участок материала, а упомянутые первый и второй участки материала находятся в контакте друг с другом в области проведения теста.- 22012193 36. Устройство для тестов по п.35, в котором упомянутые первый и второй пути миграции пересекаются в упомянутой области проведения теста. 37. Способ проведения теста пробы на наличие лиганда, содержащий следующие операции: а) изготавливают устройство для тестов, содержащее первую полоску из сорбирующего материала,расположенную в первом местоположении, которая предназначена для приема раствора и определяет первый путь миграции, вторую полоску из сорбирующего материала, расположенную во втором местоположении, которая предназначена для приема жидкой пробы и определяет второй путь миграции, отличный от упомянутого первого пути миграции, и область проведения теста, расположенную по меньшей мере на или в одной из упомянутых полосок: упомянутой первой полоски из сорбирующего материала и упомянутой второй полоски из сорбирующего материала, причем упомянутая область проведения теста имеет иммобилизированное лигандсвязующее средство, а упомянутые первая и вторая полоски из сорбирующего материала соприкасаются друг с другом в месте расположения области проведения теста;c) после упомянутого ввода пробы вводят раствор в первое местоположение иd) производят осмотр упомянутой области проведения теста для определения показания, свидетельствующего о наличии или об отсутствии лиганда в пробе. 38. Способ по п.37, в котором упомянутое устройство для тестов имеет корпус, определяющий первое отверстие, расположенное рядом с упомянутым первым местоположением, второе отверстие, расположенное рядом с упомянутым вторым местоположением, и окно, расположенное рядом с упомянутой областью проведения теста, через которое видна упомянутая область проведения теста, а введение пробы осуществляют через упомянутое второе отверстие в упомянутое второе местоположение,введение раствора осуществляют через упомянутое первое отверстие в упомянутое первое местоположение, при этом производят осмотр через упомянутое окно. 39. Способ проведения теста пробы на наличие лиганда с использованием устройства по п.33,включающий следующие этапы:a) вводят пробу в устройство для тестов по п.1;b) осматривают область проведения теста, наблюдая исчезновение видимого индикатора;c) после исчезновения видимого индикатора в устройство для тестов вводят раствор иd) производят осмотр области проведения теста для определения показания, свидетельствующего о наличии или об отсутствии лиганда в пробе. 40. Способ по п.39, включающий в себя осмотр области проведения теста с целью установления,захвачен ли коньюгат, имеющий маркер, областью проведения теста. 41. Способ по п.40, в котором упомянутое устройство для проведения тестов снабжено первой сорбирующей полоской для прима раствора и формирования первого пути миграции для раствора и для коньюгата, имеющего маркер, вторым сорбирующим материалом, имеющим второе место расположения для получения образца и формирования второго пути миграции, отличного от первого пути, где область проведения теста расположена на или в первой сорбирующей полоске и/или второй сорбирующей полоске, при этом первая и вторая сорбирующие полоски соприкасаются в месте проведения теста. 42. Способ по п.41, в котором второй путь миграции расположен в стороне от второго расположения, по крайней мере, до области проведения теста так, что продвижение жидкой пробы во второе место расположения требует времени, в течение которого жидкий образец распространяется в области проведения теста, не смачивая при этом моментально область проведения теста по мере продвижения.
МПК / Метки
МПК: C12M 3/00, G01N 15/06, C12M 1/34, G01N 21/00, G01N 31/22, B01L 3/00, G01N 33/566, G01N 33/00, C12Q 1/00, G01N 33/53
Метки: двухканальное, иммунологических, устройство, анализов
Код ссылки
<a href="https://eas.patents.su/30-12193-dvuhkanalnoe-ustrojjstvo-dlya-immunologicheskih-analizov.html" rel="bookmark" title="База патентов Евразийского Союза">Двухканальное устройство для иммунологических анализов</a>
Предыдущий патент: Гравитационный градиентометр
Следующий патент: Способ сохранения состояния безопасности электронного оборудования при отказе, основанный на принципе комплексной безопасности при отказе
Случайный патент: Способ и устройство для введения оборудования в трубопровод и перемещения его по трубопроводу












