Фунгицидные 2-метоксибензофеноны.
Номер патента: 2606
Опубликовано: 27.06.2002
Авторы: Куртце Юрген, Штумм Карл-Отто, Райхерт Гюнтер, Коттер Хенри Ван Туиль, Моршхойзер Герд, Рениг Аннерозе Эдит Элизе, Вальдек Андреас, Зимон Вернер, Альберт Гвидо
Формула / Реферат
1. Соединение формулы I

где R1 обозначает атом галогена или С1-С10 алкильную группу;
R2 обозначает атом водорода, галогена, С1-С10 алкил, C1-С10 алкокси- или нитрогруппу, или
R1 и R2 вместе обозначают группу формулы -СН=СН-СН=СН-;
R3 и R4, каждый независимо, обозначают С1-С10 алкильную или бензильную группу, необязательно замещенную одним или несколькими атомами галогена, нитро- или цианогруппой, циклоС1-С10алкилом, галогенС1-С10алкилом, галогенциклоС1-С10алкилом, С1-С10алкокси, галогенС1-С10алкокси, фенилом, галоген- или дигалогенфенилом или пиридилом; и
n равно целому числу от 0 до 3.
2. Соединение по п.1, где
R1 обозначает атом хлора или метильную группу;
R2 обозначает атом водорода, хлора или брома;
R3 обозначает С1-5 алкильную группу;
R4 обозначает С1-5 алкильную группу или группу бензила, необязательно замещенную, по меньшей мере, атомом галогена или С1-4 алкилом или алкоксигруппой; и
n равно 0.
3. Соединение по п.2, выбранное из группы, состоящей из
6,6'-диметил-2,2',3',4'-тетраметоксибензофенона,
6,6'-диметил-3'-пентокси-2,2',4'-триметоксибензофенона,
5-бром-6,6'-диметил-2,2',3',4'-тетраметоксибензофенона,
5-хлор-6,6'-диметил-2,2',3',4'-тетраметоксибензофенона,
5-иод-6,6'-диметил-2,2',3',4'-тетраметоксибензофенона,
6-хлор-6'-метил-2,2',3',4'-тетраметоксибензофенона,
5-бром-6-хлор-6'-метил-2,2',3',4'-тетраметоксибензофенона,
6-хлор-5,6'-диметил-2,2',3',4'-тетраметоксибензофенона,
2'-бутокси-6-хлор-6'-метил-2,3',4'-триметоксибензофенона,
2'-бутокси-6-хлор-5,6'-диметил-2,2',3'-триметоксибензофенона,
6-хлор-2'-(2-фторбензилокси)-6'-метил-2,3',4'-триметоксибензофенона,
6-хлор-2'-(4-фторбензилокси)-6'-метил-2,3',4'-триметоксибензофенона,
5-бром-6,6'-диметил-3'-пентилокси-2,2',4'-триметоксибензофенона,
6-хлор-6'-метил-2'-пентилокси-2,3',4'-триметоксибензофенона,
6-хлор-2'-(3-метилбутилокси)-6'-метил-2,3',4'-триметоксибензофенона,
2'-бензилокси-6-хлор-6'-метил-2,3',4'-триметоксибензофенона,
6-хлор-2'-(3-метилбензилокси)-6'-метил-2,3',4'-триметоксибензофенона,
6-хлор-2'-(4-метилбензилокси)-6'-метил-2,3',4'-триметоксибензофенона,
6-хлор-2-дифторметокси-6'-метил-2',3',4'-триметоксибензофенона,
1-(6'-метил-2',3',4'-триметоксибензоил)-2-метоксинафталина,
1-(6'-метил-2',3',4'-триметоксибензоил)-2-дифторметоксинафталина.
4. Способ получения соединения по п.1, где n равно 0, который включает взаимодействие соединения формулы II
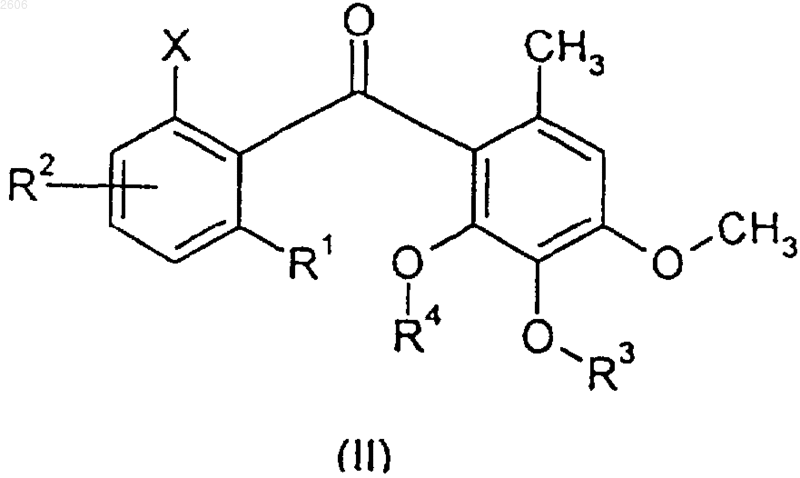
где R1, R2, R3 и R4 имеют значения, раскрытые в п.1, и Х обозначает атом фтора или хлора, с метанолятом щелочного металла.
5. Способ получения соединения по п.1, который включает
(а) взаимодействие соединения формулы III
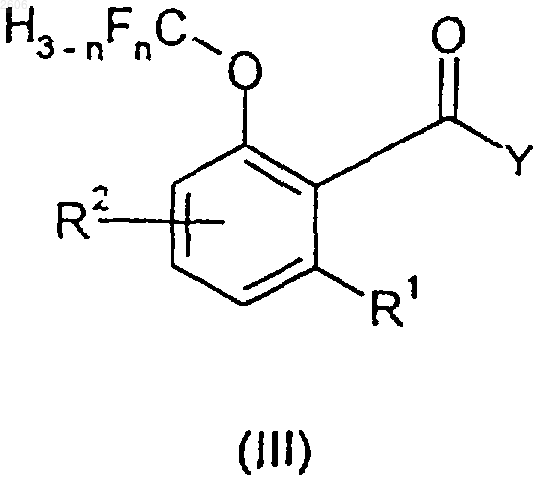
где R1, R2 и n имеют значения, раскрытые в п.1, и Y обозначает уходящую группу или гидроксигруппу,
с соединением формулы IV
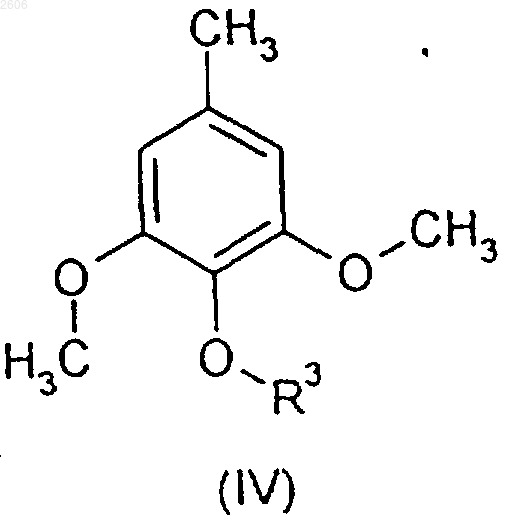
где R3 имеет значение, раскрытое в п.1, в присутствии кислоты Льюиса или дегидратирующего агента, и
(б) необязательно обработку полученного продукта соединением формулы V
R4-O-Met, (V)
где R4 обозначает С1-С10 алкильную или бензильную группу, необязательно замещенную одним или несколькими атомами галогена, нитро- или цианогруппой, циклоалкилом, галогеналкилом, галогенциклоалкилом, алкокси, галогеналкокси, фенилом, галоген- или дигалогенфенилом или пиридилом и при условии, что алкильная группа не является метилом и Met обозначает атом щелочного металла.
6. Способ получения соединения формулы III по п.5, где R2 обозначает атом галогена, который включает на стадии (а) взаимодействие соединения формулы VI
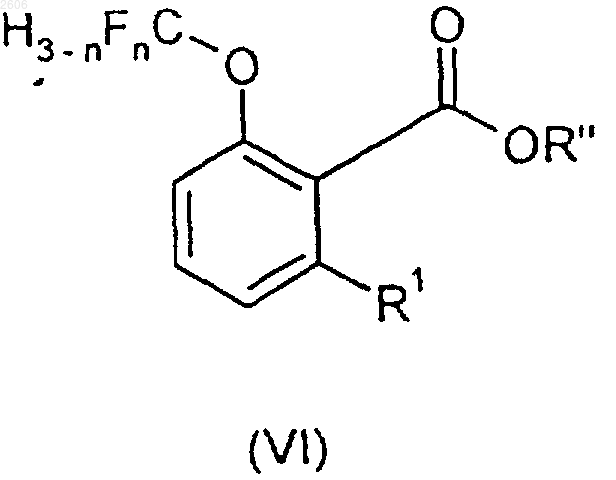
где R1 и n имеют значения, раскрытые в п.1, и R" обозначает атом водорода или алкильную группу, с галогенирующим агентом.
7. Способ получения соединения формулы III по п.5, где R2 обозначает атом галогена, который включает
(а) взаимодействие соединения формулы VI

где R1 и n имеют значения, раскрытые в п.1; и
R" обозначает алкильную группу,
с галогенирующим агентом;
(б) необязательный гидролиз полученного галогенированного алкилбензоата и
(в) необязательную обработку полученной галогенированной бензойной кислоты тионилхлоридом.
8. Композиция, которая включает фунгицидно эффективное количество, по меньшей мере, одного соединения по п.1 и носитель.
9. Способ борьбы с грибками или болезнью растений в очаге, вызванной грибками, который включает обработку очага соединением по п.1.
10. Способ борьбы с грибками или болезнью растений в очаге, вызванной грибками, который включает обработку очага композицией по п.8.
11. Способ по п.9, где болезнь растения вызывается аскомицетами.
12. Способ по п.10, где болезнь растения вызывается аскомицетами.
13. Способ по п.9, где грибки являются членом подгруппы Erysiphales.
14. Способ по п.13, где грибок выбирают из Erysiphe graminis, Erysiphe cichoracearum, Podosphaera leucotricha или Uncinula necator.
15. Способ по п.10, где грибок является членом подгруппы Erysiphales.
16. Способ по п.15, где грибок выбирают из Erysiphe graminis, Erysiphe cichoracearum, Podosphaera leucotricha или Uncinula necator.
17. Способ получения соединения формулы III по п.6, где R2 обозначает атом брома, который включает взаимодействие соединения формулы VI, где R1 обозначает алкильную группу, n равно 0 и R" обозначает атом водорода, с бромом.
18. Способ получения соединения формулы III по п.17, где взаимодействие между соединением формулы VI и бромом проводят в присутствии полярного протонного растворителя.
19. Соединение, имеющее формулу
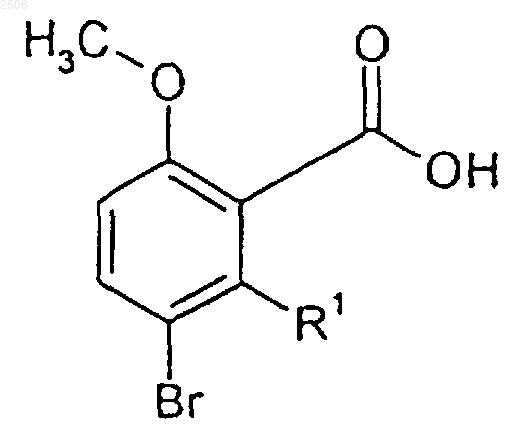
где R1 обозначает алкильную группу.
Текст
1 Это изобретение относится к некоторым соединениям бензофенона, способу их получения, составам, содержащим такие соединения,способу борьбы с грибами в очаге заражения,включающему обработку этого очага такими соединениями, и их применению в качестве фунгицидов. Производство пищевых продуктов базируется на разнообразных сельскохозяйственных технологиях, чтобы обеспечить возрастающие потребности населения в продуктах питания так, чтобы они оставались способными удовлетворить эти потребности, питательными и легко доступными на стеллажах для хранения продовольствия. Фунгициды относятся к одной из этих сельскохозяйственных технологий, которые доступны для мирового сообщества. Фунгициды являются агрохимическими соединениями, которые защищают сельскохозяйственные культуры и пищевые продукты от грибков и грибковых болезней. Сельскохозяйственным культурам и пищевым продуктам постоянно угрожают разнообразные грибковые организмы,которые, если их оставить без контроля, могут вызвать гибель сельскохозяйственных культур и потерю урожая. В частности, аскомицеты как фактор, вызывающий заболевания мучнистой росой, являются постоянно существующей угрозой, особенно для зерновых и плодовых культур. Однако применения фунгицидных средств при нормах расхода контролирующих заболевания, могут вызвать фитотоксичное повреждение целевых растений. Соединения данного изобретения раскрыты в общей формуле европейской патентной(ЕР) заявки ЕР 0727141, которая опубликована 21 августа 1996 г. ЕР заявка раскрывает соединения, имеющие активность против патогенных грибков, но относительно низкое системное воздействие (на организм растения в целом). В ЕР заявке не описаны замещенные бензофеноны, где первая фенильная группа замещена метоксигруппой в положении 2 и атомом галогена или алкильной группой в положении 6 и вторая фенильная группа замещена тремя алкоксигруппами и одной метильной группой. Краткое описание изобретения Данное изобретение представляет соединение формулы I где R1 обозначает атом галогена или алкильную группу;R2 обозначает атом водорода или галогена или алкил, алкокси- или нитрогруппу; илиR1 и R2 вместе обозначают группу формулы -СН=СН-СН=СН-;R3 и R4, каждый независимо, обозначают необязательно замещенную алкильную группу иn равно целому числу от 0 до 3. Соединения сочетают относительно высокую селективную фунгицидную активность для различных сельскохозяйственных растений со сравнительно высокой системностью воздействия. Цель данного изобретения - обеспечить высоко системные фунгицидные соединения. Целью изобретения является также обеспечение способов борьбы с нежелательными грибками путем контактирования указанных растений с фунгицидно эффективным количеством соединений. Другая цель изобретения - обеспечить фунгицидные составы избирательного действия,содержащие эти соединения в качестве активных ингредиентов. Эти и другие цели и особенности изобретения будут более очевидными из подробного описания, приведенного ниже, и из приложенной формулы изобретения. Подробное описание предпочтительных воплощений изобретения Неожиданно было обнаружено, что соединения формулы I где R1-R4 и n имеют значения, указанные выше,обладают одновременно относительно высокой фунгицидной активностью против патогенных грибов, в частности тех, которые вызывают заболевания мучнистой росой, и имеют сравнительно высокое системное действие. В общих выражениях, за исключением иначе установленного, как используется здесь,термин атом галогена может обозначать атом брома, хлора или фтора, в особенности атом брома или хлора. Необязательно замещенные фрагменты молекулы могут быть незамещенными или могут иметь от одного вплоть до максимально возможного числа заместителей. Обычно присутствуют 0-2 заместителя. Каждая необязательно замещенная группа независимо замещена одним или несколькими атомами галогена или группами нитро, циано, циклоалкила, предпочтительно С 3-6 циклоалкила, циклоалкенила, предпочтительно С 3-6 циклоалкенила, галогеналкила,предпочтительно C1-6 галогеналкила, галогенциклоалкила, предпочтительно С 3-6 галогенциклоалкила, алкокси, предпочтительно C1-6 алкокси, галогеналкокси, предпочтительно C1-6 гало 3 геналкокси, фенила, галоген- или дигалогенфенила или пиридила. Обычно, за исключением иначе указанного, термины алкил и алкокси, как используются здесь по отношению к радикалу или части молекулы, относятся к радикалу или части молекулы нормального или изостроения. Как правило, такие радикалы имеют вплоть до 10, в особенности вплоть до 6 атомов углерода. Соответственно, алкил или алкоксидруппа имеет от 1 до 6 атомов углерода, предпочтительно от 1 до 5 атомов углерода. Предпочтительными алкильными группами являются метил, этил, н-пропил,изобутил или Н-бутил. Изобретение в особенности относится к соединениям общей формулы I, где любая алкильная часть групп R1-R4, которые могут быть нормального или изостроения, содержит вплоть до 10 атомов углерода, предпочтительно вплоть до 9 атомов углерода, более предпочтительно вплоть до 6 атомов углерода, и где каждая необязательно замещенная группа независимо замещена одним или несколькими атомами галогена или группами нитро, циано, циклоалкила, предпочтительно С 3-6 циклоалкила, циклоалкенила, предпочтительно С 3-6 циклоалкенила,галогеналкила, предпочтительно C1-6 галогеналкила, галогенциклоалкила, предпочтительно С 3-6 галогенциклоалкила, алкокси, предпочтительно C1-6 алкокси, галогеналкокси, предпочтительно C1-6 галогеналкокси, фенила или пиридила, где фенильная часть необязательно замещена одним или несколькими заместителями, выбранными из атомов галогена, циано-, C1-6 алкильной и C1-6 алкоксигрупп. Изобретение, главным образом, относится к соединениям общей формулы I, где R1 обозначает атом галогена, в частности хлора, C1-10 алкил нормального или изостроения, в особенности C1-3 алкильную группу нормального строения, болеe предпочтительно метильную группу, незамещенную или замещенную, по меньшей мере, одной необязательно замещенной фенилгруппой. Изобретение особенно относится к соединениям общей формулы I, где R2 обозначает атом водорода или галогена, в частности, атом хлора, брома или иода, нитро, C1-10 алкил илиC1-10 галогеналкилгруппу, наиболее предпочтительно атом водорода, хлора или брома. Если R2 отличается от водорода, он наиболее предпочтительно прикреплен в орто-положении к радикалу R1. Изобретение, главным образом, относится к соединениям общей формулы I, где R3 и R4,каждый независимо, обозначают необязательно замещенный С 1-5 алкил нормального или изостроения, в особенности C1-3 алкильную группу,наиболее предпочтительно незамещенную или замещенную метильную группу. Эта метильная группа предпочтительно незамещена или замещена фенильной группой, которая является не 002606 4 замещенной или замещенной 1-5, предпочтительно 1-2 атомами галогена или группами С 1-4 алкил, или С 1-4 алкокси. Соединения бензофенона согласно формуле I являются маслами, камедями или, преимущественно, кристаллическими твердыми веществами и обладают ценными фунгицидными свойствами. Например, они могут использоваться в агрохимии или родственных областях, таких как садоводство и виноградарство, для борьбы с фитопатогенными грибками, особенно аскомицетами, в частности заболеванием мучнистой росой, такими, которые вызываются Erysiphe graminis, Podosphaera Leucotricha, Uncinulanecator и тому подобное. Указанные соединения бензофенона обладают высокой фунгицидной активностью в широком диапазоне концентраций и могут быть использованы в сельском хозяйстве без вредных фитотоксичных эффектов. Более того, соединения согласно изобретению обнаруживают целебное и остаточное регулирование грибков и грибковых болезней,таких как мучнистая роса злаков, огурцов и винограда, и улучшенное системное действие через листву по сравнению с обычными фунгицидами. Полезные результаты подавления фитопатогенных грибов получены с соединением, указанным в формуле I, гдеR1 обозначает атом хлора или метильную группу;R3 обозначает C1-5 алкил или бензильную группу, необязательно замещенную одним или несколькими атомами галогена или одной или несколькими С 1-4 алкильными, или алкоксигруппами; иn обозначает 0 или 2, в особенности 0. Если R2 обозначает Сl или Вr, он предпочтительно присоединен к кольцу бензола в ортоположении по отношению к радикалу R1. В особенности предпочтительны соединения формулы IA где R1 обозначает атом хлора или метильную группу;R2 обозначает атом водорода, хлора или брома или метильную группу иR1 обозначает атом водорода или С 1-4 алкил или фенильную группу, необязательно замещенную одним или несколькими атомами фтора или одной или несколькими С 1-4 алкильными группами. В особенности предпочтительны соединения формулы IB где R' обозначает атом водорода или C1-6 алкильную или фенильную группу, необязательно замещенную одним или несколькими атомами фтора или одной или несколькими С 1-4 алкильными группами. Особенно хорошие результаты в плане подавления фитопатогенных грибов получают при использовании, например, следующих соединений формулы I: 6,6'-диметил-2,2',3'4'-тетраметоксибензофенон,6,6'-диметил-3'-пентокси-2,2',4'-триметоксибензофенон,5-бром-6,6'-диметил-2,2',3',4'-тетраметоксибензофенон,5-хлор-6,6'-диметил-2,2',3',4'-тетраметоксибензофенон,5-иод-6,6'-диметил-2,2',3',4'-тетраметоксибензофенон,6-хлор-6'-метил-2,2',3',4'-тетраметоксибензофенон,5-бром-6-хлор-6'-метил-2,2',3',4'-тетраметоксибензофенон,6-хлор-5,6'-диметил-2,2',3',4'-тетраметоксибензофенон,2'-н-бутокси-6-хлор-6'-метил-2,3',4'-триметоксибензофенон,2'-н-бутокси-6-хлор-5,6'-диметил-2,2',3'триметоксибензофенон,6-хлор-2'-(2-фторбензилокси)-6'-метил 2,3',4'-триметоксибензофенон,6-хлор-2'-(4-фторбензилокси)-6'-метил 2,3',4'-триметоксибензофенон,5-бром-6,6'-диметил-3'-н-пентилокси 2,2',4'-триметоксибензофенон,6-хлор-6'-метил-2'-н-пентилокси-2,3',4'триметоксибензофенон,6-хлор-2'-(3-метилбутилокси)-6'-метил 2,3',4'-триметоксибензофенон,2'-бензилокси-6-хлор-6'-метил-2,3',4'триметоксибензофенон,6-хлор-2'-(3-метилбензилокси)-6'-метил 2,3',4'-триметоксибензофенон,6-хлор-2'-(4-метилбензилокси)-6'-метил 2,3',4'-триметоксибензофенон,6-хлор-2-дифторметокси-6'-метил-2,3',4'триметоксибензофенон,1-(6'-метил-2,3',4'-триметоксибензоил)-2 метоксинафталин,1-(6'-метил-2,3'4'-триметоксибензоил)-2 дифторметоксинафталин. Данное изобретение также обеспечивает способ (А) получения соединения формулы I,где n равно 0, который включает обработку соединения общей формулы II где R1, R2, R3 и R4 имеют значения, указанные выше, и Х обозначает атом фтора или хлора, метилатом щелочного металла, предпочтительно метилатом натрия. Другой возможностью для получения соединений формулы I является способ (В), который включает стадии(а) осуществления реакции соединения формулы III где R1, R2 и n имеют значения, указанные выше; и Y обозначает уходящую группу, в частности атом хлора или гидроксигруппу,с соединением формулы IV(Y=уходящая группа) или дегидратирующего агента (Y=ОН), предпочтительно пентоксидом фосфора или РОСl3, и(б) необязательной обработки полученного бензофенона формулы I, где R4 обозначает метилгруппу, соединением формулы VR4-O-Met,(V) 4 где R обозначает необязательно замещенную алкилгруппу, отличную от метила; иMet обозначает атом щелочного металла,предпочтительно натрий. Соединения формулы III, где R2 обозначает атом галогена, предпочтительно получают способом (С), который включает стадии(а) осуществления реакции соединения формулы VIR" обозначает атом водорода или алкильную группу,с галогенирующим агентом,(б) необязательного гидролиза полученного галогенированного алкилбензоата (R"=алкил) и(в) необязательной обработки полученной галогенированной бенэойной кислоты тионилхлоридом. Исходные материалы формул II, IV, V и VI являются известными продуктами, исходные материалы формулы III являются частично известными и частично новыми продуктами. Соответственно, изобретение предоставляет новые промежуточные соединения формулы где R1 обозначает алкильную группу, в особенности метилгруппу. Исходные материалы формул II, IV, V и VI могут быть получены согласно принятым способам или обычным их адаптациям. Заместители, которые являются несовместимыми с выбранными условиями реакции, могут быть введены после образования бензофенона. Они могут быть образованы известными способами,такими как последовательная дериватизация или замещение подходящей группы, или путем отщепления подходящей защитной группы. Реакцию между 2-галогенбензофеноном формулы II и метилатом щелочного металла предпочтительно проводят в присутствии растворителя, такого как простые эфиры, подобные тетрагидрофурану, диэтиловому эфиру, третбутил-метиловому эфиру, или диметоксиэтан или метанол или смеси этих растворителей. Молярное отношение между соединением формулы II и метилатом щелочного металла предпочтительно находится в диапазоне от 0,3 до 1,9 при температуре между 25 и 120 С. Реакцию Фриделя-Крафтса между соединениями формулы III и IV осуществляют в присутствии катализатора - кислоты Льюиса в соответствии с хорошо известными методикамиFеСl3, АlСl3, SnCl4, ZnCl2, TiCl4, SbCl5 и ВF3,которые могут быть в молярном эквивалентном количестве (на основе бензоилхлорида формулыIII). Однако возможно использование меньших количеств катализатора при повышенных температурах, соответственно при температурах кипения флегмы, предпочтительными катализаторами в этих условиях являются FеСl3, I2,ZnCl2, железо, медь, сильные сульфоновые кислоты, такие как F3 СSО 3 Н, и кислотные ионообменные смолы, такие как Amberlyst 15 иNafion. Предпочтительным катализатором является FеСl3 в 0,001-0,2 молярном отношении при температуре около 50 до 180 С. Реакция может быть проведена в растворителе, инертном в условиях реакции, например, в этиленили метиленхлориде, бензоле, октане, декане или смесях растворителей, или в отсутствие 8 растворителя, обычно путем использования одного из реагентов в избытке, например, в диапазоне от 1:5 до 5:1. Если используют АlСl3, молярное отношение предпочтительно находится в диапазоне от 0,5 до 2 и подходящими растворителями являются, например, метиленхлорид или этиленхлорид при температуре обычно между 10 и 70 С. В другом предпочтительном способе согласно изобретению бензойную кислоту формулы III (Y=ОН) подвергают реакции с соединением формулы IV в присутствии пентоксида фосфора при температурах около 0 до 50 С,предпочтительно при комнатной температуре или в присутствии РОСl3 при температурах от около 50 до 150 С, предпочтительно при температуре кипения флегмы. Галогенирование бензоата формулы VI предпочтительно проводят в присутствии инертного растворителя. Предпочтительными галогенирующими агентами являются, например, сульфурилхлорид, бром и N-иод-сукцинимид. Если R1 обозначает атом галогена, предпочтительны высоко полярные растворители,такие как спирты или карбоновые кислоты, в особенности, уксусная кислота. Если R1 обозначает алкильную группу, в особенности, метильную группу, предпочтительны неполярные растворители, такие как тетрахлорметан. Если реакцию проводят с бромом при температуре между 0 и 40 С, предпочтительно при комнатной температуре, галогенирование имеет место,преимущественно, в орто-положении по отношению к радикалу R1. В предпочтительном воплощении соединения формулы III, где R2 обозначает атом брома, получают путем реакции соединения формулы VI, где R1 обозначает алкильную группу, n равно 0 и R" обозначает атом водорода с бромом. Эту стадию бромирования предпочтительно проводят в присутствии полярного протонного растворителя, такого как алифатический спирт или алифатическая карбоновая кислота, в особенности, уксусная кислота. Бромирование может быть осуществлено подходящим образом в присутствии слабого основания или буферной системы, такой как ацетат натрия или карбонат натрия. Одним воплощением способа настоящего изобретения является способ, в котором бром используют в количестве, выбранном из величин в диапазоне между 1,0 и 1,5, в особенности 1,05-1,2 молярных эквивалентов по отношению к исходному соединению формулы VI. Реакцию между соединением формулы VI и бромом проводят, как правило, при температуре, достаточной для оптимального превращения соединения формулы VI в соединение формулы III. Это понятие обозначает, что температура достаточно высока, чтобы обеспечить это превращение, но также достаточно низка, чтобы избежать разложения исходного материала и 9 продукта. Реакцию проводят предпочтительно при температурах между 0 С и 40 С, в особенности,при комнатной температуре. Реакцию между соединением формулы VI и бромом проводят, как правило, в течение периода времени, достаточного для оптимального превращения соединения формулы VI в соединение формулы III. Это понятие обозначает период времени, достаточно продолжительный для превращения максимального количества исходного материала в соединение формулы III. Реакцию проводят предпочтительно при времени реакции между 1 и 40 ч, в особенности, между 5 и 24 ч. Способы, описанные ниже, могут быть аналогично применены к другим исходным материалам при желании. Благодаря превосходной толерантности растений, соединения формулы I могут использоваться при культивации всех растений, где нежелательна инфекция контролируемыми грибами, например, злаков, овощей, бобов, яблонь,винограда. Отсутствие фитотоксичности для целевой культуры при дозах подавления грибов является характерным признаком данного изобретения. Соответственно, изобретение также предоставляет фунгицидный состав, композицию,которая содержит носитель и в качестве активного ингредиента, по меньшей мере, одно соединение формулы I, как указано выше. Предложен также способ получения такого состава,который предусматривает приведение соединения формулы I, как указано выше, в тесную взаимосвязь по меньшей мере с одним носителем. Такой состав может содержать единственное соединение или смесь различных соединений данного изобретения. Предполагается также, что различные изомеры или смеси изомеров могут иметь различные уровни или спектры активности, и поэтому составы могут содержать индивидуальные изомеры или смеси изомеров. Состав согласно изобретению предпочтительно содержит от 0,5 до 95% активного ингредиента. Носителем в составе согласно изобретению является любой материал, с которым активный ингредиент смешивают, чтобы облегчить нанесение на очаг, который следует обработать, который может быть, например, растением, семенами или почвой, или чтобы облегчить хранение, транспортировку или манипулирование. Носитель может быть твердым или жидким, включая материал, который обычно бывает газообразным, но который сжат до превращения в жидкость, и любые носители, обычно используемые в составлении фунгицидных препаратов, могут быть использованы. Композиции могут производиться хорошо установленными методами, например, в виде эмульсионных концентратов, растворов, которые можно распылять непосредственно или раз 002606 10 бавленными, разбавленных эмульсий, смачиваемых порошков, растворимых порошков, дустов, гранул, диспергируемых в воде гранулятов,микроинкапсулятов. Форма нанесения, такая как разбрызгивание, распыление, диспергирование, дождевание, может быть выбрана, как и препараты, в соответствии с желательными целями и заданными условиями. Препараты, т.е. составы, которые содержат, по меньшей мере, одно соединение, соответствующее общей формуле I, и, необязательно, твердые и/или жидкие дополнительные и вспомогательные вещества, могут быть получены широко известными процедурами, например,интенсивным перемешиванием и/или измельчением активных ингредиентов с другими веществами, такими как наполнители, растворители,твердые носители и, необязательно, поверхностно-активные соединения или вспомогательные вещества. Растворителями могут быть ароматические углеводороды, предпочтительно фракции C8C12, например ксилолы или смеси ксилолов, замещенные нафталины, сложные эфиры фталевой кислоты, такие как дибутил- или диоктилфталат, алифатические углеводороды, например циклогексан или парафины, спирты и гликоли, а также их простые и сложные эфиры, например этанол, этиленгликоль, простой моно- и диметиловый эфир, кетоны, такие как циклогексанон, сильно полярные растворители, такие какN-метил-2-пирролидон,диметилсульфоксид,алкилформамиды, эпоксидированные растительные масла, например эпоксидированное кокосовое или соевое масло, вода. Часто приемлемыми являются смеси различных жидкостей. Твердые носители, которые могут быть использованы для дустов или диспергируемых порошков, могут быть минеральными наполнителями, такими как кальцит, тальк, каолин, монтмориллонит, аттапульгит. Физические свойства могут быть улучшены добавлением высокодисперсного силикагеля или высокодисперсных полимеров. Носители для гранулятов могут быть пористым материалом, таким как пемза,битый кирпич, сепиолит, бентонит, несорбционными носителями могут быть кальцит или песок. Кроме того, может быть использовано множество предварительно гранулированных неорганических и органических материалов,таких как доломит или измельченные растительные остатки. Фунгицидные препараты часто составляют и транспортируют в концентрированной форме,которая затем разбавляется пользователем перед нанесением. Наличие небольших количеств носителя, который является поверхностноактивным веществом, облегчает этот процесс разбавления. Поэтому предпочтительно, чтобы один носитель в препарате согласно изобретению был поверхностно-активным веществом. Например, препарат может содержать, по 11 меньшей мере, два носителя, по меньшей мере,один из которых является поверхностноактивным веществом. Подходящими поверхностно-активными веществами могут быть неионогенные, анионогенные или катионогенные поверхностно-активные вещества с хорошими диспергирующими, эмульгирующими и смачивающими свойствами в зависимости от характера соединения, соответствующего общей формуле I, которое будет использоваться в препарате. Поверхностно-активные вещества могут также обозначать смеси поверхностно-активных веществ. Подходящими поверхностно-активными веществами могут быть так называемые водорастворимые мыла, а также водорастворимые синтетические поверхностно-активные соединения. Мылами обычно являются соли щелочных металлов, щелочно-земельных металлов и необязательно замещенного аммония с высшими жирными кислотами (С 10-С 20), например натриевые или калийные соли олеиновой, или стеариновой кислоты, или смесей натуральных жирных кислот, которые получают, например,из кокосового или таллового масла. Кроме того,могут быть использованы метилтауриновые соли жирных кислот. Однако предпочтительно использовать так называемые синтетические поверхностноактивные вещества, особенно жирные сульфонаты, жирные сульфаты, сульфонированные производные бензимидазола или алкиларилсульфонаты. Жирные сульфаты или жирные сульфонаты обычно используют в виде солей со щелочными, щелочно-земельными металлами или необязательно замещенным аммонием, и они имеют алкильную часть из 8-22 атомов углерода, где алкил также обозначает алкильную часть кислотных остатков, таких как натриевая или кальциевая соль лигнинсульфоновой кислоты,додецилата серной кислоты или смеси жирных спиртов, полученных из натуральных жирных кислот. Сюда относятся также соли сложных эфиров серной кислоты, сульфоновых кислот и продуктов присоединения (аддуктов) жирных спиртов и этиленоксида. Сульфонированные производные бензимидазола предпочтительно содержат 2 остатка сульфоновой кислоты и остаток жирной кислоты с 8-22 атомами углерода. Алкиларилсульфонатами являются, например,соли натрия, кальция и триэтиламмония додецилбензолсульфоновой кислоты, дибутилнафталинсульфоновой кислоты или продукта реакции конденсации нафталинсульфоновой кислоты и формальдегида. Кроме того, могут быть использованы фосфаты, такие как соли сложного эфира фосфорной кислоты аддукта п-нонилфенол-(4-14) этиленоксида или фосфолипиды. 12 Неионогенными поверхностно-активными веществами предпочтительно являются полигликольэфирные производные алифатических или циклоалифатических спиртов, насыщенных или ненасыщенных жирных кислот и алкилфенолов, которые имеют от 3 до 10 групп простого гликолевого эфира и от 8 до 20 атомов углерода в (алифатическом) углеводородном остатке и от 6 до 18 атомов углерода в алкильном остатке алкилфенолов. Другими подходящими неионогенными поверхностно-активными веществами являются водорастворимые, содержащие от 20 до 250 групп простого этиленгликолевого эфира полиаддукты этиленоксида и пропиленгликоля, этилендиаминопропиленгликоля и алкилпропиленгликоля с 1-10 атомами углерода в алкильной части; вещества обычно содержат от 1 до 5 звеньев этиленгликоля на звено пропиленгликоля. Примерами неионогенных поверхностноактивных веществ являются нонилфенолполиэтоксиэтанолы, простой полигликолевый эфир касторового масла, полиаддукты этиленоксида и полипропилена, трибутилфеноксиполиэтоксиэтанол, полиэтиленгликоль, октилфеноксиполиэтоксиэтанол. Кроме того, могут быть использованы сложные эфиры жирных кислот полиоксиэтиленсорбитана, такие как триолеат полиоксиэтиленсорбитана. Катионогенными поверхностно-активными веществами предпочтительно являются соли четвертичного аммония, которые имеют, по меньшей мере, один алкильный остаток с 8-22 атомами углерода, и, кроме того, остатки низшего необязательно галогенированного алкила,бензила или гидроксилакила. Соли предпочтительно являются галогенидами, метилсульфатами или алкилсульфатами, например, хлорид стеарилтриметиламмония или бромид бензилбис(2-хлорэтил)этиламмония. Композиции по изобретению могут быть,например, приготовлены в виде смачиваемых порошков, дустов, гранул, растворов, эмульгируемых концентратов, эмульсий, суспензионных концентратов и аэрозолей. Смачиваемые порошки обычно содержат 25, 50 или 75% мас./мас. активного ингредиента и обычно содержат в дополнение к твердому инертному носителю 3-10% мас./мас. диспергатора и, если необходимо, 0-10% мас./мас. стабилизатора(стабилизаторов) и/или другие добавки, такие как вещества, улучшающие проницаемость или липкость. Дусты обычно готовят в виде концентрата дуста, имеющего состав, подобный составу смачиваемого порошка, но без диспергатора,и они могут быть разбавлены в поле дополнительным твердым носителем, чтобы получить состав, обычно содержащий 0,5-10% мас./мас. активного ингредиента. Гранулы обычно получают с размерами между 10 и 100 меш ASTM(прибл. 2,00-0,15 мм), и они могут быть изготовлены по технологии агломерирования или импрегнирования. Обычно гранулы будут содержать 0,5-75% активного ингредиента и 010% мас./мас. добавок, таких как стабилизатор,поверхностно-активные вещества, замедляющие высвобождение модификаторы и связующие. Так называемые сухие сыпучие порошки состоят из относительно небольших гранул,имеющих относительно высокую концентрацию активного ингредиента. Эмульгируемые концентраты обычно содержат в дополнение к растворителю или смеси растворителей 1-50% мас./об. активного ингредиента, 2-20% маc./об. эмульгаторов и 0-20% мас./об. других добавок,таких как стабилизаторы, вещества, улучшающие проницаемость и ингибиторы коррозии. Суспензионные концентраты обычно составляют так, чтобы получить устойчивый не оседающий текучий продукт, и они обычно содержат 10-75% мас./мас. активного ингредиента, 0,515% мас./мас. диспергаторов, 0,1-10% мас./мас. суспендирующих агентов, таких как защитные коллоиды и тиксотропные средства, 0-10% других добавок, таких как пеноподавители, ингибиторы коррозии, стабилизаторы, вещества, улучшающие проницаемость и липкость, и воду или органическую жидкость, в которой активный ингредиент по существу нерастворим; определенные органические твердые вещества или неорганические соли могут быть растворены в препарате, чтобы способствовать предотвращению осаждения или в качестве антифризов для воды. Водные дисперсии и эмульсии, например препараты, полученные путем разбавления водой смачиваемого порошка или концентрата согласно изобретению, также входят в объем изобретения. Указанные эмульсии могут быть типа вода-в-масле или масло-в-воде и могут иметь густую консистенцию типа майонеза. Препарат изобретения может также содержать другие ингредиенты, например, другие соединения, обладающие гербицидными, инсектицидными или фунгицидными свойствами. Особый интерес для улучшения продолжительности защитного действия соединений этого изобретения представляет использование носителя, который будет обеспечивать замедленное высвобождение фунгицидных соединений в окружающую среду растения, которое должно быть защищено. Такие замедленно высвобождающиеся препараты могут, например,быть внесены в почву вблизи корней растения или могут включать клейкий компонент, позволяющий наносить их непосредственно на стебель растения. Как предметы торговли препараты предпочтительно могут быть в концентрированной форме, однако, пользователь обычно применяет разбавленные препараты. Препараты могут 14 быть разбавлены до концентрации 0,001% активного ингредиента (а.и.). Обычно используют дозы в диапазоне от 0,01 до 10 кг а.и./га. Композиции изобретения могут содержать также другие соединения, имеющие биологическую активность, например соединения, имеющие подобную или дополнительную фунгицидную активность, или соединения, имеющие регулирующую рост растений, гербицидную или инсектицидную активность. Другим фунгицидным соединением может быть, например, соединение, которое способно бороться с болезнями злаков (например, пшеницы), такими как болезни, вызываемые Erysipha,Puccinia, Septoria, Gibberella и Helminthosporiumspp., болезни, передаваемые через семена или почву, и ложная и настоящая мучнистая роса на винограде и мучнистая роса и парша яблок и т.д. Такие смеси фунгицидов могут иметь более широкий спектр действия, чем одно соединение общей формулы I. Примерами другого фунгицидного соединения являются карбендазим, беномил, тиофанатметил, тиабендазол, фуберидазол, этридиазол, дихлорфлуанид, цимоксанил, оксадиксил,офурас, металаксил, фуралаксил, беналаксил,фосэтилалюминий, фенаримол, ипродион, процимидион, винклозолин, пенконазол, миклобутанил, R0151297, S3308, пиразофос, этиримол,диталимфос, тридеморф, трифорин, нуаримол,триазбутил, гуазатин, триацетатная соль 1,1'иминоди(октаметилен)дигуанидина, пропиконазол, прохлораз, флутриафол, гексаконазол, флусилазол, триадимефон, триадименол, диклобутразол, фенпропиморф, пирифенокс, ципроконазол, тебуконазол, эпоксиконазол, 4-хлор-N(циано(этокси)метил)бензамид, фенпропидин,хлорозолинат, диниконазол, имизалил, фенфурам, карбоксин, оксикарбоксин, метфуроксам,додеморф, бластицидин S, касугамицин, эдифенфос, китазин Р, циклогексимид, фталид,пробеназол, изопротиолан, трициклазол, пироквилон, хлорбензтиазон, неоазозин, полиоксин D,валидамицин А, мепронил, флутоланил, пенцикурон, дикломезин, феназиноксид, диметилдитиокарбамат никеля, теклофталам, битертанол,бупиримат, этаконазол, стрептомицин, ципофурам, билоксазол, хинометионат, диметиримол,1-(2-циано-2-метоксииминоацетил)-3-этилмочевина, фенапанил, толклофосметил, пироксифур,полирам, манеб, манкозеб, каптафол, хлороталонил, анилазин, тирам, каптан, фолпет, зинеб,пропинеб, сульфур, динокап, бинапакрил, нитротализопропил, додин, дитианон, фентин гидроксид, фентин ацетат, текназен, хинтозен, дихлоран, медьсодержащие соединения, такие как оксихлорид меди, сульфат меди и смесь Bordeaux, а также органические ртутные соединения, крезоксимметил, азоксистробин, SSF-126,пириметанил, ципродинил, спироксамин, флудиоксонил, хиноксифен, карпропамид, метконазол, диметоморф, фамоксадон, пропанокарб, 15 флуметовер, фенпиклонил, флуазинам, мепанипирим, триазоксид. Кроме того, сопрепараты согласно изобретению могут содержать, по меньшей мере, один бензофенон формулы I и какой-либо агент из следующих классов агентов биологического контроля, таких как вирусы, бактерии, нематоды, грибки и другие микроорганизмы, которые пригодны для борьбы с насекомыми, сорняками или болезнями растений или для индуцирования резистентности у растения-хозяина. Примерами таких агентов биологического контроля являются: Bacillus thuringiensis, Verticillium lecanii,Autugraphica californica NPV, Beauvaria bassiana,Ampelomyces quisqualis, Bacilis subtilis, Pseudomonas fluorescens, Streptomyces griseoviridis иTrichoderma harzianum. Более того, сопрепараты согласно изобретению могут содержать, по меньшей мере, одно соединение формулы I и химический агент, который индуцирует системную приобретенную резистентность у растений, такой как, например,никотиновая кислота или ее производные илиBION. Соединения общей формулы I могут быть смешаны с почвой, торфом или другой укореняющей средой для защиты растений от болезней, связанных с семенами, болезней, передаваемых через почву или лиственных грибных болезней. Изобретение также передает применение в качестве фунгицида соединения общей формулы I, как определено выше, или препарата, как определено выше, и способ борьбы с грибами в очаге заражения, который содержит обработку таким соединением или препаратом очага, которым могут быть, например, растения, подвергающиеся или подвергнутые грибковой атаке,семена таких растений или среда, на которой такие растения выращиваются или будут выращиваться. Данное изобретение пригодно для широкого применения для защиты сельскохозяйственных и декоративных растений против грибковой атаки. Типичные сельскохозяйственные растения, которые могут быть защищены, включают виноград, зерновые культуры, такие как пшеница и ячмень, рис, сахарная свекла, фрукты, арахис, картофель, овощи и томаты. Продолжительность защиты обычно зависит от выбранного конкретного соединения, а также разнообразных внешних факторов, таких как климат, влияние которых обычно снижают за счет использования подходящего препарата. Следующие примеры далее иллюстрируют данное изобретение. Следует понимать, однако,что изобретение не ограничивается только конкретными примерами, данными ниже. Пример 1. Получение 6,6'-диметил 2,2',3',4'-тетраметоксибензофенона. 1 А. 2-Метокси-6-метилбензойная кислота.(5,0 г, 25 ммоль), воды (10 мл), метанола (40 мл) и гидроксида натрия (2,1 г, 50 ммоль) нагревают с обратным холодильником при перемешивании. Реакционную смесь разбавляют водой(150 мл) и подкисляют концентрированной хлористо-водородной кислотой. Твердое вещество собирают путем фильтрования, промывают водой и сушат, получая темно-желтые кристаллы,2,1 г, т.пл. 136 С. 1 В. 2-Метокси-6-метилбензоилхлорид. Смесь 1 А (1,7 г, 10,2 ммоль) и тионилхлорида (2 мл) нагревают при кипении с обратным холодильником в течение 1 ч. Смесь концентрируют и полученный бензоилхлорид используют без дальнейшей очистки. 1 С. 6,6'-Диметил-2,2',3',4'-тетраметоксибензофенон. Смесь 3,4,5-триметокситолуола (1,86 г,10,2 ммоль), 1 В (10,2 ммоль), хлорида алюминия (1,33 г, 10 ммоль) и дихлорметана (20 мл) перемешивают при 0 С. Реакция протекает при 0 С с образованием хлористого водорода. Затем реакционную смесь перемешивают следующие 4 ч при комнатной температуре. Затем медленно добавляют при 0 С смесь разбавленной хлористо-водородной кислоты и этилацетата(1:1 об./об.; 100 мл). Органическую фазу концентрируют и остаток рекристаллизуют из метанола. Твердый материал собирают путем вакуумного фильтрования, три раза промывают смесью метанол/вода (3:1 об./об.; 100 мл каждый раз) и сушат, получая белые кристаллы 1,0 г (30,3%), т.пл. 84 С. Пример 2. Получение 6,6'-диметил-2'-нбутокси-2,3',4'-триметоксибензофенона. Смесь н-бутанола (5 мл) и гидрида натрия(60% в масле, 10 ммоль) перемешивают, пока не прекратится образование газообразного Н 2. Смесь 1 С (0,7 г, 2,2 ммоль) и диметоксиэтана(15 мл) добавляют к полученной реакционной смеси. Затем реакционную смесь нагревают с обратным холодильником при перемешивании в течение 24 ч. Смесь воды и этилацетата(1:1 об./об.; 100 мл) затем медленно добавляют при комнатной температуре. Органическую фазу отделяют, концентрируют и остаток очищают колоночной хроматографией (петролейный эфир:этилацетат, 95:5 об./об), получая чистый продукт в виде желтого масла, 0,2 г (24,4%). Пример 3. Получение 6-хлор-2'-пентилокси-6'-метил-2,3',4'-триметоксибензофенона. Смесь метилата натрия в метаноле(полученного согласно ЕР 0727141, 2,69 г, 6,5 ммоль) и диметоксиэтана (20 мл) нагревают при 80 С с перемешиванием в течение 24 ч. Смесь воды и этилацетата (1:1 об./об.; 100 мл) затем медленно добавляют при комнатной температуре. Органическую фазу отделяют и концентри 17 руют, и остаток очищают колоночной хроматографией (дихлорметан), получая чистый продукт в виде желтого масла, 0,52 г, (19,7%). Пример 4. Получение 5-бром-6-хлор-6'метил-2,2',3',4'-тетраметоксибензофенона. 4 А. Этил-5-бром-6-хлор-2-метоксибензоат. Смесь этил-6-хлор-2-метоксибензоата (1,8 г, 8,4 ммоль), брома (1,41 г, 8,8 ммоль) и уксусной кислоты (5 мл) перемешивают при комнатной температуре в течение 24 ч. Реакционную смесь выливают в воду и экстрагируют этилацетатом. Органическую фазу отделяют и концентрируют, и осадок очищают колоночной хроматографией (петролейный эфир:этилацетат, 95:5 об./об), получая чистый продукт в виде желтого масла, 1,7 г, (69%). 4 В. 5-Бром-6-хлор-2-метоксибензойная кислота. Смесь 4 А (1,7 г, 5,8 ммоль), воды (10 мл),этанола (20 мл) и гидроксида натрия (0,5 г,12,5 ммоль) нагревают с обратным холодильником при перемешивании. Реакционную смесь разбавляют водой (80 мл) и подкисляют концентрированной хлористо-водородной кислотой. Твердый материал собирают путем фильтрования, промывают водой и сушат, получая белые кристаллы, 1,3 г (85%), т.пл. 186-188 С. 4 С. 5-Бром-6-хлор-2-метоксибензоилхлорид. Смесь 4 В (1,2 г, 4,6 ммоль), дихлорметана(15 мл) и оксалилхлорида (1 мл) перемешивают при комнатной температуре в течение 2 ч. Смесь концентрируют и полученный бензоилхлорид используют без дальнейшей очистки. 4D. 5-Бром-6-хлор-6'-метил-2,2',3',4'-тетраметоксибензофенон. Смесь 3,4,5-триметокситолуола (0,83 г,4,6 ммоль), 4 С (4,6 ммоль), хлорида алюминия(0,62 г, 4,6 ммоль) и дихлорметана (20 мл) перемешивают при комнатной температуре в течение 3 ч. Затем добавляют смесь воды и этилацетата (1:1 об./об.; 50 мл). Органическую фазу концентрируют и остаток кристаллизуют из диизопропилового эфира и рекристаллизуют из метанола. Твердый материал собирают путем вакуумного фильтрования, промывают водой и сушат, получая желтые кристаллы, 0,7 г,(35,4%), т.пл. 87-88 С. Пример 5. Получение 1-(6'-метил-2',3',4'триметоксибензоил)-2-метоксинафталина. 5 А. Метил(2-метоксинафт-1-ил)карбоксилат. Смесь 2-гидроксинафт-1-илкарбоновой кислоты (18,82 г, 100 ммоль), гидроксида натрия(8,8 г, 220 ммоль), диметилсульфата (31,5 г,250 ммоль) и воды (200 мл) нагревают до 70 С с перемешиванием в течение 20 ч. Затем реакционную смесь охлаждают до комнатной температуры и экстрагируют этилацетатом дважды. Объединенные органические фазы концентрируют и остаток используют без дальнейшей очистки.(12 г, 300 ммоль) нагревают с обратным холодильником при перемешивании. Реакционную смесь экстрагируют диэтиловым эфиром дважды. Водную реакционную смесь фильтруют и подкисляют концентрированной хлористоводородной кислотой. Твердый материал собирают путем фильтрования, промывают водой и сушат, получая желтые кристаллы, 9,45 г(97,4%), т.пл. 175-176 С. 5 С. 1-(6'-Метил-2',3',4'-триметоксибензоил)-2-метоксинафталин. Смесь 5 В (2,02 г, 10 ммоль), 3,4,5-триметокситолуола (1,82 г, 10 ммоль), Р 2 О 5 (10,0 г) и дихлорметана перемешивают при комнатной температуре в течение 16 ч. Затем дихлорметан отгоняют и остаток разбавляют этилацетатом. Органическую фазу промывают водой и концентрируют. Остаток очищают колоночной хроматографией (петролейные эфиры: этилацетат,8:2 об./об.) и рекристаллизуют из смеси петролейный эфир:диизопропиловый эфир (1:1 об./об.). Твердый материал собирают путем вакуумного фильтрования, промывают холодной смесью петролейный эфир:диизопропиловый эфир (1:1 об./об.) и сушат, получая белые кристаллы, 0,9 г (24,6%), т.пл. 72 С. Пример 6. Получение 5-бром-6,6'-диметил 2,2',3',4'-тетраметоксибензофенона. 6 А. Этил-5-бром-6-метил-2-метоксибензоат. Смесь этил-6-метил-2-метоксибензоата(8,4 г, 43,2 ммоль), брома (6,9 г, 43,2 ммоль) и тетрахлорметана (170 мл) перемешивают при комнатной температуре в течение 60 ч. Реакционную смесь выливают в воду и экстрагируют этилацетатом. Органическую фазу отделяют и концентрируют. Сырой продукт получают в виде желтого масла, 10,3 г (87%) и используют без дальнейшей очистки. 6 В. 5-Бром-6-метил-2-метоксибензойная кислота. Смесь 6 А (9,8 г, 34,1 ммоль), воды (40 мл),этанола (80 мл) и гидроксида натрия (2,7 г,68,3 ммоль) нагревают с обратным холодильником при перемешивании в течение 42 ч. Реакционную смесь разбавляют водой (80 мл), подкисляют концентрированной хлористо-водородной кислотой и экстрагируют дихлорметаном. Органическую фазу отделяют и концентрируют. Твердый материал собирают путем фильтрования, промывают водой и сушат, получая не совсем белые кристаллы, 5,4 г (61%), т.пл. 8183 С. 6 С. 5-Бром-6,6'-диметил-2,2',3',4'-тетраметоксибензофенон. Смесь 6 В (24 г, 10 ммоль), 3,4,5-триметокситолуола (1,82 г; 10 ммоль), Р 2O5 (10,0 г) и дихлорметана (150 мл) перемешивают при комнатной температуре в течение 16 ч. Затем дихлорметан отгоняют и остаток разбавляют этилацетатом. Органическую фазу промывают водой и концентрируют. Остаток очищают колоночной хроматографией (петролейный эфир: этилацетат, 8:2 об./об.) и рекристаллизуют из диизопропилового эфира. Твердый материал собирают путем вакуумного фильтрования,промывают холодной смесью петролейные эфиры:диизопропиловый эфир (1:1 об./об.) и сушат,получая белые кристаллы, 2,2 г, (54%), т.пл. 8991 С. Примеры 7-49. Используя, по существу, те же процедуры,описанные выше для примеров 1-6, и используя стандартные методики дериватизации, где они подходят, получают следующие соединения,показанные в табл. 1 и 2: Таблица 1 метил метил метил Н Н Н Н Н Н Н Н метил метил метил метил метил метил Вr Вr Вr Вr Вr Вr Вr Вr Н метил метил метил метил метил метил метил метил метил метил метил метил метил метил метил метил метил метил метил метил метил метил метил метил метил метил метил метил метил метил метил н-бутил СО-этил Н н-пропил н-бутил н-пентил 3-метилбутил метил масло масло масло масло масло метил метил метил метил Т.пл.,С н-пентил масло метил метил масло метил масло метил метил метил метил метил метил(642,0 г, 3,3 моль), воды (2,5 л), этанола (4,0 л) и гидроксида натрия (270 г, 6,6 моль) нагревают с обратным холодильником при перемешивании в течение 20 ч. Затем этанол отгоняют и реакционную смесь разбавляют водой, подкисляют концентрированной хлористо-водородной кислотой. Твердый материал собирают путем вакуумного фильтрования, промывают водой и сушат, получая не совсем белые кристаллы,460,0 г (83,9%). 50 В. 5-Бром-6-метил-2-метоксибензойная кислота. Смесь брома (102 мл, 2,0 моль) и уксусной кислоты (225 мл) добавляют к смеси 50 А(304,0 г, 1,8 моль), ацетата натрия (164,0 г,2,0 моль) и уксусной кислоты (3,0 л) при температуре от 10 до 15 С. Реакционную смесь перемешивают при комнатной температуре в течение 16 ч. Твердый материал собирают путем вакуумного фильтрования, промывают водой и сушат, получая не совсем белые кристаллы,321,0 г (72, 6%), т.пл. 81-83 С. 50 С. 5-Бром-6,6'-диметил-2,2',3',4'-тетраметоксибензофенон (240 г, 1,0 моль) подвергают реакции с 3,4,5-триметокситолуолом (182 г,1,0 моль) в присутствии Р 2O5 (1,0 кг) и дихлорметана, как описано в примере 6, получая белые кристаллы, 220 г (54%), т.пл. 89-91 С. Последовательность стадий омыления(гидроксидом натрия) и бромирования, описанная в примерах 50 А и 50 В, соответственно, обратна той, что использована в примерах 6 В и 6 А, выше. Бромирование, описанное в примерах 50 В и 6 А,осуществляют со свободной кислотой и сложным эфиром, соответственно. Условия реакции также отличаются, как, например, в примере 50 В, где используют полярный протонный 21 растворитель (уксусная кислота) и буферную соль (ацетат натрия). В примере 6 А используют неполярный апротонный растворитель (тетрахлорметан). Пример 51. Получение 6,6'-диметил-5 фтор-2,2',3',4'-тетраметоксибензофенона. 51 А. 2-Трет-бутил-4-фтор-5-метилфенол. Смесь 4-фтор-3-метилфенола (12,60 г,0,1 моль), трет-бутилхлорида (25 мл) и FеСl3 нагревают с обратным холодильником в течение 16 ч. Избыток трет-бутилхлорида отгоняют и остаток очищают колоночной хроматографией(петролейный эфир:этилацетат, 95:5 об./об.), получая чистый продукт в виде желтого масла,15,3 г (84%). 51 В. 6-Бром-2-трет-бутил-4-фторметилфенол. Смесь 51 А (0,91 г), тетрахлорметана (20 мл), N-бромсукцинимида (0,89 г) и АlСl3 перемешивают при окружающей температуре в течение 3 суток. Реакционную смесь фильтруют и концентрируют. Полученное желтое масло (1,25 г) используют без дальнейшей очистки. 51 С. 2-Бром-4-фтор-3-метилфенол. Смесь 51 В (18,5 г), бензола (120 мл) и АlСl3 (6,5 г) нагревают с обратным холодильником в течение 5 ч. Реакционную смесь охлаждают до комнатной температуры и разбавляют этилацетатом и водой. Органическую фазу отделяют и концентрируют. Остаток очищают колоночной хроматографией (петролейный эфир:этилацетат, 95:5 об./об.), получая чистый продукт в виде белых кристаллов, 9,0 г (62%). 51D. 2-Бром-6-фтор-3-метокситолуол. Смесь 51 С (9,0 г), карбоната калия (6 г),диметилсульфата (6 г) и ацетонитрила (150 мл) нагревают с обратным холодильником в течение 1 ч. Реакционную смесь охлаждают до комнатной температуры, разбавляют водой и экстрагируют диэтиловым эфиром дважды. Органическую фазу отделяют и концентрируют, и остаток (9,0 г) используют без дальнейшей очистки. 51 Е. 3-Фтор-6-метокси-2-метилбензойная кислота. Раствор н-бутиллития в гексане (18,1 мл,2,5 моль/л) медленно добавляют к смеси 51D(9,0 г) и тетрагидрофурана (90 мл) при -78 С. Полученную реакционную смесь насыщают диоксидом углерода при -78 С и позволяют нагреться до окружающей температуры. Реакционную смесь выливают в воду, подкисляют и экстрагируют диэтиловым эфиром дважды. Органическую фазу сушат и концентрируют. Остаток (3,9 г) используют без дальнейшей очистки. 51F. 6,6'-Диметил-5-фтор-2,2',3',4'-тетраметоксибензофенон. 22 Биологические исследования А. Системное воздействие через листву. Мучнистая роса пшеницы (МРП). Реципиент: пшеница (Triticum aestivum L.),разновидность Kanzler Патоген: Erysiphe graminis DC. f.sp. triticiE. Marchal Методика испытания 1. Зерна пшеницы (8/горшок) высаживают в пластмассовые горшки диаметром 8 см в теплице. 2. Когда первый лист полностью распустится, оставляют по четыре растения на каждый горшок, из которых два помечают постоянным маркером на 5 см ниже кончика листа на верхней поверхности листа. Таким образом, в каждом горшке находится два обработанных полоской и необработанных растения. 3. Пипетку используют, чтобы нанести 5 мкл приготовленного в виде препарата соединения в виде полоски на нижнюю поверхность листа, противоположную метке. Нанесенная полоска должна перекрывать всю ширину листа. После нанесения растения не перемещают до тех пор, пока полоски не высохнут (полчаса или дольше). 4. Когда обработанные растения высохнут,их переносят в теплицу и оставляют там на 2 суток, чтобы позволить осуществиться перемещению соединений. Растения обеспечивают донным увлажнением. 5. Через двое суток после нанесения растения инокулируют путем обсыпания их конидиями настоящей мучнистой росы в теплице. Оценки обычно делают через 7-8 суток после инокуляции. Оценка Три типа перемещения соединения определяют путем оценивания болезни в трех участках каждого обработанного полоской листа. Трансламинарное перемещение: Участок болезни в процентах оценивают для трансламинарной площади полоски (отмеченная площадь на верхней поверхности листа непосредственно напротив той, куда была нанесена полоска на нижней поверхности листа; ширина полоски приблизительно 5 мм). Трансламинарное подавление болезни рассчитывают затем по следующей формуле: Дистальное перемещение и проксимальное перемещение Дистальную и проксимальную зоны, свободные от болезни, на верхней поверхности листа измеряют в мм. Дистальное направление это направление от полоски к апексу листа и проксимальное направление - от полоски к пазухе (основанию) листа. Рассчитывают процентную долю зоны, свободной от болезни, по отношению ко всему расстоянию между полоской и апексом или пазухой листа. Если болезнь 23 заметно слабее в дистальной или проксимальной зоне, это также отмечают. Препарат и контроли 1. Соединения вводят в состав системы растворитель/поверхностно-активное вещество,содержащей 5% ацетона и 0,05% Tween 20 в деионизированной воде. Соединения в форме препарата подготавливают, используя деионизированную воду. Соединения обычно испытывают при 400 ч. на млн. 2. Два вида контролей включают растения, обработанные полоской раствором растворитель/поверхностно-активное вещество и инокулированные (контроль растворителя); необработанные растения, которые инокулируют (инокулированный контроль). Результаты этой оценки показаны в табл. 3. Таблица 3. Системное воздействие через листву Проксимальн. Дистальное ТрансламиПримерперемещение, перемещение, нарная акмм от полоски мм от полоски тивность, % 1 10 50 100 10 6 46 100 Стандарт 1 4 5 100 Стандарт 2 8 28 100 Следующие соединения, которые известны из ЕР 0727141, были использованы в качестве стандартов: Стандарт 1: 2,6-дихлор-6'-метил-2',3',4'триметоксибензофенон Стандарт 2: 2',3',4'-триметокси-2,6,6'триметилбензофенон В-1. Сравнение фунгицидной активности 2-метоксибензофенонов с 2,6-дихлор- и 2,6 диметилбензофеноном. Испытуемые болезни:(а) Настоящая мучнистая роса пшеницы(б) Настоящая мучнистая роса ячменяE. Marchal Методика испытания Это испытание является испытанием защитного средства на день ноль в борьбе с мучнистыми росами пшеницы и ячменя. 1. Зерна пшеницы или ячменя (приблизительно 8-10/горшок) высаживают в пластмассовые горшки диаметром 6 см и выдерживают в теплице. 2. Когда первый лист полностью распустится, приготовленные в виде препаратов испытуемые соединения распыляют в дозе 200 л/га с 24 помощью навесного перемещаемого опрыскивателя с единственным соплом. Затем растениям дают высохнуть на воздухе. 3. Инокуляция следует примерно через три часа после нанесения соединения. Растения устанавливают на стеллажах теплицы с донными увлажняющими матами и инокулируют их опылением конидиями с инфицированных мучнистой росой растений (исходные культуры в возрасте 10-14 суток). 4. Болезнь на первом листе как процентную площадь листа с симптомами/признаками болезни оценивают около 7 дней после инокуляции. Кончики и основания листьев исключают из оценки. Подавление болезни в процентах рассчитывают затем по следующей формуле: Технология приготовления препарата, соединения сравнения и контроли 1. Технические соединения вводят в состав системы растворитель/поверхностно-активное вещество, содержащей 5% ацетона и 0,05%Tween 20 в деионизированной воде. Соединения растворяют в ацетоне перед добавлением к воде;Tween 20 может быть добавлен либо с ацетоном, либо с водой. Разбавления делают, используя систему растворитель/поверхностно-активное вещество. Испытуемые соединения обычно испытывают в диапазоне концентраций, перекрывающем несколько порядков величин, и затем рассчитывают величины ЭД для сравнения соединений. Соединения в форме препаратов подготавливают, используя деионизированную воду. 2 . Два вида контролей включают растения, обработанные раствором растворитель/поверхностно-активное вещество и инокулированные (контроль растворителя); необработанные растения, которые инокулируют (инокулированный контроль). Результаты этой оценки показаны в табл. 4. Таблица 4. Фунгицидная активность 2 метоксибензофенонов (величины ЭД 90). Сравнение фунгицидной активности 2 метоксибензофенонов с 2,6-дихлор- и 2,6 диметилбензофеноном. Приведены результаты испытаний защитного средства на день 0, в которых все аналоги испытывались бок-о-бок. ЭД 90, ч. на млн Пример 2-меток- Сравнение Стансибензофенона 2 дарт 1 4 6 7 10 45 Хиноксифен 20 4 5 0,1 7 7 0,1 12 8 6 7 0,9 6 8 0,1 26 Соединения наносят как технический материал, приготовленный с 0,5% ацетона, 0,05% 25 В-2. Сравнение лечебной и остаточной фунгицидной активности 2-метоксибензофенонов с 2,6-дихлор- и 2,6-диметилбензофеноном. Испытуемые болезни:(а) Мучнистая роса пшеницы (МРП). Реципиент: пшеница (Triticum aestivum L.),разновидность Kanzler Патоген: Erysiphe graminis DC. f.sp. tritici(б) Мучнистая роса огурца (МРО). Реципиент: огурец (Cucumis sativus L.),разновидность Bush pickle Патоген: Erysiphe cichoracearum DC. Методика испытания Эта процедура испытания предназначена для лечебного и остаточного подавления заболеваний мучнистой росой. 1. Зерна пшеницы (приблизительно 810/горшок) или семена огурца (1 семя/горшок) высаживают в пластмассовые горшки диаметром 6 см и выдерживают в теплице. 2. Когда первый лист (пшеницы) или семядоли (огурца) полностью распустятся, приготовленные в виде препаратов испытуемые соединения распыляют в дозе 200 л/га с помощью навесного перемещаемого опрыскивателя с единственным соплом. Затем растениям дают высохнуть на воздухе. 3. Инокуляцию производят на 2 суток раньше обработки в случае лечебных оценок и через 3 суток после обработки в случае оценок остаточного действия. Для инокуляции растения устанавливают на стеллажах теплицы с донными увлажняющими матами и инокулируют их опылением конидиями с инфицированных мучнистой росой растений (исходные культуры в 26 возрасте 10-14 суток). Между инокуляцией и обработкой для лечебных оценок и между обработкой и инокуляцией для оценок остаточного действия растения выдерживают в теплицах с донным увлажнением. 4. Болезнь на первом листе (пшеницы) или на семядолях (огурца) как процентную площадь листа с симптомами/признаками болезни оценивают около 7 суток после инокуляции. В случае пшеницы кончики и основания листьев исключают из оценки. Подавление болезни в процентах рассчитывают затем по следующей формуле: Технология приготовления препарата,соединения сравнения и контроли 1. Технические соединения вводят в состав системы растворитель/поверхностно-активное вещество, содержащей 5% ацетона и 0,05%Tween 20 в деионизированной воде. Соединения растворяют в ацетоне перед добавлением к воде;Tween 20 может быть добавлен либо с ацетоном, либо с водой. Разбавления делают, используя систему растворитель/поверхностно-активное вещество. Соединения в форме препаратов подготавливают, используя деионизированную воду. 2 . Два вида контролей включают растения, обработанные раствором растворитель/поверхностно-активное вещество и инокулированные (контроль растворителя); необработанные растения, которые инокулируют (инокулированный контроль). Результаты этой оценки показаны в табл. 5. Таблица 5 Лечебная и остаточная фунгицидная активность 2-метоксибензофенонов Подавление болезни (% эффективности) Болезнь Доза Испытание (ч. на млн) Стандарт 1 Стандарт 2 Пример 2-метоксибензофенона 1 6 4 Испытание А В А/В А/В В 1250 79 92 88/85 98/87 61 МРП 125 60 74 79/65 95/89 71 2 da С 12,5 31 55 69/52 90/61 55 100 100/100 100/100 100 100 1250 МРП 100 100/100 100/100 81 83 125 3 da R 99 100/100 90/100 70 75 12,5 100 100/100 100/100 89 100 1250 МРО 97 92/92 5/61 6 0 125 3 da R 8 2/35 2/3 14 0 12,5 2 da C = 2 дня лечебное действие - Инокуляция за 2 дня до нанесения. 3 da R = 3 дня остаточное действие - Инокуляция через 3 дня после нанесения. где R1 обозначает атом галогена или С 1-С 10 алкильную группу;R1 и R2 вместе обозначают группу формулы -СН=СН-СН=СН-;R3 и R4, каждый независимо, обозначают С 1-С 10 алкильную или бензильную группу, необязательно замещенную одним или несколькими атомами галогена, нитро- или цианогруппой, циклоС 1-С 10 алкилом, галогенС 1-С 10 алкилом, галогенциклоС 1-С 10 алкилом, С 1-С 10 алкокси, галогенС 1-С 10 алкокси, фенилом, галогенили дигалогенфенилом или пиридилом; иn равно целому числу от 0 до 3. 2. Соединение по п.1, гдеR1 обозначает атом хлора или метильную группу;R4 обозначает С 1-5 алкильную группу или группу бензила, необязательно замещенную, по меньшей мере, атомом галогена или С 1-4 алкилом или алкоксигруппой; и 28 5-бром-6,6'-диметил-3'-пентилокси-2,2',4'триме-токсибензофенона,6-хлор-6'-метил-2'-пентилокси-2,3',4'триметоксибензофенона,6-хлор-2'-(3-метилбутилокси)-6'-метил 2,3',4'-триметоксибензофенона,2'-бензилокси-6-хлор-6'-метил-2,3',4'триметоксибензофенона,6-хлор-2'-(3-метилбензилокси)-6'-метил 2,3',4'-триметоксибензофенона,6-хлор-2'-(4-метилбензилокси)-6'-метил 2,3',4'-триметоксибензофенона,6-хлор-2-дифторметокси-6'-метил-2',3',4'триме-токсибензофенона,1-(6'-метил-2',3',4'-триметоксибензоил)-2 меток-синафталина,1-(6'-метил-2',3',4'-триметоксибензоил)-2 ди-фторметоксинафталина. 4. Способ получения соединения по п.1,где n равно 0, который включает взаимодействие соединения формулы II где R1, R2, R3 и R4 имеют значения, раскрытые в п.1, и Х обозначает атом фтора или хлора, с метанолятом щелочного металла. 5. Способ получения соединения по п.1,который включает (а) взаимодействие соединения формулы III где R1, R2 и n имеют значения, раскрытые в п.1,и Y обозначает уходящую группу или гидроксигруппу,с соединением формулы IV где R3 имеет значение, раскрытое в п.1, в присутствии кислоты Льюиса или дегидратирующего агента, и(б) необязательно обработку полученного продукта соединением формулы VR4-O-Met,(V) 4 где R обозначает С 1-С 10 алкильную или бензильную группу, необязательно замещенную одним или несколькими атомами галогена, нитро- или цианогруппой, циклоалкилом, галогеналкилом, галогенциклоалкилом, алкокси, галогеналкокси, фенилом, галоген- или дигалогенфенилом или пиридилом и при условии, что алкильная группа не является метилом и Met обозначает атом щелочного металла. 6. Способ получения соединения формулыIII по п.5, где R2 обозначает атом галогена, который включает на стадии (а) взаимодействие соединения формулы VIR" обозначает атом водорода или алкильную группу,с галогенирующим агентом. 7. Способ получения соединения формулы(б) необязательный гидролиз полученного галогенированного алкилбензоата и(в) необязательную обработку полученной галогенированной бензойной кислоты тионилхлоридом. 8. Композиция, которая включает фунгицидно эффективное количество, по меньшей мере, одного соединения по п.1 и носитель. 30 9. Способ борьбы с грибками или болезнью растений в очаге, вызванной грибками, который включает обработку очага соединением по п.1. 10. Способ борьбы с грибками или болезнью растений в очаге, вызванной грибками, который включает обработку очага композицией по п.8. 11. Способ по п.9, где болезнь растения вызывается аскомицетами. 12. Способ по п.10, где болезнь растения вызывается аскомицетами. 13. Способ по п.9, где грибки являются членом подгруппы Erysiphales. 14. Способ по п.13, где грибок выбирают из Erysiphe graminis, Erysiphe cichoracearum,Podosphaera leucotricha или Uncinula necator. 15. Способ по п.10, где грибок является членом подгруппы Erysiphales. 16. Способ по п.15, где грибок выбирают из Erysiphe graminis, Erysiphe cichoracearum,Podosphaera leucotricha или Uncinula necator. 17. Способ получения соединения формулы III по п.6, где R2 обозначает атом брома, который включает взаимодействие соединения формулы VI, где R1 обозначает алкильную группу, n равно 0 и R" обозначает атом водорода, с бромом. 18. Способ получения соединения формулы III по п.17, где взаимодействие между соединением формулы VI и бромом проводят в присутствии полярного протонного растворителя. 19. Соединение, имеющее формулу
МПК / Метки
МПК: A01N 35/04, C07C 49/84
Метки: 2-метоксибензофеноны, фунгицидные
Код ссылки
<a href="https://eas.patents.su/16-2606-fungicidnye-2-metoksibenzofenony.html" rel="bookmark" title="База патентов Евразийского Союза">Фунгицидные 2-метоксибензофеноны.</a>
Предыдущий патент: Устройство и способ для отбора и первичной подготовки проб ткани для молекулярной генной диагностики
Следующий патент: Замещенные 6,6-гетеро-бициклические производные
Случайный патент: Запорно-пломбировочное устройство




















