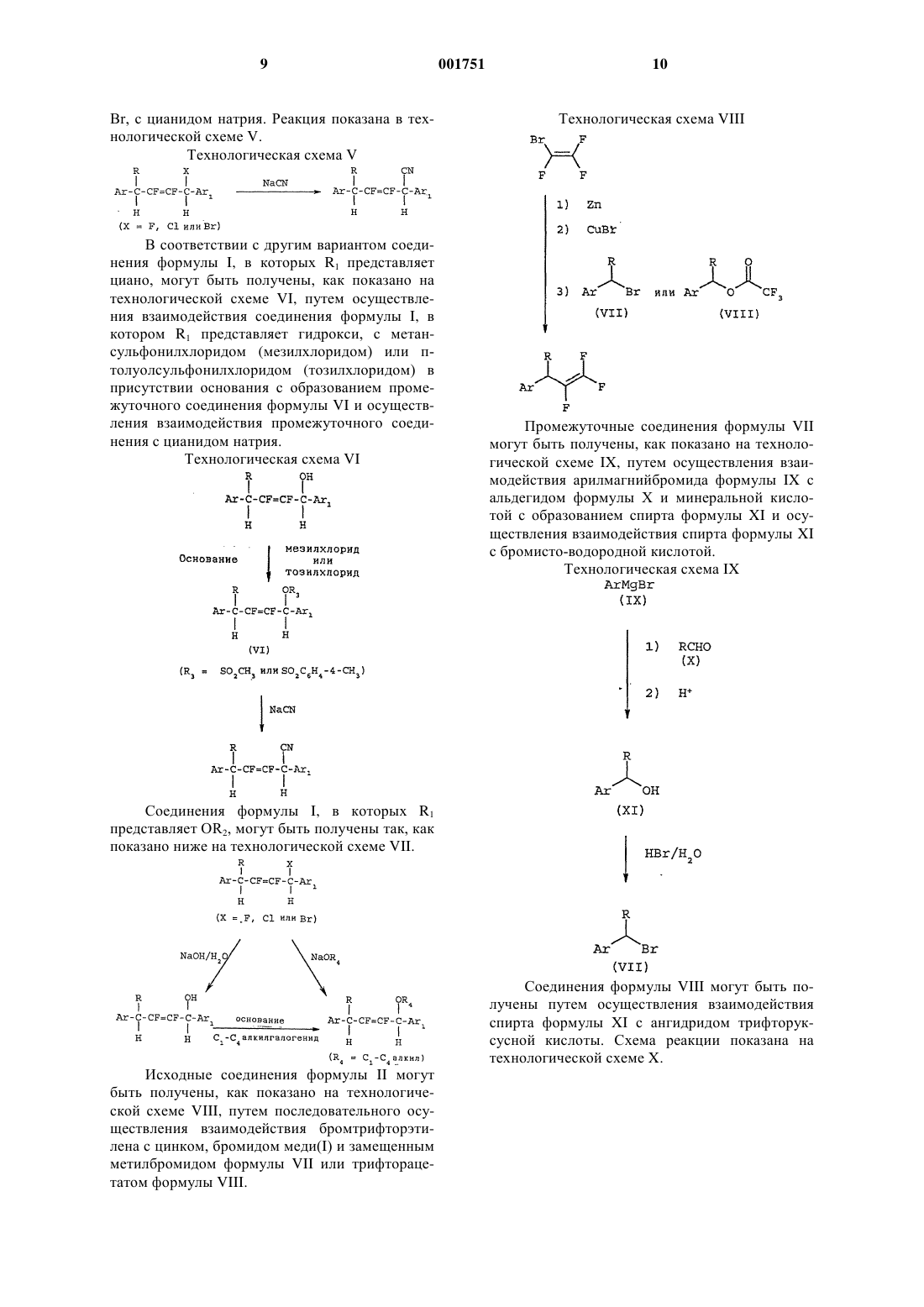
1,4-диарил-2,3-дифтор-2-бутены в качестве инсектицидов и акарицидов.
Формула / Реферат
1. 1,4-Диарил-2,3-дифтор-2-бутены общей формулы
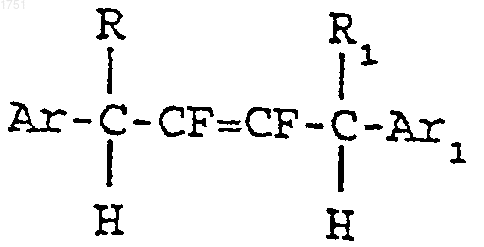
где Аr представляет собой фенил, необязательно замещенный любым сочетанием одной-трех групп, выбранных из галогена, С1-С4алкила, С1-C4алкокси и С1-С4галогеналкокси;
R представляет собой водород, С1-С4алкил или С3-С6циклоалкил;
R1 представляет собой водород;
Аr1 представляет собой феноксифенил, необязательно замещенный любым сочетанием одной-шести групп, выбранных из галогена, С1-С4алкила, C1-С4галогеналкила, С1-С4алкокси или С1-С4галогеналкокси.
2. Соединение по п.1, в котором
R представляет собой изопропил, трифторметил или циклопропил;
R1 представляет собой водород; и
Аr1 представляет собой 3-феноксифенил, необязательно замещенный любым сочетанием одной-шести групп, выбранных из галогена, С1-С4алкила, C1-С4галогеналкила, С1-С4алкокси или С1-С4галогеналкокси.
3. Соединение по п.2, в котором R представляет собой изопропил.
4. Соединение по п.3, выбранное из группы, включающей 4-(п-хлорфенил)-2,3-дифтор-5-метил-1-(м-феноксифенил)-2-гексен, (Е)-изомер;
4-(п-хлорфенил)-2,3-дифтор-1-(4-фтор-3-феноксифенил)-5-метил-2-гексен, (Е)-изомер;
2,3-дифтор-5-метил-1-(м-феноксифенил)-4-[п-(трифторметокси)фенил]-2-гексен, (Е)-изомер;
4-(п-этоксифенил)-2,3-дифтор-1-(м-феноксифенил)-5-метил-2-гексен, (Е)-изомер;
4-(п-этоксифенил)-2,3-дифтор-1-(4-фтор-3-феноксифенил)-5-метил-2-гексен, (Е)-изомер;
2,3-дифтор-1-(4-фтор-3-феноксифенил)-5-метил-4-[п-(трифторметокси)фенил]-2-гексен, (Е)-изомер;
2,3-дифтор-4-(п-фторфенил)-5-метил-1-(м-феноксифенил)-2-гексен, (Е)-изомер; и
2,3-дифтор-1-(4-фтор-3-феноксифенил)-4-(п-фторфенил)-5-метил-2-гексен, (Е)-изомер.
5. Способ борьбы с вредными насекомыми и клещами, который включает контактирование указанных вредителей или их кормовой базы, места обитания или мест размножения с пестицидно эффективным количеством соединения по п.1.
6. Способ по п.5, в котором
R представляет собой изопропил, трифторметил или циклопропил;
R1 представляет собой водород; и
Аr1 представляет собой 3-феноксифенил, необязательно замещенный любым сочетанием одной-шести групп, выбранных из галогена, С1-С4алкила, С1-С4галогеналкила, С1-С4алкокси или С1-С4галогеналкокси.
7. Способ по п.6, в котором R представляет собой изопропил.
8. Способ по п.7, в котором соединение выбирают из группы, включающей
4-(п-хлорфенил)-2,3-дифтор-5-метил-1-(м-феноксифенил)-2-гексен, (Е)-изомер;
4-(п-хлорфенил)-2,3-дифтор-1-(4-фтор-3-феноксифенил)-5-метил-2-гексен, (Е)-изомер;
2,3-дифтор-5-метил-1-(м-феноксифенил)-4-[п-(трифторметокси)фенил]-2-гексен, (Е)-изомер;
4-(п-этоксифенил)-2,3-дифтор-1-(м-феноксифенил)-5-метил-2-гексен, (Е)-изомер;
4-(п-этоксифенил)-2,3-дифтор-1-(4-фтор-3-феноксифенил)-5-метил-2-гексен, (Е)-изомер;
2,3-дифтор-1-(4-фтор-3-феноксифенил)-5-метил-4-[п-(трифторметокси)фенил]-2-гексен, (Е)-изомер;
2,3-дифтор-4-(п-фторфенил)-5-метил-1-(м-феноксифенил)-2-гексен, (Е)-изомер; и
2,3-дифтор-1-(4-фтор-3-феноксифенил)-4-(п-фторфенил)-5-метил-2-гексен, (Е)-изомер.
9. Способ защиты растущих растений от нападения вредных насекомых и клещей или заражения ими, который включает нанесение на листву растений или внесение в почву или воду, где они растут, пестицидно эффективного количества соединения по п.1.
10. Способ по п.9, в котором соединение выбирают из группы, включающей
4-(п-хлорфенил)-2,3-дифтор-5-метил-1-(м-феноксифенил)-2-гексен, (Е)-изомер;
4-(п-хлорфенил)-2,3-дифтор-1-(4-фтор-3-феноксифенил)-5-метил-2-гексен, (Е)-изомер;
2,3-дифтор-5-метил-1-(м-феноксифенил)-4-[п-(трифторметокси)фенил]-2-гексен, (Е)-изомер;
4-(п-этоксифенил)-2,3-дифтор-1-(м-феноксифенил)-5-метил-2-гексен, (Е)-изомер;
4-(п-этоксифенил)-2,3-дифтор-1-(4-фтор-3-феноксифенил)-5-метил-2-гексен, (Е)-изомер;
2,3-дифтор-1-(4-фтор-3-феноксифенил)-5-метил-4-[п-(трифторметокси)фенил]-2-гексен, (Е)-изомер;
2,3-дифтор-4-(п-фторфенил)-5-метил-1-(м-феноксифенил)-2-гексен, (Е)-изомер; и
2,3-дифтор-1-(4-фтор-3-феноксифенил)-4-(п-фторфенил)-5-метил-2-гексен, (Е)-изомер.
11. Способ по п.10, в котором соединение наносят на растения или вносят в почву или воду, где растения растут, при норме приблизительно от 0,1 до 4,0 кг/га.
12. Композиция для борьбы с вредными насекомыми или клещами, которая содержит сельскохозяйственно-приемлемый носитель и пестицидно эффективное количество соединения по п.1.
13. Композиция по п.12, в которой
R представляет собой изопропил, трифторметил или циклопропил;
R1 представляет собой водород; и
Аr1 представляет собой 3-феноксифенил, необязательно замещенный любым сочетанием одной-шести групп, выбранных из галогена, С1-С4алкила, С1-С4галогеналкила, С1-С4алкокси или С1-С4галогеналкокси.
14. Композиция по п.13, в которой R представляет собой изопропил.
15. 3-Арил-1,2-дифтор-1-пропены общей формулы
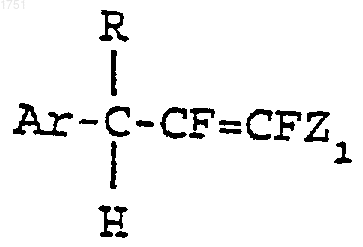
где Аr представляет собой фенил, необязательно замещенный любым сочетанием одной-трех групп, выбранных из галогена, С1-С4алкила, С1-С4галогеналкила, С1-С4алкокси или С1-С4галогеналкокси;
1- или 2-нафтил, необязательно замещенный любым сочетанием одной-трех групп, выбранных из галогена, С1-С4алкила, С1-С4галогеналкила, С1-С4алкокси или С1-С4галогеналкокси; или
5- или 6-членное гетероароматическое кольцо, необязательно замещенное любым сочетанием одной-трех групп, выбранных из галогена, С1-С4алкила, С1-C4галогеналкила, С1-С4алкокси или С1-С4галогеналкокси;
R представляет водород, С1-C4алкил, С1-С4галогеналкил, С3-С6циклоалкил или С3-С6галогенциклоалкил;
Z1 представляет водород или F, и
их оптические и (Е)- и (Z)-изомеры.
16. Соединение по п.15, в котором
Аr представляет собой фенил, необязательно замещенный любым сочетанием одной-трех групп, выбранных из галогена, С1-С4алкила, C1-С4галогеналкила, С1-С4алкокси или С1-С4галогеналкокси; и
R представляет собой С1-С4алкил, С1-С4галогеналкил, С3-С6циклоалкил или С3-С6галогенциклоалкил.
17. Соединение по п.16, в котором R представляет собой изопропил.
18. Способ получения соединения, имеющего структурную формулу
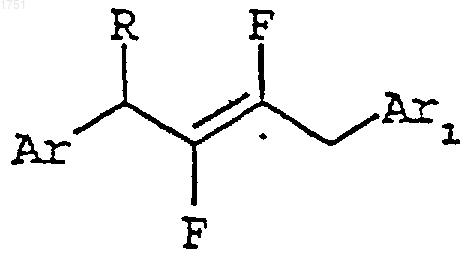
где Аr, Аr1 и R - такие, как определено в п.1,
включающий осуществление взаимодействия 3-арил-1,1,2-трифтор-1-пропена, имеющего структурную формулу
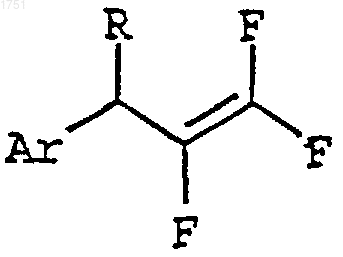
где Аr и R такие, как описано выше, с бис(2-метоксиэтокси)-алюминийгидридом натрия и минеральной кислотой с образованием 3-арил-1,2-дифтор-1-пропена, имеющего структурную формулу
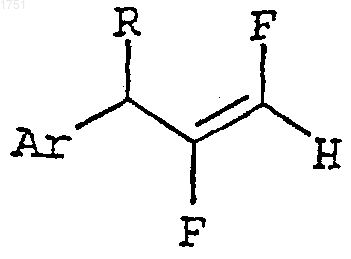
где Аr и R - такие, как описано выше, и затхь осуществление взаимодействия 3-арил-1,2-дифтор-1-пропена с алкиллитием, хлоридом цинка, тетракис(трифенилфосфин)палладием(0) и замещенным метилгалогенидом, имеющим структурную формулу
ZCH2Аr1
где Z представляет Сl, Вr или I, и Аr1 такой, как описано выше.
19. Способ по п.18, в котором
R представляет собой изопропил; и
Аr1 представляет собой 3-феноксифенил, необязательно замещенный любым сочетанием одной-шести групп, выбранных из галогена, С1-C4алкила, C1-С4галогеналкила, С1-С4алкокси или С1-С4галогеналкокси.
Текст
1 Предпосылки создания изобретения Вредные насекомые и клещи уничтожают растущие и убранные сельскохозяйственные культуры. В Соединенных Штатах вынуждены бороться с тысячами видов указанных вредителей сельскохозяйственных культур. В частности, особенно опустошительными для сельскохозяйственных культур являются нападения совок табачных, совок южных и блошек длинноусых. Несмотря на наличие сейчас коммерческих инсектицидов и акарицидов, вредные насекомые и клещи все еще наносят вред сельскохозяйственным культурам как растущим, так и убранным. Поэтому продолжаются исследования по созданию новых, более эффективных инсектицидов и акарицидов. Известны некоторые фторолефиновые соединения, обладающие инсектицидной и акарицидной активностью (см., например, US 5248834; GB 2288803-A; WO 94/06741; WO 97/16067 и одновременно рассматриваемую заявку на патент США 08/856244, поданную 29 мая 1997 г.). Однако фторолефиновые соединения, раскрытые в указанных патентах и заявках на патент, не входят в объем настоящего изобретения. В US 5248834 в общем раскрыты некоторые 1-арил-1-(3-арил-1,2-дифторпроп-1 енил)-циклопропаны. Но в этом патенте не раскрывается способ получения этих соединений. ВUS 5248834 фактически нет способа получения каких-либо фторолефинов. Таким образом, задачей настоящего изобретения является создание соединений, которые были бы высокоэффективны в борьбе с вредными насекомыми и клещами. Задачей настоящего изобретения является также создание способа борьбы с вредными насекомыми и клещами. И еще одной задачей настоящего изобретения является создание способа защиты растущих и убранных сельскохозяйственных культур от повреждения, вызванного нападением насекомых и клещей и заражением ими. Указанные и другие задачи настоящего изобретения станут более очевидны из следующего ниже подробного описания. Краткое изложение существа изобретения В соответствии с настоящим изобретением предлагаются 1,4-диарил-2,3-дифтор-2-бутены,полезные в качестве инсектицидных и акарицидных средств. Эти соединения полезны также для защиты растений от повреждения, вызванного нападением насекомых и клещей и заражения ими. 1,4-Диарил-2,3-дифтор-2-бутены по настоящему изобретению имеют структурную формулу где Ar представляет собой фенил, необязательно замещенный любым сочетанием одной-трех групп, выбранных из галогена, С 1-С 4 алкила, С 1 С 4 алкокси и С 1-С 4 галогеналкокси;R1 представляет собой водород; Аr1 представляет собой феноксифенил, необязательно замещенный любым сочетанием одной-шести групп, выбранных из галогена, С 1 С 4 алкила, С 1-С 4 галогеналкила, С 1-С 4 алкокси или С 1-С 4 галогеналкокси. Предпочтительным соединением формулыR1 представляет собой водород; и Аr1 представляет собой 3-феноксифенил,необязательно замещенный любым сочетанием одной-шести групп, выбранных из галогена, С 1 С 4 алкила, С 1-С 4 галогеналкила, С 1-С 4 алкокси или С 1-С 4 галогеналкокси. Особенно предпочтительным является соединение, в котором R представляет собой изопропил. Наиболее предпочтительным является соединение, выбранное из группы, включающей 4-(п-хлорфенил)-2,3-дифтор-5-метил-1-(мфеноксифенил)-2-гексен, (Е)-изомер; 4-(п-хлорфенил)-2,3-дифтор-1-(4-фтор-3 феноксифенил)-5-метил-2-гексен, (Е)-изомер; 2,3-дифтор-5-метил-1-(м-феноксифенил)4-[п-(трифторметокси)фенил]-2-гексен, (Е)-изомер; 4-(п-этоксифенил)-2,3-дифтор-1-(м-феноксифенил)-5-метил-2-гексен, (Е)-изомер; 4-(п-этоксифенил)-2,3-дифтор-1-(4-фтор-3 феноксифенил)-5-метил-2-гексен, (Е)-изомер; 2,3-дифтор-1-(4-фтор-3-феноксифенил)-5 метил-4-[п-(трифторметокси)фенил]-2-гексен,(Е)-изомер; 2,3-дифтор-4-(п-фторфенил)-5-метил-1-(мфеноксифенил)-2-гексен, (Е)-изомер; и 2,3-дифтор-1-(4-фтор-3-феноксифенил)-4(п-фторфенил)-5-метил-2-гексен, (Е)-изомер. В соответствии с настоящим изобретением также предлагается способ борьбы с вредными насекомыми и клещами, который включает контактирование указанных вредителей или их кормовой базы, места обитания или мест размножения с пестицидно эффективным количеством соединения формулы I. При этом эффективными являются те соединения, в которых 3 Аr1 представляет собой 3-феноксифенил,необязательно замещенный любым сочетанием одной-шести групп, выбранных из галогена, C1 С 4 алкила, C1-С 4 галогеналкила, С 1-С 4 алкокси или С 1-С 4 галогеналкокси, в частности, соединение, в котором R представляет собой изопропил. Особенно эффективным является способ борьбы с вредными насекомыми и клещами,когда соединение выбирают из группы, включающей 4-(п-хлорфенил)-2,3-дифтор-5-метил-1-(мфеноксифенил)-2-гексен, (Е)-изомер; 4-(п-хлорфенил)-2,3-дифтор-1-(4-фтор-3 феноксифенил)-5-метил-2-гексен, (Е)-изомер; 2,3-дифтор-5-метил-1-(м-феноксифенил)4-[п-(трифторметокси)фенил]-2-гексен, (Е)-изомер; 4-(п-этоксифенил)-2,3-дифтор-1-(м-феноксифенил)-5-метил-2-гексен, (Е)-изомер; 4-(п-этоксифенил)-2,3-дифтор-1-(4-фтор-3 феноксифенил)-5-метил-2-гексен, (Е)-изомер; 2,3-дифтор-1-(4-фтор-3-феноксифенил)-5 метил-4-[п-(трифторметокси)фенил]-2-гексен,(Е)-изомер; 2,3-дифтор-4-(п-фторфенил)-5-метил-1-(мфеноксифенил)-2-гексен, (Е)-изомер; и 2,3-дифтор-1-(4-фтор-3-феноксифенил)-4(п-фторфенил)-5-метил-2-гексен, (Е)-изомер. Кроме того, в соответствии с настоящим изобретением предлагается способ защиты растущих растений от нападения вредных насекомых и клещей или заражения ими, который включает нанесение на листву растений или внесение в почву или воду, где они растут, пестицидно эффективного количества соединения формулы I. Предпочтительными являются соединения,выбранные из группы, включающей 4-(п-хлорфенил)-2,3-дифтор-5-метил-1-(мфеноксифенил)-2-гексен, (Е)-изомер; 4-(п-хлорфенил)-2,3-дифтор-1-(4-фтор-3 феноксифенил)-5-метил-2-гексен, (Е)-изомер; 2,3-дифтор-5-метил-1-(м-феноксифенил)4-[п-(трифторметокси)фенил]-2-гексен, (Е)-изомер; 4-(п-этоксифенил)-2,3-дифтор-1-(м-феноксифенил)-5-метил-2-гексен, (Е)-изомер; 4-(п-этоксифенил)-2,3-дифтор-1-(4-фтор-3 феноксифенил)-5-метил-2-гексен, (Е)-изомер; 2,3-дифтор-1-(4-фтор-3-феноксифенил)-5 метил-4-[п-(трифторметокси)фенил]-2-гексен,(Е)-изомер; 2,3-дифтор-4-(п-фторфенил)-5-метил-1-(мфеноксифенил)-2-гексен, (Е)-изомер; и 2,3-дифтор-1-(4-фтор-3-феноксифенил)-4(п-фторфенил)-5-метил-2-гексен, (Е)-изомер. При этом соединение наносят на растения или вносят в почву или воду, где растения растут, при норме приблизительно от 0,1 до 4,0 кг/га. В соответствии с настоящим изобретением предлагается также композиция для борьбы с 4 вредными насекомыми или клещами, которая содержит сельскохозяйственно-приемлемый носитель и пестицидно эффективное количество соединения формулы I. Предпочтительная композиция содержит соединение формулы I, в которой R представляет собой изопропил, трифторметил или циклопропил;R1 представляет собой водород; и Аr1 представляет собой 3-феноксифенил,необязательно замещенный любым сочетанием одной-шести групп, выбранных из галогена, С 1 С 4 алкила, C1-С 4 галогеналкила, С 1-С 4 алкокси или С 1-С 4 галогеналкокси. Особенно предпочтительная композиция содержит соединение формулы I, в котором R представляет собой изопропил. Настоящее изобретение также относится к промежуточным 3-арил-1,2-дифтор-1-пропенам общей формулы XIII где Аr представляет собой фенил, необязательно замещенный любым сочетанием одной-трех групп, выбранных из галогена, С 1-С 4 алкила, С 1 С 4 галогеналкила, С 1-С 4 алкокси или С 1-С 4 галогеналкокси; 1- или 2-нафтил, необязательно замещенный любым сочетанием одной-трех групп, выбранных из галогена, С 1-С 4 алкила, С 1 С 4 галогеналкила,С 1-С 4 алкокси или С 1 С 4 галогеналкокси, или 5- или 6-членное гетероароматическое кольцо, необязательно замещенное любым сочетанием одной-трех групп,выбранных из галогена, С 1-С 4 алкила, С 1 С 4 галогеналкила, С 1-С 4 алкокси или С 1-С 4 галогеналкокси;Z1 представляет водород или F, и их оптические и (Е)- и (Z)-изомеры. Предпочтительно промежуточное соединение, в котором Аr представляет собой фенил, необязательно замещенный любым сочетанием однойтрех групп, выбранных из галогена, С 1C4 алкила, С 1-С 4 галогеналкила, С 1-С 4 алкокси или С 1-С 4 галогеналкокси; иR представляет собой С 1-С 4 алкил, С 1 С 4 галогеналкил, С 3-С 6 циклоалкил или C3 С 6 галогенциклоалкил. Особенно предпочтительно промежуточное соединение, в котором R представляет собой изопропил. В соответствии с настоящим изобретением предложен способ получения соединения,имеющего структурную формулу где Аr, Аr1 и R - такие, как определено выше,для соединений формулы I, включающий осуществление взаимодействия 3-арил-1,1,2 трифтор-1-пропена, имеющего структурную формулу где Аr и R - такие, как описано выше, и затем осуществление взаимодействия 3-арил-1,2 дифтор-1-пропена с алкиллитием, хлоридом цинка, тетракис(трифенилфосфин)палладием(0) и замещенным метилгалогенидом, имеющим структурную формулуZCH2Ar1 где Z представляет Сl, Вr или I, и Ar1 - такой,как описано выше. Предпочтителен способ, согласно которому получают соединение, где R представляет собой изопропил; иAr1 представляет собой 3-феноксифенил,необязательно замещенный любым сочетанием одной-шести групп, выбранных из галогена, С 1C4 алкила, С 1-С 4 галогеналкила, С 1-С 4 алкокси или С 1-С 4 галогеналкокси. Подробное описание изобретения 1,4-Диарил-2,3-дифтор-2-бутены по настоящему изобретению имеют структурную формулу I где Аr, Аr1, R и R1 - такие, как описано выше для формулы I. Кроме того, инсектицидно и гербицидно активными могут являться соединения, соответствующие вышеприведенной формуле I, в которой Аг представляет собой фенил, замещенный одной-тремя группами, такими как С 1 С 4 галогеналкилом или гидрокси, или их сочетанием; 1- или 2-нафтил, необязательно замещенный любым сочетанием одной-трех групп: галогена, С 1-С 4 алкила, С 1-С 4 галогеналкила, С 1-С 4 алкокси или С 1-С 4 галогеналкокси, или 6 5- или 6-членное гетероароматическое кольцо, необязательно замещенное любым сочетанием одной-трех групп: галогена, С 1 С 4 алкила, С 1-С 4 галогеналкила, С 1-С 4 алкокси или С 1-С 4 галогеналкокси;R2 представляет собой водород или С 1C4 алкил; и Аr1 представляет собой фенил, необязательно замещенный любым сочетанием однойпяти групп: галогена, С 1-С 4 алкила, С 1-С 4 галогеналкила, C1-С 4 алкокси или С 1-C4 галогеналкокси; дифенил, необязательно замещенный любым сочетанием одной-пяти групп: галогена, С 1-С 4 алкила, С 1-C4 галогеналкила, С 1 С 4 алкокси или С 1-С 4 галогеналкокси; феноксипиридил, необязательно замещенный любым сочетанием одной-пяти групп: галогена, С 1-С 4 алкила, С 1-С 4 галогеналкила, С 1 С 4 алкокси или С 1-С 4 галогеналкокси; бензилпиридил, необязательно замещенный любым сочетанием одной-пяти групп: галогена, С 1-С 4 алкила, С 1-С 4 галогеналкила, С 1 С 4 алкокси или C1-С 4 галогеналкокси; бензилфенил, необязательно замещенный любым сочетанием одной-пяти групп: галогена,С 1-С 4 алкила, С 1-С 4 галогеналкила, С 1-С 4 алкокси или C1-С 4 галогеналкокси; бензоилфенил, необязательно замещенный любым сочетанием одной-пяти групп: галогена,С 1-С 4 алкила, С 1-С 4 галогеналкила, С 1-С 4 алкокси или C1-С 4 галогеналкокси; 1- или 2-нафтил, необязательно замещенный любым сочетанием одной-трех групп: галогена, С 1-С 4 алкила, С 1-С 4 галогеналкила, С 1 С 4 алкокси или С 1-С 4 галогеналкокси; или 5- или 6-членное гетероароматическое кольцо, необязательно замещенный любым сочетанием одной-трех групп: галогена, С 1 С 4 алкила, С 1-С 4 галогеналкила, С 1-С 4 алкокси или С 1-С 4 галогеналкокси; и их оптические и (E)- и (Z)-изомеры. В контексте настоящего изобретения 5- и 6-членные гетероароматические кольца включают (но не ограничиваются ими) пиридильное,пиразолильное, имидазолильное, триазолильное, изоксазолильное, тетразолильное, пиразинильное, пиридазинильное, триазинильное, фуранильное, тиенильное и тиазолильное кольца,каждое из которых является необязательно замещенным так, как описано выше для формулыI. Примерами вышеуказанного галогена являются фтор, хлор, бром и иод. Термины "С 1 С 4 галогеналкил", "С 3-С 6 галогенциклоалкил" и"C1-C4 галогеналкокси" означают соответственно С 1-С 4 алкильную группу, С 3-С 6 циклоалкильную группу и С 1-С 4 алкоксигруппу, замещенную одним или несколькими атомами галогена. 7 1,4-Диарил-2,3-дифтор-2-бутены по настоящему изобретению особенно полезны для борьбы с совками табачными, совками южными и блошками длинноусыми. В предпочтительном варианте осуществления настоящего изобретения атомы фтора,присоединенные к углеродным атомам с двойной связью в соединениях формулы I, находятся в (Е)-конфигурации по отношению друг к другу. Соединения формулы I, в которых R1 представляет водород, могут быть получены согласно изобретению вышеописанным способом, как показано на технологической схеме I,путем осуществления взаимодействия 3-арил 1,1,2-трифтор-1-пропена формулы II с бис(2 метоксиэтокси)алюминийгидридом натрия и минеральной кислотой, такой как хлористо-водородная кислота, с образованием 3-арил-1,2 дифтор-1-пропена формулы III и затем осуществления взаимодействия соединения формулы III с алкиллитием, таким как н-бутиллитий, хлоридом цинка, тетракис(трифенилфосфин)палладием(0) и замещенным метилгалогенидом формулы IV. Технологическая схема I Соединения формулы I, в которых атомы фтора у двойной связи находятся в Zконфигурации, могут быть получены путем изомеризации описанных выше соединений,которые преимущественно находятся в (Е)конфигурации, с использованием традиционных методов, таких как воздействие света. Соединения формулы I, в которых R1 представляет F, Cl или Вr, могут быть получены взаимодействием соединения формулы I, в котором R1 представляет гидрокси, с тионилхлоридом, тионилбромидом или трифторидом диэтиламиносеры. Схема реакции показана ниже на технологической схеме III. Технологическая схема III В соответствии с другим вариантом соединения формулы I, в которых R1 представляет Сl или Вr, могут быть получены путем галогенирования соединения формулы I, в котором R представляет водород, с хлорирующим агентом, таким как N-хлорсукцинимид, или бромирующим агентом, таким как N-бромсукцинимид. Схема реакции показана ниже на технологической схеме IV. Технологическая схема IV Соединения формулы I, в которых R1 представляет гидрокси, могут быть получены,как показано на технологической схеме II, путем осуществления взаимодействия 3-арил-1,2 дифтор-1-пропена формулы III с алкиллитием,таким как н-бутиллитий, и альдегидом формулы Соединения формулы I, в которых R1 представляет циано, могут быть получены путем осуществления взаимодействия соединения формулы I, в котором R1 представляет F, Сl или В соответствии с другим вариантом соединения формулы I, в которых R1 представляет циано, могут быть получены, как показано на технологической схеме VI, путем осуществления взаимодействия соединения формулы I, в котором R1 представляет гидрокси, с метансульфонилхлоридом (мезилхлоридом) или птолуолсульфонилхлоридом (тозилхлоридом) в присутствии основания с образованием промежуточного соединения формулы VI и осуществления взаимодействия промежуточного соединения с цианидом натрия. Технологическая схема VI Промежуточные соединения формулы VII могут быть получены, как показано на технологической схеме IX, путем осуществления взаимодействия арилмагнийбромида формулы IX с альдегидом формулы Х и минеральной кислотой с образованием спирта формулы XI и осуществления взаимодействия спирта формулы XI с бромисто-водородной кислотой. Технологическая схема IX Соединения формулы I, в которых R1 представляет ОR2, могут быть получены так, как показано ниже на технологической схеме VII. Исходные соединения формулы II могут быть получены, как показано на технологической схеме VIII, путем последовательного осуществления взаимодействия бромтрифторэтилена с цинком, бромидом меди(I) и замещенным метилбромидом формулы VII или трифторацетатом формулы VIII. Соединения формулы VIII могут быть получены путем осуществления взаимодействия спирта формулы XI с ангидридом трифторуксусной кислоты. Схема реакции показана на технологической схеме X. Промежуточные спирты формулы XI могут быть также получены, как показано на технологической схеме XI, путем осуществления взаимодействия арилбромида формулы XII с алкиллитием, таким как н-бутиллитий, и альдегидом формулы X. Технологическая схема XI Другие способы получения соединений формулы I будут очевидны из примеров, представленных ниже. 1,4-Диарил-2,3-дифтор-2-бутены по настоящему изобретению эффективны в борьбе с вредными насекомыми и клещами. Эти соединения эффективны также в защите растущих или убранных сельскохозяйственных культур от повреждения, вызванного нападением насекомых и клещей и заражением ими. Насекомые, в борьбе с которыми эффективны 1,4-диарил-2,3-дифтор-2-бутены по настоящему изобретению, включают чешуекрылых (Lepidoptera), таких как совки табачные,совки капустные, совки хлопковые, совки малые, совки южные и моль капустная; равнокрылых (Homoptera), таких как тли, цикадки, дельфациды и белокрылки; пузыреногих (Thysanoptera), таких как трипсы; жесткокрылых (Coleaptera), таких как долгоносики хлопковые, жуки колорадские, южные блошки длинноусые, западные блошки длинноусые и жуки горчичные; и прямокрылых (Orthoptera), таких как настоящие саранчовые, сверчки, кузнечики и тараканы. Клещи-паразиты (Acarina), для борьбы с которыми можно использовать соединения по настоящему изобретению, включают клещей,таких как клещики двупятнистые паутинные,клещики паутинные карминные, клещи травяные береговые, клещи земляничные, клещи волочковые цитрусовые и клещи лепрозисные. 12 При нанесении соединения формулы I,диспергированного в воде или другом жидком носителе, на растения или почву, в котором указанные культуры растут, для защиты растений от нападения насекомых и клещей и заражения ими практически эффективное его количество составляет обычно примерно 10-10000 частей на миллион и предпочтительно примерно 100-5000 ч/млн. 1,4-Диарил-2,3-дифтор-2-бутены по настоящему изобретению эффективны также в борьбе с вредными насекомыми и клещами при нанесении на листву растений и/или внесении в почву или воду, где упомянутые растения растут, в количестве, достаточном для обеспечения нормы активного компонента в пределах от 0,1 до 4,0 кг/га. Хотя соединения по настоящему изобретению эффективны в борьбе с вредными насекомыми и клещами при использовании их в отдельности, но их можно также использовать в сочетании с другими биологическими химикатами, включая другие инсектициды и акарициды. Например, соединения формулы I по настоящему изобретению можно эффективно применять в сочетании с пиретроидами, фосфатами, карбаматами, циклодиенами, эндотоксином Bacillus thuringiensis (Bt,), форамидинами,фенольными соединениями олова, хлорированными углеводородами, бензоилфенилмочевинами, пирролами и им подобным. Композиции по настоящему изобретению могут быть приготовлены в форме эмульгирующихся концентратов, текучих концентратов или смачивающихся порошков, которые разводят водой или другим подходящим полярным растворителем, обычно in situ (на месте), и затем наносят в виде разбавленного спрея. Указанные композиции могут быть также изготовлены в виде сухих спрессованных гранул, гранулированных препаратов, дустов, пылевидных концентратов, суспензионных концентратов, микроэмульсий и тому подобным, и все их можно наносить (вносить) на семена, в почву, в воду и/или на листву, чтобы обеспечить необходимую защиту растений. Такие препаративные формы или композиции по настоящему изобретению включают соединение по настоящему изобретению (или комбинации таких соединений), смешанное(ые) с одним или несколькими сельскохозяйственно-приемлемыми инертными твердыми или жидкими носителями. Эти композиции содержат пестицидно эффективное количество указанного соединения или соединений, которое можно изменять в зависимости от конкретного соединения, вредителя,предназначенного для уничтожения, и способа применения. Специалисты в данной области могут легко определить пестицидно эффективное количество без излишнего экспериментирования. 13 Чтобы облегчить дальнейшее понимание изобретения, далее представлены примеры,предназначенные в основном для иллюстрации более конкретных деталей настоящего изобретения. Примеры не следует считать ограничивающими объем настоящего изобретения, так как полный объем изобретения определен в пунктах формулы изобретения. Пример 1. Получение п-хлоризопропилбензилового спирта. К раствору изомасляного альдегида (9,08 мл, 0,1 моль) в диэтиловом эфире при -5 С добавляют 1 М раствор п-хлорфенилмагнийбромида в диэтиловом эфире (100 мл). По окончании добавления реакционную смесь перемешивают всю ночь при комнатной температуре,разбавляют смесью воды со льдом и подкисляют 10%-ной хлористо-водородной кислотой. Разделяют фазы и водную фазу экстрагируют диэтиловым эфиром. Органическую фазу и экстракты объединяют, промывают последовательно насыщенным раствором гидрокарбоната натрия, водой и солевым раствором, сушат над безводным сульфатом натрия и концентрируют в вакууме с получением масла. Колоночная хроматография масла с использованием силикагеля и 33%-ного раствора метиленхлорида в гексанах дает указаный в заголовке продукт в виде бесцветного масла (14 г), которое идентифицируют путем спектрального анализа методом ЯМР. Используя по существу такую же процедуру, получают следующие соединения: Смесь п-хлоризопропилбензилового спирта (33,08 г) в 48%-ной бромистоводородной кислоте (330 мл) перемешивают при комнатной температуре в течение 1 ч и экстрагируют гексанами. Объединенные органические экстракты промывают последовательно насыщенным раствором гидрокарбоната натрия и водой, сушат над безводным сульфатом натрия и концентрируют в вакууме с получением указанного в заголовке продукта в виде желтого масла (42,98 г), которое идентифицируют путем спектрального анализа методом ЯМР. Используя по существу такую же процедуру, получают следующие соединения: Смесь цинковой пыли (15,72 г) и бромтрифторэтилена (48,34 г, 0,30 моль) в N,Nдиметилформамиде нагревают до 38 С. После перемешивания при 38 С в течение нескольких минут температуру реакционной смеси повышают до 65 С в течение 30 мин. Затем реакционную смесь перемешивают в течение 90 мин и охлаждают до -5 С. Далее к охлажденной смеси добавляют бромид меди(I) (34,5 г, 0,24 моль). Реакционную смесь перемешивают при комнатной температуре в течение 1 ч, обрабатывают последовательно 1-(1-бром-2-метилпропил)-4 хлорбензолом (18,56 г, 0,075 моль) и лимоненом(5 капель), перемешивают при 49 С на протяжении всей ночи, охлаждают и разбавляют насыщенным раствором хлорида аммония (400 мл) и концентрированным раствором аммиака(100 мл). Полученную водную смесь экстрагируют гексанами. Объединенные органические экстракты промывают последовательно водой,10%-ной хлористо-водородной кислотой, водой,насыщенным раствором гидрокарбоната натрия и водой, сушат над безводным сульфатом натрия и концентрируют в вакууме с получением масла. Колоночная хроматография масла с использованием силикагеля и гексанов дает указанный в заголовке продукт в виде масла(5,54 г), которое идентифицируют путем спектрального анализа методом ЯМР. Используя по существу такую же процедуру, получают следующие соединения: Раствор 3-(п-хлорфенил)-1,1,2-трифтор-4 метил-1-пентена (2,48 г, 0,01 моль) в тетрагидрофуране охлаждают до -8 С, обрабатывают по каплям 3,4 М раствором бис(2-метоксиэтокси) алюминийгидрида натрия в толуоле (3,1 мл),перемешивают всю ночь при комнатной температуре, разбавляют водой, подкисляют 10%-ной хлористо-водородной кислотой и экстрагируют метиленхлоридом. Объединенные органические экстракты промывают последовательно водой,насыщенным раствором гидрокарбоната натрия и водой, сушат над безводным сульфатом натрия и концентрируют в вакууме с получением указанного в заголовке продукта в виде желтого масла (2,10 г), которое идентифицируют путем спектрального анализа методом ЯМР. 16 Используя по существу такую же процедуру, получают следующие соединения: Раствор 3-(п-хлорфенил)-1,2-дифтор-4 метил-1-пентена (0,69 г, 0,003 моль) в тетрагидрофуране охлаждают до -70 С, обрабатывают 2,5 М раствором н-бутиллития в гексане (1,2 мл),перемешивают при -60 С в течение 1 ч, обрабатывают 0,5 М раствором хлорида цинка в тетрагидрофуране (6 мл), перемешивают при -60 С в течение 1 ч, обрабатывают последовательно раствором тетракис(трифенилфосфин)палладия(0) (0,081 г) в тетрагидрофуране и раствором простого -бром-м-толилфенилового эфира(0,789 г, 0,003 моль) в тетрагидрофуране, перемешивают при комнатной температуре всю ночь, разбавляют водой, подкисляют 10%-ной хлористо-водородной кислотой и экстрагируют метиленхлоридом. Объединенные органические экстракты промывают водой, сушат над безводным сульфатом натрия и концентрируют в вакууме с получением масла. Колоночная хроматография масла с использованием силикагеля и пентана дает масло, которое очищают перегонкой по Кугельрору (Kugelrohr) и в результате получают указанный в заголовке продукт в виде бледно-желтого масла (0,46 г), которое идентифицируют путем спектрального анализа методом ЯМР. Используя по существу такую же процедуру, получают следующие соединения: Состояние бесцветное масло бледно-желтое масло желтое масло желтое масло желтое масло бесцветное масло бледно-желтое масло коричневое масло п-этокси Раствор п-бромфенетола (2,01 г, 0,01 моль) в тетрагидрофуране охлаждают до -65 С, обрабатывают по каплям 2,5 М раствором нбутиллития в гексане (4 мл), перемешивают в течение 20 мин при температуре от -55 С до-65 С, обрабатывают по каплям раствором изомасляного альдегида (0,91 мл, 0,01 моль) в тетрагидрофуране, перемешивают всю ночь при комнатной температуре, разбавляют смесью воды со льдом, подкисляют 10%-ной хлористоводородной кислотой и экстрагируют метиленхлоридом. Объединенные органические экстракты промывают последовательно водой, насыщенным раствором гидрокарбоната натрия и водой, сушат над безводным сульфатом натрия и концентрируют в вакууме с получением указанного в заголовке продукта в виде рыжеватокоричневого масла (1,95 г), которое идентифицируют путем спектрального анализа методом ЯМР. Используя по существу такую же процедуру, получают следующие соединения: Смесь ангидрида трифторуксусной кислоты (18 мл) в четыреххлористом углероде охлаждают на водяной бане со льдом, обрабатывают порциями раствора п-этоксиизопропилбензилового спирта (9,0 г) в ССl4, перемешивают при комнатной температуре в течение 1 ч, концентрируют в вакууме, разбавляют ССl4 и концентрируют в вакууме с получением указанного в заголовке продукта в виде коричневого масла(13,23 г), которое идентифицируют путем спектрального анализа методом ЯМР. Используя по существу такую же процедуру, получают следующее соединение: Раствор 2,3-дифтор-4-(п-метоксифенил)-5 метил-1-(м-феноксифенил)-2-гексена, (Е)-изомера (0,408 г, 0,001 моль) в метиленхлориде охлаждают до -10 С, обрабатывают по каплям 1 М раствором трибромида бора в метиленхлориде (1,0 мл, 0,001 моль), перемешивают всю ночь при комнатной температуре, охлаждают,разбавляют метанолом и концентрируют в вакууме с получением остатка. Остаток растворяют в метиленхлориде. Полученный раствор промывают последовательно насыщенным раствором гидрокарбоната натрия и водой, сушат над безводным сульфатом натрия и концентрируют в вакууме с получением коричневого масла. Колоночная хроматография масла с использованием силикагеля и метиленхлорида дает указанный в заголовке продукт в виде бледножелтого масла (0,355 г), которое идентифицируют путем спектрального анализа методом ЯМР. Смесь п-[2,3-дифтор-1-изопропил-4-(мфеноксифенил)-2-бутен-1-ил]фенола,(Е)-изомера (0,173 г), диоксана (6 мл) и воды (4,5 мл) обрабатывают последовательно дифторхлорметаном (70 капель) и гидроксидом натрия (0,217 г), перемешивают при 70 С в течение 1 ч, охлаждают, обрабатывают дополнительно дифторхлорметаном (50 капель) и гидроксидом натрия(0,245 г), нагревают при 58-66 С в течение 3 ч,охлаждают, обрабатывают дополнительно дифторхлорметаном (50 капель) и гидроксидом натрия (0,185 г), нагревают еще 2,5 ч, перемешивают всю ночь при комнатной температуре и разбавляют водой. Полученную водную смесь экстрагируют метиленхлоридом. Объединенные органические экстракты промывают водой, сушат над безводным сульфатом натрия и концентрируют в вакууме с получением светлокоричневого масла. Колоночная хроматография масла с использованием силикагеля и метиленхлорида дает указанный в заголовке продукт в виде бесцветного масла (0,134 г), которое идентифицируют путем спектрального анализа методом ЯМР. Пример 10. Оценка инсектицидных и акарицидных свойств испытуемых соединений. Растворы для испытаний готовят путем растворения испытуемого соединения в 35%ной смеси ацетона в воде с обеспечением концентрации 10000 частей на миллион. Последующие разбавления производят по необходимости водой. Гусеницы Spodoptera eridania третьей возрастной стадии, совка южная (SAW) Лист фасоли лимской длиной до 7-8 см погружают в испытуемый раствор при перемешивании на 3 с и дают обсохнуть в вытяжном шкафу. Затем лист помещают на чашку Петри(10010 мм), на дне которой находится влажная фильтровальная бумага и десять гусениц третьей возрастной стадии. Через 5 дней производят осмотр для выявления смертности, сниженного питания или каких-либо отклонений от нормальной линьки.Diabrotica virgifera, virgifera Leconte, блошка длинноусая западная (WCR) третьей возрастной стадии В широкогорлую стеклянную банку с навинчивающейся крышкой емкостью 30 мл помещают 1 см 3 тонко измельченного талька. На 20 тальк наносят пипеткой 1 мл соответствующего испытуемого ацетонового раствора, обеспечивая 1,25 мг активного компонента на банку. Банки помещают в слабый ток воздуха до тех пор, пока не испарится ацетон. Сухой тальк разрыхляют и в каждую банку добавляют 1 см зерен проса, служащих пищей для насекомых, и 25 мл влажной почвы. Банку закрывают крышкой и содержимое подвергают тщательному механическому перемешиванию. Затем в каждую банку помещают 10 блошек третьей возрастной стадии и банки закрывают не плотно с тем,чтобы обеспечить воздухообмен для личинок. Через 5 дней обработки определяют смертность. Недостающих личинок считают мертвыми, поскольку они быстро разлагаются и их нельзя найти. Концентрации активного компонента,используемые в этом испытании, соответствуют приблизительно 50 кг/га.Heliothis virescens, совка табачная (TBW) третьей возрастной стадии Семядоли хлопка погружают в испытуемый раствор и затем дают им возможность обсохнуть в вытяжном шкафу. После обсыхания каждую из них разрезают на 4 части и по 10 частей помещают в пластмассовые медицинские чашки емкостью 30 мл, в которых находятся кусочки влажных зубоврачебных тампонов длиной 5-7 мм. В каждую чашку помещают 1 гусеницу третьей возрастной стадии и закрывают чашку картонной крышкой. Обработку продолжают 3 дня, после чего вычисляют смертность и оценивают повреждение снижения питания.Aphis fabae, смешанная возрастная стадия,тля бобовая (ВА) За день до испытания горшки с одиночными растениями настурции (Tropaeolum sp.) высотой около 5 см заражают примерно 100-200 тлями. Каждый горшок обрызгивают испытуемым раствором в течение 2 оборотов поворотного (4 об/мин) стола в вытяжном шкафу. Струю направляют так, чтобы полностью покрыть растения тлей. Обрызганные горшки устанавливают на белые поддоны и выдерживают 2 дня, после чего оценивают смертность.Tetranychus urticae (OP-устойчивая линия),клещик паутинный двупятнистый (TSM) Отбирают растения фасоли лимской с первичными листами, выросшими до 7-8 см, и, удалив лишние, оставляют по одному растению на горшок. Из зараженного листа, взятого из основной колонии, вырезают небольшой кусочек и помещают на каждый лист испытуемого растения. Это делают примерно за 2 ч до обработки, чтобы дать клещам возможность, перемещаясь по растению, отложить яйца. Размер вырезанной части зараженного листа варьируют так,чтобы получить примерно 100 клещей на лист. В момент обработки при испытании кусочек листа, использованный для переноса клещей,снимают и выбрасывают. Вновь зараженные растения погружают на 3 с в испытуемый рас 21 твор с перемешиванием и затем помещают в вытяжной шкаф для обсушивания. Через 2 дня лист извлекают и определяют смертность. Испытания оценивают по шкале, показанной ниже, и полученные результаты представляют в табл. 1. Соединениям, использованным в вышеописанных оценочных испытаниях, присваивают номер и идентифицируют их по названию. В табл. 1 данные приведены по номеру соединения. Шкала оценок 0 = нет эффекта 1 = 10-25% убитых 2 = 26-35% убитых 3 = 36-45% убитых 4 = 46-55% убитых 22 Соединения, оцененные как инсектициды и акарициды Номер соединения 1 4-(п-хлорфенил)-2,3-дифтор-5-метил-1-(мфеноксифенил)-2-гексен, (Е)-изомер 2 4-(п-хлорфенил)-2,3-дифтор-1-(4-фтор-3 феноксифенил)-5-метил-2-гексен,(Е)-изомер 3 2,3-дифтор-5-метил-1-(м-феноксифенил)-4[п-(трифторметокси)фенил]-2-гексен,(Е)-изомер 4 4-(п-этоксифенил)-2,3-дифтор-1-(м-феноксифенил)-5-метил-2-гексен, (Е)-изомер 5 4-(п-этоксифенил)-2,3-дифтор-1-(4-фтор-3 феноксифенил)-5-метил-2-гексен,(Е)-изомер 6 2,3-дифтор-1-(4-фтор-3-феноксифенил)-5 метил-4-[п-(трифторметокси) фенил]-2 гексен, (Е)-изомер 7 2,3-дифтор-4-(п-фторфенил)-5-метил-1-(мфеноксифенил)-2-гексен, (Е)-изомер 8 2,3-дифтор-1-(4-фтор-3-феноксифенил)-4(п-фторфенил)-5-метил-2-гексен,(Е)-изомер Таблица 1 Оценка инсектицидных и акарицидных свойств Номер соединения 1 2 3 4 5 6 7 8 где Аr представляет собой фенил, необязательно замещенный любым сочетанием одной-трех групп, выбранных из галогена, С 1-С 4 алкила, С 1C4 алкокси и С 1-С 4 галогеналкокси;R1 представляет собой водород; Аr1 представляет собой феноксифенил, необязательно замещенный любым сочетанием одной-шести групп, выбранных из галогена, С 1 С 4 алкила, C1-С 4 галогеналкила, С 1-С 4 алкокси или С 1-С 4 галогеналкокси. 2. Соединение по п.1, в которомR1 представляет собой водород; и Аr1 представляет собой 3-феноксифенил,необязательно замещенный любым сочетанием одной-шести групп, выбранных из галогена, С 1 С 4 алкила, C1-С 4 галогеналкила, С 1-С 4 алкокси или С 1-С 4 галогеналкокси. 3. Соединение по п.2, в котором R представляет собой изопропил. 4. Соединение по п.3, выбранное из группы, включающей 4-(п-хлорфенил)-2,3-дифтор-5 метил-1-(м-феноксифенил)-2-гексен,(Е)-изомер; 4-(п-хлорфенил)-2,3-дифтор-1-(4-фтор-3 феноксифенил)-5-метил-2-гексен, (Е)-изомер; 2,3-дифтор-5-метил-1-(м-феноксифенил)4-[п-(трифторметокси)фенил]-2-гексен, (Е)-изомер; 4-(п-этоксифенил)-2,3-дифтор-1-(м-феноксифенил)-5-метил-2-гексен, (Е)-изомер; 4-(п-этоксифенил)-2,3-дифтор-1-(4-фтор-3 феноксифенил)-5-метил-2-гексен, (Е)-изомер; 2,3-дифтор-1-(4-фтор-3-феноксифенил)-5 метил-4-[п-(трифторметокси)фенил]-2-гексен,(Е)-изомер; 2,3-дифтор-4-(п-фторфенил)-5-метил-1-(мфеноксифенил)-2-гексен, (Е)-изомер; и 2,3-дифтор-1-(4-фтор-3-феноксифенил)-4(п-фторфенил)-5-метил-2-гексен, (Е)-изомер. 5. Способ борьбы с вредными насекомыми и клещами, который включает контактирование указанных вредителей или их кормовой базы, 23 места обитания или мест размножения с пестицидно эффективным количеством соединения по п.1. 6. Способ по п.5, в которомR1 представляет собой водород; и Аr1 представляет собой 3-феноксифенил,необязательно замещенный любым сочетанием одной-шести групп, выбранных из галогена, С 1 С 4 алкила, С 1-С 4 галогеналкила, С 1-С 4 алкокси или С 1-С 4 галогеналкокси. 7. Способ по п.6, в котором R представляет собой изопропил. 8. Способ по п.7, в котором соединение выбирают из группы, включающей 4-(п-хлорфенил)-2,3-дифтор-5-метил-1-(мфеноксифенил)-2-гексен, (Е)-изомер; 4-(п-хлорфенил)-2,3-дифтор-1-(4-фтор-3 феноксифенил)-5-метил-2-гексен, (Е)-изомер; 2,3-дифтор-5-метил-1-(м-феноксифенил)4-[п-(трифторметокси)фенил]-2-гексен, (Е)-изомер; 4-(п-этоксифенил)-2,3-дифтор-1-(м-феноксифенил)-5-метил-2-гексен, (Е)-изомер; 4-(п-этоксифенил)-2,3-дифтор-1-(4-фтор-3 феноксифенил)-5-метил-2-гексен, (Е)-изомер; 2,3-дифтор-1-(4-фтор-3-феноксифенил)-5 метил-4-[п-(трифторметокси)фенил]-2-гексен,(Е)-изомер; 2,3-дифтор-4-(п-фторфенил)-5-метил-1-(мфеноксифенил)-2-гексен, (Е)-изомер; и 2,3-дифтор-1-(4-фтор-3-феноксифенил)-4(п-фторфенил)-5-метил-2-гексен, (Е)-изомер. 9. Способ защиты растущих растений от нападения вредных насекомых и клещей или заражения ими, который включает нанесение на листву растений или внесение в почву или воду,где они растут, пестицидно эффективного количества соединения по п.1. 10. Способ по п.9, в котором соединение выбирают из группы, включающей 4-(п-хлорфенил)-2,3-дифтор-5-метил-1-(мфеноксифенил)-2-гексен, (Е)-изомер; 4-(п-хлорфенил)-2,3-дифтор-1-(4-фтор-3 феноксифенил)-5-метил-2-гексен, (Е)-изомер; 2,3-дифтор-5-метил-1-(м-феноксифенил)4-[п-(трифторметокси)фенил]-2-гексен, (Е)-изомер; 4-(п-этоксифенил)-2,3-дифтор-1-(м-феноксифенил)-5-метил-2-гексен, (Е)-изомер; 4-(п-этоксифенил)-2,3-дифтор-1-(4-фтор-3 феноксифенил)-5-метил-2-гексен, (Е)-изомер; 2,3-дифтор-1-(4-фтор-3-феноксифенил)-5 метил-4-[п-(трифторметокси)фенил]-2-гексен,(Е)-изомер; 2,3-дифтор-4-(п-фторфенил)-5-метил-1-(мфеноксифенил)-2-гексен, (Е)-изомер; и 2,3-дифтор-1-(4-фтор-3-феноксифенил)-4(п-фторфенил)-5-метил-2-гексен, (Е)-изомер. 11. Способ по п.10, в котором соединение наносят на растения или вносят в почву или во 001751 24 ду, где растения растут, при норме приблизительно от 0,1 до 4,0 кг/га. 12. Композиция для борьбы с вредными насекомыми или клещами, которая содержит сельскохозяйственно-приемлемый носитель и пестицидно эффективное количество соединения по п.1. 13. Композиция по п.12, в которойR1 представляет собой водород; и Аr1 представляет собой 3-феноксифенил,необязательно замещенный любым сочетанием одной-шести групп, выбранных из галогена, С 1 С 4 алкила, С 1-С 4 галогеналкила, С 1-С 4 алкокси или С 1-С 4 галогеналкокси. 14. Композиция по п.13, в которой R представляет собой изопропил. 15. 3-Арил-1,2-дифтор-1-пропены общей формулы где Аr представляет собой фенил, необязательно замещенный любым сочетанием одной-трех групп, выбранных из галогена, С 1-С 4 алкила, С 1 С 4 галогеналкила,С 1-С 4 алкокси или С 1 С 4 галогеналкокси; 1- или 2-нафтил, необязательно замещенный любым сочетанием одной-трех групп, выбранных из галогена, С 1-С 4 алкила, С 1 С 4 галогеналкила, С 1-С 4 алкокси или С 1-С 4 галогеналкокси; или 5- или 6-членное гетероароматическое кольцо, необязательно замещенное любым сочетанием одной-трех групп, выбранных из галогена, С 1-С 4 алкила, С 1-C4 галогеналкила, С 1 С 4 алкокси или С 1-С 4 галогеналкокси;Z1 представляет водород или F, и их оптические и (Е)- и (Z)-изомеры. 16. Соединение по п.15, в котором Аr представляет собой фенил, необязательно замещенный любым сочетанием однойтрех групп, выбранных из галогена, С 1 С 4 алкила, C1-С 4 галогеналкила, С 1-С 4 алкокси или С 1-С 4 галогеналкокси; и включающий осуществление взаимодействия 3 арил-1,1,2-трифтор-1-пропена, имеющего структурную формулу 26 где Аr и R такие, как описано выше, и затем осуществление взаимодействия 3-арил-1,2 дифтор-1-пропена с алкиллитием, хлоридом цинка, тетракис(трифенилфосфин)палладием(0) и замещенным метилгалогенидом, имеющим структурную формулуR представляет собой изопропил; и Аr1 представляет собой 3-феноксифенил,необязательно замещенный любым сочетанием одной-шести групп, выбранных из галогена, С 1C4 алкила, C1-С 4 галогеналкила, С 1-С 4 алкокси или С 1-С 4 галогеналкокси.
МПК / Метки
МПК: A01N 31/14, C07C 43/29
Метки: инсектицидов, акарицидов, 1,4-диарил-2,3-дифтор-2-бутены, качестве
Код ссылки
<a href="https://eas.patents.su/14-1751-14-diaril-23-diftor-2-buteny-v-kachestve-insekticidov-i-akaricidov.html" rel="bookmark" title="База патентов Евразийского Союза">1,4-диарил-2,3-дифтор-2-бутены в качестве инсектицидов и акарицидов.</a>
Предыдущий патент: Способ лечения заболеваний, связанных с образованием конкрементов
Следующий патент: Терапевтическое лечение глазных заболеваний, связанных с фактором роста сосудистого эндотелия
Случайный патент: Замещенные [2-(1-пиперазинил)этокси]метильные соединения, способ их получения и их применение