Эффективные противоопухолевые лекарственные средства
Номер патента: 5564
Опубликовано: 28.04.2005
Авторы: Джавацци Рафаэлла, Д'инкальчи Маурицио, Фэрклот Глинн Томас, Такахаси Наото, Гешер Андреас, Вейтмен Стив
Формула / Реферат
1. Применение ET-743 для изготовления лекарственного препарата для эффективного лечения опухоли посредством комбинированной терапии, включающей применение ET-743 в синергической комбинации с другим противоопухолевым лекарственным средством.
2. Применение противоопухолевого лекарственного средства для изготовления лекарственного препарата для эффективного лечения опухоли посредством комбинированной терапии, включающей применение противоопухолевого лекарственного средства в синергической комбинации с ET-743.
3. Применение по п.1 или 2, при котором ET-743 образует часть этого лекарственного препарата.
4. Применение по п.1 или 2, при котором ET-743 представлен в форме отдельного лекарственного препарата.
5. Применение по п.4, при котором отдельный лекарственный препарат, содержащий ET-743, вводится в одно и то же время, что и лекарственный препарат, содержащий противоопухолевое лекарственное средство.
6. Применение по п.4, при котором отдельный лекарственный препарат, содержащий ET-743, вводится в другое время, чем лекарственный препарат, содержащий противоопухолевое лекарственное средство.
7. Применение по любому из предшествующих пунктов, при котором комбинированная терапия включает ET-743 и антрациклин.
8. Применение по п.7, при котором комбинированная терапия включает ET-743 и доксорубицин.
9. Применение по любому из пп.1-6, при котором комбинированная терапия включает ET-743 и противоопухолевое соединение на основе платины.
10. Применение по п.9, при котором противоопухолевое соединение на основе платины представляет собой цисплатин или карбоплатин.
11. Применение по любому из пп.1-6, при котором комбинированная терапия включает ET-743 и противоопухолевое таксановое лекарственное средство.
12. Применение по п.11, при котором противоопухолевое таксановое лекарственное средство представляет собой паклитаксел или доцетаксел.
13. Применение по любому из пп.1-6, при котором комбинированная терапия включает ET-743 и антиметаболитное противоопухолевое лекарственное средство.
14. Применение по п.6, при котором антиметаболитное противоопухолевое лекарственное средство представляет собой гемцитрабин или 5-фторурацил.
15. Применение по любому из пп.1-6, при котором комбинированная терапия включает ET-743 и противоопухолевое лекарственное средство, направленное против топоизомеразы.
16. Применение по п.14, при котором противоопухолевое лекарственное средство, направленное против топоизомеразы представляет собой SN-38.
17. Применение по любому из предшествующих пунктов, при котором комбинированная терапия дополнительно включает дексаметазон.
Текст
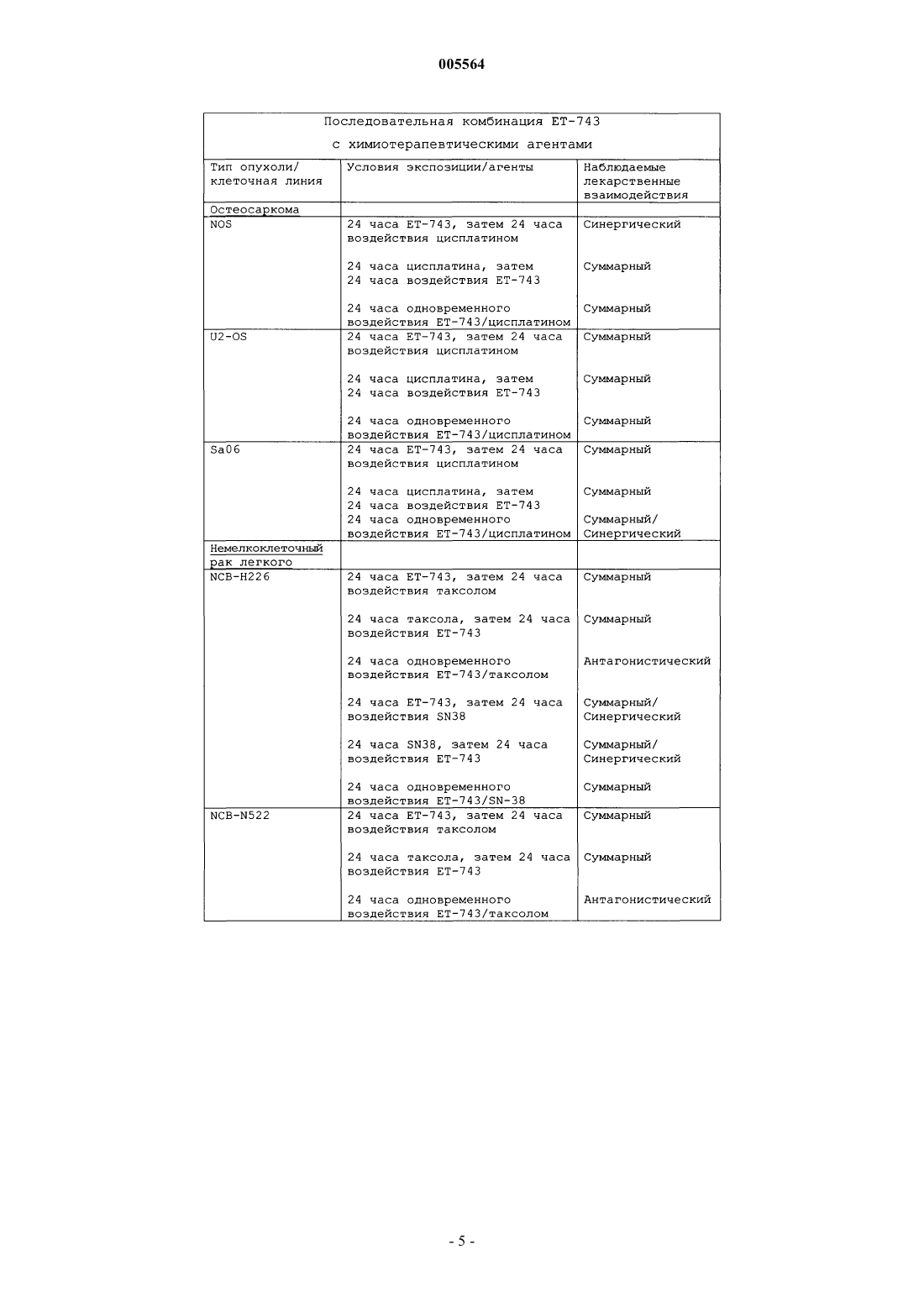
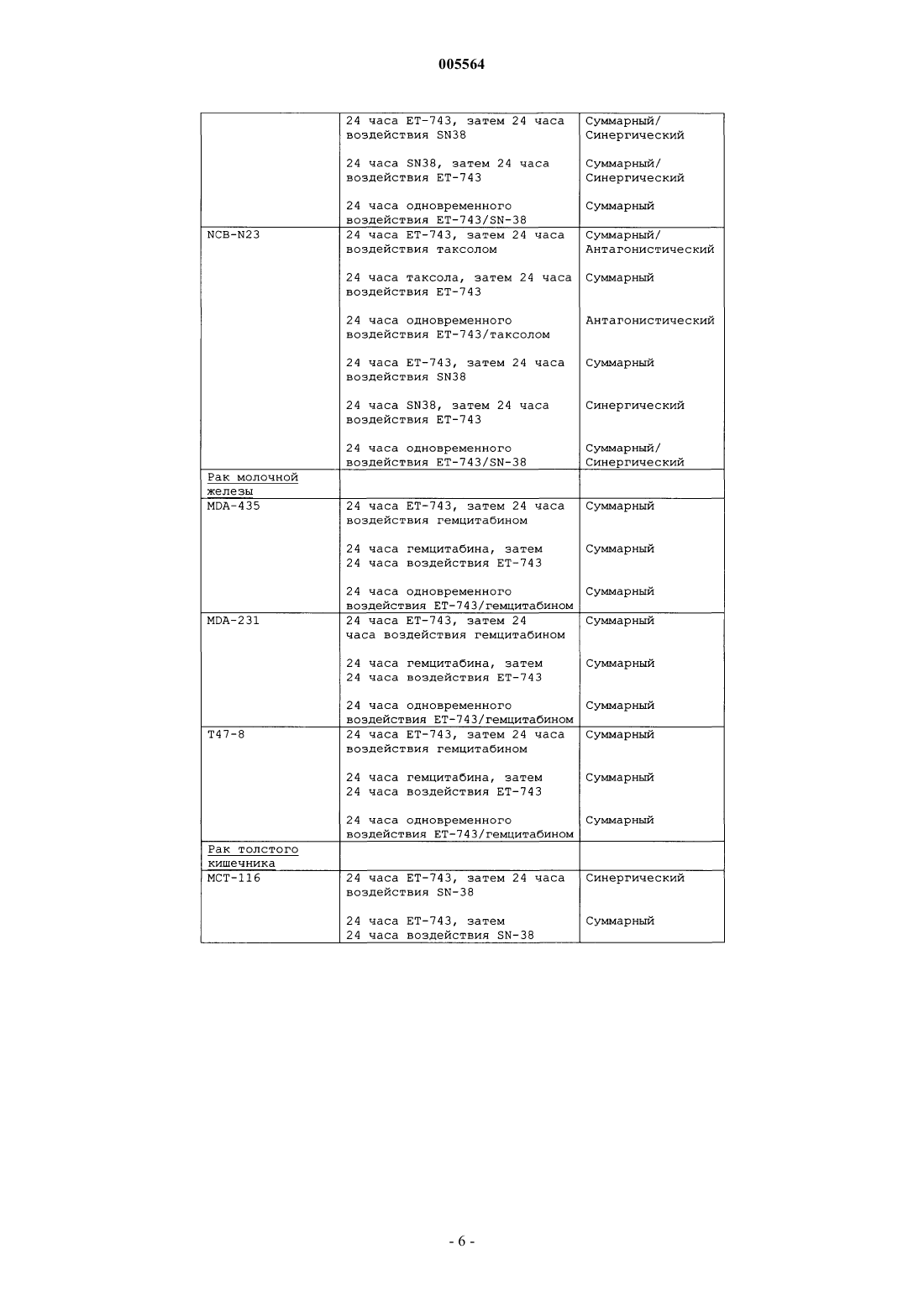
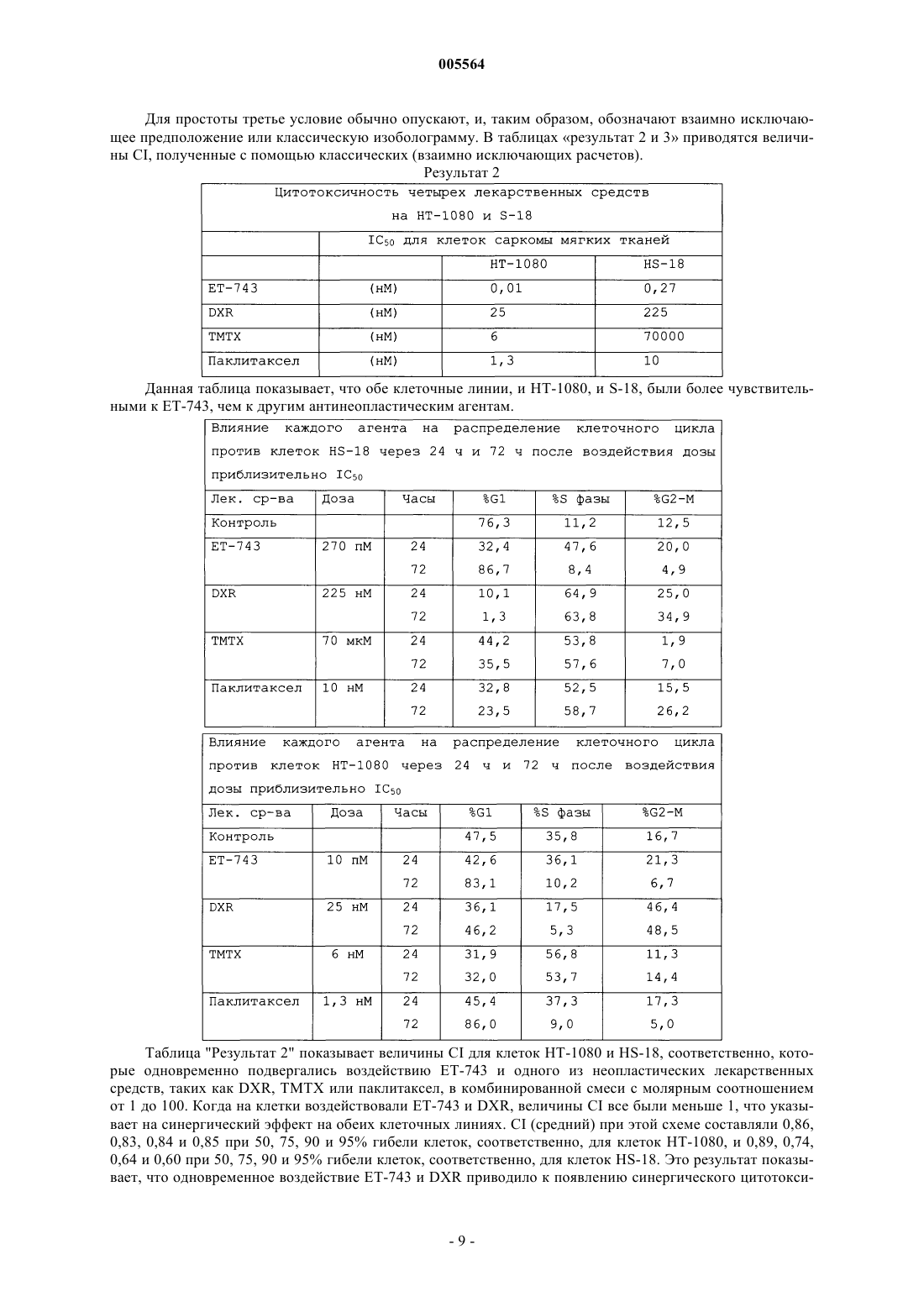
005564 Настоящее изобретение относится к эффективным противоопухолевым лекарственным средствам. Эктеинасцидин 743, ЕТ 743, представляет собой противоопухолевый агент, полученный из морского источника. Предпосылки к созданию изобретения Заявка WO0069441, опубликованная 23 ноября 2000 г., раскрывает композиции и применения ЕТ 743 для лечения рака. Данный текст включен в качестве ссылки. Краткое описание сущности изобретения В соответствии с одним аспектом настоящего изобретения авторы разработали эффективные комбинированные лекарственные средства на основе эктеинасцидина 743, с использованием других лекарственных средств. Предпочтительные варианты осуществления изобретения Другие лекарственные средства могут составлять часть одной и той же композиции или представлять собой отдельные композиции для введения в одно и то же время или в разное время. Идентичность других лекарственных средств специально не ограничивается, и подходящие кандидаты включают:a) лекарственные средства с антимитотическим эффектом, особенно те, которые нацелены на элементы цитоскелета, включая модуляторы микротрубочек, такие как таксановые лекарственные средства(такие как таксол, паклитаксел, таксотер, доцетаксел), подофилотоксины или алкалоиды барвинка (винкристин, винбластин);c) алкилирующие агенты, такие как азотистые иприты (такие как циклофосфамид или ифосфамид);d) лекарственные средства, которые нацелены на ДНК, такие как антрациклиновые лекарственные средства адриамицин, доксорубицин, фарморубицин или эпирубицин;e) лекарственные средства, которые нацелены на топоизомеразы, такие как этопозид;f) гормоны и агонисты или антагонисты гормонов, такие как эстрогены, антиэстрогены (тамоксифен и родственные соединения) и андрогены, флутамид, лейпрорелин, гозерелин, ципротрон или октреотид;g) лекарственные средства, которые нацелены на сигнальную трансдукцию в опухолевых клетках,включая производные антител, такие как герцептин;h) алкилирующие лекарственные средства, такие как лекарственные средства на основе платиныi) лекарственные средства, потенциально воздействующие на метастазы опухолей, такие как ингибиторы металлопротеиназ матрикса;j) средства генной терапии и десенсибилизирующие агенты;k) терапевтические антитела; 1) другие биологически активные соединения морского происхождения, особенно дидемнины, такие как аплидин;n) противовоспалительные лекарственные средства, в частности, дексаметазон; и о) противорвотные лекарственные средства, в частности, дексаметазон. В качестве части описания настоящего патента заявители включают серию примеров и с настоящего момента будут ссылаться на них. Данные примеры демонстрируют повышенную эффективность ЕТ 743, когда его применяют в комбинации с другими лекарственными средствами, и относится к различным комбинациям с использованием ЕТ-743. Пример 1 относится к эффективным комбинациям ЕТ-743 и доксорубицина в отношении ингибирования опухолевого роста у бестимусных мышей при саркомах морских видов животных и человека. Пример 2 показывает, что эктеинасцидин 743 (ЕТ-743) и доксорубицин оказывают синергическое цитотоксическое действие на линиях саркомы мягких тканей НТ-1080 и HS-18. Указанные два примера показывают более чем суммарные эффекты комбинации ЕТ-743 с антрациклинами (в частности, доксорубицином), которая является более эффективной в отношении опухолей человека (в данных конкретных примерах - против саркомы), чем каждый из них по отдельности; данный эффект наблюдается независимо от последовательности введения. Данные результаты внушают ясные надежды в том, что касается лечения пациентов. Пример 3 показывает синергический цитотоксический эффект ЕТ-743 и цисплатина. Пример 4 представляет последовательную оценку ЕТ-743 в комбинации с химиотерапевтическими агентами против ряда клеточных линий опухолей человека, в частности, комбинаций ЕТ-743 с доксорубицином, таксолом, SN-38, цисплатином и гемцитабином. Указанные два примера показывают более чем суммарные эффекты комбинации ЕТ-743 с платиновыми противоопухолевыми соединениями (в частности, с цисплатином), с нуклеозидным аналогом гемцитабином и с ингибитором топоизомеразы II (SN38, который представляет собой активный агент, получаемый из пролекарства СРТ-11, лекарственного средства группы камптотецина). И снова данные комбинации являются более эффективными в отношении опухолей человека чем каждое из лекарственных-1 005564 средств по отдельности (в данных конкретных примерах - против различных опухолевых клеток: яичника, толстого кишечника, легкого, молочной железы, костной саркомы); их эффекты в некоторых случаях зависели от последовательности введения. И снова, данные результаты внушают ясные надежды в том,что касается лечения пациентов. Интересно, что синергическое действие не было четко спрогнозировано: пример 4 показывает, что у большинства испытанных комбинаций синергизм не наблюдался (действительно, в некоторых случаях наблюдался антагонизм). Пример 5 относится к оценке комбинаций ЕТ-743 с доксорубицином или триметрексатом или паклитакселом. Он показывает более чем суммарные эффекты комбинации ЕТ-743 с антрациклинами (в частности,с доксорубицином), которая является более эффективной в отношении опухолей человека чем каждое из лекарственных средств по отдельности (в данных конкретных примерах - против саркомы); их эффекты не зависели от последовательности введения. Данные результаты внушают ясные надежды в том, что касается лечения пациентов. Примеры 6-8 подтверждают и дополняют предыдущие примеры, и, особенно, показывают синергизм ЕТ-743 и доксорубицина, а также ЕТ-743 с цисплатином. Пример 9 показывает эффективность разного рода при использовании комбинаций по настоящему изобретению, когда дексаметазон в высоких дозах защищает от гепатотоксичности эктеинасцидина-743(ЕТ-743). В целом, настоящее изобретение, таким образом, относится к композициям, способам лечения, способам изготовления композиций и к связанным с ними вариантам осуществления настоящего изобретения. Настоящее изобретение относится также к соединениям по настоящему изобретению для применения в способе лечения, и к применению соединений для изготовления композиции для лечения злокачественной опухоли. Таким образом, настоящее изобретение относится к способу лечения любого млекопитающего, особенно человека, страдающего злокачественной опухолью, который включает введение пораженному индивидууму терапевтически эффективного количества соединения по настоящему изобретению или его фармацевтической композиции. Настоящее изобретение относится также к фармацевтическим препаратам, включающим фармацевтически приемлемый носитель, которые содержат в качестве активного ингредиента соединение или соединения по настоящему изобретению, а также к способам их изготовления. Примеры фармацевтических композиций включают любую твердую форму (таблетки, пилюли, капсулы, гранулы и т.п.) или жидкую форму (растворы, суспензии или эмульсии) подходящего состава, для перорального, местного или парентерального введения, и они могут содержать чистое соединение или его комбинацию с любым носителем или другими фармакологически активными соединениями. Данные композиции могут нуждаться в стерильности, если их вводят парентерально. Введение соединений или композиций по настоящему изобретению можно осуществлять любым подходящим способом, таким как внутривенная инфузия, оральное, интраперитонеальное и внутривенное введение. Заявители предпочитают, чтобы время инфузии составляло до 24 ч, более предпочтительно 2-12 ч, наиболее предпочтительно 2-6 ч. Особенно желательны кратковременные инфузии, которые позволяют осуществлять лечение, не оставляя пациента в клинике на ночь. Однако инфузия может продолжаться от 12 до 24 ч и даже дольше, если это необходимо. Инфузию можно осуществлять с подходящими интервалами, например от 2 до 4 недель. Фармацевтические композиции, содержащие соединения по настоящему изобретению, можно доставлять с помощью липосом или наносфер, композиций с замедленным высвобождением или с помощью любых других обычных средств доставки. Правильная дозировка соединений будет изменяться в зависимости от конкретной композиции,способа введения и конкретного места, пациента и опухоли, по поводу которой проводится лечение. Также следует принимать во внимание другие факторы, такие как возраст, масса тела, пол, характер питания, время введения, скорость выведения, состояние пациента, комбинации лекарственных средств,реакции чувствительности и тяжесть заболевания. Введение можно осуществлять непрерывно или периодически, в пределах максимально переносимой дозы. Комбинации по настоящему изобретению можно применять у пациентов, плохо поддающихся лечению. WO0069441 содержит информацию по поводу схем дозирования ЕТ-743 и иную информацию по применению комбинированной терапии по настоящему изобретению. Примеры настоящего изобретения Пример 1. Эффективные комбинации ЕТ-743 и доксорубицина для ингибирования опухолевого роста в отношении мышиной и человеческой саркомы у бестимусных мышей. У ЕТ-743 имеется подтвержденная клиническая активность в отношении пациентов с саркомой мягких тканей и кости, которые не поддавались предыдущей химиотерапии, включающей доксорубицин(Dx) и изосфамид. С точки зрения потенциальной клинической ценности комбинирования ЕТ-743 с Dx,заявители изучали данную комбинацию против мышиной фибросаркомы UV2237, ее mdr-резистентной-2 005564 сублинии UV2237/ADR и человеческого ксенотрансплантата рабдомиосаркомы ТЕ 671. Как ЕТ-743, так иDx по отдельности были эффективны против мышиной фибросаркомы UV2237, в то время как каждый из них не был активен или маргинально активен против UV2237/ADR и ТЕ 671. Однако комбинация ЕТ 743 и Dx была эффективной в отношении всех трех моделей. Синергизм был частично выражен в отношении человеческой рабдомиосаркомы ТЕ 671 и проявлялся независимо от последовательности введения или комбинации лекарственных средств. После однократных в/в введений, выполненных, когда опухоль ТЕ 671 составляла приблизительно 100 мг, величины ингибирования массы опухоли (TWI) и log10 убитых клеток (LCK) составляли, соответственно, 46% и 0,132 для ЕТ-743 (0,1 мг/кг) в отдельности, 50% и 0,33 для Dx (10 мг/кг) в отдельности, 77% и 0,924 для ЕТ-743 (0,1 мг/кг) и Dx (10 мг/кг) при одновременном введении, 82% и 1,12 для комбинации ЕТ-743 (0,1 мг/кг), введенного за 1 ч до Dx (10 мг/кг), и 75% и 0,85 для комбинации ЕТ-743(0,1 мг/кг), введенного через 1 ч после Dx (10 мг/кг). Приведенные данные наводят на мысль о том, что комбинация ЕТ-743 и Dx может также быть эффективной в отношении опухолей, которые являются нечувствительными или недостаточно чувствительными к данным лекарствам в отдельности, что дает основание для клинических исследований с использованием данной комбинации. Пример 2. Эктеинасцидин 743 (ЕТ 743) и доксорубицин оказывают синергическое цитотоксическое действие в отношении линий саркомы мягких тканей НТ-1080 и HS-18. Две клеточные линии саркомы, НТ-1080, клеточную линию фибросаркомы, чувствительную к ЕТ 743 (IC50 = 10 пм), и HS-18, клеточную линию липосаркомы, менее чувствительную к ЕТ-743 (IC5 = 270 пм), оценивали на токсичность к ЕТ-743 в комбинации с доксорубицином, триметрексатом или паклитакселом. Когда ЕТ-743 использовали в комбинации с каждым из данных лекарственных средств при постоянном молярном соотношении и анализировали способом Chou и Talalay, были получены синергические эффекты (72 ч инкубации) с комбинацией ЕТ-743 - доксорубицин, но не с комбинацией ЕТ-743 с триметрексатом или паклитакселом. Когда клетки подвергали воздействию ЕТ-743 в течение 72 ч, и доксорубицина, триметрексата или паклитаксела в течение последних 48 ч инкубации, синергические эффекты также были получены с доксорубицином против обеих клеточных линий саркомы. Интересно, что последовательность паклитаксел, а затем - ЕТ-743 была более эффективной, чем обратная последовательность. Данные результаты обнадеживают в отношении клинических испытаний доксорубицина в комбинации с ЕТ-743 для лечения пациентов с саркомой мягких тканей, поскольку оба указанных лекарственных средства показали активность в отношении данного заболевания. Пример 3. Синергический цитотоксический эффект ЕТ-743 и цисплатина. Эктеинасцидин 743 (ЕТ 743) продемонстрировал отличную противоопухолевую активность на нескольких доклинических системах и обещает быть активным в клинических условиях. ЕТ-743 связываетN2 гуанины в малой бороздке и влияет на транскрипцию (Minuzzo et al., RNAS, Vol. 97, 6780-84, 2000). Ранее проводившиеся исследования указывают, что чувствительность к ЕТ-743 дефицитных клеток после репарации за счет ошибочного спаривания оснований (MMR) и профицитных клеток является одинаковой. NER дефицитные клетки, весьма чувствительные к цисплатину, в 6-8 раз менее чувствительны к ЕТ-743. На основании различных механизмов, участвующих в репарации ЕТ-743 и цисплатина,и в силу потенциальной клинической заинтересованности в данной комбинации, заявители осуществили исследования для оценки цитотоксических эффектов ЕТ-743 и цисплатина на нескольких клеточных линиях опухолей человека. В данном исследовании использовали клеточную линию рака яичника человекаIgrove-1, сублинию, резистентную к ЕТ-743 (IG/PSC/ET), клеточную линию рака толстого кишечника человека НСТ 116, (MMR дефицитную) и HCT11-ch3 (MMR профицитную). На клетки воздействовали в течение 1 или 24 ч различными концентрациями ЕТ-743 или цисDDР,по отдельности или в комбинациях, и оценивали цитотоксичность с помощью колориметрического анализа после окрашивания сульфородамином В. Во всех клеточных линиях наблюдался синергический эффект как при 1-часовой, так и при 24-часовой экспозиции. Интересно, что у НСТ 116, резистентных к цисDDР, ЕТ-743 был отчетливо способен реверсировать чувствительность даже при концентрациях ЕТ 743, которые по отдельности были малоэффективными. Все вместе эти данные дают основание для проведения клинических исследований, комбинирующих ЕТ-743 с цисDDР. Пример 4. Комбинации ЕТ-743 с доксорубицином, таксолом, SN-38, цисплатином и гемцитабином. ЕТ-743 оценивали в комбинации с доксорубицином, таксолом, Sn-38, цисплатином и гемцитабином против ряда клеточных линий опухолей человека. Данные исследования были спланированы таким образом, чтобы определить тип лекарственного взаимодействия между ЕТ-743 и обычными химиотерапевтическими агентами, а также влияние последовательности воздействия на противоопухолевую активность. Для описания типа лекарственного взаимодействия использовались множественные комбинации ЕТ-743 с обычными цитотоксическими агентами при свободном выборе моделей (Laska, et al., Biometrics 50:834,1994). Данные исследования предполагают, что независимо от экспозиции наиболее типично наблюдался суммарный характер лекарственного взаимодействия.-3 005564 Синергическое лекарственное взаимодействие наблюдалось, когда ЕТ-743 комбинировали против опухолевых клеточных линий немелкоклеточного рака легких (с предварительной экспозицией SN-38),остеосаркомы (с предварительной экспозицией ЕТ-743, а затем - цисплатином), рака молочной железы (с предварительной экспозицией ЕТ-743, а затем - гемцитабином), рака толстого кишечника (с предварительной экспозицией ЕТ-743, а затем - SN-38 и одновременной экспозицией SN-38). Наблюдался суммарный/синергический характер лекарственного взаимодействия (с предварительной экспозицией ЕТ 743, а затем - SN-38 против NSCL; с предварительной экспозицией SN-38 против рака толстого кишечника и NSCL; одновременная экспозиция с цисплатином против остеосаркомы и SN-38 против линийNSCL). Были отмечены свидетельства антагонизма, когда таксол применяли одновременно против двух линий NSCL, и доксорубицин - против клеточной линии рабдомиосаркомы. Указанные исследования наводят на мысль о том, что ЕТ-743, который находится на II фазе клинических испытаний, можно было бы комбинировать с несколькими цитотоксическими агентами против обширного ряда типов опухолей. Материалы и методы Культура клеток Опухолевые клеточные линии рака молочной железы человека (MDA-435, MDA-231, Т-470), немелкоклеточного рака легкого (NCI-Н 522, NCI-H226, NCI-H23), рака толстого кишечника (НСТ-116, НТ 29, Colo-320), остеосаркомы (HOS, U-2, OS, SaOS-2), рабдомиосаркомы (RH1, RH30, RD) выращивали в среде RPMI-1640 с добавлением 10% фетальной бычьей сыворотки и 2 мМ L-глутамина. Все маточные культуры поддерживали во флаконах 75 см 2 при 37 С в термостатах с увлажнением в атмосфере с 5% СO2 - 95% воздуха. Анализ IC50: Предварительно определенное количество опухолевых клеток в стадии экспоненциального роста инокулировали в 96-луночные планшеты для клеточных культур и оставляли стабилизироваться на 24 ч. После этого к клеткам добавляли планшет с лекарственными средствами, состоящий из серийных разведений ЕТ-743 или обычных химиотерапевтических агентов. Клетки 24-часовой экспозиции инкубировали в течение трех дней, после чего добавляли МТТ на 4 ч. Полученные кристаллы формазана затем солюбилизировали кислотой/спиртом и определяли поглощение (570 нм для теста/630 нм для стандарта) с использованием микропланшет-ридера. Результаты выражали как процент убитых опухолевых клеток по сравнению со средовыми контролями. Изучение комбинаций Для изучения комбинаций использовали схему концентраций (выраженных как процент от IС 50 отдельных агентов), чтобы охарактеризовать тип взаимодействия, показанный ниже: Статистический анализ изучения комбинаций Статистические сравнения осуществляли с каждой испытуемой комбинацией (75:25 - ЕТ 743/обычные агенты) и конечной точкой (100:0 - ЕТ-743 и 0:100 обычные агенты). Статистически значимые наблюдения требуют, чтобы существовала разница между величиной поглощения комбинации (ЕТ 743 и обычных агентов) и обеими конечными точками (ЕТ-743 и обычных агентов по отдельности). Если большинство величин ( 3 из 5) находились статистически выше или ниже данной линии, то это определяется, соответственно, как антагонизм или синергизм. В другом случае характер взаимодействия более походит на суммарное взаимодействие. Интерпретация является очень трудной, если имеется значительный наклон к линии, соединяющей конечные точки. Если наклон кривых IC50 для отдельных агентов идентичен (маловероятно), то можно, со временем, определить тип взаимодействия. Выводы-Резюме Данные исследования предполагают, что, независимо от последовательности воздействия ЕТ-743 и обычных химиотерапевтических агентов, наиболее часто наблюдается лекарственное взаимодействие по принципу суммарного. Свидетельства синергизма наблюдались, когда клеточные линии NSCL NCl-H522 и NCl-H23 подвергали предварительному воздействию SN-38, предварительному воздействию ЕТ-743 с цисплатином против остеосаркомы HOS, гемцитабином против клеточной линии рака молочной железы Т-470, SN-38 против рака толстого кишечника НСТ-116 и одновременному воздействию SN-38 против клеточной линии рака толстого кишечника Colo-320. Свидетельства антагонизма наблюдались, когда таксол применяли одновременно против клеточных линий NSCL NCl-H522 и NCl-H23, и доксорубицин - против опухолевой клеточной линии рабдомиосаркомы RHI. Пример 5. Взаимодействие между ЕТ-743 и другими антинеопластическими агентами. Хотя ЕТ-743 в настоящее время проходит клинические испытания в отношении злокачественных опухолей человека, механизмы противоопухолевой активности ЕТ-743 еще не до конца понятны. Целью настоящего исследования являлась оценка природы взаимодействия между ЕТ-743 и другими антинеопластическими агентами (доксорубицином; DXR, триметрексатом; ТМТХ и паклитакселом; таксолом) с использованием индекса комбинации (CI) по способу Chou и Talalay. Для того, чтобы лучше понять, каким образом ЕТ-743 можно было бы использовать клинически, в настоящем исследовании использовали анализы SRB для изучения цитотоксичности, вызываемой комбинированием ЕТ-743 с тремя другими антинеопластическими агентами, при различных схемах введения, на двух клеточных линиях саркомы мягких тканей, НТ-1080 и HS-18, in vitro. DXR был единственным агентом, который демонстрировал синергизм, независимо от последовательности введения, при комбинировании с ЕТ-743. Одновременное воздействие ЕТ-743 с DXR приводило к синергическим взаимодействиям на обеих клеточных линиях.CI (средние) по схеме составляли 0,86, 0,83, 0,84 и 0,85 при 50, 75, 90 и 95% гибели клеток, соответственно, на клетках НТ-1080, и 0,89, 0,74, 0,64 и 0,60 при 50, 75, 90 и 95% гибели клеток, соответственно,на клетках HS-18. Последовательное введение с ЕТ-743 за 24 ч до DXR представляло собой наиболее эффективный режим против обеих клеточных линий; это приводило к устойчиво низкому CI приблизительно до уровня гибели клеток 90% для обеих клеточных линий. Воздействие таксолом до воздействия ЕТ-743 также представляло собой эффективный режим. Данные результаты предполагают, что комбинацию ЕТ-743 и DXR необходимо далее изучать в клинических испытаниях для лечения саркомы мягких тканей. Материалы и методы Химические реактивы ЕТ-743 получали от компании Pharma-Mar S. A (Tres Cantos, Madrid, Испания) и изготавливали из него 2 мМ маточный раствор в диметилсульфоксиде. Паклитаксел и DXR получали от компании SigmaChemical Co. (St. Louis, МО). ТМТХ получали от компании Warner-Lambert (Parke-Davis, Ann Arbor,Mich.). Культура клеток Клеточные линии саркомы мягких тканей, НТ-1080 и HS-18 поддерживали в виде монослойных культур в RPMI-1640, содержащей 10% фетальной бычьей сыворотки. Анализ цитотоксичности с использованием SRB Цитотоксичность лекарственных средств определяли с помощью анализа цитотоксичности с использованием SRB, который выполняли на 96-луночных микротитрационных планшетах, как описано. Клетки засевали в две дублирующие лунки (5000 клеток на лунку) и подвергали воздействию лекарственных средств при различных концентрациях. Клетки фиксировали 50% раствором ТСА в течение 1 ч, и в каждую лунку добавляли 0,4% SRB (Sigma). После 30 мин инкубирования планшет промывали 1% уксусной кислотой и считывали на 570 нм на микропланшет-ридере Biowhitaker 2001. Лунки с клетками, не содержавшие лекарственных средств, и со средой и лекарственными средствами, но без клеток, использовали как положительный и отрицательный контроли, соответственно. Одновременное воздействие ЕТ-743 и DXR, ТМТХ или паклитакселом Клетки засевали в 96-луночные планшеты, как описано ранее. На клетки воздействовали семью различными концентрациями лекарственных средств по отдельности или комбинированной смесью при молярном соотношении 1:100 (ЕТ-743: другие лекарственные средства). После 72 ч воздействия ингибирование роста определяли с помощью анализа SRB. Последовательное воздействие ЕТ-743 и DXR, ТМТХ или паклитакселом Используя те же условия эксперимента, которые описаны выше, заявители подвергали клетки воздействию трех различных концентраций лекарственных средств, которые представляют IC25, IC50, IC75 ЕТ-743, DXR, ТМТХ и паклитаксела, соответственно. После 24 ч предварительного воздействия ЕТ-743 или комбинированным лекарственным средством в соответствующие лунки добавляли вторые лекарственные средства на 48 ч. Ингибирование роста определяли с помощью анализа SRB. Анализ клеточного цикла На клетки в фазе экспоненциального роста воздействовали лекарственными средствами в течение нескольких часов или оставляли их без воздействия лекарственных средств. Затем клетки собирали и фиксировали в ледяном 70% метаноле. ДНК окрашивали йодидом пропидия, как описано ранее. Десять тысяч окрашенных клеток анализировали на клеточном сортере с возбуждением флюоресценции BectonDickinson (FACS). Определение синергизма и антагонизма и построение изоболограмм Величины CI рассчитывали с помощью уравнения Chou-Talalay, которое учитывает как активность(Dm или IC50), так и форму кривой доза-эффект (величину m). Общее уравнение для классической изоболограммы (CI = 1) выводят следующим образом:CI = (D)1/(Dx)1 + (D)2/(Dx)2 (A) где (Dx)1 и (Dx)2 в знаменателях представляют собой дозы (или концентрации) для D1 (ЕТ-743) и D2(другое лекарственное средство) по отдельности, что дает Х% ингибирования, в то время как (D)1 и (D)2 в числителях представляют собой дозы ЕТ-743 и другого лекарственного средства в комбинации, которые также ингибировали Х% (т.е., изоэффективные). CI1, CI = 1, CI1 означают синергизм, суммарный эффект и антагонизм, соответственно.(Dx)1 или (Dx)2 можно легко рассчитать по уравнению медиана-эффект Chou и Chou et al:(B) где Dm представляет собой дозу медиана-эффект, которую получают из антилогарифма Х-отрезка, отсекаемого на оси ординат графика медиана-эффект, X-log (D) против Y-log[fa/(1-fa)] или Dm = 10 -(Y-отрезок)/m, а m представляет собой наклон графика медиана-эффект. Компьютерная программа Chou и Chou позволяет производить автоматические расчеты величин m, Dm, Dx и CI. Из (Dm)1, (Dm)2 и D1 + D2 легко построить изоболограммы, автоматически основанные на уравнении А. Для консервативных взаимно не исключающих изоболограмм двух агентов к уравнению А добавляют третье условие, (D1) (D2)/(DX)1(DX)2.-8 005564 Для простоты третье условие обычно опускают, и, таким образом, обозначают взаимно исключающее предположение или классическую изоболограмму. В таблицах результат 2 и 3 приводятся величины CI, полученные с помощью классических (взаимно исключающих расчетов). Результат 2 Данная таблица показывает, что обе клеточные линии, и НТ-1080, и S-18, были более чувствительными к ЕТ-743, чем к другим антинеопластическим агентам. Таблица "Результат 2" показывает величины CI для клеток НТ-1080 и HS-18, соответственно, которые одновременно подвергались воздействию ЕТ-743 и одного из неопластических лекарственных средств, таких как DXR, ТМТХ или паклитаксел, в комбинированной смеси с молярным соотношением от 1 до 100. Когда на клетки воздействовали ЕТ-743 и DXR, величины CI все были меньше 1, что указывает на синергический эффект на обеих клеточных линиях. CI (средний) при этой схеме составляли 0,86,0,83, 0,84 и 0,85 при 50, 75, 90 и 95% гибели клеток, соответственно, для клеток НТ-1080, и 0,89, 0,74,0,64 и 0,60 при 50, 75, 90 и 95% гибели клеток, соответственно, для клеток HS-18. Это результат показывает, что одновременное воздействие ЕТ-743 и DXR приводило к появлению синергического цитотокси-9 005564 ческого эффекта. Напротив, когда на клетки воздействовали ЕТ-743 и ТМТХ или паклитакселом, наблюдался антагонистический цитотоксический эффект. График CI получали для обеих клеточных линий, которые первоначально подвергали воздействию ЕТ-743 в течение 24 ч, а затем - DXR в течение 48 ч. В обеих клеточных линиях последовательное воздействие ЕТ-743 и DXR приводило к появлению синергического цитотоксического эффекта, величина CI для НТ-1080 при уровне гибели клеток 80% составляла 0,640,12, а та же величина для HS-18 при уровне гибели клеток 88% составляла 0,240,06. Напротив, последовательное воздействие DXR и ЕТ-743 (результат 3 а, нижняя фигура) показало, на первый взгляд, хорошую величину CI, однако величина CI для НТ-1080 при уровне гибели клеток 80% составляла 1,000,03, что указывало на суммарный эффект двух агентов, кроме того, CI при самой высокой фракции гибели была хуже, чем при средней фракции гибели для обеих клеточных линий. Когда клетки подвергали воздействию ЕТ-743, а затем - ТМТХ, величины CI для НТ-1080 показывали около единицы или более единицы, что указывает на антагонистический или суммарный характер эффекта двух данных агентов. Напротив, те же величины для HS-18 все были менее 0,6, что указывает на синергический эффект двух данных агентов. Когда на клетки воздействовали сначала ТМТХ, а затем ЕТ-743, наблюдался суммарный эффект в обеих клеточных линиях, НТ-1080 и HS-18. Последовательное воздействие паклитакселом и ЕТ-743 производило синергическое цитотоксическое действие. Когда на клетки воздействовали паклитакселом, а затем - ЕТ-743, величина CI для НТ 1080 при уровне гибели клеток 89% составляла 0,920,06, а та же величина для HS-18 при уровне гибели клеток 78% составляла 0,380,13. Заключение ЕТ-743 являлся высокоактивным агентом против клеток саркомы мягких тканей человека, особенно против клеточной линии злокачественной фибросаркомы НТ-1080.DXR при комбинировании с ЕТ-743 демонстрировал синергизм, независимо от последовательности воздействия, однако последовательность ЕТ-743, а затем - DXR была более эффективной против обеих клеточных линий. Воздействие паклитакселом, а затем - ЕТ-743 также являлось эффективным режимом против клеток саркомы мягких тканей человека, в то время как одновременное воздействие было антагонистическим. Пример 6. Комбинации химиотерапевтических агентов с эктеинасцидином 743 (ЕТ 743) против солидных опухолей in vivo. Несколько уникальных механизмов действия было описано для ЕТ-743, включая связывание с малой бороздкой ДНК, алкилирование N2 гуанина, ингибирование транскрипции гена MDR1 (Jin et al.,PNAS 97, 6775, 2000; Minuzzo et al., PNAS 97, 6780, 2000) и противодействие активации нуклеарного рецептора SXR (Synold et al., Nature Med. 7, 584, 2001). В качестве единственного агента ЕТ-743 ингибирует рост опухоли in vivo, достигая полных ремиссий (CR), против нескольких опухолевых линий человека (Hendriks et al., Ann. Oncol. 10, 1233, 1999), включая меланому (MEXF 989), NSCL (LXFL 529), рака яичника (HOC 22) и рака молочной железы (МХ-1). Эффективность ЕТ-743 в комбинации с лекарственными средствами, которые действуют с помощью других механизмов, может предоставить возможности для снижения токсичности лекарственного средства или потенцировать эффективность лекарственного средства при резистентных или рецидивирующих злокачественных опухолях. Для указанной оценки несколько агентов, включая доксорубицин (DOX; 8 мг/кг), цисплатин (DDP; 12 мг/кг) и винбластин (VINB; 6 мг/кг) вводили до/после ЕТ-743 (0,2 мг/кг), с 1 ч предварительного воздействия qdx5, в одну или более из следующих опухолей: хондросаркому (CSHA), остеосаркому (OSAFH), фибросаркому (SW684), яичника (MRI-H-1834), NSCL (LX-1) и почки (MRI-H-121), с активностью,определяемой как 50% Т/С. На модели полого волокна (HF) последовательность DOX, 1 ч предварительного воздействия ЕТ-743 была устойчиво более эффективной, чем ЕТ-743 в отдельности, в отношении хондросаркомы (6% против 10%), фибросаркомы (33% против 48%) и остеосаркомы (20% против 34%). Ксенотрансплантаты остеосаркомы показали сходные результаты - 17% против 43%. HF исследования с DPP показали, что воздействие ЕТ-743 с предварительным воздействием DDP было более эффективным, чем ЕТ-743 в отдельности при опухоли яичника (28% против 100%) и хондросаркоме (15% против 19%), и показало эквивалентную активность при остеосаркоме (36% Т/С). Данные по ксенотрансплантатам подтверждают, что последовательность воздействия ЕТ-743 с предварительным воздействиемDDP является более эффективной, чем ЕТ-743 в отдельности (35% против 66%). Наблюдалось одно исключение с NSCL, когда ЕТ-743 в отдельности был неактивным (62% Т/С), но воздействие DPP, а затем ЕТ-743 вызывало CR ( 1% Т/С). В почечных ксенотрансплантатах ЕТ-743 в отдельности был очень активным (22% Т/С), но ЕТ-743 с последующим VINB также вызывал CR ( 1% Т/С). На подходе отдельные исследования с другими обычными агентами на опухолевых ксенотрансплантатах рака молочной железы, почки, меланомы и опухолей желудка. Пример 7. Доклиническая активность и биораспределение комбинаций эктеинасцидина 743 (ЕТ 743) и доксорубицина (DOX) в рабдомиосаркоме человека.- 10005564 ЕТ-743 представляет собой первый агент из нового класса противоопухолевых агентов, который демонстрирует противоопухолевую активность. ЕТ-743 показал активность у пациентов с саркомой,рефракторной к DOX и ифосфамиду. С точки зрения его потенциала в качестве эффективного лекарственного средства, заявители изучили (1) доклиническую противоопухолевую активность комбинацииET-743/DOX против рабдомиосаркомы человека ТЕ 671 и (2) возможные взаимодействия между лекарственными средствами и их биораспределение у бестимусных мышей и в ксенотрансплантатах опухолей.In vitro: Эффект каждого лекарственного средства или комбинации после воздействий в течение 1 ч оценивали с помощью клоногенного анализа. ЕТ-743 или DOX по отдельности показали противоопухолевую активность против клеток ТЕ 671. Комбинация, согласно анализу изоболограммы и индексу комбинации, была по меньшей мере суммарной в отношении нескольких опухолевых клеточных линий,включая ТЕ 671.In vivo: Однократно в/в бестимусным мышам вводили (ЕТ-743, 0,1 мг/кг; DOX, 10 мг/кг), когда опухоли-ксенотрансплантаты достигали массы приблизительно 100 мг. Ингибирование массы опухоли/величины log10 гибели клеток составляли 46%/0,132 для ЕТ-743 в отдельности, 50%/0,33 для DOX в отдельности, 77%/0,924 для ЕТ-743 и DOX при одновременном введении, 82%/1,12 для комбинации ЕТ 743, введенном за 1 ч до DOX, и 75%/0,85, когда ЕТ-743 вводили через 1 ч после DOX. Синергический эффект также наблюдался против мышиной фибросаркомы UV2237 и против его сублинии UV2237/ADR с множественной резистентностью к лекарственным средствам. Указанные данные показывают синергический эффект ET-743/DOX, который, как представляется,не зависит от последовательности введения или комбинации лекарственных средств по данным экспериментам, полученным к настоящему времени. Ни плазменные, ни опухолевые концентрации DOX не отличались достоверно друг от друга, когда DOX вводили в отдельности или в комбинации с ЕТ-743. Оценка фармакокинетики (РК) ЕТ-743 в отдельности или в комбинации с DOX в настоящее время изучается. Комбинация ЕТ-743 и DOX оказывается in vitro суммарной, но синергической in vivo в отношении рабдомиомы ТЕ 671. На РК профиль DOX не влияет одновременное воздействие ЕТ-743. Указанные данные дают основания для изучения данной комбинации в ранних клинических испытаниях. Пример 8. ЕТ-743 и цисплатин (DDP) показывают in vitro и in vivo синергизм против клеточных линий саркомы и рака яичника человека. Заявители показали в данном исследовании, что ЕТ-743 усиливает активность DDP как in vitro, так и in vivo. На нескольких клеточных линиях злокачественных опухолей, включая рак тонкого кишечника человека (НСТ 116), рак яичника (Igrov-1, А 2780), их резистентных сублиниях (Igrov-1/PSC-ET и 1 А 9,соответственно) и рабдомиосаркоме (ТЕ 671), более низкие концентрации ЕТ-743, используемого в качестве единственного агента, могли потенцировать активность DDP по меньшей мере в 2 раза. Концентрации, соответствующие IC30/IC50 ЕТ-743 обеспечивали как суммарный, так и синергический эффекты. Указанные результаты привели к исследованиям in vivo с использованием моделей ксенотрансплантатов для изучения эффективных комбинаций лекарственных средств с ЕТ-743. Для п/к трансплантированной ТЕ 671, частично чувствительной как к ЕТ-743, так и к DDP, комбинация двух лекарственных средств оказывала противоопухолевое действие, которое было гораздо больше, чем то, которое достигалось одним из двух лекарственных средств, использовавшихся при их соответственных MTD уровнях. Опухоль яичников 1 А 9, которая обычно резистентна как к ЕТ-743, так и кDDP в качестве единственных агентов, в комбинации давала ингибирование опухолевого роста более чем на 50%. Ортотопически трансплантированная карцинома яичника человека НОС 8, производящая опухолевые узелки в перитонеальной полости с асцитом, которая является резистентной к ЕТ-743 и частично чувствительной к DDP, в комбинации давала резкое повышение выживаемости даже в дозе ЕТ-743 0,05 мг/кг (1/4 MTD) и не проявляла какой бы то ни было значимой токсичности. Доза ЕТ-743 0,15 мг/кг выраженно повышала выживаемость, но наблюдалось также повышение токсичности, на что указывало уменьшение массы тела, которое было достоверно более выражено, чем то, которое наблюдалось после лечения каждым из данных лекарственных средств. Данные открытия предлагают серьезное обоснование для планирования клинических испытаний с использованием комбинации ЕТ-743 и DDP при саркомах и раках яичников. В настоящее время проводятся in vitro и in vivo исследования для выяснения механизмов, лежащих в основе синергизма между ЕТ-743 и DDP при злокачественных опухолях указанных типов. Пример 9. Дексаметазон (dex) в высоких дозах защищает от гепатотоксичности эктеинасцидина 743 (ЕТ 743) у крыс. ЕТ-743, агент, полученный из морских оболочников, в настоящее время проходит II фазу клинических испытаний. Он продемонстрировал клиническую активность против сарком, и предварительные данные предполагают его активность против карциномы молочной железы и яичника. Однако гепатотоксичность, которая характеризуется обратимым трансаминитом, наблюдается у большинства пациентов,подвергшихся лечению, и холестаз - у малой части пациентов. У наиболее чувствительного вида животных, крысы, токсичность ЕТ-743 проявляется некрозом печени и воспалением желчного протока. В свете противовоспалительной активности dex заявители изучили его влияние на повреждение печени у крыс,- 11005564 индуцированное ЕТ-743. Самки крысы Wistar получали однократную в/в дозу ЕТ-743 (40 мкг/кг). Некоторые крысы получали предварительное лечение в виде однократной пероральной дозы dex 1, 5, 10 или 20 мг/кг за 24 ч до введения ЕТ-743. Патологию печени и концентрации в плазме щелочной фосфатазы(ALP), аспартат-аминотрансферазы (GOT) и общего билирубина (ТВ) оценивали в течение периодов времени до 3 дней после введения ЕТ-743. Обычные гистологические срезы печени исследовали с помощью светового микроскопа. Через 2 дня после лечения ЕТ-743 в печени у крыс, которые получали только ЕТ-743, имелись воспаление желчного протока, резкие дегенеративные изменения в билиарных эпителиальных клетках и зоны некроза печени. Уровни в плазме крови ALP и GOT были значительно повышены через 2 дня. Холестаз выражался в резком повышении концентрации ТВ в плазме, которое начиналось на 2 день после введения ЕТ-743. Индуцированные ЕТ-743 гистологические изменения и повышение в плазме ALP, GOT и ТВ полностью отсутствовали у крыс, которые предварительно получали 10 или 20 мг/кг dex. В то время как dex в дозе 1 мг/кг оказывал слабое защитное действие, 5 мг/кг оказывали умеренное защитное действие. Уровни в плазме ЕТ-743 у крыс, которые получали dex (50 мг/кг) ежедневно, в течение 3 дней до введения ЕТ-743, не уменьшались по сравнению с теми крысами, которые получали только ЕТ-743. Кроме того, активность ЕТ-743 против меланомы В 16, имплантированной мышам, дексаметазоном не нарушалась. Данные открытия предполагают, что добавление дексаметазона в высоких дозах к схеме лечения ЕТ-743 может улучшить его гепатотоксичность у пациентов со злокачественными опухолями. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Применение ЕТ-743 для изготовления лекарственного препарата для эффективного лечения опухоли посредством комбинированной терапии, включающей применение ЕТ-743 в синергической комбинации с другим противоопухолевым лекарственным средством. 2. Применение противоопухолевого лекарственного средства для изготовления лекарственного препарата для эффективного лечения опухоли посредством комбинированной терапии, включающей применение противоопухолевого лекарственного средства в синергической комбинации с ЕТ-743. 3. Применение по п.1 или 2, при котором ЕТ-743 образует часть этого лекарственного препарата. 4. Применение по п.1 или 2, при котором ЕТ-743 представлен в форме отдельного лекарственного препарата. 5. Применение по п.4, при котором отдельный лекарственный препарат, содержащий ЕТ-743, вводится в одно и то же время, что и лекарственный препарат, содержащий противоопухолевое лекарственное средство. 6. Применение по п.4, при котором отдельный лекарственный препарат, содержащий ЕТ-743, вводится в другое время, чем лекарственный препарат, содержащий противоопухолевое лекарственное средство. 7. Применение по любому из предшествующих пунктов, при котором комбинированная терапия включает ЕТ-743 и антрациклин. 8. Применение по п.7, при котором комбинированная терапия включает ЕТ-743 и доксорубицин. 9. Применение по любому из пп.1-6, при котором комбинированная терапия включает ЕТ-743 и противоопухолевое соединение на основе платины. 10. Применение по п.9, при котором противоопухолевое соединение на основе платины представляет собой цисплатин или карбоплатин. 11. Применение по любому из пп.1-6, при котором комбинированная терапия включает ЕТ-743 и противоопухолевое таксановое лекарственное средство. 12. Применение по п.11, при котором противоопухолевое таксановое лекарственное средство представляет собой паклитаксел или доцетаксел. 13. Применение по любому из пп.1-6, при котором комбинированная терапия включает ЕТ-743 и антиметаболитное противоопухолевое лекарственное средство. 14. Применение по п.6, при котором антиметаболитное противоопухолевое лекарственное средство представляет собой гемцитрабин или 5-фторурацил. 15. Применение по любому из пп.1-6, при котором комбинированная терапия включает ЕТ-743 и противоопухолевое лекарственное средство, направленное против топоизомеразы. 16. Применение по п.14, при котором противоопухолевое лекарственное средство, направленное против топоизомеразы, представляет собой SN-38. 17. Применение по любому из предшествующих пунктов, при котором комбинированная терапия дополнительно включает дексаметазон. Евразийская патентная организация, ЕАПВ Россия, 109012, Москва, Малый Черкасский пер., 2/6
МПК / Метки
МПК: A61K 45/06, A61P 35/00
Метки: эффективные, лекарственные, средства, противоопухолевые
Код ссылки
<a href="https://eas.patents.su/13-5564-effektivnye-protivoopuholevye-lekarstvennye-sredstva.html" rel="bookmark" title="База патентов Евразийского Союза">Эффективные противоопухолевые лекарственные средства</a>
Предыдущий патент: Противовоспалительные и иммуносупрессорные соединения, ингибирующие клеточную адгезию
Следующий патент: Композиция для профилактики или лечения слабоумия, включающая производное гидроксикоричной кислоты или экстракт растения рода angelicae, содержащий его
Случайный патент: Капсулы для ингаляции