Производные оксаиндена, способ их получения (варианты), фармацевтический состав на их основе, их применение и способ лечения с их использованием
Номер патента: 25
Опубликовано: 26.02.1998
Авторы: Семереди Каталин, Чёргё Маргит, Эдьед Андраш, Сантаи Чаба, Ковач Габор, Гадо Клара, Такач Габорне, Гиглер Габор, Новак Лайош, Ковач Петер, Пирок Дьордь, Шимиг Дьюла, Божинг Даниэль, Блашко Габор, Драбант Шандор
Формула / Реферат
1. Производные оксаиндена общей формулы (I),
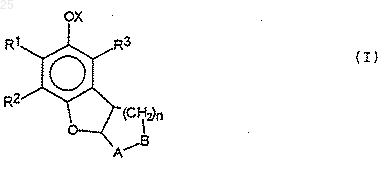
где R1 представляет собой низший С1-4 алкил, низшую С1-4 алкоксигруппу или низший С3-6 циклоалкил,
R2 представляет собой водород, низший С1-4 алкил или низший С3-6 циклоалкил, R3 представляет собой водород, низший С1-4 алкил, низшую С1-4 алкоксигруппу или бензилоксигруппу, Х представляет собой водород, алифатический С1-4 ацил или бензоиловую или нафтоиловую группу, возможно замещенные одной или более нитро или С1-4 алкоксигруппой(-ами) или группой формулы R5 R6=N-R7 где R5, R6 и R7 каждый представляет собой С1-4 низший алкилен или R5 и R6 вместе с атомом азота, к которому они присоединены, образуют пиперидил или морфолиновую группу, А и В вместе образуют этиленовую или виниленовую группу и n равно 1, 2 или 3, их стереоизомеры и фармацевтически приемлемые соли, полученные присоединением кислот.
2. Соединения по п.1, где R1 представляет собой низший алкил, R2 и R3 независимо представляют собой водород, низший алкил, Х представляет собой водород, А и В вместе образуют виниленовую группу, а n равно 1 или 2.
3. Соединения по п. 1, где R1 представляет собой низший алкил, R2 и R3 представляют собой независимо водород, низший алкил, Х представляет собой водород, А и В вместе образуют этилен, а n равно 1 или 3.
4. Соединения общей формулы (I): цис-4,6,7-триметил-2,3,3а,8а-тетрагидро-1Н-8-оксациклопента[а]инден-5-ол, 1,2,4-триметил-4b,6,7,8,9,9а-гексагидро-5Н-10-оксабензо[а]азулен-3-ол и цис-4,6,7,-триметил-3а, 8а-дигидро-3Н-8-оксациклопента[а]инден-5-ол.
5. Способ получения соединений общей формулы (I), где Х представляет собой водород, а А и В образуют виниленовую группу, характеризующийся тем, что включает взаимодействие гидрохинона формулы (II)
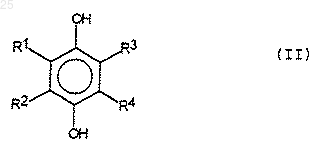
где R1, R2 и R3 как указано в п.1 и R4 представляет собой водород или низший алкокси, с производными циклоалкена формулы (III),

где n как указано в п. 1, в присутствии растворителя и каталитического количества сильной кислоты.
6. Способ по п.5, отличающийся тем, что дополнительно осуществляют каталитическую гидрогенизацию конечного продукта с получением соединений общей формулы (I), где А и В образуют этиленовую группу.
7. Способ получения соединений общей формулы (I) (вариант), где Х представляет собой водород, а А и В образуют этиленовую группу, отличающийся тем, что включает взаимодействие гидрохинона формулы (II), где R1, R2 и R3 как указано в п.1 и R4 - водород, с производными циклоалкадиена формулы (IV), в присутствии каталитического количества сильной кислоты.

8. Способ по пп.5 и 7, отличающийся тем, что конечный продукт ацилируют или диалкиламиноалкилируют.
9. Способ по п.5, отличающийся тем, что взаимодействие проводят в апротонном растворителе, предпочтительно ароматическом углеводороде.
10. Способ по пп. 5 или 9, отличающийся тем, что в качестве сильной кислоты используют п-толуолсульфокислоту, камфор-10-сульфокислоту или бензолсульфокислоту.
11. Способ по пп.5, 9 или 10, отличающийся тем, что взаимодействие проводят при повышенной температуре, предпочтительно от 60 до 110°С.
12. Способ по п.6, отличающийся тем, что каталитическую гидрогенизацию проводят в полярном растворителе.
13. Способ по пп.6 или 12, отличающийся тем, что в качестве катализатора гидрогенизации используют палладий.
14. Способ по п.6 или по пп. 12 или 13, отличающийся тем, что взаимодействие проводят при комнатной температуре.
15. Способ по п. 7, отличающийся тем, что в качестве сильной кислоты используют п-толуолсульфокислоту, камфор-10-сульфокислоту или бензолсульфокислоту.
16. Способ по п.7 или п.15, отличающийся тем, что взаимодействие проводят в безводном апротонном растворителе.
17. Способ по п.7 или по пп. 15 -16, отличающийся тем, что взаимодействие проводят при повышенной температуре, предпочтительно в интервале от 30 до 90°С.
18. Фармацевтический состав, содержащий в качестве активного компонента соединение общей формулы (I) или его фармацевтически приемлемую соль, полученную присоединением кислоты, в смеси с подходящим инертным твердым или жидким фармацевтическим носителем.
19. Применение соединений общей формулы (I) или их фармацевтически приемлемых солей, полученных присоединением кислоты, для получения фармацевтического состава, пригодного, в частности, для лечения аллергических заболеваний, заболеваний суставов, астмы, заболеваний гастротракта и кожи.
20. Способ лечения аллергических, суставных, язвенных, и астматических заболеваний, включающий назначение пациенту эффективного количества соединения общей формулы (I) или его фармацевтически приемлемой соли, полученной присоединением кислоты.
Текст
Настоящее изобретение относится к новым производным оксаиндена, способу Их получения, фармацевтическим составам, включающим эти новые производные, применению указанных производных оксаиндена для лечения заболеваний И приготовления фармацевтических составов, пригодных при лечении заболеваний.(10) 2760-6]. В литературе отсутствуют указания на какую-либо активность этих соединений.В заявке на Европейский Патент Ля 84856 описаны соединения, аналогичные соединениям, предложенным в изобретении. В заявке отмечено ингибирующее действие в отношении язвы, а также гипотензивная активность.В соответствии с настоящим изобретением, предложены соединения общей формулы (1), ОХ я 2 (Счдп А/Вгде К представляет собой низший СИ алкил, низшуюСИ алкоксигруппу или низший СИ Циклоалкил, К 2 представляет собой водород, низший СИ алкил Или низший С Циклоалкил, КЗ представляет собой водород, низший СИ алкил, низшую СИ алкоксигруппу или бензилоксигруп ПУ, Х Представляет собой водород, алифатический СИ аЦИл или бензоиловую или нафтоиловую группу,возможно замещенные одной или более нитро или СИ алкоксигрупПои(-ами) Или группои формулы К 5 К=11-К 7, где 115, 116 и К 7 каждый представляет собой СИ низший алкилен Или К 5 И КБ вместе с атомом азота,к которому они присоединены, образуют пиперидилИЛИ МОрфОЛИНОВуЮ ГруППу, А и В вместе образуют этиленовую Или виниленовую группу И п равно 1, 2 Или 3, Их стереоизомеры и фармацевтически приемлемые соли, полученные присоединением кислот.Новые соединения общей формулы (1) проявляют сильное ингибирующее действие по отношению к энзиму 5-липоксИгеназЬ 1 (5-ЬО).В соответствии с изобретением в предпочтительной группе соединений общей формулы (1) К представляет низший алкил, 112 И 113 представляют собой независимо водород, низший алкил. Х представляет собой водород, А и В вместе представляют виниленовую группу, а п равно 1 Или 2.В другой предпочтительной группе соединений общей формулы (1) в соответствии с изобретением К Представляет собой низший алкил, К 2 и К 3 представляют собой независимо водород, низший алкил, Х - водород, А и В вместе образуют этиленовую группу, а п равно 1 Или 3.Особенно предпочтительными примерами соединений в соответствии с изобретением являются следующие: ЦИс-4,6,7-триметИл-2,3 ,За,8 а-тегра 1 идро-1 Н-8 оксаЦИклоПента[а]инден-5-ол, 1,2,4-триметил 4 Ь,6,7,8,9,9 а-гексагИдро-5 Н- 1 0- оксабензо[а]азулен-3 ол И ЦИс-4,6,7,-триметил-3 а,8 а-дигидро-3 Н-8-оксациклопента [а] Инден-5-ол.УПотребляемь 1 й везде в опИсанИИ И формуле изобретения термин низшие относится к группам или соединениям с числом атомов углерода от 1 до 4 или, в случае Циклоалкильных групп, с числом атомов углерода от 3 до 6. Термин низший алкил относится к линейным или разветвленным группам, например,таким, как метил, этил, н-пропил, Изо-пропил, н-бутил и т.п., из которых предпочтительной группой является метил. Термин низший ЦИклоалкИл относится к Циклическим группам с числом атомов углерода от 3 до 6(например, Циклопропил, Циклобутил, Циклопентил И Циклогексил). Подходящими низшими алкоксигруппами являются метокси, этокси, пропокси, изопропокси И т.п., Из которых предпочтительной группой является метоксигруппа. Термин аЦИл относится к алифатическим СИ аЦил илИ бензоил или нафтоил группам, возможно замещенным одной или более нитро Или СИ алкоксигруппами.В соответствии с еще одним аспектом Изобретения предложен способ получения соединений общей формулы (1), включающий:а) для получения соединения общей формулы(1), где А И В вместе образуют вИнИленовую группу,К, 112 ,К 3, Х И п - как указано выше, осуществляют взаимодействие производного гИдрохИнона общей формулы (11), 3 000025 4где К, 112 и 113 такие же, как указано выше, И 114 представляет собой водород или низший алкокси, с производным Циклоалкена обЩей формулы (111)где п как указано выше, в растворителе, в присутствии каталитического количества сильной кислоты, и, при необходимости, ацилирование или алкилирование полученного таким образом соединения обЩей формулы (1), где Х представляет собой водород,илиб) для получения соединений обЩей формулы(1), где А и В вместе образуют этиленовую группу,осуществляютб 1) каталитическую гидрогенизацию соединения обЩей формулы (1), где А и В вместе образуют виниленовую группу, Х - водород а К 32,113 и п как указано выше, или62) взаимодействие производного гидрохинона обшей формулы (11), где КЦККЗ - как указано выше, а 114 - водород, с производным Цикло-алкадиена обшей формулы (1/), Сндпгде п - как указано выше, в растворителе, в присутствии каталитического количества сильной кислоты, и, при необходимости, ацилирование или диалкиламиноалкилирование полученного соединения обЩей формулы (1), где Х представляет собой водород, а также, при возможности и желании, превращение полученного таким образом основания обЩей формулы (1) в соль, полученную присоединением кислоты.В соответствии с вариантом (а) способа, предложенного в изобретении, реакцию производного гидрохинона обЩеЙ формулы (11) с производным Циклоалкена обшей формулы (111) проводят в растворителе, в присутствии каталитического количества сильной кислоты. В качестве растворителя используют безводные апротоннь 1 е растворители, предпочтительно ароматические углеводороды, такие как бензол, толулол и ксилол, или галогенированные углеводороды (например, метиленхлорид, хлороформ, 1,2-дихлорэтан и др.). Реакцию проводят в присутствии каталитического количества сильной кислоты (например, п-толуолсульфокислоты, камфорсульфокислоты или бензолсульфокислоты, предпочтительно, камфорсульфокислоты).Взаимодействие проводят при повышенной температуре, предпочтительно от 60 до 1 10 С. Полученное таким образом соединение обЩей формулы (1) может быть выделено, например, путем охлаждения реакционной смеси до комнатной температуры, встряхивания смеси с некоторым количеством воды, разделения фаз, экстракции водной фазы подходящим органическим растворителем (например, дихлорметаном),промывки и сушки комбинированных органических фаз и выпаривания растворителя. Полученное таким образом соединение обЩей формулы (1) может быть,при необходимости, очищено путем перекристаллизации или колонной хроматографией.В соответствии с вариантом (б) способа, предложенного в изобретении, получают соединение обшей формулы (1), в котором А и Б вместе образуют этиленовую группу. В соответствии с вариантом (б 1) способа, соединение обЩей формулы (1), в котором А и Б вместе образуют виниленовую группу, Х представляет собой водород, а К, К 2, КЗ и п - как указано выше,подвергают каталитической гидрогенизации. В качестве катализатора предпочтительно используют палладий (например, палладий, нанесенный на уголь). Каталитическую гидрогенизацию можно проводить в полярном растворителе (предпочтительно в низшем спирте, например, метаноле) при температуре от О до 30 С, при атмосферном или несколько повышенном давлении. Взаимодействие проводят предпочтительно при комнатной температуре и атмосферном давлении. Полученное таким образом соединение общей формулы (1), где Х - водород, выделяют из реакционной смеси путем отделения на фильтре катализатора,выпаривания фильтрата и, при необходимости, очишают путем перекристаллизации или колонной хроматографии.В соответствии с вариантом (62) способа, предложенного в изобретении, проводят взаимодействие производного гидрохинона обшей формулы (11) с Циклоалкадиеном обЩей формулы (1/). Реакцию проводят в присутствии каталитического количества сильной кислоты. В качестве кислоты используют, например, п-толуолсульфокислоту, камфорсульфокислоту или бензолсульфокислоту. Реакцию проводят в растворителе, предпочтительно безводном апротонном растворителе. В качестве реакционной среды предпочтительно используют бензол, толуол, ксилол или их смеси. Взаимодействие проводят предпочтительно при повышенной температуре, преимущественно при температуре от 30 до 90 С. Полученное таким образом соединение обЩей формулы (1), содержащее водород на месте Х, выделяют от реакционной смеси,например, путем охлаждения последней до комнатной температуры, промывки, сушки и выпаривания. Остаток при необходимости очищают путем перекристаллизации или колонной хроматографии.Соединение обЩей формулы (1), содержащее в качестве Х атом водорода и полученное по любой из указанных выше реакций, можно ацилировать илиалкилировать. Ацилирование может быть проведено с использованием органичеких карбоновых кислот,содержащих ацильную группу, которую требуется ввести, или их функциональных производных (например,галогенидов кислот, ангидридов кислот и т.п.). В качестве галогенидов кислот предпочтительно используют хлориды кислот.Если в качестве ацилирующего агента используют карбоновую кислоту, реакцию предпочтительно проводят в апротонном биполярном растворителе (таком, как диметилформамид), в присутствии конденсирующего агента. В качестве конденсирующего агента можно использовать, например, соединения карбодиимидного типа (предпочтительно дициклогексилкарбодиимид).Ацилирование с использованием ангидридов кислот можно проводить в неполярнь 1 х апротонных растворителях ( например, эфире, диоксане, бензоле,хлороформе, дихлорметане и т.п.). Реакцию проводят в присутствии агента, связывающего кислоту (например, карбонатов щелочных металлов, гидрида натрия или органических оснований). Некоторые органические основания ( например, пиридин) могут служить одновременно растворителями и агентами, связь 1 вающими кислоту.Ацилирование галогенидами кислот, предпочтительно хлоридами кислот, можно проводить в инертном органическом растворителе. В качестве реакционной среды можно использовать алифатические эфирь 1 (например, диэтиловый эфир, тетрагидрофуран и т.п.) или алифатические углеводороды, возможно галогенированнь 1 е (например, дихлорметан), однако роль реакционной среды может выполнять также агент,связывающий кислоту (например, пиридин).Температуру реакции можно варьировать в Широких пределах, однако предпочтительно проводить реакцию при комнатной температуре. Предпочтительно также проводить реакцию в присутствии агента,связывающего кислоту. Для этой цели можно использовать органические четвертичные основания (например триэтиламин, пиридин, М-метилморфолин и др.). В некоторых случаях органические основания могут служить растворителями и агентами, связывающими кислоту.Алкилирование соединений общей формулы (1),содержащих в качестве Х атом водорода, можно проводить с использованием 115 Кб-М-алкилгалогенидов,где 115 и Кб- как указано выще. Алкилирование предпочтительно проводят в присутствии оснований (например, гидроксидов щелочных металлов, карбонатов щелочных металлов, алкоксидов щелочных металлов, гидрида натрия или органических оснований).Соединения общей формулы (1), где Х обозначает группу формулы ЮКМ-КС могут образовывать соли кислотного присоединения с фармацевтически приемлемыми кислотами. Для этой цели могут бытьиспользованы неорганические кислоты (например,галогенводороды, такие как гидрохлористая или гидробромистая кислоты, серная, фосфорная или пергалоиднь 1 е кислоты, такие как перхлорная кислота), органические карбоновые кислоты (например, фумаровая, уксусная, пропионовая, гликолевая, малеиновая,гидроксималеиновая, аскорбиновая, лимонная, яблочная, салициловая, молочная, Коричная, бензойная,фенилуксусная, пара-аминобензойная, пара-гидроксибензойная, пара-аминосалициловая кислота и др.),алкилсульфоновые кислоты (например, метансульфокислота, этансульфокислота) или арил-сульфоновые кислоты (например, пара-толуолсульфоновая, парабромфенилсульфоновая, нафтилсульфоновая, сульфанильная кислоты).Исходные соединения общих формул (11), (111) и(1/), используемые для получения соединений общей формулы (1), известны. Эти соединения доступны на рынке или могут быть получены в соответствии с описаниями, приведенными в литературе [7/.Ва 1 е 1: .1 о 11 ша 1 оГ С 11 еш 1 са 1 5 ос 1 ету 1941., 662; Ь.11.Оше 11 е: а 1.: там же,1952 , 4035; Е. Кпоеуена 3 е 1 е: а 1.:Вег 1 с 111 е,34, 3993 (1901);Новые соединения общей формулы (1) являются сильными ингибиторами энзима 5-липоксигеназы (5150). Эти соединения на один -два порядка более эффективны, чем АА-86 1 , хорощо известный селективный ингибитор энзима 5-липоксигеназы (5-ЬО). Ингибиторы 5-липоксигеназы (5-ЬО), проявляющие активность как 111 у 1 гго, так и 111 у 1 уо, могут быть использованы для лечения аллергических заболеваний (например,аллергических ринитов), заболеваний суставов (например, ревматоидного артрита), заболеваний желудочно-кишечного тракта (например, язвенного колита),астмы и некоторых кожных заболеваний (например,псориаза).Эффективность новых соединений продемонстрирована следующими экспериментами.1. Измерение активности энзима 5-ЬО, приготовленного из лейкоцитов человека в бесклеточной системе.Активность энзима измеряли в соответствии с модифицированным методом К.Ос 111 и др., описанным в литературе [К.Ос 111,.Т.Уо 111111 ого, .Уашашого,К.Та 111;ис 111, Т.М 1 уашо[о: А 1 ас 1111 о 11 ате 5-11 роху 3 е 11 ае оГ 3 и 111 еа р 13 рег 1 го 11 еа 1 ро 1 у 111 огр 11 о 11 ис 1 еа 1 1 е 111 осуге,.1.В 1 о 1.С 11 еш. 258 , 5754-5758, (1983)]. В основу метода положен следующий принцип: в системе 111 111110, в результате реакции, катализируемой 5-ЬО, из арахидоновой кислоты образуется 5-гидроперокси-6,8,1 1,14 эйкозатетраеновая кислота (5-ГПЭТЕ), которая затем превращается в 5-гидрокси-6, 8, 11, 14-эйкозатетраеновую кислоту (5-ГЭТЕ). Обе кислоты, 5-ГПЭТЕ и 5 Г ЭТЕ), имеют максимум поглощения при 236 нм, поэтому активность 5-1 О энзима можно определить по изменению поглощения при 236 нм. Энзим 5-ЬО былполучен из полиморфонуклеарнь 1 х лейкоцитов человека путем обычной процедуры очистки. Клетки были очищены И лизованы в ультразвуковом дезинтеграторе. Лизат был отделен в центрифуге и энзим в цитозоле частично очищен фракционированием сульфатом аммония (осаждение энзима происходило при 50%ном насыщении). Реакционную смесь (5 0 мМ трис-НС 1, рН = 7,5; 2 мМ СаС 12, 0,1 ММ АТФ, 0,02 мМ арахидоновой кислоты) инкубировали при 37 С в течение 5 мин. Реакция начиналась при добавлении арахидоновой кислоты и заканчивалась при добавлении 10 мМ лимонной кислоты. Полученные таким образом 5-ГПЭТЕ и 5-ГЭТЕ экстрагировали смесью диэтилового эфира и гексана, взятых в соотношении 6:4, и измеряли поглощение органической фазой при 236 нм с помощью спектрофотометрии.2. Определение активности энзима 5-ЬО лейкоцитов человека путем измерения их продуктивности при синтезе и выделении лейкотриенов В 4Определение проводили в соответствии с методикой Н.М 1 та и др.[Н.Мпа, УХЩ ап ТБЬШа: Ейесг оГ АА-86 1 , а 5-11 роху 3 епае 1 п 111 Ь 1 гот оп 1 еи 1 отг 1 епе уш 11 е 1 ш 11 пп 1 ап ро 1 уп 1 огр 11 оппс 1 еат 1 еи 1 осуте апа оп сус 1 ооху 11 епае ап 12-1 йрохугепазе аспуйпез ш 1111 шап р 1 аге 1 етз. А 11 ег 3 у 41, 493-498, (1986)]. В основу метода положен следующий принцип: ионо-фор кальция А-23187 индуцирует реакцию синтеза и вь 1 деления ЬТВ, полиморфоядерными лейкоцитами человека. Количество выделенного в инкубационную среду ЬТВд характеризует активность энзима 5-ЬО неповрежденных клеток. В качестве инкубационной среды использовали сбалансированную среду Нап 1 а(1-1 ВВ),в которую добавили 17 мМ Трис-НС 1 (рН 7,2), 1,22 мМ СаС 12, 1 ММ М 3 С 12, 0,001 мМ А-23 1 87 и 104 РМ 11 лейкоцитов на 1 мл реакционной смеси. Реакцию начинали при добавлении ионофора, а затем инкубировали при 37 С в течение 15 мин. Реакцию прекращали путем добавления 5 ММ ЕВТА и охлаждения образцов на ледяной бане. Образцы затем центрифугировали и определяли количество ЬТВд в центрифугате радиоиммунологическим методом (ША).Воспаление уха у мышей было индуцировано арахидоновой кислотой по модифицированной методике, описанной Уопщуом И др.[Уопп].М.,5 р 1 ге,13.А.,Вес 1 ог 1,СП.,7/а,;пег,В.,Ва 11 агоп,51.,Ве Уоипд, Ь.М.: Т 11 е шоизе еаг шйашшатогу гезропзе гогор 1 са 1 агас 1 поп 1 с асШ, .1.1 пует.1 Эегшато 1., 82 ., 367371(1984)]. Эксперименты проводили на женских особях мышей рода ММШ весом от 25 до 30 мг (8 особей/ группу). Препарат наносили местно в ацетоне или этаноле автоматической пипеткой по 10 мкл на внутреннюю и внешнюю поверхности уха. Через 30 мин после применения препарата или носителя на обе стороны левого уха кистью наносили 3 мг арахидоновой кислоты в 20 мкл ацетона, а обе стороны правого уха обрабатывали только 20 мкл ацетона. Через 60 мин живот ных убивали эфиром, а затем из обоих ушей вырезали по диску диаметром 7 мм. Массу каждого диска определяли на аналитических весах и рассчитывали разность массы левого и правого уха в каждой группе. Величину 11350 определяли путем построения графика зависимости логарифма дозы от отклика в процентах в сравнении с животными, обработанными только носителем.4. Тест на анафилактический шок у мышей, индуцированный РАР.Использовали модифицированную методику Уоип: и др. [Уоип 3,.1.М., Ма 1 опеу,Р] .,.111 ЬЬ,.11.,С 1 ат 1,.1 ..,: РЬаппасо 1 о 31 са 1 шуезгйгатйоп оГ 1116 шеспапйзшз о 1 р 1 ате 1 ет асцуапп: Гасгог паисед шопаЩу 111 т 11 е шоизе, Ргоа 31 ап 11 п, 30., 545-551(1985)]. Эксперименты проводили на мужских особях мышей рода ЫМШ весом от 20 до 25 мг (10 особей/группу). Испытываемые соединения суспендировали в 0,4% метилцеллюлозе и наносили внутрибрюшинно в количестве 10 мл/кг. Мыши в контрольной группе получали только носитель. Через 30 мин после этого животные получали РАР внутривенно дозой 100 мкг/кг(5 мл/кг). Смертность определяли через 1 ч после применения РАР. Каждый опыт повторяли три раза (п = 30). Было проведено сравнение смертности обработанных животных и контрольной группы. Величины 11350 рассчитывали методом линейного регрессионного анализа.Результаты представлены в таблице. В качестве сравнительных веществ использовали фенидон (1-фенил-З-пира-золидинон), АА-861 (2-12-гидрокси-5,10 додекадиинил)-3,5,6-триметил-п-бензохинон) И НОСАКак видно из приведенной таблицы, в этих испь 1 таниях действие некоторых соединений в соответствии с изобретением превосходит действие селективного ингибитора энзима 5-липоксигеназы АА-86 1 , в то время как их активность сравнима с активностью двойных ингибиторов фенидона и НОСА.В соответствии с еще одним аспектом изобретения, предложены фармацевтические составы, содержаЩие в качестве активного компонента соединение общей формулы (1) или его фармацевтически приемлемую соль, полученную присоединением кислоты,в смеси с подходящим инертным твердым или жидким фармацевтическим носителем.Фармацевтические КОМПОЗИЦИИ В СООТВСТСТВИИ С НЗСТОЯЩИМ ИЗОбрСТСНИСМ МОГУТ бЫТЬ ПОЛУЧСНЫ ИЗВССТНЫМИ МСТОДаМИ ПУТМ СМСШСНИЯ ЗКТИВНОГО ИНГредиента С ПОДХОДЯЩИМ инертным НСТОКСИЧНЫМ тверДЬ 1 М ИЛИ ЖИДКИМ НОСИТСЛСМ И перевода СМССИ В гале новую форму.Предпочтительной конечной формой соединений общей формулы (1) являются таблетки или драже,однако эти соединения могут быть применены в виде
МПК / Метки
МПК: C07D 307/77, A61K 31/34
Метки: основе, получения, производные, оксаиндена, лечения, состав, использованием, применение, способ, фармацевтический, варианты
Код ссылки
<a href="https://eas.patents.su/13-25-proizvodnye-oksaindena-sposob-ih-polucheniya-varianty-farmacevticheskijj-sostav-na-ih-osnove-ih-primenenie-i-sposob-lecheniya-s-ih-ispolzovaniem.html" rel="bookmark" title="База патентов Евразийского Союза">Производные оксаиндена, способ их получения (варианты), фармацевтический состав на их основе, их применение и способ лечения с их использованием</a>
Предыдущий патент: Фармацевтическая композиция, содержащая в качестве активного начала уратоксидазу, и лиофилизат для ее получения
Следующий патент: Способ полимеризации олефинов в газовой фазе.
Случайный патент: Вагонная железнодорожная тележка и ее элементы