Композиция молекулярного сита ssz-61 и его синтез
Формула / Реферат
1. Молекулярное сито, имеющее мольное отношение оксида первого четырехвалентного элемента к оксиду второго четырехвалентного элемента, отличного от указанного первого четырехвалентного элемента, трехвалентного элемента, пятивалентного элемента или их смеси, более 15 и имеющее после прокаливания рентгеновские дифракционные линии из табл. I.
2. Молекулярное сито, имеющее мольное отношение оксида, выбранного из группы, состоящей из диоксида кремния, оксида германия и их смесей, к оксиду, выбранному из оксида алюминия, оксида галлия, оксида железа, оксида бора, оксида титана, оксида индия, оксида ванадия и их смесей, примерно 15 и имеющее после прокаливания рентгеновские дифракционные линии из табл. I.
3. Молекулярное сито по п.2, где оксиды включают диоксид кремния и оксид алюминия.
4. Молекулярное сито по п.2, где оксиды включают диоксид кремния и оксид бора.
5. Молекулярное сито по п.1, где указанное молекулярное сито преимущественно находится в водородной форме.
6. Молекулярное сито по п.1, где указанное молекулярное сито, по существу, не имеет кислотности.
7. Молекулярное сито, имеющее следующий состав, в свежеприготовленном и в безводном состоянии, в терминах мольных отношений:
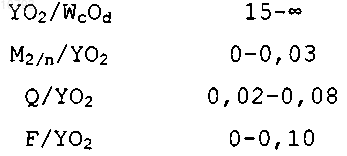
где Y представляет собой кремний, германий или их смесь; W представляет собой алюминий, галлий, железо, бор, титан, индий, ванадий или их смесь; с равно 1 или 2; d равно 2, когда с равно 1, или d равно 3 или 5, когда с равно 2; М представляет собой катион щелочного металла, катион щелочно-земельного металла или их смеси; n представляет собой валентность М и Q представляет собой катион, выбранный из группы, состоящей из нижеследующего:
8. Молекулярное сито по п.7, где W представляет собой алюминий и Y представляет собой кремний.
9. Молекулярное сито по п.7, где W представляет собой бор и Y представляет собой кремний.
10. Молекулярное сито по п.7, где Q представляет собой
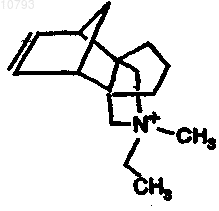
11. Молекулярное сито по п.7, где Q представляет собой
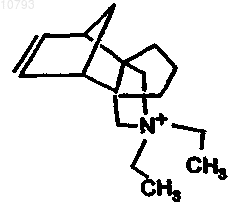
12. Молекулярное сито по п.7, где Q представляет собой
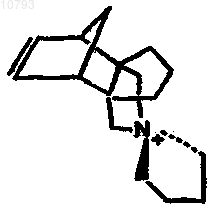
13. Молекулярное сито по п.7, где Q представляет собой
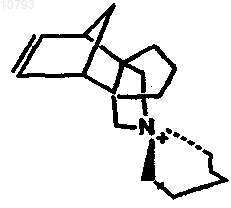
14. Молекулярное сито по п.7, где Q представляет собой
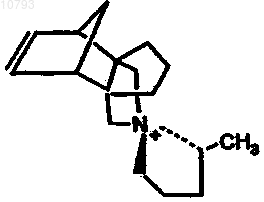
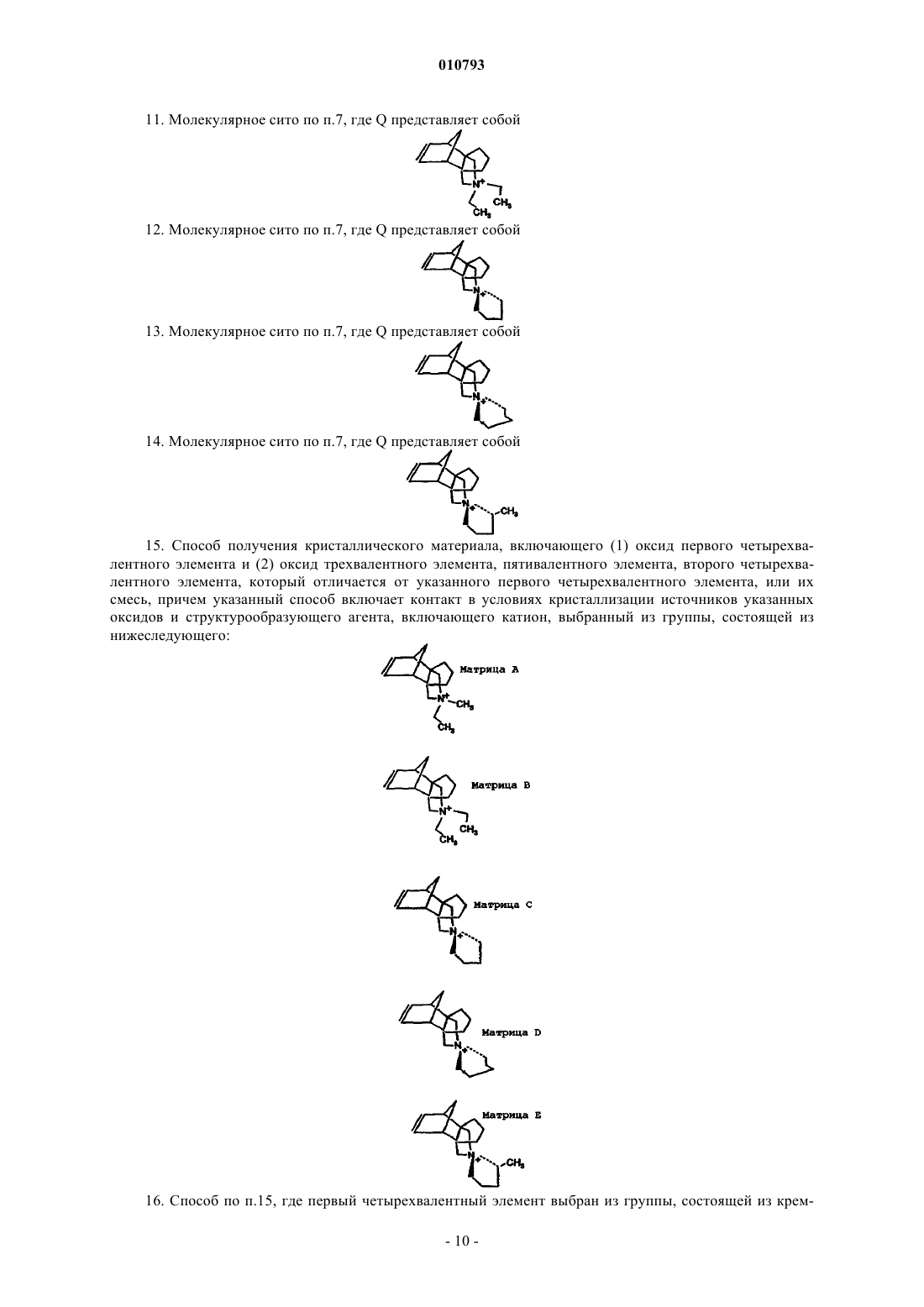
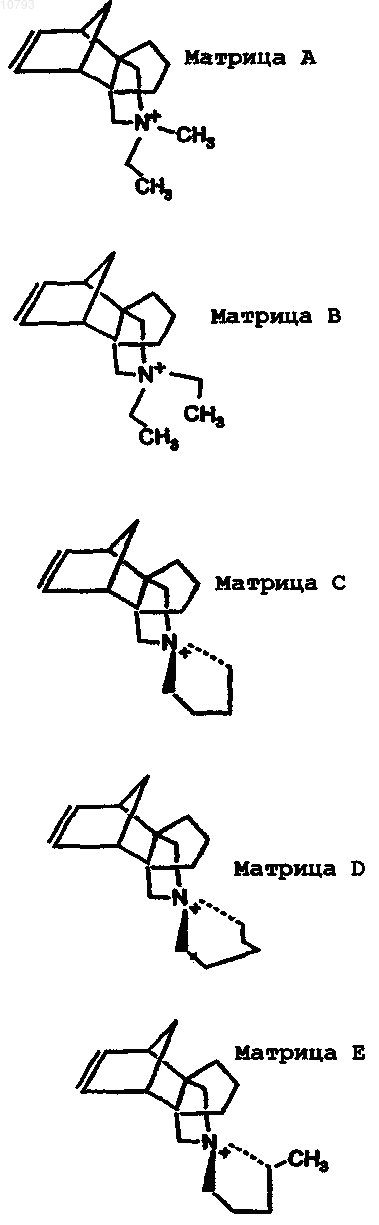
15. Способ получения кристаллического материала, включающего (1) оксид первого четырехвалентного элемента и (2) оксид трехвалентного элемента, пятивалентного элемента, второго четырехвалентного элемента, который отличается от указанного первого четырехвалентного элемента, или их смесь, причем указанный способ включает контакт в условиях кристаллизации источников указанных оксидов и структурообразующего агента, включающего катион, выбранный из группы, состоящей из нижеследующего:

16. Способ по п.15, где первый четырехвалентный элемент выбран из группы, состоящей из кремния, германия и их комбинаций.
17. Способ по п.15, где второй трехвалентный элемент, пятивалентный элемент или четырехвалентный элемент выбраны из группы, состоящей из алюминия, галлия, железа, бора, титана, индия, ванадия и их комбинаций.
18. Способ по п.17, где второй трехвалентный элемент или четырехвалентный элемент выбран из группы, состоящей из алюминия, бора, титана и их комбинаций.
19. Способ по п.16, где первый четырехвалентный элемент представляет собой кремний.
20. Способ по п.15, где структурообразующий агент представляет собой
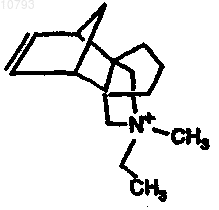
21. Способ по п.15, где структурообразующий агент представляет собой

22. Способ по п.15, где структурообразующий агент представляет собой
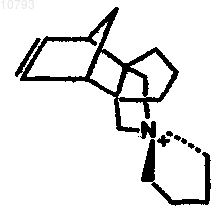
23. Способ по п.15, где структурообразующий агент представляет собой
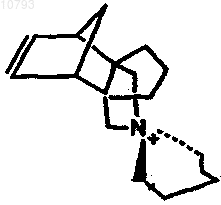
24. Способ по п.15, где структурообразующий агент представляет собой
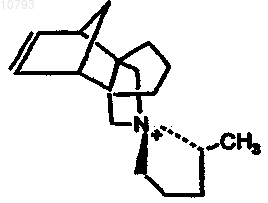
25. Способ по п.15, где кристаллическое вещество после прокаливания имеет рентгеновские дифракционные линии из табл. I.
Текст
010793 Область техники, к которой относится изобретение Настоящее изобретение относится к новому кристаллическому молекулярному ситу SSZ-61, способу получения SSZ-61 с использованием группы катионов тетрациклического азония в качестве структурообразующего агента и к использованию SSZ-61 в качестве адсорбента. Уровень техники Из-за своих уникальных ситовых свойств, а также каталитических свойств, кристаллические молекулярные сита и цеолиты особенно применимы в таких областях использования, как конверсия углеводородов, осушка и разделение газов. Хотя было описано много различных кристаллических молекулярных сит, продолжает существовать потребность в новых цеолитах с желаемыми свойствами для разделения газов и осушки, углеводородных и химических конверсий и для других областей использования. Новые цеолиты могут содержать новые пористые внутренние структуры, обеспечивающие увеличенные селективности в данных процессах. Кристаллические алюмосиликаты обычно получают из водных реакционных смесей, содержащих оксиды щелочных или щелочно-земельных металлов, диоксид кремния и оксид алюминия. Кристаллические боросиликаты обычно получают в подобных реакционных условиях, за исключением того, что вместо алюминия используют бор. Варьируя условия синтеза и состав реакционной смеси, различные цеолиты часто могут быть получены. Сущность изобретения Настоящее изобретение направлено на группу кристаллических молекулярных сит с уникальными свойствами, названных здесь как молекулярное сито SSZ-61 или просто SSZ-61. Предпочтительно SSZ-61 получают в виде его силикатной, алюмосиликатной, титаносиликатной,германосиликатной, ванадосиликатной, ферросиликатной или боросиликатной формы. Термин силикат относится к молекулярному ситу, имеющему высокое мольное отношение диоксида кремния к оксиду алюминия, предпочтительно мольное отношение больше, чем 100, включая молекулярные сита,содержащие полностью диоксид кремния. Используемый здесь термин алюмосиликат относится к молекулярному ситу, содержащему как оксид алюминия, так и диоксид кремния, и термин боросиликат относится к молекулярному ситу, содержащему как оксиды бора, так и кремния. В соответствии с настоящим изобретением, предлагается молекулярное сито, имеющее мольное отношение (1) оксида первого четырехвалентного элемента к (2) оксиду трехвалентного элемента, пятивалентного элемента, второго четырехвалентного элемента, отличного от указанного первого четырехвалентного элемента, или их смеси, примерно более 15 и имеющее после прокаливания рентгеновские дифракционные линии из табл. I. Далее, в соответствии с настоящим изобретением, предлагается молекулярное сито, имеющее мольное отношение (1) оксида выбранного из диоксида кремния, оксида германия и их смеси к (2) оксиду, выбранному из оксида алюминия, оксида галлия, оксида железа, оксида бора, оксида титана, оксида индия, оксида ванадия и их смесей, примерно более 15 и имеющее после прокаливания рентгеновские дифракционные линии из табл. I, приведенной ниже. Следует отметить, что мольное отношение первого оксида или смеси первых оксидов ко второму оксиду может быть бесконечным, т.е., второй оксид в молекулярном сите может отсутствовать. В данных случаях молекулярное сито является полностью силикатным молекулярным ситом или германосиликатом. Настоящее изобретение далее предлагает такое молекулярное сито, имеющее состав после синтеза и в безводном состоянии, в терминах мольных отношений, который следует ниже: где Y представляет собой кремний, германий или их смесь; W представляет собой алюминий, галлий, железо, бор, титан, индий, ванадий или их смеси; с равно 1 или 2; d равно 2, когда с равно 1 (т.е., W является четырехвалентным), или d равно 3 или 5, когда с равно 2 (т.е., d равно 3, когда W является трехвалентным или 5, когда W является пятивалентным); М представляет собой катион щелочного металла,катион щелочно-земельного металла или их смеси; n представляет собой валентность М (т.е. 1 или 2), иQ представляет собой катион тетрациклического азония. Кроме того, в соответствии с настоящим изобретением предлагается способ получения кристаллического материала, включающего (1) оксид первого четырехвалентного элемента и (2) оксид трехвалентного элемента, пятивалентного элемента, второго четырехвалентного элемента, который отличается от указанного первого четырехвалентного элемента, или их смесь, и имеющий мольное отношение первого оксида ко второму оксиду более чем 15, причем указанный способ включает контакт в условиях кристаллизации источников указанных оксидов и структурообразующего агента, включающего катион тетрациклического азония.-1 010793 Детальное описание настоящего изобретения Настоящее изобретение включает группу кристаллических крупнопористых молекулярных сит, названных здесь молекулярное сито SSZ-61 или просто SSZ-61. Используемый здесь термин крупнопористый означает имеющий средний размер диаметра пор более чем около 6,0 , предпочтительно примерно от 6,5 до 7,5 или более. При приготовлении SSZ-61 катион тетрациклического азония используют в качестве структурообразующего агента ("SDA"), также известного как матрица кристаллизации. SDA, применимый для приготовления SSZ-61, имеет следующие структуры: 1-азоний-13-метилпентацикло [8.-1. 4.33,8.14,7. 03,8]гептадец-5-ен Катион SDA связан с анионом (Х-), которым может являться любым анионом, который не вредит образованию цеолита. Типичные анионы включают галоген, например, фторид, хлорид, бромид и йодид,гидроксид, ацетат, сульфат, тетрафторборат, карбоксилат и аналогичные. Гидроксид является наиболее предпочтительным анионом. В общем, SSZ-61 получают контактом активного источника одного или более оксидов, выбранных из группы, состоящей из оксидов одновалентных элементов, оксидов двухвалентных элементов, оксидов трехвалентных элементов, оксидов четырехвалентных элементов и/или пятивалентных элементов, с катионом тетрациклического азония SDA.SSZ-61 получают из реакционной смеси, имеющей состав, представленный в таблице А ниже.(a) получение водного раствора, содержащего источники по меньшей мере одного оксида, способного образовать кристаллическое молекулярное сито, и катион тетрациклического азония, способный образовать SSZ-61, имеющего анионный противоион, который не вредит образованию SSZ-61;(b) поддержание водного раствора в условиях, достаточных для образования кристаллов SSZ-61; и(c) выделение кристаллов SSZ-61. Таким образом, SSZ-61 может содержать кристаллическое вещество и SDA в комбинации с металлическими и неметаллическими оксидами, связанными в тетраэдрической координации через общие атомы кислорода с образованием сшитой трехмерной кристаллической структуры. Металлические и неметаллические оксиды включают один или комбинацию оксидов первого четырехвалентного элемента(ов), и один или комбинацию трехвалентного элемента(ов), пятивалентного элемента(ов), второго четырехвалентного элемента(ов), отличного от первого четырехвалентного элемента(ов), или их смесь. Первый четырехвалентный элемент(ы) предпочтительно выбирают из группы, содержащей кремний,германий и их комбинацию. Более предпочтительно, первый четырехвалентный элемент представляет собой кремний. Трехвалентный элемент, пятивалентный элемент и второй четырехвалентный элемент(который отличается от первого четырехвалентного элемента), предпочтительно, выбирают из группы,состоящей из алюминия, галлия, железа, бора, титана, индия, ванадия и их комбинации. Более предпочтительно, второй трехвалентный или четырехвалентный элемент представляет собой алюминий или бор. Типичные источники оксида алюминия для реакционной смеси включают алюминаты, оксид алюминия, коллоидный алюминий, оксид алюминия на золе диоксида кремния, гидратированные гели оксида алюминия, такие как Al(OH)3, и соединения алюминия, такие как Al(NO3)3, AlCl3 и Al2(SO4)3. Типичные источники диоксида кремния включают силикаты, гидрогель диоксида кремния, кремниевую кислоту, коллоидальный диоксид кремния, коллоидный кремнезем, тетра-алкилортосиликаты и гидроксиды кремния. Бор, а также галлий, германий, титан, индий, ванадий и железо можно добавить в формах, соответствующих их алюминиевым и кремниевым аналогам. Источник цеолитного реагента может обеспечивать источник алюминия или бора. В большинстве случаев источник цеолита также обеспечивает источник диоксида кремния. Источник цеолита в своей дезалюминированной или деборированной форме можно также использовать в качестве источника диоксида кремния, причем дополнительный добавленный кремний использует, например, традиционные источники, перечисленные выше. Использование источника цеолитного реагента в качестве источника оксида алюминия для настоящего процесса более полно описано в патенте США 5225179, выданном 6 июля 1993 Накагаве, озаглавленном Method of Making Molecular Sieves, описание которого включено здесь в качестве ссылки. Типично, в реакционной смеси используют гидроксид щелочного металла и/или гидроксид щелочно-земельного металла, например гидроксид натрия, калия, лития, цезия, рубидия, кальция и магния; однако, данный компонент может отсутствовать при условии, что поддерживается эквивалентная основность. SDA можно использовать для обеспечения иона гидроксида. Так, это может быть полезно, например, для ионного обмена галогенида на гидроксид ион, таким образом, уменьшая или исключая требуемое количество гидроксида щелочного металла. Катион щелочного металла или катион щелочноземельного металла может быть частью свежесинтезированного кристаллического оксидного материала для уравновешивания зарядов валентных электронов. Реакционную смесь выдерживают при повышенной температуре до тех пор, пока не образуются кристаллы SSZ-61. Гидротермальную кристаллизацию обычно проводят при аутогенном давлении, при температуре от 100 до 200 С, предпочтительно от 135 до 160 С. Период кристаллизации типично составляет более 1 дня и предпочтительно примерно от 3 до 20 дней. Предпочтительно молекулярное сито готовят с использованием умеренного перемешивания или встряхивания. В процессе стадии гидротермальной кристаллизации, кристаллы SSZ-61 могут спонтанно зарождаться из реакционной смеси. Использование SSZ-61 кристаллов в качестве затравочного материала мо-3 010793 жет дать преимущество, уменьшая время, необходимое для протекания полной кристаллизации. Кроме того, затравка может приводить к улучшенной чистоте продукта, полученного промотированием зарождения кристалла и/или образования SSZ-61, минуя какие-либо нежелательные фазы. При использовании в качестве затравки кристаллы SSZ-61 добавляют в количестве от 0,1 и 10 мас.% первого оксида четырехвалентного элемента, например диоксида кремния, используемого в реакционной смеси. Как только кристаллы молекулярного сита образовались, твердый продукт выделяют из реакционной смеси методом стандартного механического разделения, таким как фильтрование. Кристаллы промывают водой и затем сушат, например, при температуре от 90 до 150 С в течение от 8 до 24 ч, получая свежесинтезированные кристаллы SSZ-61. Этап сушки может быть выполнен при атмосферном давлении или под вакуумом. Свежеполученный SSZ-61 имеет мольное отношение оксида, выбранного из диоксида кремния, оксида германия и их смесей, к оксиду, выбранному из оксида алюминия, оксида галлия, оксида железа,оксида бора, оксида титана, оксида индия, оксида ванадия и их смесей, примерно более 15; и имеет после прокаливания рентгеновские дифракционные линии из табл. I, приведенной ниже. Кроме того, SSZ-61 имеет состав непосредственно после синтеза (т.е., до удаления SDA из SSZ-61) и в безводном состоянии,в терминах мольных отношений, показанный ниже в табл. В. Таблица ВSSZ-61 можно получить с мольным отношением YO2/WcOd, равным , т.е. по существу WcOd может отсутствовать в SSZ-61. В этом случае, SSZ-61 будет представлять собой полностью материал из диоксида кремния или германосиликат. Таким образом, в типичном случае, когда используют оксиды кремния и, необязательно, германия, SSZ-61 может быть приготовлен по существу не содержащим алюминия,т.е. имеющим мольное отношение диоксида кремния к оксиду алюминия, равное . Метод увеличения мольного отношения диоксида кремния к оксиду алюминия состоит в использовании стандартного кислотного выщелачивания или обработке хелатами. Однако по существу не содержащий алюминий SSZ61 может быть синтезирован с использованием источников кремния, по существу, не содержащих алюминий, в качестве главного компонента тетраэдрического оксида металла, если также присутствует бор. Затем бор можно удалить, при желании, обработкой боросиликата SSZ-61 уксусной кислотой при повышенной температуре (как описано в Jones et al., Chem. Mater., 2001, 13, 1041-1050) для получения варианта SSZ-61 полностью из диоксида кремния. SSZ-61 также может быть получен непосредственно в виде боросиликата. При желании бор можно удалить, как описано выше, и заместить на атомы металла методами, известными из уровня техники. Более низкие отношения диоксида кремния к оксиду алюминия также можно получить с использованием методов, которые внедряют алюминий в кристаллическую решетку. Например, внедрение алюминия может происходить путем термической обработки цеолита в сочетании со связующим из оксида алюминия или растворенным источником оксида алюминия. Такие процедуры описаны в патенте США 4 559 315, выданном 17 декабря 1985 Чангу с соавт. Считается, что SSZ-61 содержит новую структуру решетки или топологию, которая характеризуется своей рентгенограммой. SSZ-61 после прокаливания имеет кристаллическую структуру, порошковая рентгенограмма которого демонстрирует характеристические линии, показанные в табл. I и, таким образом, отличается от других молекулярных сит. Представленные рентгенограммы основаны на шкале относительной интенсивности, в которой самая сильная линия в рентгенограмме обозначается величиной 100; W (слабая) менее 20; М (средняя) от 20 до 40; S (сильная) от 40 до 60; VS (очень сильная) более чем 60. Табл. IA, приведенная ниже, демонстрирует линии порошковой рентгенограммы для прокаленногоSSZ-61, включая действительные относительные интенсивности. Таблица IА. Прокаленный SSZ-61 Порошковые рентгенограммы определяют стандартным методом. Излучение представляло собой Кальфа/дублет меди. Высоту пиков и их положения, в виде функции от 2, гдепредставляет собой брэгговский угол, считывают из относительных интенсивностей пиков, и d, межплоскостное расстояние в Ангстремах, относящееся к зарегистрированной полосе, может быть рассчитано. Разброс в измерениях угла (два тета) рассеяния, из-за погрешности прибора и различий между двумя индивидуальными образцами, оценивается как 0,1. Характерные пики из рентгенограммы прокаленного SSZ-61 показаны в табл. I. Прокаливание может приводить к изменениям в интенсивностях пиков в сравнении с рентгенограммами свежеприготовленного образца, а также к незначительным сдвигам в рентгенограмме. Молекулярное сито, полученное обменом металлических или других катионов, присутствующих в молекулярном сите, на различные дру-5 010793 гие катионы (такие как Н+ или NH4+) дает, по существу, ту же самую рентгенограмму, хотя опять могут быть незначительные сдвиги в межплоскостном расстоянии и вариации в относительных интенсивностях пиков. Несмотря на эти незначительные отклонения, основная кристаллическая решетка остается неизменной в результате данных обработок. Кристаллический SSZ-61 можно использовать свежеприготовленным (как синтезирован), но предпочтительно можно термически обработать (прокалить). Обычно желательно удалить катионы щелочного металла ионным обменом и заместить их водородом, аммонием или любым желаемым металлическим ионом. Молекулярное сито может быть выщелочено хелатирующим агентом, например ЭДТУ или разбавленными кислотными растворами, для увеличения мольного отношения диоксида кремния к оксиду алюминия. Молекулярное сито также можно обработать паром; обработка паром делает кристаллическую решетку устойчивой к воздействию кислот. Металлы можно вводить в молекулярное сито замещением некоторых катионов в молекулярном сите на металлические катионы методом стандартного ионного обмена (см., например, патенты США 3140249, выданный 7 июля 1964 Планку с соавт.; 3140251, выданный 7 июля 1964 Планку с соавт.; 3140253, выданный 7 июля 1964 Планку с соавт.). Типичные замещающие катионы могут включать катионы металлов, например, редкоземельных металлов, металлов группы IA, группы IIA и группы VIII, а также их смеси. Из замещающих металлических катионов особенно предпочтительны такие катионы металлов, как редкоземельные, Mn, Ca, Mg, Zn, Cd, Pt, Pd, Ni, Co, Ti, Al, Sn и Fe. Водород, аммоний и металлические компоненты могут быть введены ионным обменом в SSZ-61.SSZ-61 также можно импрегнировать металлами, или металлы могут быть физически и тщательно смешаны с SSZ-61, используя стандартные методы, известные из уровня техники. Типичные ионообменные методы включают контакт синтетического молекулярного сита с раствором, содержащим соль желаемого замещающего катиона или катионов. Хотя можно использовать широкий ряд солей, особенно предпочтительными являются хлориды и другие галогениды, ацетаты, нитраты и сульфаты. Молекулярное сито обычно прокаливают перед процедурой ионного обмена для того, чтобы удалить органическое вещество, присутствующее в каналах и на поверхности, так как это приводит к более эффективному ионному обмену. Типичные ионообменные методы раскрыты в различных патентах, включая патент США 3140249, выданный 7 июля 1964 Планку с соавт.; 3140251, выданный 7 июля 1964 Планку с соавт., и 3140253, выданный 7 июля 1964 Планку с соавт. После контакта с раствором соли желаемого замещающего катиона, молекулярное сито обычно промывают водой и сушат при температуре в диапазоне от 65 до около 200 С. После промывания молекулярное сито можно прокалить на воздухе или в инертном гаае при температурах в диапазоне примерно от 200 до 800 С в течение периода времени в диапазоне от 1 до 48 ч или более, чтобы получить каталитически активный продукт, особенно полезный в процессах конверсии углеводородов. Независимо от катионов, присутствующих в синтезированном SSZ-61, пространственное расположение атомов, которые образуют основную кристаллическую решетку молекулярного сита, остается по существу неизменным.SSZ-61 можно получить в разнообразных физических формах. Вообще говоря, молекулярное сито может быть в форме порошка, гранулы или сформованного продукта, такого как экструдат, имеющего размер частицы, достаточный для прохода через сито размером 2-меш (Tyler) и быть удержанным на сите размером 400-меш (Tyler). В случаях, когда катализатор является сформованным, например, экструзией с органическим связующим, SSZ-61 может быть экструдирован до сушки, или высушен или частично высушен и затем экструдирован.SSZ-61 может быть смешан с другими материалами, устойчивыми к температуре и другим условиям, применяемым в процессах конверсии органических веществ. Такие матричные материалы включают активные и неактивные материалы и синтетические или встречающиеся в природе цеолиты, а также неорганические материалы, такие как глины, диоксид кремния и оксиды металлов. Примеры таких материалов и способ, которым их можно использовать, описываются в патенте США 4910006, выданном 20 мая 1990 Зонсу с соавт., и в патенте США 5316753, выданном 31 мая 1994 Накагаве с соавт., каждый из которых включен здесь ссылкой во всей своей полноте.SSZ-61 применим в качестве адсорбента. Примеры Следующие далее примеры демонстрируют, но не ограничивают настоящее изобретение. Пример 1. Синтез матрицы В-6 010793 Анион (Х-) связан с катионом и может представлять собой любой анкон, который не мешает образованию SSZ-61. Типичные анионы включают галоген, например фторид, хлорид, бромид и йодид, гидроксид, ацетат, сульфат, тетрафторборат, карбоксилат и аналогичнные. Гидроксид является наиболее предпочтительным анионом. Структурообразующий агент (SDA) 8-азоний-8,8-диэтилтетрацикло[4.3.3.12,5.01,6]тридец-3-ен катион синтезируют процедурой, описанной ниже. К раствору свежее крекированного циклопентадиена (40 грамм) в 1200 мл дихлорметана добавляют ангидрид 1-циклопентен-1,2-дикарбоновой кислоты (30 грамм). Реакционную смесь перемешивают при комнатной температуре в течение нескольких дней. Желаемый продукт, 8-окса-тетрацикло [4.3.3.12,5. 01,6]тридец-3-ен-7,9-дион, выделяют перекристаллизацией(после удаления растворителя) из смеси 2/1 этиловый эфир/дихлорметан при охлаждении. Затем продукт реагирует с первичным амином в воде при 85 С в течение 3 дней в закрытой системе. Например, 4,5 г тетрациклического ангидрида помещают в тефлоновую чашку объемом 125 см 3 реактора Парра с 10 мл этиламина (70% в Н 2 О) и 0,30 г 4-диметиламинопиридина в качестве катализатора. После нагревания в течение трех дней реакционную смесь охлаждают, и при мягком перемешивании осаждают желаемый имид. Осадок собирают фильтрованием и сушат под вакуумом. Восстановление предшествующего имида до соответствующего амина К суспензии гидрида литий-алюминия (2,52.) в тетрагидрофуране (55 мл) при 0 С (с помощью ледяной бани) в 250 мл трехгорлой колбе, по каплям (с помощью капельной воронки) при механическом перемешивании добавляют имид (5 г), растворенный в 40 мл ТГФ. Как только весь имид добавлен, ледяную баню заменяют на колбонагреватель, и реакционную смесь кипятят с обратным холодильником в течение ночи. Колбонагреватель меняют на ледяную баню и реакционную смесь разбавляют 50 мл диэтилового эфира. Реакцию вызывают добавлением 15 мл 15% раствора NaOH по каплям при энергичном перемешивании. Как только добавление NaOH завершено, реакционная смесь серого цвета превращается в бесцветную жидкость с белым осадком. Смесь фильтруют, и фильтрат сушат над MgSO4. Фильтрование и концентрирование фильтрата при пониженном давлении на роторном испарителе дает 4,12 г желаемого продукта. Кватернизация этилйодидом (синтез 8-азоний-8,8-диэтилтетрацикло [4.3.3.12,5. 01,6]тридец-3-ен йодида, матрица В) К раствору 5 г 8-аза-8-этилтетрацикло[4.3.3.12,5.01,6]тридец-3-ена в 60 мл безводного метанола добавляют 9,4 г этилйодида. Реакционную смесь механически перемешивают в течение 48 ч при комнатной температуре. Затем добавляют дополнительный эквивалент этилйодида (4,7 г) и реакционную смесь далее перемешивают при комнатной температуре в течение дополнительных 48 ч. Реакционную смесь концентрируют при пониженном давлении на роторном испарителе, получая йодидную соль в виде окрашенного в желтоватый цвет твердого вещества. Данную йодидную соль очищают перекристаллизацией. Данную процедуру осуществляют полным растворением йодидной соли в ацетоне и затем осаждением путем добавления этилового эфира к раствору ацетона. Процедура дает белый порошок с очень чистыми 1 Н и 13 С ЯМР спектрами, и точный элементный анализ данного продукта. Ионный обмен 8-азоний-8,8-диэтилтетрацикло [4.3.3.12,5.01,6]тридец-3-ен йодид (4,10 г) растворяют в 12 мл воды в 100-мл пластиковой бутылке. К раствору добавляют 8,4 г ионообменной смолы-ОН (Bio Rad AG1-X8) и смесь перемешивают при комнатной температуре в течение ночи. Продукт собирают удалением смолы фильтрованием после 3-4 дней обмена. Образец раствора титруют, чтобы определить молярность ОН для последующего использования в синтезе цеолита. Примеры 2-5. Синтезы матриц А, С, D и Е Матрицу А синтезируют кватернизацией 8-аза-8-этилтетрацикло [4.3. 3.12,5.01,6]тридец-3-ена с метилйодидом. Матрицы С-Е получают, используя методологию, описанную выше. Исходный имид, 8 азатетрацикло[4.3.3.12,5.01,6]тридец-3-ен-7,9-дион, синтезируют взаимодействием тетрациклического ангидрида с аммиаком, и при восстановлении LiAlH4 он дает незамещенный вторичный циклический амин,8-азатетрацикло [4.3.3.12,5.01,6]тридец-3-ен. Кватернизация данного амина с подходящим дигалогенидом в присутствии КНСО 3 дает желаемую матрицу (матрица С из 1,4-дийодобутана, матрица D из 1,5 дийодобутана, и матрица Е из 2-метил-1,4-дийодобутана). Следует понимать, что другие производные могут быть приготовлены выбором реагента, образующего имид, совместно с выбором стадии алкилирования. Пример 6. Типичный синтез SSZ-61 В тефлоновый цилиндр объемом 23 см 3 (тарированную) добавляют раствор 8-азоний-8,8 диэтилтетрацикло[4.3.3.12.5.01,6]тридец-3-ен гидроксида (4 ммоль матрицы В) и 1,66 г тетраэтилортосиликата (8 мМ SiO2). Данный материал помещают в вытяжной шкаф и оставляют для испарения (этанола) в течение нескольких дней и затем Н 2 О/SiO2 отношение регулируют до 20. При перемешивании добавляют 0,148 г 50% HF, используя пластиковый шпатель. Полученный в результате гель удаляют, помещают в стальной автоклавный реактор Парра и нагревают в печи при 150 С, вращая со скоростью 43 об./мин. Реакцию контролируют проверкой рН геля и наблюдением за образованием кристаллов с ис-7 010793 пользованием сканирующего электронного микроскопа (СЭМ) с интервалами в шесть дней. Реакция завершается после нагревания в течение 18 дней при условиях, описанных выше. Как только кристаллизация закончена, смесь фильтруют через пористый стеклянный фильтр. Собранное твердое вещества тщательно моют водой и затем промывают ацетоном (20 мл) для удаления органических остатков. Твердое вещество оставляют сохнуть на воздухе в течение ночи и затем сушат в сушильном шкафу при 120 С в течение 1 ч. Взаимодействие дает 0,38 г SSZ-61. Рентгеноструктурный и ИК анализ порошка показывает,что продукт является SSZ-61. Пример 7. Прокаливание SSZ-61 Вещество из примера 6 прокаливают следующим образом. Тонкий слой вещества нагревают в муфельной печи от комнатной температуры до 120 С со скоростью 1 С в минуту и выдерживают при 120 С в течение 3 ч. Затем температуру поднимают до 540 С с той же скоростью и выдерживают при этой температуре в течение пяти часов, после чего ее увеличивают до 594 С и выдерживают еще в течение 5 ч. В процессе нагревания над SSZ-61 пропускают смесь воздуха с азотом 50/50 со скоростью 20 стандартных кубических футов (0,57 стандартных кубических метров) в минуту. Пример 8. Синтез SSZ-61SSZ-61 синтезируют так, как описано в примере 6, за исключением того, что взаимодействие проводят при 170 С. Пример 12. Синтез SSZ-61SSZ-61 синтезируют так, как описано в примере 10, за исключением того, что взаимодействие проводят при 170 С. Пример 13. Синтез SSZ-61SiO2/Al2O3 равно 150 и в качестве источника алюминия используют Al(NO3)3. Пример 14. Анализ по адсорбции аргонаSSZ-61 имеет объем микропор, по меньшей мере, 0,06 см 3/г на основании изотермы адсорбции аргона при 87,3 К (-186 С), зарегистрированной на ASAP 2010 приборе от Micromerities. Доза при низком давлении составляла 2,00 см 3/г (станд. услов.) с 15 с равновесным интервалом. Изотерму адсорбции аргона анализировали, используя формальный подход метода функционала электронной плотности (DFT) и параметры, выведенные для пор активированного угля Оливером (Porous Mater. 1995, 2,9) с использованием адаптации Saito Foley способа формального подхода Horvarth-Kawazoe (Microporous Materials, 1995,3, 531) и традиционный t-графический метод (J. Catalysis, 1965, 4, 319). Анализ установил крупнопористое молекулярное сито. Пример 15. Адсорбция 1,3,5-триизопропилбензола Адсорбционная емкость SSZ-61 по газофазным углеводородам измеряли при комнатной температуре с помощью весов Cahn C-2000, соединенных с компьютером через цифровой интерфейс ATI-Cahn. 1,3,5-триизопропилбензол использовали в качестве молекулы адсорбата, являющейся калиберной пробкой. 1,3,5-триизопропилбензол (жидкость) имел чистоту 99,5+% (Aldrich), как было установлено ГХ анализом, и его использовали без дополнительной очистки. Пары адсорбата подавали из жидкой фазы. Относительное давление пара Р/Р 0 поддерживали при 0,3, регулируя температуру жидкого адсорбата с использованием охлаждающего циркулятора. Перед проведением адсорбционных экспериментов прокаленный SSZ-61 дегазировали при 350 С под вакуумом, составляющим по меньшей мере 10-3 торр, в течение 5 ч. Адсорбционную емкость представили в миллилитрах жидкости на грамм сухого SSZ-61, основываясь на плотности жидкой фазы адсорбата, адсорбированного в порах образца. Данные по адсорбции 1,3,5-триизопропилбензола собирали после 5 дней.SSZ-61 имеет адсорбционную емкость по 1,3,5-триизопропидбензолу, равную 0,079 мл/г для продукта из примера 7. Данная величина относит SSZ-61 к группе цеолитов, которые обычно больше, чем 12-членное кольцо (несомненно для высококремнистых, одномерных систем). ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Молекулярное сито, имеющее мольное отношение оксида первого четырехвалентного элемента к оксиду второго четырехвалентного элемента, отличного от указанного первого четырехвалентного элемента, трехвалентного элемента, пятивалентного элемента или их смеси, более 15 и имеющее после прокаливания рентгеновские дифракционные линии из табл. I. 2. Молекулярное сито, имеющее мольное отношение оксида, выбранного из группы, состоящей из-8 010793 диоксида кремния, оксида германия и их смесей, к оксиду, выбранному из оксида алюминия, оксида галлия, оксида железа, оксида бора, оксида титана, оксида индия, оксида ванадия и их смесей, примерно 15 и имеющее после прокаливания рентгеновские дифракционные линии из табл. I. 3. Молекулярное сито по п.2, где оксиды включают диоксид кремния и оксид алюминия. 4. Молекулярное сито по п.2, где оксиды включают диоксид кремния и оксид бора. 5. Молекулярное сито по п.1, где указанное молекулярное сито преимущественно находится в водородной форме. 6. Молекулярное сито по п.1, где указанное молекулярное сито, по существу, не имеет кислотности. 7. Молекулярное сито, имеющее следующий состав, в свежеприготовленном и в безводном состоянии, в терминах мольных отношений: где Y представляет собой кремний, германий или их смесь; W представляет собой алюминий, галлий,железо, бор, титан, индий, ванадий или их смесь; с равно 1 или 2; d равно 2, когда с равно 1, или d равно 3 или 5, когда с равно 2; М представляет собой катион щелочного металла, катион щелочно-земельного металла или их смеси; n представляет собой валентность М и Q представляет собой катион, выбранный из группы, состоящей из нижеследующего: 8. Молекулярное сито по п.7, где W представляет собой алюминий и Y представляет собой кремний. 9. Молекулярное сито по п.7, где W представляет собой бор и Y представляет собой кремний. 10. Молекулярное сито по п.7, где Q представляет собой-9 010793 11. Молекулярное сито по п.7, где Q представляет собой 12. Молекулярное сито по п.7, где Q представляет собой 13. Молекулярное сито по п.7, где Q представляет собой 14. Молекулярное сито по п.7, где Q представляет собой 15. Способ получения кристаллического материала, включающего (1) оксид первого четырехвалентного элемента и (2) оксид трехвалентного элемента, пятивалентного элемента, второго четырехвалентного элемента, который отличается от указанного первого четырехвалентного элемента, или их смесь, причем указанный способ включает контакт в условиях кристаллизации источников указанных оксидов и структурообразующего агента, включающего катион, выбранный из группы, состоящей из нижеследующего: 16. Способ по п.15, где первый четырехвалентный элемент выбран из группы, состоящей из крем- 10010793 ния, германия и их комбинаций. 17. Способ по п.15, где второй трехвалентный элемент, пятивалентный элемент или четырехвалентный элемент выбраны из группы, состоящей из алюминия, галлия, железа, бора, титана, индия, ванадия и их комбинаций. 18. Способ по п.17, где второй трехвалентный элемент или четырехвалентный элемент выбран из группы, состоящей из алюминия, бора, титана и их комбинаций. 19. Способ по п.16, где первый четырехвалентный элемент представляет собой кремний. 20. Способ по п.15, где структурообразующий агент представляет собой 21. Способ по п.15, где структурообразующий агент представляет собой 22. Способ по п.15, где структурообразующий агент представляет собой 23. Способ по п.15, где структурообразующий агент представляет собой 24. Способ по п.15, где структурообразующий агент представляет собой 25. Способ по п.15, где кристаллическое вещество после прокаливания имеет рентгеновские дифракционные линии из табл. I.
МПК / Метки
МПК: B01J 29/04
Метки: синтез, композиция, сита, молекулярного, ssz-61
Код ссылки
<a href="https://eas.patents.su/12-10793-kompoziciya-molekulyarnogo-sita-ssz-61-i-ego-sintez.html" rel="bookmark" title="База патентов Евразийского Союза">Композиция молекулярного сита ssz-61 и его синтез</a>
Предыдущий патент: Способ извлечения ценных металлов из сульфидных руд цветных металлов
Следующий патент: Способ создания анизотропной петрофизической вычислительной модели подземной области
Случайный патент: Способ реконструкции системы газоснабжения