Применение олигоуронатов для лечения повышенной вязкости слизи
Номер патента: 15436
Опубликовано: 31.08.2011
Авторы: Драгет Курт Ингар, Тэйлор Кэтрин, Смидсрод Олав Асмунд
Формула / Реферат
1. Способ лечения человека или субъекта, не являющегося человеком, для борьбы с повышенной вязкостью слизи в дыхательных путях, включающий нанесение на поверхность слизистой оболочки указанных путей путем введения в дыхательные пути указанного субъекта эффективного количества физиологически приемлемого олигоуроната, где указанный олигоуронат происходит из природного источника.
2. Способ по п.1, где указанный олигоуронат происходит из природного альгинатного источника.
3. Способ по п.1 или 2, где указанный олигоуронат содержит гулуроновую кислоту в виде мономера.
4. Способ по любому из пп.1-3, где указанный олигоуронат представляет собой 4-25-мер.
5. Способ по любому из пп.1-4 для лечения муковисцидоза.
6. Способ по любому из пп.1-4 для лечения синусита.
7. Способ по любому из пп.1-4 для лечения хронических обструктивных заболеваний легких.
8. Применение физиологически приемлемого олигоуроната, как он определен в любом из пп.1-4, для изготовления лекарственного средства, пригодного для ингаляционного введения, для применения в лечении повышенной вязкости слизи в дыхательных путях.
9. Применение по п.8 для изготовления лекарственного средства, пригодного для ингаляционного введения, для применения в лечении муковисцидоза.
10. Применение по п.8 для изготовления лекарственного средства, пригодного для ингаляционного введения, для применения в лечении синусита.
11. Применение по п.8 для изготовления лекарственного средства, пригодного для ингаляционного введения, для применения в лечении хронических обструктивных заболеваний легких.
12. Фармацевтическая композиция, пригодная для ингаляционного введения, содержащая физиологически приемлемый олигоуронат вместе с физиологически приемлемым носителем или эксципиентом, где указанный олигоуронат представляет собой 3-25-мер и происходит из природного источника.
13. Композиция по п.12, содержащая дополнительный физиологически приемлемый агент, уменьшающий вязкость слизи.
14. Композиция по п.12 или 13, содержащая олигоуронат, который содержит гулуроновую кислоту в виде мономера.
15. Композиция по любому из пп.12-14, содержащая ДНКазу.
16. Спрей-аппликатор, включающий емкость и генератор капель, где указанная емкость содержит водный раствор физиологически приемлемого олигоуроната, как он определен в п.3 или 4.
Текст
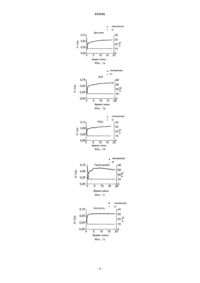
Дата публикации и выдачи патента Номер заявки ПРИМЕНЕНИЕ ОЛИГОУРОНАТОВ ДЛЯ ЛЕЧЕНИЯ ПОВЫШЕННОЙ ВЯЗКОСТИ СЛИЗИ Согласно изобретению предложен способ лечения человека или субъекта, не являющегося человеком, для борьбы с повышенной вязкостью слизи в дыхательных путях, включающий нанесение на поверхность слизистой оболочки указанных путей у указанного субъекта эффективного количества физиологически приемлемого олигоуроната.(71)(73) Заявитель и патентовладелец: ЭнТиЭнЮ ТЕКНОЛОДЖИ ТРАНСФЕР АС (NO) 015436 Данное изобретение относится к способу лечения человека или животных, не являющихся человеком, особенно млекопитающих, олигоуронатами для борьбы с повышенной вязкостью слизи, например для улучшения отхождения слизи, особенно из дыхательных путей, как например в случае ХОЗЛ (хронические обструктивные заболевания легких), особенно из пазух и легких, в частности в лечении муковисцидоза (CF), хронического обструктивного заболевания легких и синусита. Муковисцидоз является самым распространенным летальным генетическим заболеванием в европейской популяции. Это заболевание вызвано мутацией в гене, кодирующем трансмембранный регулятор муковисцидоза (CFTR), хлоридный канал, представленный в секреторных и других клетках в организме. Для этого заболевания характерно наличие в организме секреции густой неустранимой слизи, которая может привести к легочному заболеванию, расстройствам пищеварения и бесплодию. Нормальная система мукоцилиарного клиренса оказывается не в состоянии выводить чрезмерно вязкую слизь, которую колонизируют микроорганизмы, повышающие, в свою очередь, вязкость слизи и способные привести к хроническому воспалению и обструкции легких. Таким образом, легочное заболевание является наибольшей проблемой со здоровьем для большинства пациентов с CF, а также является главной причиной смерти. Слизь является нормальным секретом всех отделов дыхательных путей, включая легкие. Ее основной функцией является участие в системе мукоцилиарного клиренса, которая обеспечивает очищение легких и защищает от инфекции. Система мукоцилиарного клиренса включает три главных компонента: слизь, реснички и жидкость поверхности дыхательных путей. Таким образом, эпителиальная поверхность включает бокаловидные клетки, секретирующие слизь, и реснитчатые эпителиальные клетки с располагающимся поверхностно слоем жидкости поверхности дыхательных путей и, поверх этого, слоем слизи, в которую вдаются кончики ресничек. Слизь представляет собой липкое гелеобразное вещество,состоящее преимущественно из воды (примерно 95% по массе) и муцинов, гелеобразующих молекул,отвечающих за физические свойства слизи. Реснички представляют собой маленькие волосообразные выросты на поверхности эпителиальных клеток, ритмично бьющиеся в водянистой невязкой жидкости поверхности дыхательных путей, причем кончики ресничек погружены в слой слизи. Слой слизи образует липкое защитное покрытие на поверхности легких, которое захватывает бактерии, вирусы, вдыхаемые частицы, загрязняющие агенты окружающей среды и продукты разрушения клеток. Биение ресничек служит для продвижения этого слизистого покрытия и всего того, что им захвачено, по направлению к ротовой полости и из легких. В нормальных условиях система мукоцилиарного клиренса функционирует эффективно и поддерживает легкие в чистоте и без инфекции. Если эта система перегружена, существует вторая линия защиты - кашель. Таким образом, когда в ответ на раздражение или воспаление, например,из-за вдыхаемых частиц или инфекции, секретированы повышенные уровни слизи, выброс слизи из легких происходит посредством кашлевого рефлекса. У пациентов с CF слизь в легком более густая и вязкая, чем нормальная, и реснички не так легко транспортируют эту более густую слизь. В результате система мукоцилиарного клиренса оказывается скомпрометирована и легкие становятся более восприимчивыми к инфекции. Кроме того, легкие пациента с CF, как считают, находятся в состоянии чрезмерного воспаления с постоянным низким уровнем воспаления и повышенным ответом на агенты, обычно вызывающие воспаление. Это является проблемой,поскольку частью ответа на воспаление является повышенная продукция слизи. Накапливается повышенное количество слизи, если она слишком густая для удаления с помощью системы мукоцилиарного клиренса или кашля, уменьшается жизненная емкость легких и снижается обмен кислорода через слизистую оболочку. Этот процесс обеспечивает формирование идеальной среды для бактериальной колонизации, серьезной проблемы для пациентов с CF, поскольку она также вызывает воспаление и активирует иммунный ответ. Это приводит не только к повышению секреции слизи, но также и к повышенному количеству клеток и агентов иммунного ответа, таких как макрофаги и лизоцимы. Поскольку бактерии и макрофаги гибнут, их клеточное содержимое, которое включает вязкие молекулы, такие как ДНК, высвобождается в слизь. Кроме того, некоторые из этих бактерий, например Burkholderia sp. и Pseudomonasaeruginosa, также секретируют полисахариды с высокой вязкостью, во втором случае это альгинаты. Эти молекулы дополнительно повышают вязкость слизи, в случае альгинатов, по-видимому, посредством взаимодействия с муциновой матрицей слизи, а в случае ДНК, по-видимому, посредством повышения вязкости коллоидной фазы в муциновой матрице. Таким образом, поддержание слизи в форме, которую можно транспортировать посредством ресничек, является основной целью лечения CF. Агенты, которые просто разрушают ее гелеобразную структуру, приводят к образованию жидкости, которая является такой же нетранспортабельной, как и чрезмерно вязкая слизь пациентов с CF. Поэтому важно, чтобы любой лечебный агент не разрушал гелевую матрицу, образованную гликопротеиновыми муцинами. В настоящее время авторы изобретения обнаружили, что этого можно достичь с помощью олигоуронатов, то есть олигомеров, несущих многозарядные гидроксильные группы, в частности одного, содержащего от двух до тридцати мономерных остатков. В других отделах дыхательных путей, в частности в пазухах, особенно в околоносовых пазухах,чрезмерно вязкая слизь может приводить к проблемам. Олигоуронаты также можно применять в отно-1 015436 шении этих проблем. Таким образом, согласно одному аспекту изобретения, предложен способ лечения человека или субъекта, не являющегося человеком (например, млекопитающего), для борьбы с повышенной вязкостью слизи в дыхательных путях, например для лечения пациентов с хроническим обструктивным заболеванием легких, синуситом или муковисцидозом, включающий нанесение на поверхность слизистой оболочки указанных путей у указанного субъекта эффективного количества физиологически приемлемого олигоуронатного полиола. Согласно другому аспекту этого изобретения предложено применение физиологически приемлемого олигоуроната для изготовления лекарственного средства для применения в лечении повышенной вязкости слизи дыхательных путей. Нанесение олигоуроната можно осуществлять любым способом, который доставит его на секретирующую слизь или несущую слизь поверхность дыхательных путей пациента, например околоносовых пазух или, более предпочтительно, легких. Типичным будет введение посредством ингаляции, например,жидких капель (например, аэрозоль) или порошка. Противоионами для олигоуроната могут быть любые физиологически приемлемые ионы, которые обычно используют для заряженных лекарственных веществ, например, натрий, калий, аммоний, хлорид,мезилат, меглумин и другие. Однако ионы, способствующие загущению альгината, например металлы 2 группы, предпочтительно не использовать. Несмотря на то что олигоуронат может быть синтетическим веществом, предпочтительно он является производным со средней молекулярной массой менее 100000 Да встречающегося в природе полисахарида. Предпочтительно он представляет собой от 3- до 28-мер, в частности от 4- до 25-мер, особенно от 6-до 22-мер, в частности от 8- до 15-мер, особенно 10-мер, например, с молекулярной массой в диапазоне от 350 до 6000 Да, особенно от 750 до 4500 Да. Это может быть одно соединение или это может быть смесь соединений-олигоуронатов, например, в диапазоне степеней полимеризации. Более того, остатки мономеров в олигоуронате, например моносахаридные группы, могут быть одинаковыми или различными и не все из них должны иметь электрически заряженные группы, хотя предпочтительно, чтобы большая часть (например, по меньшей мере 60%, предпочтительно по меньшей мере 80%, более предпочтительно по меньшей мере 90%) их имела. Предпочтительно, чтобы существенное большинство, например, по меньшей мере 80%, более предпочтительно по меньшей мере 90% заряженных групп имело одинаковую полярность. Отношение гидроксильных групп к заряженным группам в олигоуронате предпочтительно составляет по меньшей мере 2:1, особенно по меньшей мере 3:1. Олигоуронаты легко получить из природных источников, поскольку многие природные полисахариды содержат заряженные остатки уронатов, например, такие как остатки гулуроновой и галактуроновой кислот. Гидролиз полисахарида до олигосахарида для получения олигоуроната, применимого согласно настоящему изобретению, можно осуществлять с использованием стандартных методик лизиса полисахаридов, таких как ферментативное расщепление или гидролиз в кислой среде. После этого олигоуронаты можно отделить от продуктов разрушения полисахарида посредством хроматографии с использованием ионообменной смолы или посредством фракционированного осаждения или солюбилизации. Олигоуронаты также можно химически модифицировать, включая, но не ограничиваясь такой модификацией, как добавление заряженных групп (таких как карбоксилированные или карбоксиметилированные гликаны), и олигоуронаты можно модифицировать для изменения пластичности (например, посредством окисления периодатом). Подходящие полисахариды обсуждены, например, в "Handbook of Hydrocolloids", Ed. Phillips andWilliams, CRC, Boca Raton, Florida, USA, 2000. Однако особенно предпочтительно использование альгинатов, поскольку они встречаются в природе в виде блок-сополимеров мануроновой (М) и гулуроновой(G) кислот, а из первоисточников альгинатов можно легко получить G-блок-олигомеры. В действительности, обычно олигоуронат предпочтительно представляет собой олигогулуроновую кислоту или, менее предпочтительно, олигогалактуроновую кислоту. В тех случаях, когда в качестве исходных веществ для получения олигоуроната используют альгинаты, при необходимости можно увеличить содержание гулуроновой кислоты посредством эпимеризации с манноуронан-С-5-эпимеразами, полученными из A.vinelandii. Олигогулуроновые кислоты, подходящие для использования по изобретению, можно подходящим образом получить с помощью кислотного гидролиза альгиновой кислоты, полученной из Laminaria hyperborea, растворения при нейтральном значении рН, добавления неорганической кислоты для понижения значения рН до 3,4 для осаждения олигогулуроновой кислоты, промывания слабой кислотой, ресуспендирования при нейтральном значении рН и сублимационной сушки. Согласно другому аспекту изобретения также предложена фармацевтическая композиция, особенно композиция для ингаляционного введения, например раствор, суспензия, дисперсная система или порошок, содержащая физиологически приемлемый олигоуронат вместе с физиологически приемлемым носителем или эксципиентом, и предпочтительно также дополнительный физиологически приемлемый агент, уменьшающий вязкость слизи, например фермент, расщепляющий нуклеиновые кислоты (напри-2 015436 мер, ДНКаза, такая как ДНКаза I), гельсолин, тиол-восстанавливающий агент, ацетилцистеин, хлорид натрия, незаряженный полисахарид с низкой молекулярной массой (например, декстран), аргинин (или другие предшественники или стимуляторы синтеза оксида азота), или анионная полиаминокислота (например, поли-ASP или поли-GLU). Особенно предпочтительным является применение ДНКазы. Олигоуронат обычно можно вводить в дозах от 1 до 10000 мг, особенно от 10 до 1000 мг для взрослого человека. Оптимальную дозу без труда можно определить с помощью обычных экспериментов для определения диапазона доз, возможно с последующим исходным исследованием животной модели, например, модели на собаке. Композиции по изобретению можно изготовить с использованием общепринятых фармацевтических носителей и эксципиентов, например, растворителей (таких как вода), модификаторов осмоляльности, корригентов, регуляторов уровня рН и тому подобного. Они могут содержать дополнительные активные компоненты, например агенты, используемые для разрушения биополимеров, не включенных в муциновую матрицу слизи (например, ДНКаза, особенно rhDNase (человеческая рекомбинантная ДНКаза), антибактериальные агенты и противовоспалительные агенты. Особенно предпочтительным аспектом способа по изобретению является комбинированная терапия с применением такого дополнительного агента и олигоуроната, вводимых отдельно или вместе. Такие дополнительные агенты можно применять в их обычных дозах или даже в меньших дозах, например 50% от обычной дозы. Олигоуронаты желательно вводить в виде спрея, предпочтительно распыляемого аэрозоля, изготовленного из водного раствора, или в форме порошков, например, с модовым размером частиц приблизительно от нанометра до микрометра (например, от 10 до 50000 нм) по объему. Согласно другому аспекту изобретения предложен спрей-аппликатор, включающий емкость и генератор капель, где указанная емкость содержит водный раствор физиологически приемлемого олигоуроната. Такие спреи-аппликаторы, и несомненно олигоуронаты, можно применять в лечении заложенности пазух или носа или застоя в них, являющихся следствием простуды или других причин. Теперь изобретение будет описано дополнительно с помощью ссылок на нижеследующие неограничивающие примеры и сопроводительные графические материалы, где на фиг. 1 а-1 е представлен график комплексного модуля во времени для муцин-альгинатного геля и для того же самого геля с добавлением дозы декстрана, полиэтиленгликоля, ДНК, олигомера галактуроната натрия и олигомера гулуроната натрия соответственно; на фиг. 2 и 3 представлены столбиковые диаграммы, отражающие комплексный модуль (G) и угол сдвига фаз тех же самых гелей в конце загущения в виде процента от контрольного образца; на фиг. 4 представлена столбиковая диаграмма, отражающая напряжение пластического течения тех же самых гелей, вновь в виде процента от контрольного образца; фиг. 5 а и 5 б отражают комплексный модуль G для обработанных и необработанных образцов мокроты пациентов с CF, где Фиг. 5 б отражает G в виде процента от контрольного образца (необработанная мокрота); фиг. 5 в-5 е отражают графики G во времени; фиг. ба и 6 б отражают комплексную вязкостьдля обработанных и необработанных образцов мокроты, где Фиг. 6 б отражаетв виде процента от контрольного образца; и фиг. 7 а и 7 б отражают угол сдвига фаздля обработанных и необработанных образцов мокроты. Фиг. 7 б отражает 6 в виде процента от контрольного образца. Пример 1. Исследовали действие на модель муцин-альгинатного геля пяти олигомерных материалов: а) декстран с низкой молекулярной массой (6000 Да); б) PEG (полиэтиленгликоль) с низкой молекулярной массой (3350 Да); в) ДНК с низкой молекулярной массой; г) олигомеры галактуроната натрия; д) олигомеры гулуроната натрия (G-блоки); Олигомер гулуроната натрия получали, как было описано выше, и он имел следующие характеристики:FG 0,87, FM 0,13, FGG 0,83, FGM=FMG 0,05, FMM 0,08, FGGM=FMMG 0,04, FMGM 0,02, FGGG 0,79, DP 19. Материалы Контрольный гель состоял из 18 мг/мл муцина + 0,6 мг/мл альгината в 0,05 М NaCl. Исследуемые гели состояли из 18 мг/мл муцина + 0,6 мг/мл альгината + 4 мг/мл исследуемых веществ в 0,05 М NaCl. Определение реологических характеристик Загущение: непосредственно после перемешивания образец помещали в реометр при температуре 37 С. Температуру понижали до 10 С (0,5 градус/мин), а затем выдерживали при температуре 10 С в течение 18 ч. Характер изменений образца и образование геля измеряли постоянно. Развертка по частоте: после загущения температуру образца повышали до 37 С и мониторировали характер реологических изменений как функцию частоты.-3 015436 Развертка по давлению: при температуре 37 С мониторировали характер изменений геля как функцию возрастающего приложенного давления. Загущение Исследования показали, что олигомеры гулуроната натрия (G-блоки) способны замещать альгинат во взаимодействиях муцин-альгинат, что выражается в снижении комплексного модуля геля (G) во времени после начального загущения. Эти данные для пяти исследуемых гелей и контрольного геля представлены на фиг. 1 а-1 е соответственно. Среди других исследованных олигомерных веществ только олигомеры галактуроната натрия обладали похожим действием, демонстрируя снижение значений модулей во времени. Другие вещества(ДНК, PEG, декстран) вызывали замедление загущения, но образование геля продолжалось во времени,что отражено повышением комплексного модуля. Комплексный модуль и угол сдвига фаз гелей в конце периода загущения отображены графически на фиг. 2 и 3. Комплексный модуль представляет собой показатель общего ответа или силы системы, а угол сдвига фаз имеет отношение к балансу между жидкоподобным (liquid like) и твердоподобным (solidlike) характером изменений, где больший угол сдвига фаз указывает на преобладание жидкоподобного характера изменений. Олигомеры гулуроната натрия (G-блоки) вызывали наибольшее снижение G и наибольшее увеличение угла сдвига фаз. Характер изменений геля при развертке по частоте Все гели демонстрировали типичный для слабо вязкоупругих гелей характер изменений при развертке по частоте. Напряжение пластического течения при развертке по давлению Развертку по давлению использовали для определения давления, необходимого для того, чтобы вызвать течение в системе. Эти данные отображены графически на фиг. 4 в виде % от давления, необходимого для того, чтобы вызвать течение в контрольном геле. Эти данные дают указание на то, насколько добавленное вещество ослабило матрицу геля. Наиболее ярко выраженным действием на напряжение пластического течения обладали G-блоки (олигомеры гулуроната натрия), за которыми следовали олигомеры галактуроната натрия. Пример 2. Действие на мокроту. Образцы мокроты получили от пациентов, страдающих муковисцидозом, с достоверным диагнозом инфицирования Pseudomonas aeruginosa. Образцы осторожно перемешивали, разделяли на порции, замораживали и хранили при температуре -40 С. Методика предварительного исследования За один час до исследования образцы мокроты извлекали из морозильной камеры и помещали в холодильник (температура 4 С), перемешивали с использованием магнитной мешалки в течение 10 мин и разделяли на порции по 0,5 г. Ко всем образцам кроме одного, образца мокроты без добавок, добавили исследуемые среды. Итоговые образцы были следующими:A) 0,5 г мокроты (без добавок); Б) 0,5 г мокроты + 65 мкл 350 мМ раствора NaCl (ионная сила добавленного олигомера гулуроната);B) 0,5 г мокроты + 75 мкл олигомеров гулуроната натрия с Dp19 в концентрации 150 мг/мл; Г) 0,5 г мокроты + 75 мкл олигомеров гулуроната натрия с Dp10 в концентрации 150 мг/мл. Олигомер гулуроната натрия с Dp10 (Dp - степень полимеризации) имел следующие характеристики: FG 0,79, FM 0,11, FGG 0,76, FGM=FMG 0,03, FMM 0,07, FMGG=FGGM 0,02, FMGM 0,01, FGGG 0,74, FG(red) 0,10,FG(tot) 0,89, NG1 37, DP 10. После смешивания образцы осторожно перемешивали в течение 1 мин и затем, перед перемещением в реометр для исследования, помещали на 5 мин в холодильник. Определение реологических характеристик Определение реологических характеристик мокроты без добавок и после смешивания проводили на пластине/конусе (40 мм/1) с использованием универсального реометра Rheologica Stress-Tech при температуре 10 С для минимизации действия протеолитических ферментов. Определение реологических характеристик мокроты без добавок и мокроты после смешивания с исследуемыми средами проводили в четыре различные стадии: контроль напряжения колебаний в течение 2 мин при постоянном напряжении 0,03 и частоте 1 Гц. контроль напряжения колебаний после предварительного сдвига (1 минута при уровне сдвига 20 с-1) в течение 60 мин при постоянном напряжении 0,03 и частоте 1 Гц,развертка по частоте с диапазоном от 0,01 до 5 Гц при постоянном напряжении 0,03,развертка по давлению в диапазоне от 0,02 до 20 Па при частоте 1 Гц. На фиг. 5 а представлена столбиковая диаграмма, отражающая комплексный модуль (G) для образцов мокроты в конце исследования спустя 60 мин. На фиг. 5 б представлена столбиковая диаграмма, отражающая данные тех же самых образцов мокроты, что и на фиг. 5 а, но в виде процента от контрольного образца (мокрота без примесей). На фиг. 5 в-5 е представлены графики комплексного модуля во времени для образцов мокроты с А-4 015436 по Г. На фиг. 6 а представлена столбиковая диаграмма, отражающая комплексную вязкостьобразцов мокроты в конце исследования спустя 60 минут. На фиг. 6 б представлена столбиковая диаграмма, отражающая данные тех же самых образцов мокроты, что и на фиг. 6 а, но в виде процента от контрольного образца. На фиг. 7 а представлена столбиковая диаграмма, отражающая угол сдвига фазобразцов мокроты в конце исследования спустя 60 минут. На фиг. 7 б представлена столбиковая диаграмма, отражающая данные тех же самых образцов мокроты, что и на фиг. 3 а, но в виде процента от контрольного образца. Добавление олигомеров гулуроната заметно снижает механические свойства мокроты пациентов сCF ex vivo. Значительно снижены как комплексный динамический модуль, так и комплексная динамическая вязкость, в некоторых случаях до коэффициента 5. Образец с Dp 10 представляется более эффективным, чем образец со средней Dp 19. Результаты, полученные при приготовлении образцов мокроты как описано, также дают возможность предполагать, что мокрота пациентов с CF приобретает равновесноподобные механические свойства быстрее при наличии G-блоков с Dp10 по сравнению с наличием других компонентов (G инезависимы от времени). Однако действие на изменение угла сдвига фаз выражено не в такой степени, как на G и . Это наиболее важно, поскольку отчетливо свидетельствует о том, что механические свойства сетчатой структуры муцина сохранены, и, следовательно, он попрежнему способен функционировать как первая линия защиты против загрязняющих агентов, взвешенных в воздухе. Пример 3. Аэрозоль. Стерильный распыляемый аэрозоль, вводимый с помощью небулайзера, получают из жидкости, содержащей 3-10% натриевой соли блока гулуроновой кислоты с гулуронатом чистотой по меньшей мере 75% и степенью полимеризации между 5 и 20 и, если необходимо, поверхностно-активное соединение для стабилизации размера капель аэрозоля. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ лечения человека или субъекта, не являющегося человеком, для борьбы с повышенной вязкостью слизи в дыхательных путях, включающий нанесение на поверхность слизистой оболочки указанных путей путем введения в дыхательные пути указанного субъекта эффективного количества физиологически приемлемого олигоуроната, где указанный олигоуронат происходит из природного источника. 2. Способ по п.1, где указанный олигоуронат происходит из природного альгинатного источника. 3. Способ по п.1 или 2, где указанный олигоуронат содержит гулуроновую кислоту в виде мономера. 4. Способ по любому из пп.1-3, где указанный олигоуронат представляет собой 4-25-мер. 5. Способ по любому из пп.1-4 для лечения муковисцидоза. 6. Способ по любому из пп.1-4 для лечения синусита. 7. Способ по любому из пп.1-4 для лечения хронических обструктивных заболеваний легких. 8. Применение физиологически приемлемого олигоуроната, как он определен в любом из пп.1-4,для изготовления лекарственного средства, пригодного для ингаляционного введения, для применения в лечении повышенной вязкости слизи в дыхательных путях. 9. Применение по п.8 для изготовления лекарственного средства, пригодного для ингаляционного введения, для применения в лечении муковисцидоза. 10. Применение по п.8 для изготовления лекарственного средства, пригодного для ингаляционного введения, для применения в лечении синусита. 11. Применение по п.8 для изготовления лекарственного средства, пригодного для ингаляционного введения, для применения в лечении хронических обструктивных заболеваний легких. 12. Фармацевтическая композиция, пригодная для ингаляционного введения, содержащая физиологически приемлемый олигоуронат вместе с физиологически приемлемым носителем или эксципиентом,где указанный олигоуронат представляет собой 3-25-мер и происходит из природного источника. 13. Композиция по п.12, содержащая дополнительный физиологически приемлемый агент, уменьшающий вязкость слизи. 14. Композиция по п.12 или 13, содержащая олигоуронат, который содержит гулуроновую кислоту в виде мономера. 15. Композиция по любому из пп.12-14, содержащая ДНКазу. 16. Спрей-аппликатор, включающий емкость и генератор капель, где указанная емкость содержит водный раствор физиологически приемлемого олигоуроната, как он определен в п.3 или 4.
МПК / Метки
МПК: A61K 31/715, A61K 9/12, A61K 45/06, A61P 11/00
Метки: применение, повышенной, лечения, слизи, олигоуронатов, вязкости
Код ссылки
<a href="https://eas.patents.su/11-15436-primenenie-oligouronatov-dlya-lecheniya-povyshennojj-vyazkosti-slizi.html" rel="bookmark" title="База патентов Евразийского Союза">Применение олигоуронатов для лечения повышенной вязкости слизи</a>
Предыдущий патент: Способ моделирования технологических показателей скважин
Следующий патент: Ультразвуковой неразрушающий контроль
Случайный патент: Производные бензимидазола и их применение для лечения вирусных инфекций