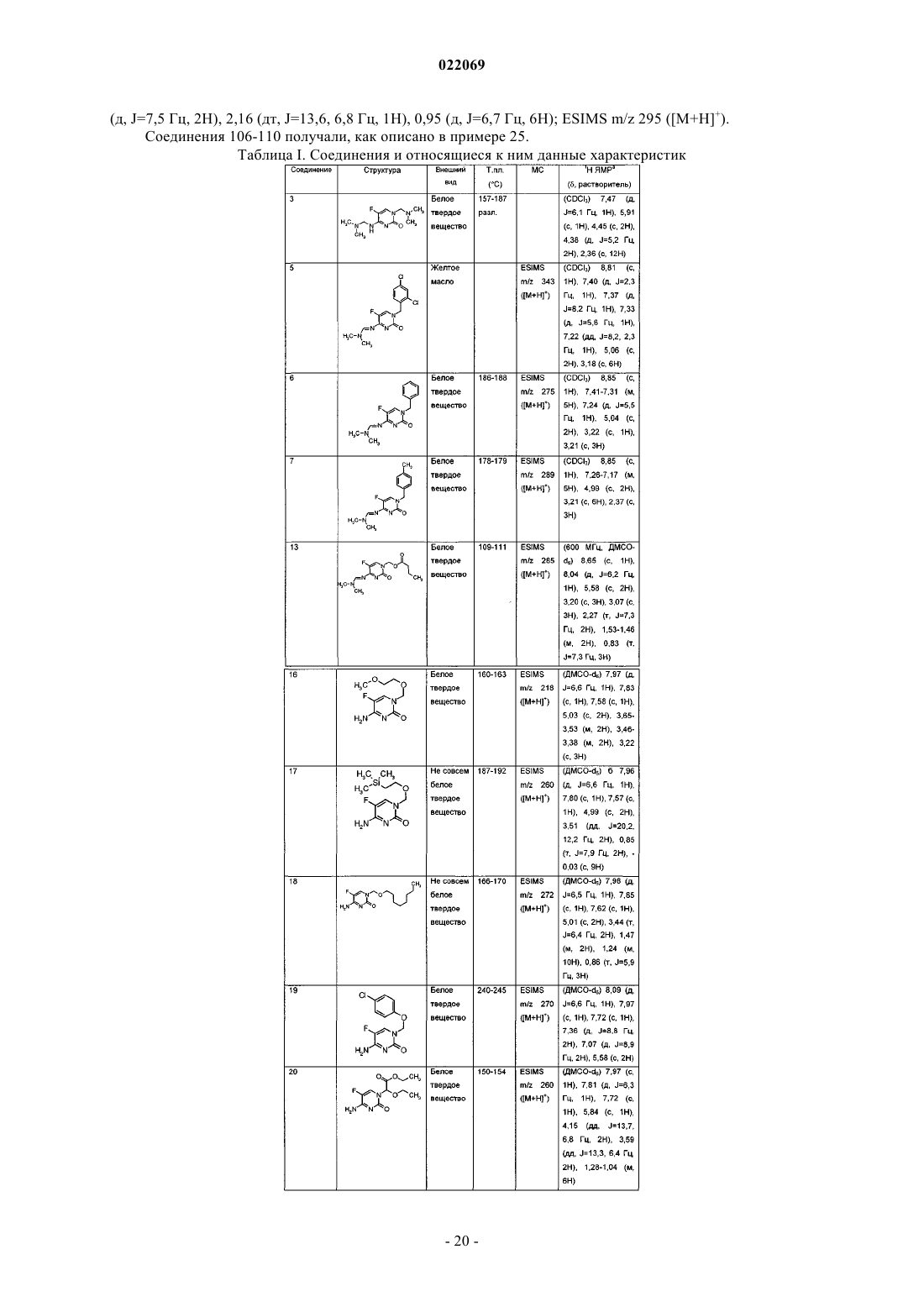
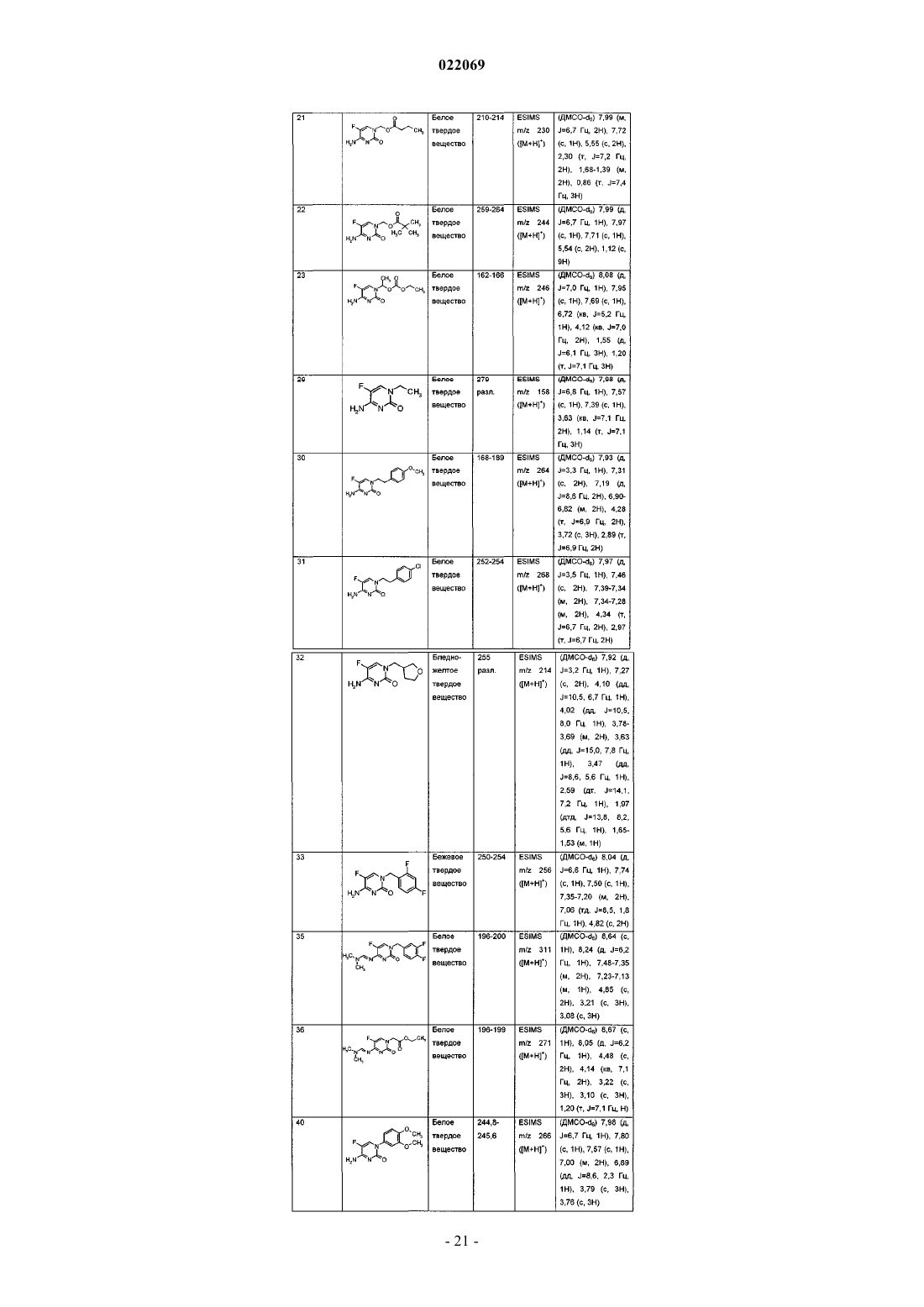
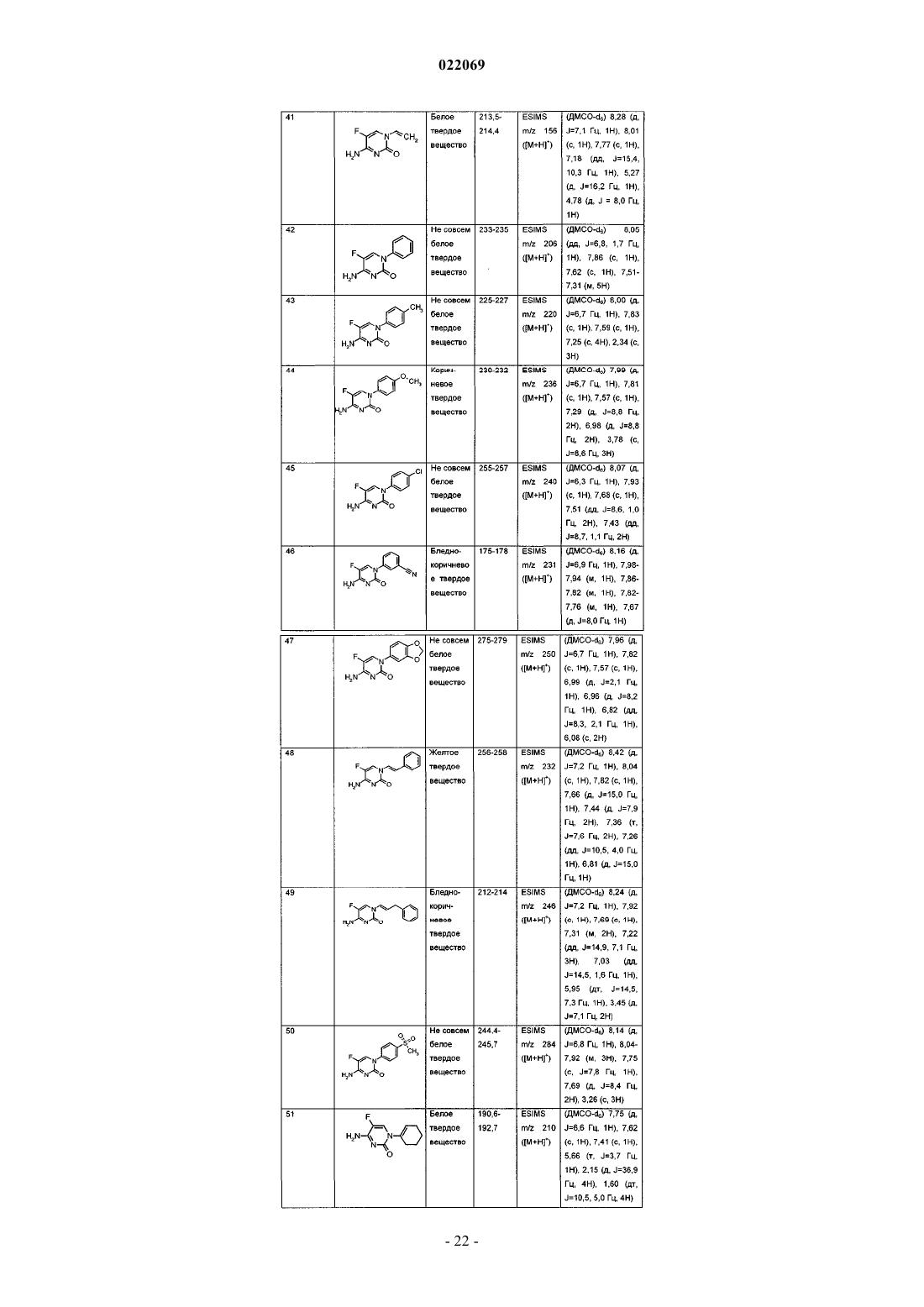
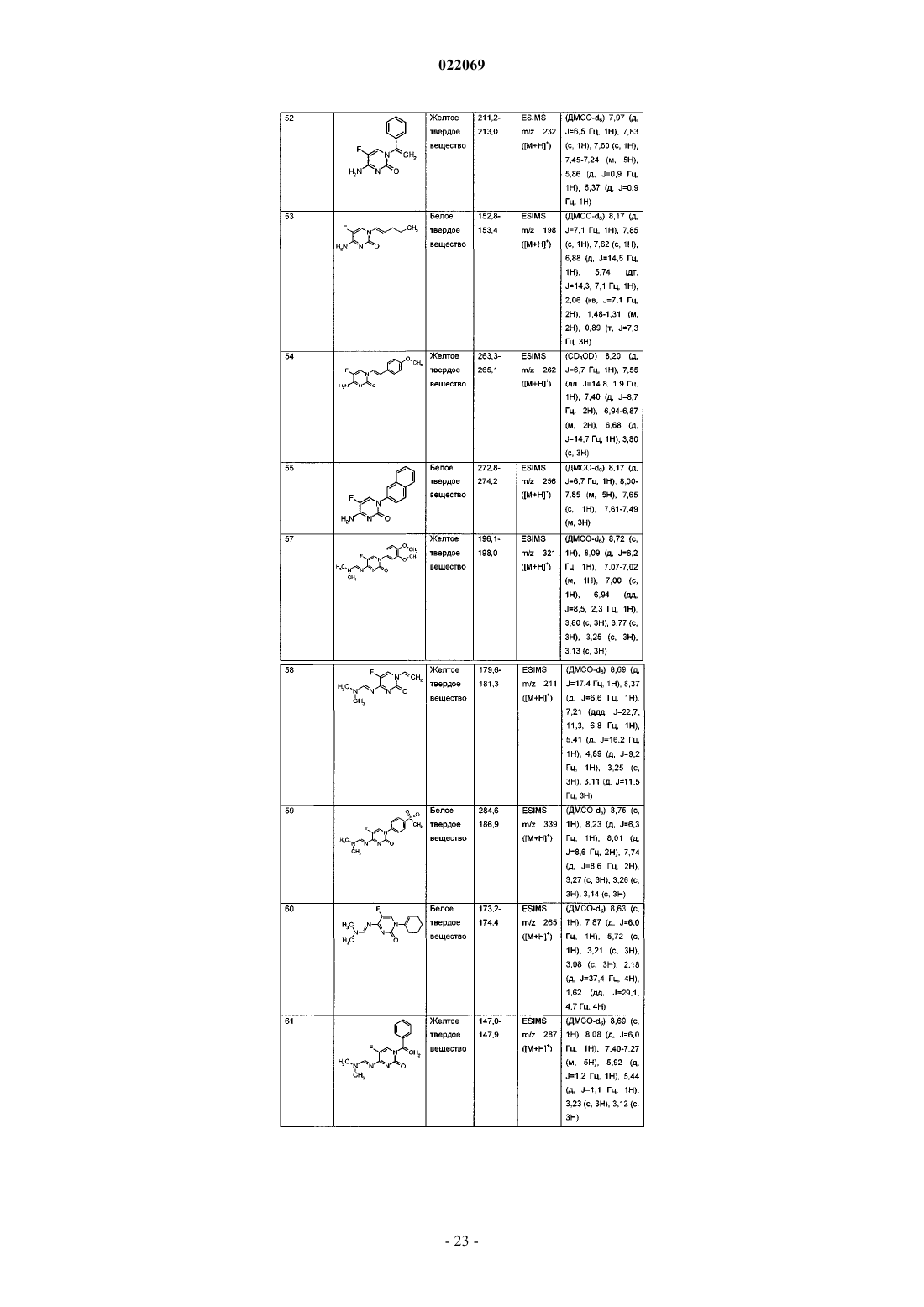
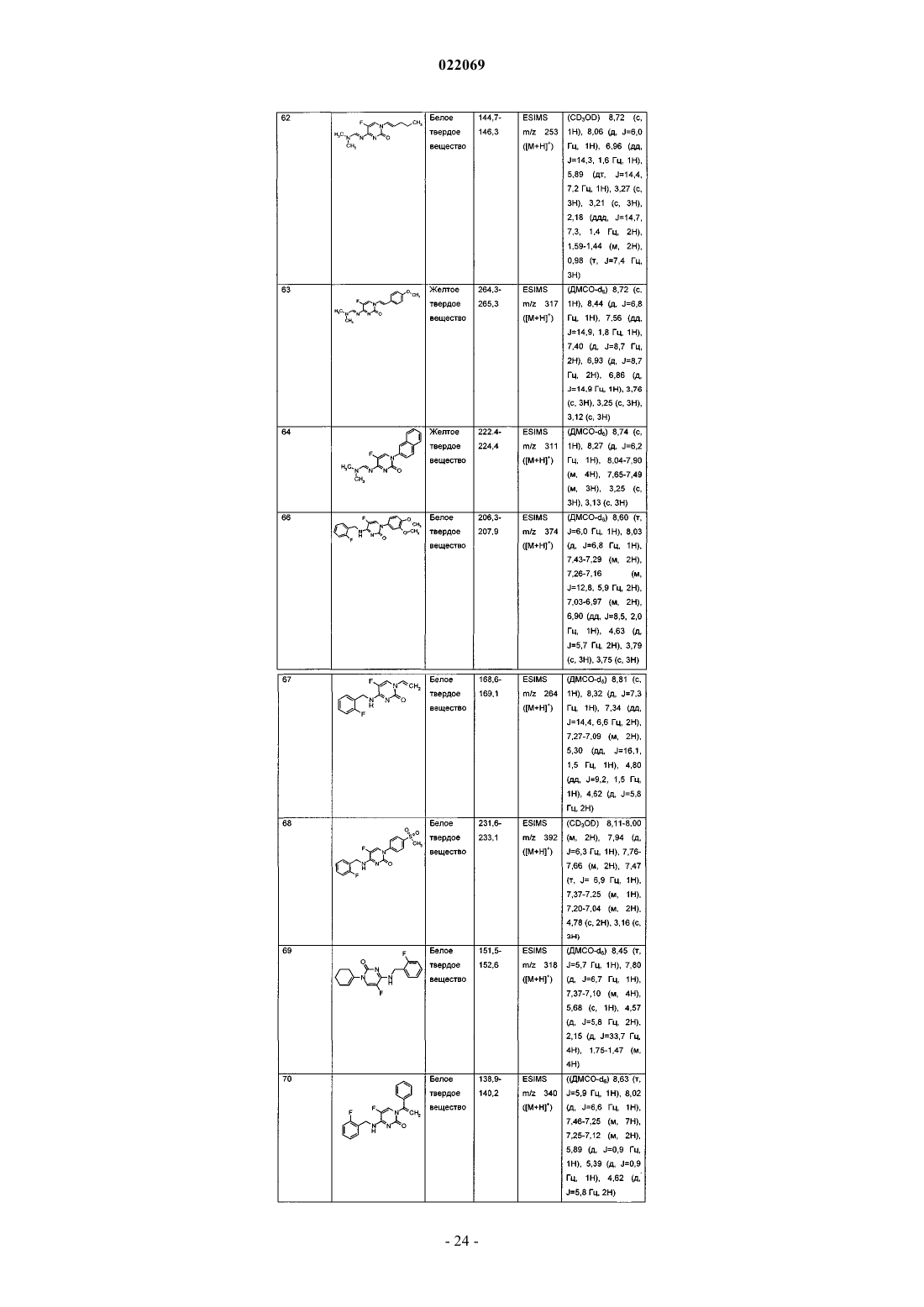
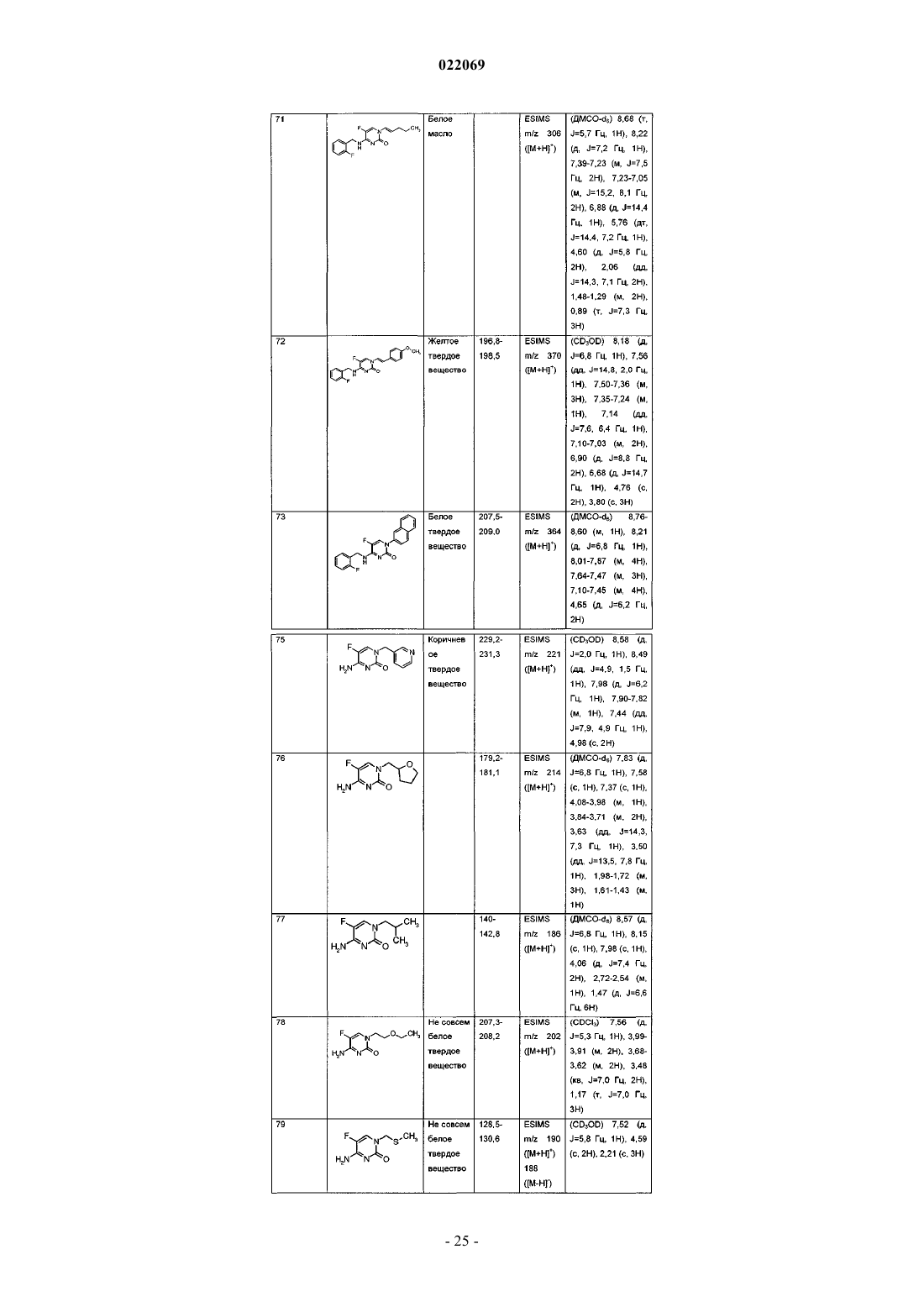
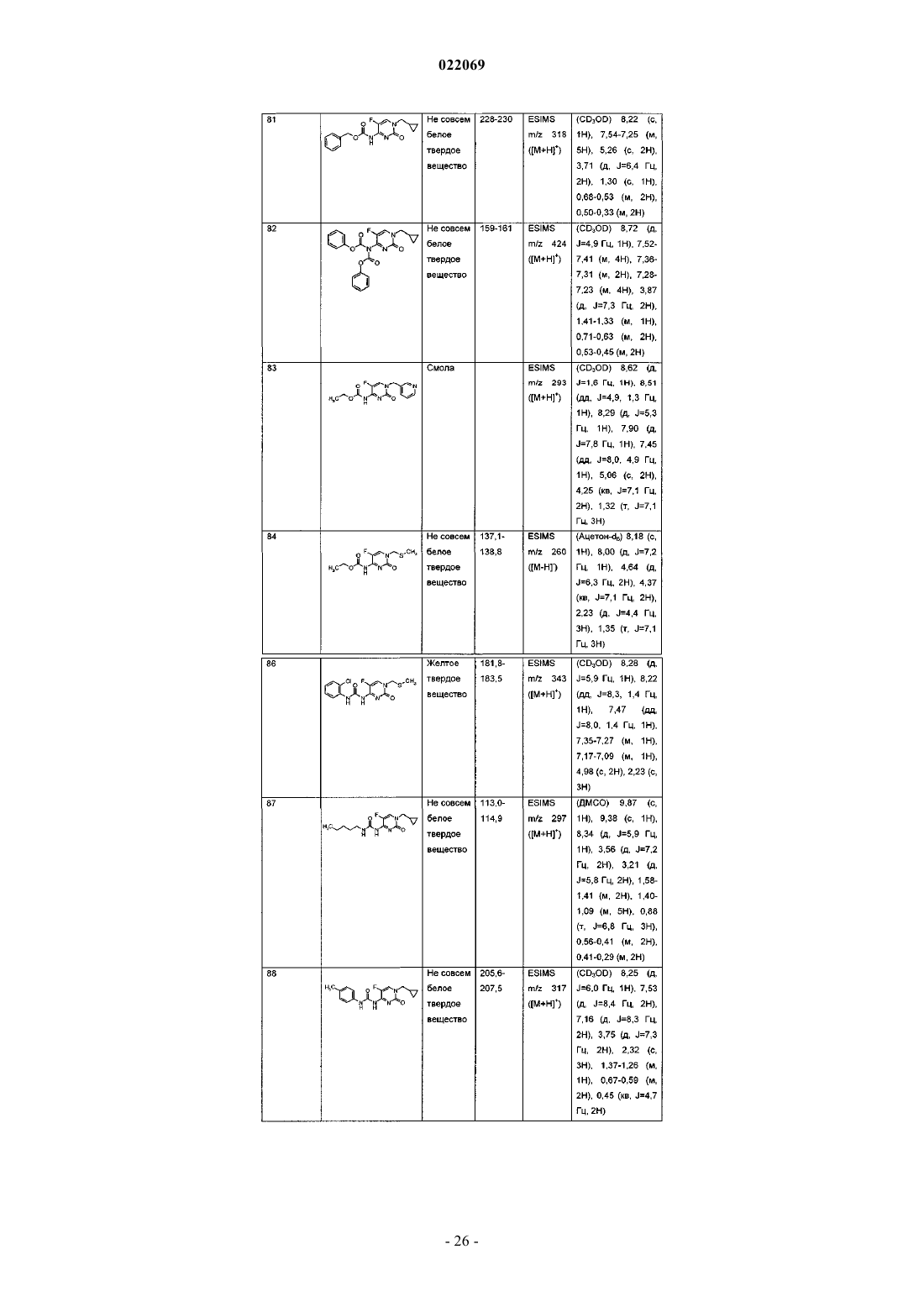
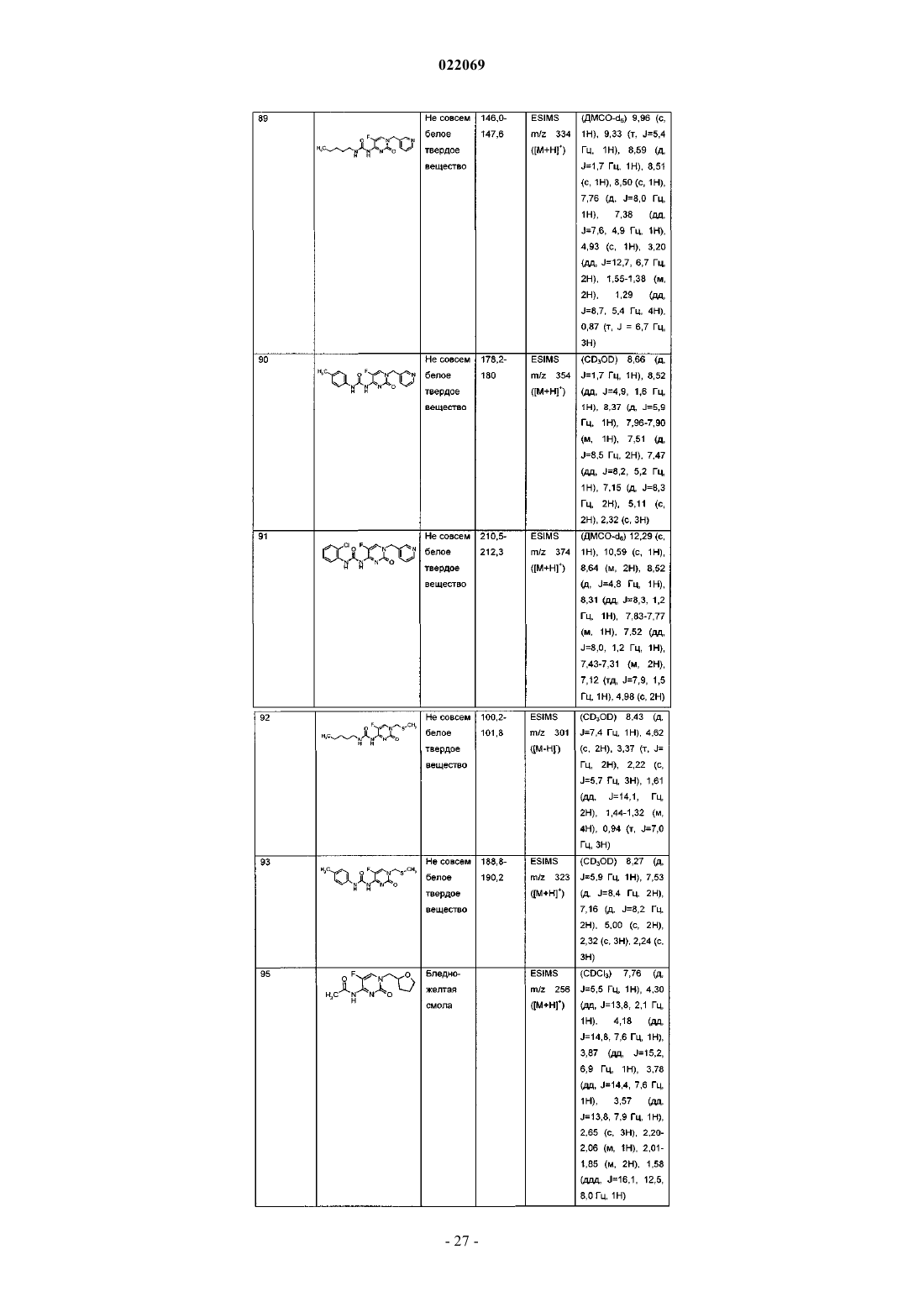
Производные 5-фторпиримидинона и их применение в качестве фунгицидов
Номер патента: 22069
Опубликовано: 30.10.2015
Авторы: Салленбергер Майкл, Оуэн В., Яо Чэнлинь, Вебстер Джеффри, Брайан Кристи, Лорсбах Бет, Мартин Тимоти П., Мейер Кевин, Джонсон Питер, Бебель Тимоти
Формула / Реферат
1. Соединение формулы I
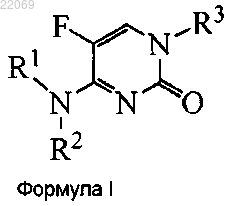
в которой R1 представляет собой Н;
С1-С6алкил, необязательно замещенный 1-3 R4;
фенил или бензил, где каждый из фенила или бензила может быть необязательно замещен 1-3 R5;
-(CHR6)mOR7;
-C(=O)R8;
-S(O)2R8;
-C(=O)OR8;
-(CHR6)mN(R9)R10 или
-C(=O)N(R9)R10;
где m равно целому числу 1-4;
R2 представляет собой Н или С1-С6алкил;
альтернативно R1 и R2 могут быть взяты вместе с образованием =CR11N(R12)R13;
R3 представляет собой С1-С6алкил, необязательно замещенный 1-3 R4, C1-С6галогеналкил, С2-С6алкоксиалкил, С2-С6алкенил, необязательно замещенный R14, фенил или бензил, где каждый из фенила или бензила может быть необязательно замещен 1-3 R5, тиофенила, бензодиоксила или нафтила;
-(CHR6)mOR7;
- (CHR6)mSR8 или
-(CHR6)mN(R9)R10;
R4 представляет собой независимо галоген, С1-С6алкил, C1-С4алкокси, амино, пиридила, тиофенила, триазолила, тетрагидрофуранила, морфолинила или пиперазинила, где пиперазинил может быть необязательно замещен 1-3 R5;
R5 представляет собой независимо галоген, С1-С6алкил, С1-С6алкокси, С1-С6алкилсульфонил или циано;
R6 представляет собой Н, С1-С6алкил;
R7 представляет собой С1-С6алкоксиалкил, С2-С6триалкилсилил, С2-С6триалкилсилилалкил, С2-С6алкилкарбонил, С1-С6алкоксикарбонил, фенил или бензил, где каждый из фенила или бензила может быть необязательно замещен 1-3 R5;
R8 представляет собой С1-С6алкил, фенил или бензил, где каждый из фенила или бензила может быть необязательно замещен 1-3 R5;
R9 представляет собой С1-С6алкил или фенил, где фенил может быть необязательно замещен 1-3 R5;
R10 представляет собой Н или С1-С6алкил;
альтернативно R9 и R10 могут быть взяты вместе с образованием морфолинила или пиперазинила, где пиперазинил может быть необязательно замещен 1-3 R5;
R11 представляет собой Н;
R12 представляет собой C1-С4алкил;
R13 представляет собой С1-С4алкил; и
R14 представляет собой фенил или бензил, где каждый из фенила или бензила может быть необязательно замещен 1-3 R5,
при условии, что данное соединение не представляет собой соединение, где R1 и R2 оба представляют собой Н и R3 представляет собой -CH=CH2, -CH2CH=CHCH2CH3, -CH2CH=С (CH3)2 или -CH3; R1 представляет собой Н и R2 и R3 оба представляют собой -CH3 или -CH2-N(CH3)2, -CH2-N(C2H5)2, -CH2-пирролидинил, -СН2пиридинил, -СН2морфолинил или -СН2метилпиперазинил.
2. Композиция для подавления грибкового патогена, содержащая соединение по п.1 и фитологически приемлемое вещество-носитель.
3. Композиция по п.1, где грибковым патогеном является парша яблок (Venturis inaequalis), пятнистость листьев пшеницы (Septoria tritici, пятнистость листьев сахарной свеклы (Cercospora beticola), пятнистость листьев арахиса (Cercospora arachidicola и Cercosporidium personatum) и черная Sigatoka бананов (Mycosphaerella fijiensis).
4. Способ борьбы с поражением грибами растений и предотвращения поражения грибами растений, включающий нанесение фунгицидно эффективного количества соединения по п.1 на растение, площадь, соседнюю с растением, почву, адаптированную для обеспечения роста растения, корни растения, листву растения и семена, адаптированные для выращивания растения.
5. Соединение по п.1, где
R1 представляет собой -(CHR6)mN(R9)(R10);
R2 представляет собой Н или метил;
R3 представляет собой -(CHR6)mN(R9)(R10);
R6 представляет собой метил;
m равно 1 и
R9 представляет собой Н;
R10 независимо представляет собой Н или метил.
6. Соединение по п.5, где соединение представляет собой
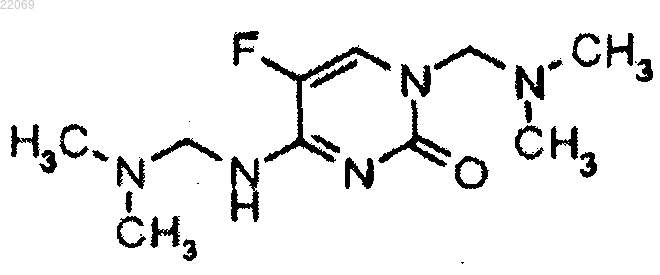
7. Соединение по п.1, где R3 выбран из группы, состоящей из -CH2-N(CH3)2, -CH2-(4-метил 1-пиперазинил) и -CH2-(4-морфолинил).
8. Соединение по п.1, где R1 выбран из группы, состоящей из -CH2-N(CH3)2, -CH2-(4-метил 1-пиперазинил) и -CH2-(4-морфолинил), и R2 представляет Н.
9. Соединение по п.1, где соединение выбрано из группы, состоящей из
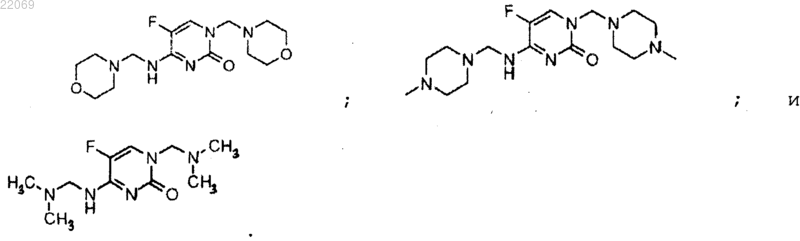
10. Соединение по п.1, где
R1 представляет собой Н;
R2 представляет собой Н и
R3 выбран из группы, состоящей из
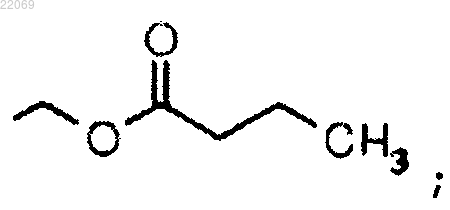
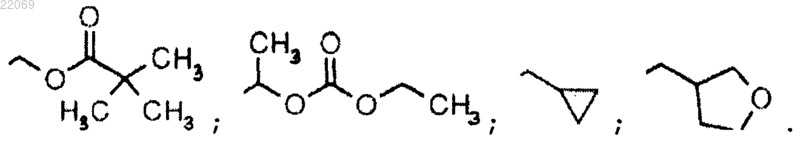
Текст
Настоящее изобретение относится к области 5-фторпиримидинонов и их производных формулы I,где все значения заместителей раскрыты в формуле изобретения, и применению этих соединений в качестве фунгицидов.(71)(73) Заявитель и патентовладелец: ДАУ АГРОСАЙЕНСИЗ ЭлЭлСи (US) Перекрестная ссылка на родственные заявки Данная заявка заявляет приоритет предварительной заявки на патент США с регистрационным 61/232177, зарегистрированной 7 августа 2009 г. Уровень техники и сущность изобретения Фунгициды являются соединениями природного или синтетического происхождения, которые действуют, защищая и/или устраняя повреждения растений, вызванные грибами. Обычно один фунгицид не является применимым во всех случаях. Поэтому продолжают исследования с целью получения фунгицидов, которые могут иметь лучшую эффективность, более просты в применении и имеют меньшую цену. Настоящее описание относится к производным 5-фторпиримидинона и их применению в качестве фунгицидов. Соединения настоящего описания могут обеспечить защиту от аскомицетов, базидиомицетов, дейтеромицетов и оомицетов. Один вариант осуществления настоящего изобретения может включать соединения формулы I в которой R1 представляет собой Н; С 1-С 6 алкил, необязательно замещенный 1-3 R4; С 1-С 6 алкенил,необязательно замещенный 1-3 R4; С 3-С 6 алкинил, необязательно замещенный 1-3 R4; фенил или бензил,где каждый из фенила и бензила может быть необязательно замещен 1-3 R5 или 5- или 6-членным насыщенным или ненасыщенным циклом, или конденсированной системой 5-6-членных колец, или конденсированной системой 6-6-членных колец, причем каждая система содержит 1-3 гетероатома, где каждое кольцо может быть необязательно замещено 1-3 R5, бифенил или нафтил, необязательно замещенный 1-3-C(=S)N(R9)R10; где m равно целому числу 1-4;R2 представляет собой Н или С 1-С 6 алкил, необязательно замещенный R4; альтернативно R1 и R2 могут быть взяты вместе с образованием =CR11N(R12)R13;R14, С 2-С 6 галогеналкенил, С 3-С 6 алкинил, фенил или бензил, где каждый из фенила или бензила может быть необязательно замещен 1-3 R5 или 5- или 6-членным насыщенным или ненасыщенным циклом, или конденсированной системой 5-6-членных колец, или конденсированной системой 6-6-членных колец,причем каждая система содержит 1-3 гетероатома, где каждое кольцо может быть необязательно замещено 1-3 R5, бифенил или нафтил, необязательно замещенный 1-3 R5;R4 представляет собой независимо галоген, С 1-С 6 алкил, С 1-С 4 галогеналкил, С 1-С 4 алкокси, С 1-С 4 галогеналкокси, С 1-С 4 алкилтио, С 1-С 4 галогеналкилтио, амино, галогентио, С 1-С 3 алкиламино, C2-С 6 алкоксикарбонил, С 2-С 6 алкилкарбонил, С 2-С 6 алкиламинокарбонил, гидроксил, С 3-С 6 триалкилсилил, фенил,необязательно замещенный 1-3 R5 или 5- или 6-членным насыщенным или ненасыщенным кольцом, содержащим 1-3 гетероатома, где каждое кольцо может быть необязательно замещено 1-3 R5;R5 представляет собой независимо галоген, С 1-С 6 алкил, С 1-С 6 галогеналкил, С 1-С 6 алкокси, С 1-С 6 галогеналкокси, С 1-С 6 алкилтио, С 1-С 6 галогеналкилтио, галогентио, амино, С 1-С 6 алкиламино, С 2-С 6 диалкиламино, С 2-С 6 алкоксикарбонил, С 2-С 6 алкилкарбонил, С 1-С 6 алкилсульфонил, нитро, гидроксил или циано;R6 представляет собой Н, С 1-С 6 алкил, С 1-С 6 алкокси, С 1-С 6 алкоксикарбонил, фенил или бензил, где каждый из фенила или бензила может быть необязательно замещен 1-3 R5;R7 представляет собой Н, С 1-С 8 алкил, С 2-С 6 алкенил, С 3-С 6 алкинил, С 1-С 6 галогеналкил, С 1-С 6 алкоксиалкил, С 2-С 6 триалкилсилил, С 2-С 6 триалкилсилилалкил, С 2-С 6 алкилкарбонил, С 1-С 6 алкоксикарбонил,фенил или бензил, где каждый из фенила или бензила может быть необязательно замещен 1-3 R5 или 5-1 022069 или 6-членным насыщенным или ненасыщенным циклом, или конденсированной системой 5-6-членных колец, или конденсированной системой 6-6-членных колец, причем каждая система содержит 1-3 гетероатома, где каждое кольцо может быть необязательно замещено 1-3 R5, бифенил или нафтил, необязательно замещенный 1-3 R5;R8 представляет собой Н, С 1-С 6 алкил, С 2-С 6 алкенил, С 3-С 6 алкинил, С 1-С 6 галогеналкил, С 1-С 6 алкоксиалкил, фенил или бензил, где каждый из фенила или бензила может быть необязательно замещен 1-3R5 или 5- или 6-членным насыщенным или ненасыщенным циклом, или конденсированной системой 5-6 членных колец, или конденсированной системой 6-6-членных колец, причем каждая система содержит 13 гетероатома, где каждое кольцо может быть необязательно замещено 1-3 R5, бифенил или нафтил, необязательно замещенный 1-3 R5;R9 представляет собой Н, С 1-С 6 алкил, С 1-С 6 галогеналкил, С 1-С 6 алкоксиалкил, С 2-С 6 алкоксикарбонил, фенил или бензил, где каждый из фенила или бензила может быть необязательно замещен 1-3 R5 или системой 5- или 6-членных насыщенных или ненасыщенных колец, или конденсированной системой 5-6-членных колец, или конденсированной системой 6-6-членных колец, причем каждая система содержит 1-3 гетероатома, где каждое кольцо может быть необязательно замещено 1-3 R5, бифенил или нафтил, необязательно замещенный 1-3 R5;R10 представляет собой Н, С 1-С 6 алкил, С 1-С 6 галогеналкил, С 1-С 6 алкоксиалкил, С 2-С 6 алкилкарбонил или бензил, где бензил может быть необязательно замещен 1-3 R5; альтернативно R9 и R10 могут быть взяты вместе с образованием 5- или 6-членного насыщенного или ненасыщенного кольца, содержащего 1-3 гетероатома, где каждое кольцо может быть необязательно замещено 1-3 R5;R12 представляет собой Н, циано, гидроксил, С 1-С 4 алкил, С 1-С 6 алкокси, С 2-С 6 алкилкарбонил, фенил или бензил, где каждый из фенила или бензила может быть необязательно замещен 1-3 R5 или 5- или 6 членным насыщенным или ненасыщенным циклом, или конденсированной системой 5-6-членных колец,или конденсированной системой 6-6-членных колец, причем каждая система содержит 1-3 гетероатома,где каждое кольцо может быть необязательно замещено 1-3 R5; бифенил или нафтил, необязательно замещенный 1-3 R5; альтернативно R11 и R12 могут быть взяты вместе с образованием 5- или 6-членного насыщенного или ненасыщенного кольца, содержащего 1-3 гетероатома, где каждое кольцо может быть необязательно замещено 1-3 R5;R13 представляет собой Н, С 1-С 4 алкил, С 1-С 6 алкокси, С 2-С 6 алкилкарбонил, фенил или бензил, где каждый из фенила или бензила может быть необязательно замещен 1-3 R5 или 5- или 6-членным насыщенным или ненасыщенным циклом, или конденсированной системой 5-6-членных колец, или конденсированной системой 6-6-членных колец, причем каждая система содержит 1-3 гетероатома, где каждое кольцо может быть необязательно замещено 1-3 R5, бифенил или нафтил, необязательно замещенный 1-3R5; и альтернативно R12 и R13 могут быть взяты вместе с образованием 5- или 6-членного насыщенного или ненасыщенного кольца, содержащего 1-3 гетероатома, где каждое кольцо может быть необязательно замещено 1-3 R5.R14 представляет собой фенил или бензил, где каждый из фенила или бензила может быть необязательно замещен 1-3 R5. Другой вариант осуществления настоящего описания может включать фунгицидную композицию для борьбы с поражением грибами или для предотвращения поражения грибами, содержащую описанные ниже соединения и фитологически приемлемое вещество-носитель. Еще другой вариант осуществления настоящего описания может включать способ борьбы с поражением грибами или предотвращения поражения грибами растений, причем способ включает стадии нанесения фунгицидно эффективного количества одного или нескольких описанных ниже соединений по меньшей мере на один из грибов, растение, площадь, соседнюю с растением, и семена, применимые для получения растения. Термин "алкил" относится к неразветвленной, разветвленной и циклической углеродной цепи,включающей метил, этил, пропил, бутил, изопропил, изобутил, третичный бутил, пентил, гексил, циклопропил, циклобутил, циклопентил, циклогексил и тому подобное. Термин "алкенил" относится к неразветвленной, разветвленной и циклической углеродной цепи,содержащей одну или несколько двойных связей и включающей этенил, пропенил, бутенил, изопропенил, изобутенил, циклогексенил и тому подобное. Термин "алкинил" относится к неразветвленной или разветвленной углеродной цепи, содержащей одну или несколько тройных связей и включающей пропинил, бутинил и тому подобное. Применяемое на всем протяжении данного описания обозначение "R" относится к группе, состоящей из С 2-С 6 алкила, С 3-С 8 алкенила или С 3-С 8 алкинила, если не указывается иначе. Термин "алкокси" относится к заместителю -OR. Термин "алкоксикарбонил" относится к заместителю -C(O)-OR. Термин "алкилкарбонил" относится к заместителю -C(O)-R. Термин "алкилсульфонил" относится к заместителю -SO2-R. Термин "галогеналкилсульфонил" относится к заместителю -SO2-R, у которого R полностью или частично замещен Cl, F, I или Br или любой их комбинацией. Термин "алкилтио" относится к заместителю -S-R. Термин "галогеналкилтио" относится к алкилтио, который замещен Cl, F, I или Br или любой их комбинацией. Термин "галогентио" относится к сере, замещенной от трех до пяти заместителями F. Термин "алкиламинокарбонил" относится к заместителю -C(O)-N(H)-R. Термин "диалкиламинокарбонил" относится к заместителю -C(O)-NR2. Термин "алкилциклоалкиламино" относится к заместителю циклоалкиламино, который замещен алкильной группой. Термин "триалкилсилил" относится к -SiR3. Термин "циано" относится к заместителю -CN. Термин "гидроксил" относится к заместителю -ОН. Термин "амино" относится к заместителю -NH2. Термин "алкиламино" относится к заместителю -N(H)-R. Термин "диалкиламино" относится к заместителю -NR2. Термин "триалкилсилилалкил" относится к заместителю -SiR3 у алкила. Термин "алкоксиалкокси" относится к -О(CH2)nO(CH2)mCH3, где n равно целому числу 1-3 и m равно 0-2. Термин "алкоксиалкил" относится к алкоксизамещению у алкила. Термин "галогеналкоксиалкил" относится к алкоксизамещению алкила, который полностью или частично замещен Cl, F, Br или I или любой их комбинацией. Термин "гидроксиалкил" относится к алкилу, который замещен гидроксильной группой. Термин "галогеналкокси" относится к заместителю -OR-X, у которого X представляет собой Cl, F,Br или I или любую их комбинацию. Термин "галогеналкил" относится к алкилу, который замещен Cl, F, I или Br или любой их комбинацией. Термин "галогеналкенил" относится к алкенилу, который замещен Cl, F, I или Br или любой их комбинацией. Термин "галогеналкинил" относится к алкинилу, который замещен Cl, F, I или Br или любой их комбинацией. Термин "галоген" или "гало" относится к одному или нескольким атомам галогена, определенным как F, Cl, Br и I. Термин "гидроксикарбонил" относится к заместителю -C(O)-OH. Термин "нитро" относится к заместителю -NO2. На протяжении всего описания ссылка на соединения формулы I означает также, что включаются оптические изомеры и соли формулы I и их гидраты. Конкретно, когда соединения формулы I содержат алкильную группу с разветвленной цепью, предполагается, что такие соединения включают оптические изомеры и их рацематы. Примеры солей включают гидрохлорид, гидробромид, гидроиодид и тому подобное. Кроме того, соединения формулы I могут включать таутомерные формы. Некоторые соединения, описанные в данном документе, могут существовать в виде одного или нескольких изомеров. Специалисту в данной области должно быть понятно, что один изомер может быть более активным, чем другие. Структуры, описанные в настоящем описании, для ясности показаны только в виде одной геометрической формы, но предполагается, что они представляют все геометрические и таутомерные формы молекулы. Специалисту в данной области понятно также, что, если не указано иначе, допустимо дополнительное замещение, если удовлетворяются правила химического связывания и энергии напряжения. Другим вариантом осуществления настоящего описания является применение соединения формулыI для защиты растения от поражения фитопатогенным организмом или обработки растения, зараженного фитопатогенным организмом, содержащее нанесение соединения формулы I или композиции, содержащей такое соединение, на почву, растение, часть растения, листву и/или семена. Кроме того, другим вариантом осуществления настоящего описания является композиция, применимая для защиты растения от поражения фитопатогенным организмом и/или обработки растения, пораженного фитопатогенным организмом, содержащая соединение формулы I и фитологически приемлемое вещество-носитель. Дополнительные отличительные признаки и преимущества настоящего изобретения станут очевидны специалисту в данной области при рассмотрении нижеследующего подробного описания иллюстративных вариантов осуществления, иллюстрирующих лучший вариант осуществления изобретения, в том виде, в котором он воспринимается в настоящее время. Подробное описание изобретения Соединения настоящего изобретения можно применять любым из различных известных способов,либо в виде соединений как таковых, либо в виде препаратов, содержащих соединения. Например, соединения можно наносить на корни, семена или листву растений для борьбы с различными грибами без нанесения ущерба коммерческой ценности растений. Препараты можно наносить в форме любого из обычно применяемых типов препаратов, например в виде растворов, дустов, смачиваемых порошков,текучих концентратов или эмульгируемых концентратов. Соединения настоящего описания предпочтительно наносят в форме препарата, содержащего одно или несколько соединений формулы I с фитологически приемлемым носителем. Концентрированные препараты можно диспергировать в воде или других жидкостях для нанесения на объект обработки или препараты могут быть подобными дусту или гранулированными, которые затем можно наносить без дополнительной обработки. Препараты можно получать согласно процедурам, которые являются обычными в сельскохозяйственной химической области. Настоящее изобретение рассматривает все наполнители, при помощи которых из одного или нескольких соединений можно получать препарат для доставки и применения его в качестве фунгицида. Обычно препараты применяют в виде водных суспензий или эмульсий. Такие суспензии или эмульсии можно получать из водорастворимых, диспергируемых или эмульгируемых в воде препаратов, которые являются твердыми веществами, обычно известными как смачиваемые порошки; или жидкостями, обычно известными как эмульгируемые концентраты, водные суспензии или концентраты суспензий. Как может быть легко понятно, можно применять любое вещество, к которому можно добавить эти соединения, при условии, что оно обеспечивает требуемую пригодность, без значительного отрицательного влияния на активность этих соединений в качестве противогрибковых агентов. Смачиваемые порошки, которые можно прессовать с образованием диспергируемых в воде гранул,содержат тесную смесь одного или нескольких соединений формулы I, инертного носителя и поверхностно-активных веществ. Концентрация соединения в смачиваемом порошке может быть от приблизительно 10 до приблизительно 90 мас.% в расчете на общую массу смачиваемого порошка, более предпочтительно от приблизительно 25 до приблизительно 75 мас.%. При получении препаратов в виде смачиваемых порошков соединения можно смешивать с тонкоизмельченным твердым веществом, таким как профиллит, тальк, мел, гипс, фуллерова земля, бентонит, аттапульгит, крахмал, казеин, глютен, монтмориллонитовые глины, диатомовые земли, очищенные силикаты или тому подобное. При таких операциях мелкоизмельченный носитель и поверхностно-активные вещества обычно смешивают с соединением(ями) и размалывают. Эмульгируемые концентраты соединений формулы I могут содержать подходящую концентрацию,такую как от приблизительно 10 до приблизительно 50 мас.% соединения в подходящей жидкости, в расчете на общую массу концентрата. Соединения можно растворять в инертном носителе, который является либо смешиваемым с водой растворителем, либо смесью не смешиваемых с водой органических растворителей и эмульгаторов. Концентраты можно разбавить водой и маслом для получения смесей для опрыскивания в форме эмульсий типа масло-в-воде. Применимые органические растворители включают ароматические соединения, особенно высококипящие нафталиновые и олефиновые составляющие нефти,такие как тяжелая ароматическая нафта. Можно также применять другие органические растворители,например терпеновые растворители, включающие производные канифоли, алифатические кетоны, такие как циклогексанон, и "комплексные" спирты, такие как 2-этоксиэтанол. Эмульгаторы, которые можно преимущественно применять в изобретении, может легко определить специалист в данной области, они включают различные неионогенные, анионогенные, катионогенные и амфотерные эмульгаторы или смесь двух или более эмульгаторов. Примеры неионогенных эмульгаторов, применимых при получении эмульгируемых концентратов, включают полиалкиленгликолевые простые эфиры и продукты конденсации алкил- и арилфенолов, алифатических спиртов, алифатических аминов или жирных кислот с этиленоксидом, пропиленоксидом, такие как этоксилированные алкилфенолы и эфиры карбоновых кислот, солюбилизированные полиолом или полиоксиалкиленом. Катионогенные эмульгаторы включают четвертичные аммониевые соединения и соли аминов жирного ряда. Анионогенные эмульгаторы включают растворимые в масле соли (например, кальция) алкиларилсульфоновых кислот, растворимые в масле соли или сульфатированные полигликолевые простые эфиры и подходящие соли фосфатированного полигликолевого простого эфира. Репрезентативными органическими жидкостями, которые можно применять при получении эмульгируемых концентратов соединений настоящего изобретения, являются ароматические жидкости, такие как ксилол, фракции пропилбензола; или смешанные нафталиновые фракции, минеральные масла, замещенные ароматические органические жидкости, такие как диоктилфталат; керосин; диалкиламиды различных жирных кислот, особенно диметиламиды жирных кислот и производные гликолей, такие как нбутиловый эфир, этиловый эфир или метиловый эфир диэтиленгликоля и метиловый эфир триэтиленгликоля и тому подобное. При получении эмульгируемого концентрата можно также применять смеси двух или более органических жидкостей. Органические жидкости включают ксилол и фракции пропилбензола, причем ксилол является наиболее предпочтительным в некоторых случаях. В жидких препаратах обычно применяют поверхностно-активные диспергирующие агенты в количестве от 0,1 до 20 мас.% в расчете на объединенную массу диспергирующего агента с одним или несколькими соединениями. Препараты могут содержать также другие совместимые добавки, например регуляторы роста растений и другие биологически активные соединения, применяемые в сельском хозяйстве. Водные суспензии содержат суспензии одного или нескольких нерастворимых в воде соединений формулы I, диспергированных в водном наполнителе при концентрации в диапазоне от приблизительно 5 до приблизительно 50 мас.% в расчете на общую массу водной суспензии. Суспензии получают тонким измельчением одного или нескольких соединений и энергичным перемешиванием измельченного вещества в наполнителе, состоящем из воды и поверхностно-активных веществ, выбранных из описанных выше некоторых типов. Для повышения плотности и вязкости водного наполнителя можно также добавлять другие компоненты, такие как неорганические соли и синтетические или природные смолы. Часто наиболее эффективным является измельчение и смешивание одновременно с приготовлением водной смеси и гомогенизацией ее в таком устройстве, как песочная мельница, шаровая мельница или гомогенизатор плунжерного типа. Водные эмульсии содержат эмульсии одного или нескольких нерастворимых в воде пестицидноактивных ингредиентов, эмульгированных в водном наполнителе при концентрации обычно в диапазоне от приблизительно 5 до приблизительно 50 мас.% в расчете на общую массу водной эмульсии. Если пестицидно-активный ингредиент является твердым веществом, его нужно растворить в подходящем, не смешиваемом с водой растворителе перед получением водной эмульсии. Эмульсии получают эмульгированием жидкого пестицидно-активного ингредиента или его не смешиваемого с водой раствора в водной среде, обычно с включением поверхностно-активных веществ, которые помогают образованию и стабилизации описываемой выше эмульсии. Это часто выполняют при помощи энергичного перемешивания,обеспечиваемого смесителями с высоким сдвигающим усилием или гомогенизаторами. Соединения формулы I можно также применять в виде гранулированных препаратов, которые являются особенно применимыми для нанесения на почву. Гранулированные препараты обычно содержат от приблизительно 0,5 до приблизительно 10 мас.% в расчете на общую массу гранулированного препарата, соединения(ий), диспергированного в инертном носителе, который состоит целиком из крупнозернистого инертного материала или содержит в качестве большей части такой инертный материал, как аттапульгит, бентонит, диатомит, глина или аналогичное недорогое вещество. Такие препараты обычно получают растворением соединений в подходящем растворителе и нанесением раствора на гранулированный носитель, который был предварительно получен в виде частиц подходящего размера в диапазоне от приблизительно 0,5 до приблизительно 3 мм. Подходящим растворителем является растворитель, в котором соединение растворяется в значительном количестве или растворяется полностью. Такие препараты можно также получать образованием густой массы или пасты носителя и соединения и растворителя и измельчением и сушкой ее для получения требуемых гранулированных частиц. Дусты, содержащие соединения формулы I, можно получить тесным смешиванием одного или нескольких соединений в порошкообразной форме с дустом подходящего сельскохозяйственного носителя,такого как, например, каолиновая глина, измельченная вулканическая порода и тому подобное. Дусты могут в подходящем случае содержать от приблизительно 1 до приблизительно 10 мас.% соединений в расчете на общую массу дуста. Препараты могут дополнительно содержать вспомогательные средства, поверхностно-активные вещества, для повышения отложения соединений на мишени, т.е. сельскохозяйственной культуре и организме, смачивания и проникновения этих соединений в такую мишень. Эти вспомогательные средства,поверхностно-активные вещества, можно необязательно применять в качестве компонента препарата или смеси резервуара. Количество вспомогательного средства, поверхностно-активные вещества, обычно варьирует от 0,01 до 1,0 об.% в расчете на объем воды для разбрызгивания, предпочтительно 0,05-0,5 об.%. Подходящие вспомогательные средства, поверхностно-активные вещества, включают, но не ограничиваются перечисленным, этоксилированные нонилфенолы, этоксилированные синтетические или природные спирты, соли эфиров сульфоянтарных кислот, этоксилированные органосиликоны, этоксилированные амины жирного ряда и смеси поверхностно-активных веществ с минеральными или растительными маслами. Препараты могут включать также эмульсии типа масло-в-воде, такие как эмульсии, описанные в заявке на патент США, регистрационный 11/495228, описание которой специально включено в настоящее описание в качестве ссылки. Препараты могут необязательно включать комбинации, которые содержат другие пестицидные соединения. Такими дополнительными пестицидными соединениями могут быть фунгициды, инсектициды, гербициды, нематоциды, митициды, артроподициды, бактерициды или их комбинации, которые являются совместимыми с соединениями настоящего изобретения в среде, выбранной для применения, и не являются антагонистическими для активности настоящих соединений. Согласно этому в таких вариантах осуществления другое пестицидное соединение применяют в качестве дополнительного ядовитого вещества для такого же или для другого пестицидного применения. Соединения формулы I и пестицидное соединение в комбинации обычно присутствуют в массовом отношении от 1:100 до 100:1. Соединения настоящего изобретения можно также сочетать с другими фунгицидами для получения их фунгицидных смесей и синергических смесей. Фунгицидные соединения настоящего описания часто применяют в сочетании с одним или несколькими другими фунгицидами для борьбы с большим разнообразием нежелательных болезней. При применении в сочетании с другим фунгицидом(ами) заявленные в настоящем описании соединения можно вводить в препарат с другим фунгицидом(ами), смешать в резервуаре с другим фунгицидом(ами) или применять последовательно с другим фунгицидом(ами). Такие другие фунгициды могут включать 2-(тиоцианатометилтио)бензотиазол, 2-фенилфенол, сульфат 8-гидроксихинолина, аметоктрадин, амисульбром, антимицин, Ampelomyces quisqualis, азаконазол, азоксистробин, Bacillus subtilis, штамм Bacillus subtilis QST713, беналаксил, беномил, бентиаваликарб-изопропил,соль бензиламинобензолсульфоната (BABS), бикарбонаты, бифенил, бисмертиазол, битертанол, биксафен, бластицидин-S, боракс, смесь Bordeaux, боскалид, бромуконазол, бупиримат, полисульфид кальция,каптафол, каптан, карбендазим, карбоксин, сарпропамид, карвон, хлазафенон, хлоронеб, хлороталонил,хлозолинат, Coniothyrium minitans, гидроксид меди, октаноат меди, оксихлорид меди, сульфат меди,сульфат меди (трехосновный), оксид меди(I), циазофамид, цифлуфенамид, цимоксанил, ципроконазол,ципродинил, дазомет, дебакарб, этиленбис-(дитиокарбамат) диаммония, дихлофлуанид, дихлорофен,диклоцимет, дикломезин, дихлоран, диэтофенкарб, дифеноконазол, дифензокват-ион, дифлуметорим,диметоморф, димоксистробин, диниконазол, диниконазол-М, динобутон, динокап, дифениламин, дитианон, додеморф, додеморфа ацетат, додин, свободное основание додина, эдифенфос, энестробин, эпоксиконазол, этабоксам, этоксихин, этридиазол, фамоксадон, фенамидон, фенаримол, фенбуконазол, фенфурам, фенгексамид, феноксанил, фенпиклонил, фенпропидин, фенпропиморф, фенпиразамин, фентин,фентина ацетат, фентина гидроксид, фербам, феримзон, флуазинам, флудиоксонил, флуморф, флуопиколид, флуопирам, флуороимид, флуоксастробин, флухинконазол, флусилазол, флусульфамид, флутианил,флутоланил, флутриафол, флуксапироксад, фолпет, формальдегид, фосетил, фосетил-алюминий, фуберидазол, фуралаксил, фураметпир, гуазатин, гуазатина ацетаты, GY-81, гексахлорбензол, гексаконазол,химексазол, имазалил, имазалила сульфат, имибенконазол, иминоктадин, иминоктадина триацетат, иминоктадина трис-(альбезилат), йодокарб, ипконазол, ипфенпиразолон, ипробенфос, ипродион, ипроваликарб, изопротиолан, изопиразам, изотианил, казугамицин, казугамицина гидрохлорида гидрат, крезоксим-метил, ламинарин, манкоппер, манкозеб, мандипропамид, манеб, мепанипирим, мепронил, мептилдинокап, хлорид ртути(II), оксид ртути(II), хлорид ртути(I), металаксил, мефеноксам, металаксил-М, метам, метам-аммоний, метам-калий, метам-натрий, метконазол, метасульфокарб, метилиодид, метилизотиоцианат, метирам, метоминостробин, метрафенон, милдиомицин, миклобутанил, набам, нитротализопропил, нуаримол, октилинон, офурас, олеиновую кислоту (жирные кислоты), орисастробин, оксадиксил, оксин-медь, окспоконазола фумарат, оксикарбоксин, пефуразоат, пенконазол, пенцикурон, пенфлуфен, пентахлорфенол, пентахлорфениллаурат, пентиопирад, фенилртути ацетат, фосфоновую кислоту, фталид, пикоксистробин, полиоксин В, полиоксины, полиоксорим, калия бикарбонат, калия гидроксихинолинсульфат, пробеназол, прохлораз, процимидон, пропамокарб, пропамокарба гидрохлорид, пропиконазол, пропинеб, прохиназид, протиоконазол, пираклостробин, пираметостробин, пираоксистробин,пиразофос, пирибенкарб, пирибутикарб, пирифенокс, пириметанил, пириофенон, пирохилон, хинокламин, хиноксифен, хинтозен, экстракт Reynoutria sachalinensis, седаксан, силтиофам, симеконазол, натрия 2-фенилфеноксид, натрия бикарбонат, натрия пентахлорфеноксид, спироксамин, серу, SYP-Z071, SYPZ048, деготь, тебуконазол, тебуфлохин, текназен, тетраконазол, тиабендазол, тифлузамид, тиофанатметил, тирам, тиадинил, толклофос-метил, толилфлуанид, триадимефон, триадименол, триазоксид, трициклазол, тридеморф, трифлоксистробин, трифлумизол, трифорин, тритиконазол, валидамицин, валифеналат, валифенал, винклозолин, зинеб, зирам, зоксамид, Candida oleophila, Fusarium oxysporum, Gliocladium spp., Phlebiopsis gigantea, Streptomyces griseoviridis, Trichoderma spp., (RS)-N-(3,5-дихлорфенил)-2(метоксиметил)сукцинимид, 1,2-дихлорпропан, 1,3-дихлор-1,1,3,3-тетрафторацетона гидрат, 1-хлор-2,4 динитронафталин, 1-хлор-2-нитропропан, 2-(2-гептадецил-2-имидазолин-1-ил)этанол, 2,3-дигидро-5-фенил-1,4-дитиина 1,1,4,4-тетраоксид, 2-метоксиэтилртути ацетат, 2-метоксиэтилртути хлорид, 2-метоксиэтилртути силикат, 3-(4-хлорфенил)-5-метилроданин, 4-(2-нитропроп-1-енил)фенилтиоцианатем, ампропилфос, анилазин, азитирам, бария полисульфид, Bayer 32394, беноданил, бенхинокс, бенталурон,бензамакрил; бензамакрил-изобутил, бензаморф, бинапакрил, сульфат бис-(метилртути), бис-(трибутилолово)оксид, бутиобат, кадмия кальция меди цинка хромат сульфат, карбаморф, СЕСА, хлорбентиазон,хлораниформетан, хлорфеназол, хлорхинокс, климбазол, циклафурамид, ципендазол, ципрофурам, декафентин, дихлон, дихлозолин, диклобутразол, диметиримол, диноктон, диносульфон, динотербон, дипиритион, диталимфос, додецин, дразоксолон, EBP, ESBP, этаконазол, этем, этирим, фенаминосульф, фенапанил, фенитропан, 5-фторцитозин и его профунгициды, флуотримазол, фуркарбанил, фурконазол,фурконазол-цис, фурмециклокс, фурофанат, глиодин, гризеофульвин, галакринат, Hercules 3944, гексилтиофос, ICIA0858, изопамфос, изоваледион, мебенил, мекарбинзид, метазоксолон, метфуроксам, метилртути дициандиамид, метсульфовакс, милнеб, мукохлорный ангидрид, миклозолин, N-3,5-дихлорфенилсукцинимид, N-3-нитрофенилитаконимид, натамицин, N-этилмеркурио-4-толуолсульфонанилид,никеля бис-(диметилдитиокарбамат), OCH, фенилртути диметилдитиокарбамат, фенилртути нитрат,фосдифен, пиколинамид UK-2A и его производные, протиокарб; протиокарба гидрохлорид, пиракарболид, пиридинитрил, пироксихлор, пироксифур, хинацетол; хинацетола сульфат, хиназамид, хинконазол,-6 022069 рабензазол, салициланилид, SSF-109, сультропен, текорам, тиадифтор, тициофен, тиохлорфенфим, тиофанат, тиохинокс, тиоксимид, триамифос, триаримол, триазбутил, трихламид, урбацид, зариламид и любые их комбинации. Кроме того, соединения настоящего изобретения можно комбинировать с другими пестицидами,включающими инсектициды, нематоциды, митициды, артроподициды, бактерициды или их комбинации,которые являются совместимыми с соединениями настоящего изобретения в среде, выбранной для применения, и не являются антагонистическими для активности настоящих соединений, с образованием их пестицидных смесей и синергических смесей. Фунгицидные соединения настоящего описания можно применять в сочетании с одним или несколькими другими пестицидами для борьбы с более широким рядом нежелательных вредителей. При применении в сочетании с другими пестицидами заявленные в настоящем описании соединения можно вводить в препарат с другим пестицидом(ами), смешать в резервуаре с другим пестицидом(ами) или применять последовательно с другим пестицидом(ами). Типичные инсектициды включают, но не ограничиваются перечисленным, антибиотические инсектициды, такие как аллосамидин и турингиензин; инсектициды типа макроциклических лактонов, такие как спиносад и спинеторам; авермектиновые инсектициды, такие как абамектин, дорамектин, эмамектин, эприномектин,ивермектин и селамектин; милбемициновые инсектициды, такие как лепимектин, милбемектин, милбемицина оксим и моксидектин; арсеникаловые инсектициды, такие как кальция арсенат, меди ацетоарсенит, меди арсенат, свинца арсенат, калия арсенит и натрия арсенит; ботаникальные инсектициды, такие как анабазин, азадирахтин, d-лимонен, никотин, пиретрины, цинерины, цинерин I, цинерин II, жасмолинI, жасмолин II, пиретрин I, пиретрин II, квассиа, ротенон, гуаниа и сабадилла; карбаматные инсектициды,такие как бендиокарб и карбарил; бензофуранилметилкарбаматные инсектициды, такие как бенфуракарб,карбофуран, карбосульфан, декарбофуран и фуратиокарб; диметилкарбаматные инсектициды, такие как димитан, диметилан, гихинкарб и пиримикарб; оксимкарбаматные инсектициды, такие как аланикарб,алдикарб, альдоксикарб, бутокарбоксим, бутоксикарбоксим, метомил, нитрилакарб, оксамил, тазимкарб,тиокарбоксим, тиодикарб и тиофанокс; фенилметилкарбаматные инсектициды, такие как алликсикарб,аминокарб, буфенкарб, бутакарб, карбанолат, клоэтокарб, дикрезил, диоксакарб, ЕМРС, этиофенкарб,фенэтакарб, фенобукарб, изопрокарб, метиокарб, метолкарб, мексакарбат, промацил, промекарб, пропоксур, триметакарб, ХМС и ксилилкарб; сиккативные инсектициды, такие как борная кислота, диатомовая земля и силикагель; диамидные инсектициды, такие как хлорантранилипрол, циантранилипрол и флубендиамид; динитрофенольные инсектициды, такие как динекс, динопроп, диносам и DNOC; фторные инсектициды, такие как бария гексафторсиликат, криолит, натрия фторид, натрия гексафторсиликат и сульфлурамид; формамидиновые инсектициды, такие как амитраз, хлордимеформ, форметанат и формпаранат; фумигантные инсектициды, такие как акрилонитрил, дисульфид углерода, тетрахлорид углерода, хлороформ, хлорпикрин, парадихлорбензол, 1,2-дихлорпропан, этилформиат, этилендибромид, этилендихлорид, этилена оксид, цианид водород, йодметан, метилбромид, метилхлороформ, метиленхлорид, нафталин, фосфин, сульфурилфторид и тетрахлорэтан; неорганические инсектициды, такие как боракс, кальция полисульфид, меди олеат, хлорид ртути(I), калия тиоцианат и натрия тиоцианат; ингибиторы синтеза хитина, такие как бис-трифлурон, бупрофезин, хлорфлуазурон, циромазин, дифлубензурон,флуциклоксурон, флуфеноксурон, гексафлумурон, луфенурон, новалурон, новифлумурон, пенфлурон,тефлубензурон и трифлумурон; имитаторы ювенильных гормонов, такие как эпофенонан, феноксикарб,гидропрен, кинопрен, метопрен, пирипроксифен и трипрен; ювенильные гормоны, такие как ювенильный гормон I, ювенильный гормон II и ювенильный гормон III, агонисты гормона линьки, такие как хромафенозид, галофенозид, метоксифенозид и тебуфенозид; гормоны линьки, такие как -экдизон и экдистерон; ингибиторы линьки, такие как диофенолан; прекоцены, такие как прекоцен I, прекоцен II и прекоцен III; неклассифицированные регуляторы роста насекомых, такие как дицикланил; инсектициды,аналоги нереистоксина, такие как бенсультап, картап, тиоциклам и тиосультап; никотиноидные инсектициды, такие как флоникамид; нитрогуанидиновые инсектициды, такие как клотианидин, динотефуран,имидаклоприд и тиаметоксам; нитрометиленовые инсектициды, такие как нитенпирам и нитиазин; пиридилметиламиновые инсектициды, такие как ацетамиприд, имидаклоприд, нитенпирам и тиаклоприд; хлорорганические инсектициды, такие как бром-DDT, камфехлор, DDT, pp'-DDT, этил-DDD, HCH, гамма-HCH, линдан, метоксихлор, пентахлорфенол и TDE; циклодиеновые инсектициды, такие как альдрин,бромциклен, хлорбициклен, хлордан, хлордекон, дильдрин, дилор, эндосульфан, альфа-эндосульфан,эндрин, HEOD, гептахлор, HHDN, изобензан, изодрин, келеван и мирекс; органофосфатные инсектициды, такие как бромфенвинфос, хлорфенвинфос, кротоксифос, дихлорвос, дикротофос, диметилвинфос,фоспират, гептенофос, метокротофос, мевинфос, монокротофос, налед, нафталофос, фосфамидон, пропафос, ТЕРР и тетрахлорвинфос; органотиофосфатные инсектициды, такие как диоксабензофос, фосметилан и фентоат; алифатические органотиофосфатные инсектициды, такие как ацетион, амитон, кадузафос, хлорэтоксифос, хлормефос, демефион, демефион-О, демефион-S, деметон, деметон-О, деметон-S,деметон-метил, деметон-О-метил, деметон-S-метил, деметон-S-метилсульфон, дисульфотон, этион, этопрофос, IPSP, изотиоат, малатион, метакрифос, оксидеметон-метил, оксидепрофос, оксидисульфотон,форат, сульфотеп, тербуфос и тиометон; инсектициды типа алифатических амидов органических тиофосфатов, такие как амидитион, циантоат, диметоат, этоат-метил, формотион, мекарбам, ометоат, прото-7 022069 ат, софамид и вамидотион; оксиморганотиофосфатные инсектициды, такие как хлорфоксим, фоксим и фоксим-метил; гетероциклические органотиофосфатные инсектициды, такие как азаметифос, кумафос,кумитоат, диоксатион, эндотион, меназон, морфотион, фосалон, пираклофос, пиридафентион и хинотион; бензотиопиранорганотиофосфатные инсектициды, такие как дитикрофос и тикрофос; бензотриазинорганотиофосфатные инсектициды, такие как азинфос-этил и азинфос-метил; изоиндолорганотиофосфатные инсектициды, такие как диалифос и фосмет; изоксазолорганотиофосфатные инсектициды, такие как изоксатион и золапрофос; пиразолопиримидинорганотиофосфатные инсектициды, такие как хлорпразофос и пиразофос; пиридинорганотиофосфатные инсектициды, такие как хлорпирифос и хлорпирифос-метил; пиримидинорганотиофосфатные инсектициды, такие как бутатиофос, диазинон, этримфос,лиримфос, пиримифос-этил, пиримифос-метил, примидофос, пиримитат и тебупиримфос; хиноксалинорганотиофосфатные инсектициды, такие как хиналфос и хиналфос-метил; тиадиазолорганотиофосфатные инсектициды, такие как атидатион, литидатион, метидатион и протидатион; триазолорганотиофосфатные инсектициды, такие как изазофос и триазофос; фенилорганотиофосфатные инсектициды, такие как азотоат, бромофос, бромофос-этил, карбофенотион, хлортиофос, цианофос, цитиоат, дикартон, дихлофентион, этафос, фамфур, фенхлорфос, фенитротион, фенсульфотион, фентион, фентион-этил, гетерофос,жодфенфос, мезулфенфос, паратион, паратион-метил, фенкаптон, фоснихлор, профенофос, протиофос,сульпрофос, темефос, трихлорметафос-3 и трифенофос; фосфонатные инсектициды, такие как бутонат и трихлорфон; фосфонотиоатные инсектициды, такие как мекарфон; фенилэтилфосфонотиоатные инсектициды, такие как фонофос и трихлоронат; фенилфенилфосфонотиоатные инсектициды, такие как цианофенфос, EPN и лептофос; фосфорамидатные инсектициды, такие как круфомат, фенамифос, фостиетан, мефосфолан, фосфолан и пириметафос; фосфорамидотиоатные инсектициды, такие как ацефат, изокарбофос, изофенфос, изофенфос-метил, метамидофос и пропетамфос; фосфородиамидные инсектициды,такие как димефокс, мазидокс, мипафокс и шрадан; оксадиазиновые инсектициды, такие как индоксакарб; оксадиазолиновые инсектициды, такие как метоксадиазон; фталимидные инсектициды, такие как диалифос, фосмет и тетраметрин; пиразоловые инсектициды, такие как тебуфенпирад, толефенпирад; фенилпиразоловые инсектициды, такие как ацетопрол, этипрол, фипронил, пирафлупрол, пирипрол и ванилипрол; пиретроидные сложноэфирные инсектициды, такие как акринатрин, аллетрин, биоаллетрин,бартрин, бифентрин, биоэтанометрин, циклетрин, циклопротрин, суфлутрин, бета-суфлутрин, цигалотрин, гамма-цигалотрин, лямбда-цигалотрин, циперметрин, альфа-циперметрин, бета-циперметрин, тетациперметрин, зета-циперметрин, цифенотрин, дельтаметрин, димефлутрин, диметрин, эмпентрин, фенфлутрин, фенпиритрин, фенпропатрин, фенвалерат, эсфенвалерат, флуцитринат, флувалинат, тауфлувалинат, фуретрин, имипротрин, меперфлутрин, метофлутрин, перметрин, биоперметрин, трансперметрин, фенотрин, праллетрин, профлутрин, пиресметрин, ресметрин, биоресметрин, цисметрин, тефлутрин, тераллетрин, тетраметрин, тетраметилфлутрин, тралометрин и трансфлутрин; пиретроидные простые эфирные инсектициды, такие как этофенпрокс, флуфенпрокс, галфенпрокс, протрифенбут и силафлуофен; пиримидинаминовые инсектициды, такие как флуфенерим и пиримидифен; пирроловые инсектициды, такие как хлорфенапир; инсектициды типа тетрамовых кислот, такие как спиротетрамат; инсектициды типа тетроновых кислот, такие как спиромезифен; тиомочевиновые инсектициды, такие как диафентиурон; мочевинные инсектициды, такие как флукофурон и сулкофурон; и неклассифицированные инсектициды, такие как клозантел, нафтенат меди, кротамитон, EDX, феназафлор, феноксакрим,гидраметилнон, изопротиолан, малонобен, метафлумизон, нифлуридид, плифенат, пиридабен, пиридалил, пирифлухиназон, рафоксанид, сульфоксафлор, триаратен и триазамат и их комбинации. Кроме того, соединения настоящего изобретения можно комбинировать с гербицидами, которые являются совместимыми с соединениями настоящего изобретения в среде, выбранной для применения, и не являются антагонистическими для активности настоящих соединений, с образованием их пестицидных смесей и синергических смесей. Фунгицидные соединения настоящего описания можно применять в сочетании с одним или несколькими пестицидами для борьбы с широким рядом нежелательных растений. При применении в сочетании с гербицидами заявленные в настоящем описании соединения можно вводить в препарат с гербицидом(ами), смешать в резервуаре с гербицидом(ами) или применять последовательно с гербицидом(ами). Типичные гербициды включают, но не ограничиваются перечисленным,амидные гербициды, такие как аллидохлор, бефлубутамид, бензадокс, бензипрам, бромобутид, кафенстрол, CDEA, ципразол, диметенамид, диметенамид-Р, дифенамид, эпроназ, этнипромид, фентразамид,флупоксам, фомезафен, галозафен, изокарбамид, изоксабен, напропамид, напталам, петоксамид, пропизамид, хинонамид и тебутам; анилидные гербициды, такие как хлоранокрил, цисанилид, кломепроп, ципромид, дифлуфеникан, этобензанид, фенасулам, флуфенацет, флуфеникан, мефенацет, мефлуидид, метамифоп, моналид, напроанилид, пентанохлор, пиколинафен и пропанил; арилаланиновые гербициды,такие как бензоилпроп, флампроп и флампроп-М; хлорацетанилидные гербициды, такие как ацетохлор,алахлор, бутахлор, бутенахлор, делахлор, диэтатил, диметахлор, метазахлор, метолахлор, S-метолахлор,претилахлор, пропахлор, пропизохлор, принахлор, тербухлор, тенилхлор и ксилахлор; сульфонанилидные гербициды, такие как бензофлор, перфлуидон, пиримисульфан и профлуазол; сульфонамидные гербициды, такие как азулам, карбасулам, фенасулам и оризалин; тиоамидные гербициды, такие как хлортиамид; антибиотические гербициды, такие как биланафос; гербициды типа бензойных кислот, такие как хлорамбен, дикамба, 2,3,6-ТВА и трикамба; гербициды типа пиримидинилоксибензойной кислоты, такие как биспирибак и пириминобак; гербициды типа пиримидинилтиобензойной кислоты, такие как пиритиобак; гербициды типа фталевой кислоты, такие как хлортал; гербициды типа пиколиновой кислоты,такие как аминопиралид, клопиралид и пиклорам; гербициды типа хинолинкарбоновой кислоты, такие как хинклорак и хинмерас; мышьяковые гербициды, такие как какодиловая кислота, СМА, DSMA, гексафлурат, МАА, МАМА, MSMA, арсенит калия и арсенит натрия; бензоилциклогександионовые гербициды, такие как мезотрион, сулкотрион, тефурилтрион и темботрион; бензофуранилалкилсульфонатные гербициды, такие как бенфурезат и этофумезат; бензотиазоловые гербициды, такие как бензазолин; карбаматные гербициды, такие как азулам, карбоксазол, хлорпрокарб, дихлормат, фенасулам, карбутилат и тербукарб; карбанилатные гербициды, такие как барбан, ВСРС, карбасулам, карбетамид, СЕРС, хлорбуфам, хлорпрофам, СРРС, дезмедифам, фенизофам, фенмедифам, фенмедифам-этил, профам и свеп; гербициды типа оксима циклогексена, такие как аллоксидим, бутроксидим, клетодим, клопроксидим, циклоксидим, профоксидим, сетоксидим, тепралоксидим и тралкоксидим; циклопропилизоксазоловые гербициды, такие как изоксахлортол и изоксафлутол; дикарбоксимидные гербициды, такие как цинидонэтил, флумезин, флумиклорак, флумиоксазин и флумипропин; динитроанилиновые гербициды, такие как бенфлуралин, бутралин, динитрамин, эталфлуралин, флухлоралин, изопропалин, металпропалин, нитралин, оризалин, пендиметалин, продиамин, профлуралин и трифлуралин; динитрофеноловые гербициды,такие как динофенат, динопроп, диносам, диносеб, динотерб, DNOC, этинофен и мединотерб; гербициды типа дифениловых простых эфиров, такие как этоксифен; гербициды типа нитрофениловых простых эфиров, такие как ацифлуорфен, аклонифен, бифенокс, хлорметоксифен, хлорнитрофен, этнипромид,фтордифен, фторгликофен, фторнитрофен, фомезафен, фурилоксифен, галосафен, лактофен, нитрофен,нитрофлуорфен и оксифлуорфен; дитиокарбаматные гербициды, такие как дазомет и метам; галогенированные алифатические гербициды, такие как алорак, хлоропон, далапон, флупропанат, гексахлорацетон,йодметан, метилбромид, монохлоруксусная кислота, SMA и ТСА; имидазолиноновые гербициды, такие как имазаметабенз, имазамокс, имазапик, имазапир, имазахин и имазетапир; неорганические гербициды,такие как сульфамат аммония, боракс, хлорат кальция, сульфат меди, сульфат железа(II), азид калия,цианат калия, азид натрия, хлорат натрия и серная кислота; нитрильные гербициды, такие как бромбонил, бромоксинил, хлороксинил, дихлобенил, йодобонил, иоксинил и пираклонил; фосфорорганические гербициды, такие как амипрофос-метил, анилофос, бенсулид, биланафос, бутамифос, 2,4-DEP, DMPA,ЕВЕР, фосамин, глуфосинат, глуфосинат-Р, глифосат и пиперофос; феноксигербициды, такие как бромфеноксим, кломепроп, 2,4-DEB, 2,4-DEP, дифенопентен, дисул, эрбон, этнипромид, фентеракол и трифопсим; оксадиазолиновые гербициды, такие как метазол, оксадиаргил, оксадиазон; оксазоловые гербициды, такие как феноксасульфон; гербициды типа феноксиуксусных кислот, такие как 4-СРА, 2,4-D, 3,4DA, MCPA, МСРА-тиоэтил и 2,4,5-Т; гербициды типа феноксимасляных кислот, такие как 4-СРВ, 2,4DB, 3,4-DB, MCPB и 2,4,5-ТВ; гербициды типа феноксипропионовых кислот, такие как клопроп, 4-СРР,дихлорпроп, дихлорпроп-Р, 3,4-DP, фенопроп, мекопроп и мекопроп-Р; гербициды типа арилоксифеноксипропионовых кислот, такие как хлоразифоп, клодинафоп, клофоп, цигалофоп, диклофоп, феноксапроп,феноксапроп-Р, фентиапроп, флуазифоп, флуазифоп-Р, галоксифоп, галоксифоп-Р, изоксапирифоп, метамифоп, пропахизафоп, хизалофоп, хизалофоп-Р и трифоп; фенилендиаминовые гербициды, такие как динитрамин и продиамин; пиразоловые гербициды, такие как пироксасульфон; бензоилпиразоловые гербициды, такие как бензофенап, пирасульфотол, пиразолинат, пиразоксифен и топрамезон; фенилпиразоловые гербициды, такие как флуазолат, нипираклофен, пиоксаден и пирафлуфен; пиридазиновые гербициды, такие как кредазин, пиридафол и пиридат; пиридазиноновые гербициды, такие как бромпиразон,хлоридазон, димидазон, флуфенпир, метфлуразон, норфлуразон, оксапиразон и пиданон; пиридиновые гербициды, такие как аминопиралид, клиодинат, клопиралид, дитиопир, флуроксипир, галоксидин, пиклорам, пиколинафен, пириклор, тиазопир и триклопир; пиримидиндиаминовые гербициды, такие как ипримидам и тиоклорим; четвертичные аммониевые гербициды, такие как циперкват, диэтамкват, дифензокват, дикват, морфамкват и паракват; тиокарбаматные гербициды, такие как бутилат, циклоат, диаллат, ЕРТС, эспрокарб, этиолат, изополинат, метиобенкарб, молинат, орбенкарб, пебулат, просульфокарб, пирибутикарб, сульфаллат, тиобенкарб, тиокарбазил, триаллат и вернолат; тиокарбонатные гербициды, такие как димексано, EXD и проксан; тиомочевиновые гербициды, такие как метиурон; триазиновые гербициды, такие как дипропетрин, индазифлам, триазифлам и тригидрокситриазин; хлортриазиновые гербициды, такие как атразин, хлоразин, цианазин, ципразин, эглиназин, ипазин, мезопразин, проциазин, проглиназин, пропазин, себутилазин, симазин, тербутилазин и триэтазин; метокситриазиновые гербициды, такие как атратон, метометон, прометон, секбуметон, симетон и тербуметон; метилтиотриазиновые гербициды, такие как аметрин, азипротрин, цианатрин, дезметрин, диметаметрин, метопротрин,прометрин, симетрин и тербутрин; триазиноновые гербициды, такие как аметридион, амибузин, гексазинон, изометиозин, метамитрон и метрибузин; триазоловые гербициды, такие как амитрол, кафенстрол,эпроназ и флупоксам; триазолоновые гербициды, такие как амикарбазон, бенкарбазон, карфентразон,флукарбазон, ипфенкарбазон, пропоксикарбазон, сульфентразон и тиенкарбазон-метил; триазолопиримидиновые гербициды, такие как клорансулам, диклосулам, флоразулам, флуметсулам, метосулам, пенокссулам и пирокссулам; урацильные гербициды, такие как бензфендизон, бромацил, бутафенацил,-9 022069 флупропацил, изоцил, ленацил, сафлуфенацил и тербацил; мочевиновые гербициды, такие как бензтиазурон, кумилурон, циклурон, дихлоралмочевина, дифлуфензопир, изонорурон, изоурон, метабензтиазурон, монизоурон и норурон; фенилмочевиновые гербициды, такие как анизурон, бутурон, хлорбромурон,хлорэтурон, хлоротолурон, хлороксурон, даймурон, дифеноксурон, димефурон, диурон, фенурон, флуометурон, флуотиурон, изопротурон, линурон, метиурон, метилдимрон, метобензурон, метобромурон,метоксурон, монолинурон, монурон, небурон, парафлурон, фенобензурон, сидурон, тетрафлурон и тидиазурон; пиримидинилсульфонилмочевиновые гербициды, такие как амидосульфурон, азимсульфурон,бенсульфурон, хлоримурон, циклосульфамурон, этоксисульфурон, флазасульфурон, флуцетосульфурон,флупирсульфурон, форамсульфурон, галосульфурон, имазосульфурон, мезосульфурон, метазосульфурон, никосульфурон, ортосульфамурон, оксасульфурон, примисульфурон, пропирисульфурон, пиразосульфурон, римсульфурон, сульфометурон, сульфосульфурон и трифлоксисульфурон; триазинилсульфонилмочевиновые гербициды, такие как хлорсульфурон, циносульфурон, этаметсульфурон, йодосульфурон, метсульфурон, просульфурон, тифенсульфурон, триазулфурон, трибенурон, трифлусульфурон и тритосульфурон; тиадиазолилмочевиновые гербициды, такие как бутиурон, этидимурон, тебутиурон,тиазафлурон и тидиазурон; и неклассифицированные гербициды, такие как акролеин, аллиловый спирт,аминоциклопирахлор, азафенидин, бентазон, бензобициклон, бициклопирон, бутидазол, кальция цианамид, камбендихлор, хлорфенак, хлорфенпроп, хлорфлуразол, хлорфлуренол, цинметилин, кломазон,CPMF, крезол, цианамид, ортодихлорбензол, димепиперат, эндотал, фтормидин, флуридон, фторхлоридон, флуртамон, флутиацет, инданофан, метилизотиоцианат, OCH, оксазикломефон, пентахлорфенол,пентоксазон, ацетат фенилртути, просульфалин, пирибензоксим, пирифталид, хинокламин, родетанил,сульгликапин, тидиазимин, тридифан, триметурон, трипропиндан и тритак. Другим вариантом осуществления настоящего изобретения является способ борьбы с поражением грибами или предотвращения поражения грибами. Данный способ включает нанесение на почву, растения, корни, листву, семена или очаг распространения грибов или место, в котором нужно предотвратить заражение (например, нанесением на злаковые растения), фунгицидно эффективного количества одного или нескольких соединений формулы I. Соединения являются подходящими для обработки различных растений при фунгицидных уровнях, проявляя при этом низкую фитотоксичность. Соединения могут быть применимы в качестве защитного и/или уничтожающего грибы средства. Обнаружено, что соединения обладают значительным фунгицидным действием особенно при сельскохозяйственном применении. Многие из соединений являются особенно эффективными для применения для сельскохозяйственных культур и садовых растений. Дополнительные преимущества могут включать, но не ограничиваются перечисленным, улучшение здоровья растений; повышение урожая растений (например, получение повышенной биомассы и/или повышенного содержания ценных ингредиентов); повышение жизнестойкости растения (например, достижение повышенного роста растений и/или более зеленых листьев); улучшение качества растения (например, достижение повышенного содержания или состава некоторых ингредиентов) и повышение толерантности к абиотическому и/или биотическому стрессу растения. Специалисту в данной области должно быть понятно, что эффективность соединения в отношении действия на вышеуказанные грибы определяет общую применимость соединений в качестве фунгицидов. Соединения имеют широкие диапазоны активности против грибковых патогенов. Примерные патогенности могут включать, но не ограничиваются перечисленным, пятнистость листьев пшеницы (Septoriatritici, известную также как Mycosphaerella graminicola), паршу яблок (Venturia inaequalis) и церкоспорозную пятнистость листьев сахарной свеклы (Cercospora beticola), пятнистость листьев арахиса (Cercosporaarachidicola и Cercosporidium personatum) и других сельскохозяйственных культур и черную Sigatoka бананов (Mycosphaerella fujiensis). Точное количество наносимого активного вещества зависит не только от конкретного применяемого вещества, но также от конкретного требуемого действия, грибкового вида,который нужно подавить, и стадии его роста, а также части растения или другого продукта, который контактируют с соединением. Таким образом, все соединения и содержащие их препараты не могут быть равно эффективными при одинаковых концентрациях или против одного и того же грибкового вида. Соединения являются эффективными при применении для растений в подавляющем болезнь и фитологически приемлемом количестве. Термин "подавляющее болезнь и фитологически приемлемое количество" относится к количеству соединения, которое устраняет или подавляет болезнь растения, для которого подавление является желательным, но которое не является значительно токсичным для растения. Это количество обычно составляет от приблизительно 0,1 до приблизительно 1000 м.д. (миллионные доли), причем предпочтительным является 1-500 м.д. Точное количество требуемого соединения варьирует в зависимости от грибковой болезни, которую подавляют, типа применяемого препарата, способа применения, конкретного вида растения, климатических условий и тому подобного. Подходящая норма введения обычно находится в диапазоне от приблизительно 0,10 до приблизительно 4 фунтов/акр(приблизительно 0,01-0,45 г на квадратный метр, г/м 2). Любой диапазон требуемой величины, указанной в контексте, можно расширить или изменить без потери результата действия, которое пытаются получить, что очевидно специалисту в данной области вследствие понимания приведенного в контексте описания. Соединения формулы I можно получить с применением хорошо известных химических процедур. Промежуточные продукты, не указанные конкретно в данном описании, либо являются коммерчески доступными, их можно получить путями, описанными в химической литературе, либо их можно легко синтезировать из коммерческих исходных веществ с применением стандартных процедур. Нижеследующие примеры представлены для иллюстрации различных аспектов соединений настоящего изобретения и не должны рассматриваться как ограничение формулы изобретения. Пример 1. Получение 5-фтор-1-морфолин-4-илметил-4-[(морфолин-4-илметил)амино]-1 Н-пиримидин-2-она (1) Данное соединение получают, как описано в Int. J. Pharm. (1987, 35, 243-252). К смеси параформальдегида (240 миллиграммов (мг), 8 миллимолей (ммоль) мономера) в дихлорметане (CH2Cl2; 20 мл) в пробирке на 25 миллилитров (мл) с завинчивающейся крышкой добавляли морфолин (697 мг, 8 ммоль). Реакционную смесь перемешивали на орбитальном вибраторе на протяжении ночи при комнатной температуре. Добавляли 4-амино-5-фторпиримидин-2-ол (250 мг, 2 ммоль) и образовавшуюся гетерогенную смесь перемешивали при комнатной температуре в течение 48 ч (час). Реакционную смесь упаривали досуха и остаток обрабатывали простым эфиром (Et2O), получая при этом белое твердое вещество,которое отделяли фильтрованием и сушили, получая при этом указанное в заголовке соединение (381 мг,65%): т.пл. 156-158C; 1H ЯМР (300 МГц, CDCl3)7,46 (д, J=2,5 Гц, 1H), 5,69 (ушир.т, 1H), 4,53 (с, 2H),4,46 (д, J=2,6 Гц, 2H), 3,72 (м, 8H), 2,64 (м, 8H); ИК (ATR) 3483 (шир.), 3293 (шир.), 1680 (резк.), 1639 Это соединение получали, как описано в Int. J. Pharm. (1987, 35, 243-252). К смеси параформальдегида (240 мг, 8 ммоль мономера) в CH2Cl2 (20 мл) в пробирке на 25 мл с завинчивающейся крышкой добавляли N-метилпиперазин (813 мг, 8 ммоль). Реакционную смесь перемешивали на орбитальном вибраторе на протяжении ночи при комнатной температуре. Добавляли 4-амино-5-фторпиримидин-2-ол (250 мг, 2 ммоль) и образовавшуюся гетерогенную смесь перемешивали при комнатной температуре в течение 48 ч. Реакционную смесь упаривали досуха и остаток обрабатывали Et2O, получая при этом бежевое твердое вещество, которое отделяли фильтрованием и сушили, получая при этом указанное в заголовке соединение (247 мг, 31%): т.пл. 165-166C; 1H ЯМР (300 МГц, CDCl3)7,45 (д, J=2,5 Гц, 1H), 5,62 В ампулу на 8 мл с завинчивающейся крышкой добавляли N,N-диметилформамид (ДМФ; 1,5 мл),N'-(5-фтор-2-гидроксипиримидин-4-ил)-N,N-диметилформамидин (100 мг, 0,54 ммоль), безводный карбонат калия (K2CO3; 138 мг, 1,0 ммоль) и 4-фторбензилбромид (113 мг, 0,60 ммоль). Смесь встряхивали и нагревали до 70C в течение 2 ч и затем при комнатной температуре в течение дополнительных 16 ч. Сырую реакционную смесь фильтровали и помещали непосредственно в хроматографическую колонку с обращенной фазой. После элюирования указанное в заголовке соединение выделяли в виде белого твердого вещества (30 мг, 20%): т.пл. 134-136C; 1H ЯМР (300 МГц, CDCl3)8,68 (с, 1H), 8,07 (д, J=2,5 Гц,1H), 7,49-7,43 (м, 2H), 7,10-7,01 (м, 2H), 5,33 (с, 2H), 3,20 (с, 3H), 3,18 (с, 3H); ESIMS m/z 293 ([M+H]+). Соединения 5-7 в табл. I синтезировали, как в примере 3. К N-(5-фтор-2-гидроксипиримидин-4-ил)-4-метилбензамиду (200 мг, 0,81 ммоль) в ДМФА (5 мл) добавляли K2CO3 (22 4 мг, 1,6 ммоль) и йодметан (230 мг, 1,6 ммоль). Смесь перемешивали и нагревали до 60C в течение 30 мин и затем перемешивали в течение 16 ч при комнатной температуре. Смесь распределяли между этилацетатом (EtOAc) и водой (Н 2 О). Органическую фазу сушили над сульфатом магния (MgSO4), фильтровали и упаривали. Сырое вещество очищали хроматографией на обращенной фазой, получая при этом указанное в заголовке соединение в виде белого твердого вещества (17 мг, 8%): т.пл. 229-230C; 1 Н ЯМР (300 МГц, CDCl3)13,2 (ушир.с, 1H), 8,23-8,15 (ушир.м, 2H), 7,42-7,37 (ушир.м,1H), 7,30-7,25 (ушир.м, 2H), 3,45 (с, 3H), 2,44 (с, 3H); ESIMS m/z 262 ([M+H]+), m/z 260 ([M-H]-). Пример 5. Получение N-(5-фтор-1-метил-2-оксо-1,2-дигидропиримидин-4-ил)-N-метил-С-фенилметансульфонамида (9) 4-Амино-5-фторпиримидин-2-ол (2 грамма (г), 15,5 ммоль) перемешивали в ацетонитриле (CH3CN; 80 мл) при 50C. К нагретой смеси добавляли N,О-бис-(триметилсилил)ацетамид (BSA; 9,4 г, 46,3 ммоль) и перемешивание и нагревание продолжали в течение 1,5 ч. Добавляли фенилметансульфонилхлорид (3,2 г, 16,8 ммоль). Спустя 2 ч реакционную смесь охлаждали до комнатной температуры и распределяли между CH3CN и насыщенным раствором соли. Органическую фазу сушили над MgSO4, фильтровали,упаривали и помещали непосредственно в колонку с силикагелем, которую элюировали (градиент 0100% EtOAc в петролейном эфире). Объединение фракций, содержащих основную, УФ-абсорбирующую часть смеси продукта, давало белое твердое вещество, которое применяли без дополнительной очистки. К части этого вещества (100 мг) добавляли ДМФА (3 мл), K2CO3 (100 мг) и йодметан (100 мг) и смесь перемешивали при 60C в течение 1 ч. Реакционную смесь охлаждали до комнатной температуры и добавляли избыток гидрида натрия (NaH; 60% дисперсия в минеральном масле). Всю смесь перемешивали в течение 30 мин и затем нагревали до 45C в течение 2,5 ч. Сырую смесь фильтровали и очищали хроматографией с обращенной фазой с последующей очисткой хроматографией на нормальной фазе (градиент, 30-100% EtOAc в петролейном эфире), получая при этом указанное в заголовке соединение в виде белого твердого вещества (28 мг, 27%): т.пл. 159-160C; 1H ЯМР (300 МГц, CDCl3)7,6 (м, 1H), 7,427,41 (м, 2H), 7,38-7,36 (м, 3H), 4,8 (с, 2H), 3,5 (с, 3H), 2,82 (с, 3H); ESIMS m/z 312 ([M+H]+), m/z 310 ([MH]-). Пример 6. Получение изобутилового эфира (5-фтор-1-метил-2-оксо-1,2-дигидропиримидин-4-ил)карбаминовой кислоты (10) и изобутилового эфира (5-фтор-1-метил-2-оксо-1,2-дигидропиримидин-4 ил)метилкарбаминовой кислоты (11) 4-Амино-5-фторпиримидин-2-ол (0,5 г, 3,9 ммоль) и изобутилхлорформиат (0,58 г, 4,2 ммоль) в пиридине (5 мл) встряхивали при 60C в течение 1,5 ч. Сырую смесь распределяли между EtOAc и 1 н хлористо-водородной кислотой (HCl). Органическую фазу сушили над MgSO4, фильтровали и упаривали. Из остатка в этиловом спирте (EtOH) осаждали белое твердое вещество, которое применяли без дополнительной очистки. Часть данного вещества (100 мг), K2CO3 (125 мг) и йодметан (125 мг) добавляли к ДМФА (3 мл) и смесь перемешивали при 60C в течение 1 ч. Смесь охлаждали до комнатной температуры и добавляли избыток NaH (60% дисперсия в минеральном масле). Всю смесь перемешивали в течение 30 мин и затем нагревали при 45C в течение 2 ч. Сырую смесь фильтровали и очищали хроматографией с обращенной фазой, получая при этом указанные в заголовке соединения. Изобутиловый эфир (5-фтор-1-метил-2-оксо-1,2-дигидропиримидин-4-ил)карбаминовой кислоты выделяли в виде белого твердого вещества (16 мг): т.пл. 126-128C; 1H ЯМР (300 МГц, CDCl3)12,2(ушир.с, 1H), 7,32 (ушир.с, 1H), 3,98 (д, J=6,6 Гц, 2H), 3,4 (с, 3H), 2,02 (септ., J=6,6 Гц, 1H), 1,01 (д, J=6,6 Гц, 6H); ESIMS m/z 244 ([M+H]+), m/z 242 ([M-H]-). Изобутиловый эфир (5-фтор-1-метил-2-оксо-1,2-дигидропиримидин-4-ил)метилкарбаминовой ки- 12022069 слоты выделяли в виде прозрачного бесцветного масла (22 мг): 1 Н ЯМР (300 МГц, CDCl3)7,52 (д, J=5,5 Гц, 1H), 4,02 (д, J=6,8 Гц, 2H), 3,55 (с, 3H), 3,40 (с, 3H), 1,99 (септ., J=6,8 Гц, 1H), 0,95 (д, J=6,8 Гц, 6H); 13 С ЯМР (150 МГц, CDCl3)158,24, 158,17, 154,7, 154,1, 140,5, 138,8, 134,0, 133,7, 73,6, 38,6, 34,9, 27,9,19,2; ESIMS m/z 258 ([M+H]+). Пример 7. Получение 4-(диметиламинометиленамино)-5-фтор-2-оксо-2 Н-пиримидин-1-илметилового эфира 2,2-диметилпропионовой кислоты (12) К ДМФА (3 мл) добавляли N'-(5-фтор-2-гидрокспиримидин-4-ил)-N,N-диметилформамидин (100 мг, 0,54 ммоль), карбонат цезия (196 мг, 0,6 ммоль) и хлорметилпивалат (90 мг, 0,6 ммоль) и смесь встряхивали при комнатной температуре в течение 16 ч. Смесь распределяли между EtOAc и Н 2 О. Органическую фазу сушили над MgSO4, фильтровали и упаривали. К образовавшемуся сырому маслу добавляли Et2O (3,5 мл) и образованный осадок собирали фильтрованием. Указанное в заголовке соединение выделяли в виде белого твердого вещества (37 мг, 23%): т.пл. 193-194C; 1 Н ЯМР (300 МГц, ДМСО-d6)8,67 (с, 1H), 8,07 (д, J=6,3 Гц, 1H), 5,60 (с, 2H), 3,22 (с, 3H), 3,09 (с, 3H), 1,11 (с, 9H); ESIMS m/z 299 В 25-мл колбу типа колбы Шленка загружали 4-амино-5-фторпиримидин-2-ол (500 мг, 3,87 ммоль),CH3CN (10 мл) и BSA (1,42 мл, 5,81 ммоль). Образовавшуюся белую суспензию затем нагревали при 65C. Спустя 90 мин прозрачный бесцветный раствор охлаждали до комнатной температуры и добавляли бензилхлорметиловый простой эфир (1,07 мл, 7,72 ммоль), получая при этом непрозрачную белую суспензию. После перемешивания в течение 2 ч при комнатной температуре реакционную смесь концентрировали в вакууме, получая при этом белый остаток, который очищали колоночной хроматографией с обращенной фазой, получая при этом 4-амино-1-(бензилоксиметил)-5-фторпиримидин-2(1H)-он (14; 433 мг, 45%) в виде белого твердого вещества: т.пл. 213-217C; 1H ЯМР (400 МГц, CDCl3)7,98 (д, J=6,5 Гц,1H), 7,81 (ушир.с, 1H), 7,56 (ушир.с, 1H), 7,24-7,36 (м, 5H), 5,11 (с, 2H), 4,54 (с, 2H); ИК 3302 (интенс.),3082 (интенс.), 2939 (слабая), 2869 (слабая), 1688 (интенс.), 1619 (интенс.), 1522 (интенс.), 1468 (средняя),1333 (средняя), 1131 (слабая), 1054 (средняя) см-1; ESIMS m/z 250 ([M+H]+). 1-(Бензилоксиметил)-4-(бензилоксиметиламино)-5-фторпиримидин-2(1H)-он (15; 16,5 мг, 1,2%) получали в качестве побочного продукта в виде бесцветного масла в синтезе соединения 14: 1H ЯМР (400 МГц, CDCl3)8,85 (т, J=5,8 Гц, 1H), 8,08 (д, J=6,6 Гц, 1H), 7,22-7,39 (м, 10H), 5,15 (с, 2H), 4,87 (д, J=5,8 Гц, 2H), 4,56 (с, 2H), 4,54 (с, 2H); ИК 3248 (слабая), 3062 (слабая), 3031 (слабая), 1683 (интенс.), 1644 В 250-мл круглодонную колбу загружали N'-(5-фтор-2-гидроксипиримидин-4-ил)-N,N-диметилформамидин (1,00 г, 5,43 ммоль) и ДМФА (55 мл) с получением белой суспензии. Добавляли твердый трет-бутоксид калия (1,07 г, 9,53 ммоль) и образовавшейся бледно-желтой суспензии давали возможность перемешиваться в атмосфере азота при комнатной температуре в течение 20 мин. Затем добавляли хлорметилметилсульфид (682 микролитров (мкл), 8,14 ммоль) и смесь нагревали при 60C в течение 21 ч. Сырую реакционную смесь концентрировали в вакууме при 55C, получая при этом не совсем белый остаток, который очищали колоночной хроматографией с обращенной фазой, получая при этом N'-(5 фтор-1-метилсульфанилметил-2-оксо-1,2-дигидропиримидин-4-ил)-N,N-диметилформамидин (36 мг,25%) в виде бледно-желтого твердого вещества: т.пл. 132-136C; 1 Н ЯМР (400 МГц, CDCl3)8,68 (с, 1H),8,20 (д, J=3,2 Гц, 1H), 5,40 (с, 2H), 3,19 (с, 3H), 3,07 (с, 3H), 2,20 (с, 3H); ИК 2960 (слабая), 2926 (слабая),- 13022069 Стадия 1. К перемешиваемому магнитной мешалкой раствору 4-амино-5-фторпиримидин-2-ола(4,00 г, 31,0 ммоль) в ДМФА (100 мл) добавляли диметилацеталь N,N-диметилформамида (ДМФА-DMA; 4,00 г, 34,0 ммоль). Смесь перемешивали при комнатной температуре в течение 72 ч, разбавляли Et2O(200 мл) и фильтровали. Твердый продукт промывали гептаном, получая при этом (Е)-N'-(5-фтор-2-оксо 1,2-дигидропиримидин-4-ил)-N,N-диметилформимидамид (5,23 г, 92%) в виде белого твердого вещества: т.пл. 240-243C; 1H ЯМР (300 МГц, ДМСО-d6)10,7 (ушир.с, 1H), 8,59 (с, 1H), 7,7 (д, J=5,6 Гц, 1H), 3,18(с, 3H), 3,06 (с, 3H); ESIMS m/z 185 ([M+H]+), m/z 183 ([M-H]-). Стадия 2. Порошкообразный K2CO3 (325 меш; 2,03 г, 14,7 ммоль) добавляли к смеси продукта со стадии 1 (1,35 г, 7,35 ммоль) и -бром-п-ксилола (1,36 г, 7,35 ммоль) в ДМФА (20 мл) в атмосфере N2 при комнатной температуре. Образовавшуюся белую суспензию нагревали до 80C. После перемешивания при 80C в течение 2 ч реакционную смесь охлаждали, разбавляли EtOAc (150 мл) и раствор промывали Н 2 О (450 мл) и насыщенным (насыщ.) NaCl (150 мл). Органическую фазу сушили (Na2SO4),фильтровали и концентрировали в вакууме, получая при этом 1,01 г бледно-желтого твердого вещества. Сырое вещество растворяли в смеси EtOAc/CH2Cl2 и обрабатывали целитом (3 г). Растворитель удаляли в вакууме и остаток очищали хроматографией с нормальной фазой (градиент 0-100% EtOAc/гексаны) для удаления изомерного О-алкилированного продукта. Колонку затем элюировали раствором 90%CH2Cl2/10% CH2OH, получая при этом требуемый N-алкилированный продукт, N'-[5-фтор-1-(4-метилбензил)-2-оксо-1,2-дигидропиримидин-4-ил]-N,N-диметилформамидин (0,668 г, 32%) в виде белого твердого вещества: т.пл. 178-179C; 1 Н ЯМР (300 МГц, CDCl3)8,82 (с, 1H), 7,22-7,15 (м, 4H), 4,97 (с, 2H),3,18 (с, 3H), 3,17 (с, 3H), 2,34 (с, 3H); ESIMS m/z 289 ([M+H]+). Стадия 3. Хлорид цинка (1,24 г, 9,12 ммоль) добавляли к смеси формамидинового продукта со стадии 2 (0,656 г, 2,28 ммоль) и абсолютного EtOH (10 мл). Образовавшуюся смесь нагревали для кипячения с обратным холодильником в атмосфере N2. Смесь постепенно превращалась в светло-желтый гомогенный раствор. После кипячения с обратным холодильником в течение 90 мин образовывался осадок, и после 2 ч реакционной смеси давали возможность охладиться до комнатной температуры и концентрировали в вакууме. Остаток обрабатывали CH2Cl2 (75 мл, появление слабой мутности) и промывали Н 2 О(25 мл). Как только добавляли Н 2 О, образовывался белый осадок в обоих слоях в делительной воронке. Твердое вещество отделяли вакуумным фильтрованием. Твердое вещество промывали Н 2 О с последующим промыванием Et2O. После сушки на воздухе на протяжении ночи белое твердое вещество (0,58 г) обрабатывали смесью 1:1 CH2Cl2/MeOH (70 мл) и нагревали для кипячения с обратным холодильником(мутная смесь). Смесь фильтровали и фильтрат концентрировали в вакууме. Остаточное твердое вещество суспендировали в смеси гексаны/Et2O (3:1) и выделяли вакуумным фильтрованием, сушили на воздухе и затем сушили в вакуумном сушильном шкафу (70-80C), получая при этом N'-(5-фтор-2-гидроксипиримидин-4-ил)-N,N-диметилформамидин (0,417 г, 78%) в виде белого порошка: т.пл. 291-293C К суспензии 4-амино-5-фторпиримидин-2-ола (0,50 г, 3,87 ммоль) в ацетонитриле (CH3CN; 20 мл) добавляли BSA (1,58 г, 7,75 ммоль) и смесь нагревали до 70C в течение 1 ч, получая при этом прозрачный раствор. После охлаждения до комнатной температуры добавляли 1,4-дийодбутан (1,2 г, 3,87 ммоль) и смесь перемешивали в течение 16 ч при комнатной температуре и затем при 70C в течение 3 ч. Растворитель выпаривали и остаток очищали хроматографией на нормальной фазе (24 г SiO2; градиент 015% MeOH/CH2Cl2), получая при этом оранжевое масло. Масло растворяли в EtOAc и раствор медленно охлаждали. Образовавшееся твердое вещество собирали фильтрованием, промывали дополнительнымEtOAc и сушили, получая при этом 4-амино-5-фтор-1-(4-йодбутил)-1 Н-пиримидин-2-он (0,52 г, 43%) в виде рыжевато-коричневого твердого вещества: т.пл. 181-184C; 1H ЯМР (400 МГц, ДМСО-d6)8,56 (с,2H), 8,25 (д, J=6,7 Гц, 1H), 3,70 (т, J=6,7 Гц, 2H), 3,29 (т, J=6,7 Гц, 2H), 1,73 (м, 4H); ESIMS m/z 312 К смеси 1,2,4-триазола (0,044 г, 0,64 ммоль), трет-бутоксида калия (KOtBu; 0,072 г, 0,64 ммоль) и 18-крауна-6 (18 С 6; 0,008 г, 0,03 ммоль) в CH3CN (3,5 мл) добавляли 4-амино-5-фтор-1-(4-йодбутил)-1 Нпиримидин-2-он (0,10 г, 0,32 ммоль) и смесь нагревали до 70C и перемешивали в течение 16 ч. Образовавшийся гомогенный раствор концентрировали в вакууме, получая при этом сырой продукт в виде белого твердого вещества. Очистка хроматографией с обращенной фазой (13 г С 18; градиент 0-20%CH3CN/вода) давала 4-амино-5-фтор-1-(4-[1,2,4]триазол-1-илбутил)-1 Н-пиримидин-2-он (0,023 г, 28%) в виде белого твердого вещества: т.пл. 197-200C; 1H ЯМР (400 МГц, ДМСО-d6)8,50 (с, 1H), 7,94 (м, 2H),7,56 (с, 1H), 7,35 (с, 1H), 4,19 (т, J=6,9 Гц, 2H), 3,61 (т, J=7,0 Гц, 2H), 1,73 (м, 2H), 1,51 (м, 2H); ESIMS m/z 253 ([M+H]+), m/z 251 ([M-H]-). Пример 13. Получение 4-амино-5-фтор-1-метилпиримидин-2(1H)-она (28) В 25-мл пробирке с завинчивающейся крышкой загружали 4-амино-5-фторпиримидин-2-ол (151,0 мг, 1,17 ммоль), K2CO3 (289,2 мг, 2,09 ммоль), 18 С 6 (278,6 мг, 0,901 ммоль) и безводный ДМФА (10 мл). Добавляли метилметансульфонат (0,0814 мл, 0,961 ммоль) и образовавшуюся смесь перемешивали на роторном вибраторе при 85C в течение 21 ч. После охлаждения до комнатной температуры сырое вещество концентрировали в вакууме и очищали колоночной хроматографией с обращенной фазой, получая при этом 4-амино-5-фтор-1-метилпиримидин-2(1H)-он (61,9 мг, 37%) в виде бежевого твердого вещества: т.пл. 195C (разл.); 1 Н ЯМР (400 МГц, ДМСО-d6)7,94 (д, J=6,8 Гц, 1H), 7,52 (с, 1H), 7,32 (с, 1H), 3,18 В 25-мл пробирку с завинчивающейся крышкой загружали (Е)-N'-(5-фтор-2-гидроксипиримидин-4 ил)-N,N-диметилформимидамид (99,5 мг, 0,540 ммоль), ДМФА (2 мл) и NaH (60% дисперсия в минеральном масле; 24,5 мг, 0,613 ммоль) и перемешивали на роторном вибраторе при 50C в течение 40 мин. После охлаждения до комнатной температуры добавляли дисульфид углерода (0,036 мл, 0,599 ммоль) и реакционную смесь перемешивали на роторном вибраторе при комнатной температуре в течение 90 мин. В этой точке добавляли йодэтан (0,052 мл, 0,650 ммоль) и реакционную смесь дополнительно перемешивали при комнатной температуре в течение 3,5 ч, после чего сырую смесь концентрировали в вакууме. Сырое вещество очищали хроматографией с нормальной фазой (градиент 0-30% MeOH/CH2Cl2), получая при этом (E)-N'-(1-этил-5-фтор-2-оксо-1,2-дигидропиримидин-4-ил)-N,N-диметилформимидамид (105 мг,67%) в виде белого твердого вещества: т.пл. 157-160C; 1H ЯМР (400 МГц, ДМСО-d6)8,62 (с, 1H), 8,09 В 25-мл пробирку с завинчивающейся крышкой загружали 5-фтор-4-(2-фторбензиламино)пиримидин-2-ол (49,7 мг, 0,210 ммоль), CH3CN (1 мл) и BSA (0,054 мл, 0,0221 ммоль) и смесь перемешивали на роторном вибраторе при 65C в течение 30 мин. После охлаждения до комнатной температуры добавляли (хлорметокси)этан (0,022 мл, 0,237 ммоль) и образовавшуюся смесь перемешивали на роторном вибраторе при комнатной температуре в течение 16 ч. Сырую реакционную смесь концентрировали в вакууме и очищали хроматографией с нормальной фазой (градиент 0-25% MeOH/CH2Cl2), получая при этом 1-(этоксиметил)-5-фтор-4-(2-фторбензиламино)пиримидин-2(1H)-он (55,0 мг, 89%) в виде желтого масла: 1H ЯМР (400 МГц, ДМСО-d6)8,60 (т, J=5,8 Гц, 1H), 8,05-7,95 (м, 1H), 7,40-7,26 (м, 2H), 7,26-7,10 В 25-мл пробирку с завинчивающейся крышкой загружали NaH (60% дисперсия в минеральном масле; 20,5 мг, 0,513 ммоль) и ДМФА (2,5 мл). Добавляли 5-фтор-N-(2-фторбензил)-2-(4-метилбензилокси)пиримидин-4-амин (149 мг, 0,436 ммоль) и смеси давали возможность для перемешивания при комнатной температуре. Спустя 10 мин добавляли йодметан (0,033 мл, 0,530 ммоль) и образовавшейся смеси давали возможность перемешиваться при комнатной температуре в течение дополнительных 28 ч. После этого времени сырую реакционную смесь концентрировали в вакууме и очищали хроматографией с нормальной фазой (градиент 0-40% EtOAc/гексаны), получая при этом 5-фтор-4-2-фторбензил)(метил)амино)-1-(4-метилбензил)пиримидин-2(1H)-он (119,7 мг, 77%) в виде бесцветного масла: 1H ЯМР (400 МГц, ДМСО-d6)8,16 (д, J=9,5 Гц, 1H), 7,45-7,06 (м, 8H), 4,83 (с, 2H), 4,79 (с, 2H), 3,13 (д,J=3,3 Гц, 3H), 2,27 (с, 3H); 13 С ЯМР (101 МГц, ДМСО-d6)160,1 (д, J=244,4 Гц), 154,9 (д, J=7,1 Гц),152,9, 136,8, 136,2 (д, J=243,2 Гц), 134,2, 132,8 (д, J=37,3 Гц), 129,2 (д, J=8,2 Гц), 129,0, 128,7, 127,8, 124,6A) К раствору пентасульфида фосфора (102,6 г, 0,46 моль) в диглиме (1 л) добавляли 5-фторпиримидин-2,4(1 Н,3H)-дион (30 г, 0,23 моль). Со скоростью, определяемой выделением диоксида углерода,добавляли твердый гидрокарбонат натрия (NaHCO3; 77,3 г, 1,04 моль). Реакционную смесь перемешивали на протяжении ночи при 110C. Желтую смесь охлаждали и выливали в 1 л холодной воды. Осажденный твердый продукт выделяли фильтрованием и очищали хроматографией на нормальной фазе (градиент 10-50% EtOAc/петролейный эфир), получая при этом 5-фтор-4-тиоксо-3,4-дигидропиримидин-2(1H)он (13,4 г, 40%) в виде желтого твердого вещества: т.пл. 254-255C; 1H ЯМР (301 МГц, ДМСО-d6)7,81B) Это вещество получали процедурой, описанной в Tetrahedron (1985, 41, 5289-5293). К раствору 5-фтор-4-тиоксо-3,4-дигидропиримидин-2(1H)-она (12,4 г, 84,9 ммоль) и метоксида натрия (4,54 г, 84,9 ммоль) в MeOH (100 мл) по каплям добавляли аллилбромид (10,27 г, 84,9 ммоль) при комнатной температуре. Реакционную смесь перемешивали на протяжении ночи при комнатной температуре. После удаления растворителя остаток очищали хроматографией на нормальной фазе (градиент 10-33%EtOAc/гексан), получая при этом 4-(аллилтио)-5-фторпиримидин-2(1H)-он (6 г, 38%) в виде белого твердого вещества: т.пл. 150-152C; 1H ЯМР (301 МГц, ДМСО-d6)11,60 (с, 1H), 8,00 (д, J=4,5 Гц, 1H), 5,90C) Это вещество получали процедурой, описанной в J. Org. Chem. (2006, 71, 9183-9190). К перемешиваемой суспензии сухого Cu(ОАс)2 (1,02 г, 5,64 ммоль), 4-(аллилтио)-5-фторпиримидин-2(1H)-она(700 мг, 3,76 ммоль), тиофен-3-илбороновой кислоты (962 мг, 7,52 ммоль) и активированных молекулярных сит 3 (2 г) в сухом CH2Cl2 (30 мл) добавляли пиридин (595 мг, 7,52 ммоль) при комнатной температуре. Смесь перемешивали в течение 24 ч при температуре окружающей среды в присутствии воздуха. Реакционную смесь разбавляли CH2Cl2 (30 мл), фильтровали через подушку целита и промывали водой(50 мл) в присутствии этилендиаминтетрауксусной кислоты (EDTA; 700 мг, 2,4 ммоль). Бесцветную органическую фазу сушили над MgSO4 и концентрировали в вакууме. Остаток очищали хроматографией на нормальной фазе (элюирование постоянно смесью 2:1 петролейный эфир:EtOAc), получая при этом 4- 16022069(аллилтио)-5-фтор-1-(тиофен-3-ил)пиримидин-2(1H)-он (290 мг, 29%) в виде желтого твердого вещества: т.пл. 125-127C; 1H ЯМР (301 МГц, ДМСО-d6)8,52-8,35 (м, 1H), 7,81 (с, 1H), 7,69-7,55 (м, 1H), 7,32 (д,J=3,5 Гц, 1H), 6,05-5,81 (м, 1H), 5,36 (д, J=16,9 Гц, 1H), 5,18 (д, J=9,8 Гц, 1H), 3,89 (д, J=6,4 Гц, 2H); ESIMS m/z 269 ([M+H]+).D) Это вещество получали процедурой, описанной в J. Org. Chem. (2006, 71, 9183-9190). 4-(Аллилтио)-5-фтор-1-(тиофен-3-ил)пиримидин-2(1H)-он (330 мг, 1,23 ммоль) растворяли в растворе аммиака в метаноле (7 н, 5 мл). Реакционную смесь перемешивали на протяжении ночи при 100C в автоклаве. После удаления растворителя остаток очищали препаративной тонкослойной хроматографией, получая при этом 4-амино-5-фтор-1-(тиофен-3-ил)пиримидин-2(1H)-он (177 мг, 68%) в виде желтого твердого вещества: т. пл. 228-229C; 1H ЯМР (300 МГц, ДМСО-d6)8,11 (д, J=6,9 Гц, 1H), 7,89 (с, 1H), 7,65 (д,J=1,9 Гц, 2H), 7,56 (дд, J=5,1, 3,3 Гц, 1H), 7,29 (дд, J=5,1, 1,0 Гц, 1H); ESIMS m/z 212 ([M+H]+). Соединения 40-55 получали, как описано в примере 17. Пример 18. Получение (Е)-N'-(5-фтор-2-оксо-1-(тиофен-3-ил)-1,2-дигидропиримидин-4-ил)-N,N-диметилформимидамида (56) 4-Амино-5-фтор-1-(тиофен-3-ил)пиримидин-2(1H)-он (140 мг, 0,66 ммоль) растворяли в ДМФАDMA (5 мл). Реакционную смесь перемешивали при кипячении с обратным холодильником на протяжении ночи. Остаточный растворитель ДМФА-DMA удаляли в вакууме и остаток очищали препаративной тонкослойной хроматографией, получая при этом (Е)-N'-(5-фтор-2-оксо-1-(тиофен-3-ил)-1,2-дигидропиримидин-4-ил)-N,N-диметилформимидамид (75 мг, 43%) в виде желтого твердого вещества: т.пл. 211213C; 1H ЯМР (300 МГц, ДМСО-d6)8,73 (с, 1H), 8,22 (д, J=6,4 Гц, 1H), 7,75 (дд, J=3,2, 1,4 Гц, 1H), 7,60(1 мл) добавляли (2-фторфенил)метанамин (50 мг, 0,186 ммоль). Реакционную смесь нагревали при 100C в течение 30 мин в микроволновой печи. После охлаждения смесь очищали препаративной тонкослойной хроматографией,получая при этом 5-фтор-4-(2-фторбензиламино)-1-(тиофен-3 ил)пиримидин-2(1H)-он (41 мг, 20%) в виде белого твердого вещества: т.пл. 75-78C; 1H ЯМР (300 МГц,ДМСО-d6)8,70 (с, 1H), 8,16 (д, J=7,0 Гц, 1H), 7,66 (дд, J=3,2, 1,4 Гц, 1H), 7,57 (дд, J=5,2, 3,2 Гц, 1H),7,43-7,13 (м, 5H), 4,63 (д, J=5,5 Гц, 2H); ESIMS m/z 320 ([M+H]+). Соединения 66-73 получали, как описано в примере 19. Пример 20. Получение 4-амино-1-(циклопропилметил)-5-фторпиримидин-2(1H)-она (74) К раствору (бромметил)циклопропана (1,0 г, 7,4 ммоль) в ДМФА (20 мл) добавляли молекулярные сита (2 г) и образовавшуюся смесь перемешивали при комнатной температуре. Спустя 1 ч добавляли 4 амино-5-фторпиримидин-2-ол (1,9 г, 14,8 ммоль) и K2CO3 (5,1 г, 37 ммоль) и реакционную смесь нагревали при 90C в течение 12 ч. После охлаждения до комнатной температуры сырую реакционную смесь фильтровали через воронку Бюхнера и твердый остаток промывали EtOAc. Собранный фильтрат концентрировали в вакууме, получая при этом остаток, который очищали хроматографией на нормальной фазе(5% MeOH/EtOAc, постоянно). После перекристаллизации из метил-трет-бутилового простого эфира 4 амино-1-(циклопропилметил)-5-фторпиримидин-2(1H)-он (1,12 г, 83%) выделяли в виде белого твердого вещества: т.пл. 224-226C; 1H ЯМР (400 МГц, метанол-d4)7,86 (д, J=6,2 Гц, 1H), 3,61 (д, J=7,2 Гц, 2H),1,24 (ддд, J=12,8, 7,6, 4,8 Гц, 1H), 0,65-0,50 (м, 2H), 0,39 (кв, J=4,8 Гц, 2H); ESIMS m/z 184 ([M+H]+). Соединения 75-79 получали, как описано в примере 20.CH2Cl2 (0,90 мл) и пиридине (172,4 мг, 2,18 ммоль) при комнатной температуре и затем охлаждали до-20C. Затем к реакционной смеси по каплям добавляли этилхлорформиат (166 мг, 1,53 ммоль), поддерживая температуру реакции между -20 и -5C. После завершения добавления реакционной смеси давали возможность медленно нагреваться до комнатной температуры и перемешивали в течение 2 ч. Реакционную смесь фильтровали и твердое вещество промывали EtOAc (15 мл 3). Фильтрат концентрировали в вакууме и очищали препаративной тонкослойной хроматографией, получая при этом этил-1-(циклопропилметил)-5-фтор-2-оксо-1,2-дигидропиримидин-4-илкарбамат (70 мг, 30%) в виде бледно-желтого твердого вещества: т.пл. 90-92C; 1H ЯМР (400 МГц, метанол-d4)8,20 (с, 1H), 4,26 (кв, J=7,1 Гц, 2H),3,70 (д, J=7,2 Гц, 2H), 1,24-1,36 (м, 4H), 0,65-0,57 (м, 2H), 0,46-0,39 (м, 2H); ESIMS m/z 256 ([M+H]+). Соединения 81-84 получали, как описано в примере 21. Пример 22. Получение 1-(2-хлорфенил)-3-(1-(циклопропилметил)-5-фтор-2-оксо-1,2-дигидропиримидин-4-ил)мочевины (85) К перемешиваемому раствору 4-амино-1-(циклопропилметил)-5-фторпиримидин-2(1H)-она (150 мг,0,819 ммоль) в сухом CH3CN (7,5 мл) при комнатной температуре и в атмосфере азота добавляли 2 хлорфенилизоцианат (138,3 мг, 0,90 ммоль). После перемешивания в течение 1 ч сырую реакционную смесь фильтровали и твердые вещества промывали CH3CN (10 мл). Собранный фильтрат затем концентрировали в вакууме и сушили в высоком вакууме, получая при этом 1-(2-хлорфенил)-3-(1(циклопропилметил)-5-фтор-2-оксо-1,2-дигидропиримидин-4-ил)мочевину (160 мг, 58%) в виде не совсем белого твердого вещества: т.пл. 197-199C; 1H ЯМР (400 МГц, метанол-d4)8,26 (д, J=6,0 Гц, 1H),8,21 (дд, J=8,3, 1,5 Гц, 1H), 7,47 (дд, J=8,0, 1,4 Гц, 1H), 7,35-7,28 (м, 1H), 7,13 (тд, J=7,8, 1,5 Гц, 1H), 3,74 Это соединение получали процедурой, описанной в J. Org. Chem. (2005, 70, 7459-7467). К раствору 4-амино-5-фтор-1-тетрагидрофуран-2-ил)метил)пиримидин-2(1H)-она (200 мг, 0,94 ммоль) в сухом ТГФ (1 мл) при комнатной температуре добавляли 1-этил-3-(3-диметиламинопропил)карбодиимид (EDC; 180 мг, 0,94 ммоль) и 1 Н-бензо[d][1,2,3]триазол-1-ол (HOBt; 139 мг, 1,03 ммоль). После перемешивания в течение 10 мин добавляли тиофен-2-карбоновую кислоту (145 мг, 1,13 ммоль) и образовавшемуся раствору предоставляли возможность для перемешивания при комнатной температуре в течение 12 ч. Реакционную смесь концентрировали в вакууме, гасили насыщенным водным раствором NaHCO3 (10 мл) и экстрагировали EtOAc (25 мл 3). Объединенные экстракты промывали насыщенным водным раствором хлорида натрия (NaCl), сушили над Na2SO4, фильтровали и концентрировали роторным испарением. Очистка хроматографией на нормальной фазе (градиент 0-2% MeOH/CH2Cl2), получая при этом 4-амино 5-фтор-1-тетрагидрофуран-2-ил)метил)пиримидин-2(1H)-он (60 мг, 20%) в виде белого твердого вещества: т.пл. 168-170C; 1 Н ЯМР (400 МГц, CDCl3)12,96 (с, 1H), 7,96 (д, J=3,7 Гц, 1H), 7,63 (д, J=5,7 Гц,1H), 7,60 (д, J=4,9 Гц, 1H), 7,16-7,11 (м, 1H), 4,20-4,08 (м, 2H), 3,89 (дд, J=15,1, 6,9 Гц, 1H), 3,80 (дд,J=14,5, 7,5 Гц, 1H), 3,57 (дд, J=14,4, 7,7 Гц, 1H), 2,10 (дт, J=12,8, 6,7 Гц, 1H), 1,99-1,87 (м, 2H), 0,88 (м,1H); ESIMS m/z 324 ([М+Н]+). Соединения 95-101 получали, как описано в примере 23. Это соединение получали процедурой, описанной в J. Org. Chem. (2005, 70, 7459-7467). К раствору 4-амино-5-фтор-1-тетрагидрофуран-2-ил)метил)пиримидин-2(1H)-она (160 мг, 0,495 ммоль) в ТГФ (4 мл) при комнатной температуре добавляли по каплям BSA (0,61 мл, 2,47 ммоль). После завершения добавления по каплям добавляли комплекс боран-N,N-диизопропилэтиламин (DIPEABH3; 0,90 мл, 4,95 мл) и образовавшийся раствор перемешивали при комнатной температуре в течение 15 мин. Реакционную смесь гасили добавлением MeOH (20 мл) и смесь концентрировали в вакууме. Образовавшуюся смесь растворяли в смеси 1:1 (об.:об.) 17% аммиак в метаноле:28% аммиак в воде (135 мл) и нагревали при 50C в течение 13 ч. После охлаждения до комнатной температуре смесь экстрагировали хлороформом(CHCl3; 100 мл 2). Объединенные экстракты промывали водным раствором NaCl, сушили над Na2SO4,фильтровали и концентрировали в вакууме. Очистка препаративной тонкослойной хроматографией давала 5-фтор-1-тетрагидрофуран-2-ил)метил)-4-(тиофен-2-илметиламино)пиримидин-2(1H)-он (40 мг,26%) в виде смолистого белого твердого вещества: 1 Н ЯМР (400 МГц, ацетон-d6)7,69 (д, J=6,7 Гц, 1H),7,52 (с, 1H), 7,32 (дд, J=5,1, 1,2 Гц, 1H), 7,08 (дд, J=3,4, 0,9 Гц, 1H), 6,95 (дд, J=5,1, 3,5 Гц, 1H), 4,85 (д,J=6,0 Гц, 2H), 4,12 (ддд, J=14,6, 7,1, 3,2 Гц, 1H), 4,00 (дд, J=13,6, 2,8 Гц, 1H), 3,83 (дт, J=8,1, 6,7 Гц, 1H),3,72-3,64 (м, 1H), 3,56 (дд, J=13,6, 7,7 Гц, 1H), 2,02-1,93 (м, 1H), 1,86 (ддд, J=11,0, 8,1, 1,6 Гц, 2H), 1,671,54 (м, 1H); ИК (тонкая пленка) 3222, 3125, 3068, 2950, 2875, 1673, 1623, 1586, 1556, 1508, 1368, 1329,1186, 1139, 1065, 906 см-1; ESIMS m/z 310 ([M+H]+). Соединения 103 и 104 получали, как описано в примере 24. Пример 25. Получение 5-фтор-4-(2-фторбензиламино)-1-изобутилпиримидин-2(1H)-она (105)A) К раствору 5-фторпиримидин-2,4(1 Н,3H)-диона (5,0 г, 38 ммоль) и 1,8-диазабицикло[5.4.0]ундец-7-ена (DBU; 6,4 г, 42 ммоль) в сухом CH3CN (150 мл) при комнатной температуре в атмосфере азота добавляли по каплям 1-бром-2-метилпропан (5,3 г, 38 ммоль). Реакционную смесь затем нагревали для кипячения с обратным холодильником в течение 18 ч. После охлаждения до комнатной температуры растворитель удаляли в вакууме. Сырой остаток очищали хроматографией на нормальной фазе (градиент 0-20% EtOAc/петролейный эфир), получая при этом 5-фтор-1-изобутилпиримидин-2,4(1 Н,3H)-дион (2,5 г, 35%) в виде белого твердого вещества: т.пл. 173-174C; 1H ЯМР (400 МГц, CDCl3)8,61 (с, 1H), 7,21CH3CN (53 мл) в атмосфере азота при комнатной температуре. Смесь охлаждали до 0C, после чего по каплям добавляли триэтиламин (Et3N; 9,5 г, 92 ммоль) с последующим добавлением раствора 5-фтор-1 изобутилпиримидин-2,4(1 Н,3H)-диона (2,0 г, 11 ммоль) в CH3CN (30 мл). После перемешивания в течение 1 ч при комнатной температуре добавляли Et3N (3,6 г, 36 ммоль) и затем воду (5 мл, 280 ммоль) и реакционную смесь перемешивали в течение дополнительных 10 мин. Сырую реакционную смесь затем концентрировали в вакууме. Перекристаллизация из смеси EtOAc/петролейный эфир давала 5-фтор-1 изобутил-4-(1 Н-1,2,4-триазол-1-ил)пиримидин-2(1H)-он (1,9 г, 74%) в виде не совсем белого кристаллического твердого вещества: т.пл. 150-153C; 1 Н ЯМР (400 МГц, CDCl3)9,26 (с, 1H), 8,23 (с, 1H), 7,84 (д,J=5,7 Гц, 1H), 3,79 (д, J=7,4 Гц, 2H), 2,28 (дт, J=13,7, 6,9 Гц, 1H), 1,02 (д, J=6,7 Гц, 6H); ESIMS m/z 238([M+H]+). С) Раствор 5-фтор-1-изобутил-4-(1 Н-1,2,4-триазол-1-ил)пиримидин-2(1H)-она (500 мг, 2,1 ммоль) и 2-фторбензиламина (313 мг, 2,5 ммоль) в сухом 1,4-диоксане (10 мл) нагревали для кипячения с обратным холодильником в течение 1 ч в атмосфере азота. После охлаждения до комнатной температуры реакционную смесь концентрировали в вакууме. Перекристаллизация из смеси EtOAc/метил-трет-бутиловый простой эфир давала 5-фтор-4-(2-фторбензиламино)-1-изобутилпиримидин-2(1H)-он (545 мг, 89%) в виде не совсем белого твердого вещества; т.пл. 118-119C; 1 Н ЯМР (400 МГц, CDCl3)7,45 (тд, J=7,6,1,7 Гц, 1H), 7,35-7,28 (м, 2H), 7,13 (ддд, J=21,9, 13,9, 7,3 Гц, 3H), 5,58 (с, 1H), 4,81 (д, J=5,4 Гц, 2H), 3,56 Пример 26. Оценка фунгицидной активности: пятнистость листьев пшеницы (Mycosphaerella graminicola; анаморф: Septoria tritici; код Байера SEPTTR). Растения пшеницы (сорт Yuma) выращивали из семян в теплице в смеси 50% минеральной поч- 29
МПК / Метки
МПК: C07D 339/02
Метки: фунгицидов, применение, 5-фторпиримидинона, качестве, производные
Код ссылки
<a href="https://eas.patents.su/30-22069-proizvodnye-5-ftorpirimidinona-i-ih-primenenie-v-kachestve-fungicidov.html" rel="bookmark" title="База патентов Евразийского Союза">Производные 5-фторпиримидинона и их применение в качестве фунгицидов</a>
Предыдущий патент: Паразитицидные композиции, содержащие несколько активных агентов, способы и их применения
Следующий патент: Получение уксусной кислоты
Случайный патент: Способ удаления нефти, нефтепродуктов и/или химических загрязнителей из жидкости и/или газа и/или с поверхности