Амфифильные оксамидные органические гелеобразователи для получения гелей на основе органических растворителей, воды и углеводородного промышленного топлива
Формула / Реферат
1. Соединение общей формулы (I)
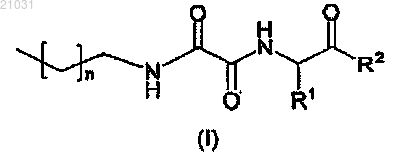
где R1 означает водород, фенил, C1-6 алкил, возможно замещенные группой R3;
R3 означает бензил или 5- или 6-членную гетероароматическую кольцевую систему, содержащую в качестве гетероатома азот, и которая по выбору дополнительно может быть замещена бензилом или гидроксилом;
R2 означает OR4, NHR4;
R4 означает водород, C1-6 алкил или бензил;
n - целое число от 1 до 12,
либо его соли.
2. Соединение по п.1, в котором
R1 означает изобутил;
R2 означает OR4, NHR4;
n - целое число от 1 до 10,
либо его соли.
3. Соединение общей формулы (I) по пп.1 и 2, в котором R2 представляет собой NH2, a n имеет значение от 2 до 10.
4. Соединение по п.2, в котором группа R2 представляет собой OR4.
5. Соединение по п.1 или 2, в котором группа R2 представляет собой ОН.
6. Соединение по п.1 или 2, в котором группа R2 представляет собой NHR4.
7. Соединение по любому из пп.1-6, в котором группа R1 представляет собой изобутильную группу.
8. Соединение по п.1, которое выбрано из следующих соединений:
N-бутилоксамидо-L-лейцин, метиловый эфир,
N-бутилоксамидо-L-лейцин,
N-бутилоксамидо-L-лейцинамид,
N-гексилоксамидо-L-лейцин, метиловый эфир,
N-гексилоксамидо-L-фенилаланин, метиловый эфир,
N-гексилоксамидо-L-лейцин,
N-гексилоксамидо-L-фенилаланин,
N-гексилоксамидо-L-лейцинамид,
N-гексилоксамид-L-фенилаланинамид,
N-додецилоксамидо-L-лейцин, метиловый эфир,
N-додецилоксамидо-L-лейцин,
N-додецилоксамидо-L-лейцинамид.
9. Способ получения соединения общей формулы (I) по п.1, включающий проведение реакции между соединениями общей формулы (II)
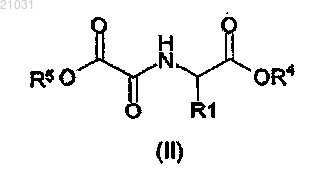
и соединениями общей формулы (V)
CH3-(CH2)n-CH2-NH2 (V)
где значения n, R1 и R4 определены в п.1, а R5 представляет собой C1-6 алкил или бензил,
для получения соединения общей формулы (Ia)

10. Способ по п.9, в котором проводят реакцию гидролиза или гидрогенолиза полученного соединения общей формулы (Ia) для получения соединений (Ib)
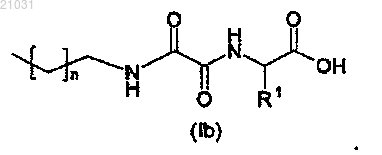
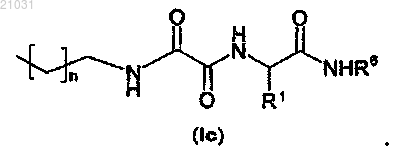
11. Способ по п.9, в котором проводят реакцию между полученными соединениями (Ia) и соединениями (VI)
R6-NH2 (VI)
для получения соединений (Ic)
12. Гель, содержащий в качестве гелеобразователя любое из соединений по п.1.
13. Гель по п.12, полученный растворением соединения по п.1 в растворителе.
14. Гель по п.13, отличающийся тем, что растворитель выбран из следующих веществ:
a) коммерческое топливо, такое как бензин или дизельное топливо;
b) органический растворитель, такой как ДМСО, ДМФА, этиловый спирт, CH3CN, ТГФ, CH2Cl2, ацетон, толуол, p-ксилол, тетралин, декалин;
с) вода или смесь воды с органическим растворителем, таким как ДМСО или ДМФА.
15. Применение соединения по п.1 для получения гелей.
16. Применение по п.15 для образования геля из промышленного топлива.
Текст
АМФИФИЛЬНЫЕ ОКСАМИДНЫЕ ОРГАНИЧЕСКИЕ ГЕЛЕОБРАЗОВАТЕЛИ ДЛЯ ПОЛУЧЕНИЯ ГЕЛЕЙ НА ОСНОВЕ ОРГАНИЧЕСКИХ РАСТВОРИТЕЛЕЙ, ВОДЫ И УГЛЕВОДОРОДНОГО ПРОМЫШЛЕННОГО ТОПЛИВА Соединения общей формулы (I) где R1 означает водород, фенил, C1-6 алкил, которые дополнительно могут быть замещены группойR3. R3 означает 5- или 6-членную ароматическую или гетероароматическую кольцевую систему,которая дополнительно может быть замещена бензильной или гидроксильной группами; R2 означает OR4, NHR4, R4 означает водород, C1-6 алкил или бензил, n - целое число от 1 до 12,либо соли упомянутых соединений, которые могут образовывать гели с промышленным топливом,органическими растворителями и водой. Область техники, к которой относится изобретение Настоящее изобретение относится к соединениям, способным к образованию гелей на основе промышленного топлива, определенных органических растворителей и воды, а также способам получения данных соединений. Изобретение также относится к гелям, образуемым данными соединениями, способам их получения и использованию гелей для различных целей. Благодаря разнообразию структур и своим физическим свойствам органические гели имеют огромный потенциал для применения в промышленности. Особый интерес данное изобретение представляет для фармацевтической промышленности при изготовлении лекарственных препаратов, для пищевой и косметической промышленности, тканевой инженерии, электрооптических/фотонных приборов, используемых в качестве сенсоров или органической матрицы при изготовлении неорганических материалов и т.д. Гелеобразование промышленного топлива и опасных органических растворителей и жидкостей может использоваться для повышения безопасности их транспортировки. Предшествующий уровень техники Исследования в области гелеобразования с использованием низкомолекулярных органических гелеобразователей в последние 15 лет привлекают повышенное внимание. Опубликован ряд работ на данную тему (П. Тереч и др. (P. Terech et al.), Chem. Rev., 97, 3133-3159 (1997 г.), Л.А. Эстофф и др. (L.A.Estoff et al.), Chem. Rev., 104, 1201-1217 (2004 г.), Ф. Фэйджес и др. (F. Fages et al.), Top. Curr. Chem., 256,77-131 (2005 г.), М. Нералагатта и др. (M. Neralagatta et al.), Chem. Soc. Rev., 34, 821-836 (2005 г.), М. де Лоос и др. (М. de Loos, et al.), Eur. J. Org. Chem. (2005 r.) 3615-3631). Первый доклад об избирательном образовании гелей на основе нефте-водяных смесей для потенциального применения при восстановлении после аварий при транспортировке нефти был сделан С. Бхаттачарией и др. (S. Bhattacharya et al.), Chem. Commun., (2001 г.) 185. В других работах описаны исследования в области образования гелей на основе промышленного топлива (Д.Р. Триведи и др. (D.R. Trivedi et al.), Chem. Mater., 18, 1470-1478 (2006 г.); Д.Р. Триведи и др.GrowthDesign. 6(9): 2114-2121, 200; М. Сузуки и др. (M. Suzuki et al.), New J.Chem., 30, 1184-1191,2006 г.; Д. Хатуа и др. (D. Khatua et al.), Langmuir 21, 109-114, 2005 г.). В нашем более раннем исследовании (В. Каплар и др. (V. Caplar et al.), Eur. J. Org. Chem., 2004 r.(19), 4048-4059) мы протестировали гелеобразующие свойства некоторых производных алкиламиноундециловой кислоты при контакте с нефтью (дизельным топливом), водой и подходящими органическими растворителями. Сущность изобретения Настоящее изобретение относится к новым амфифильным оксамидным производным, способным к образованию гелей с промышленным топливом. Кроме того, данные соединения могут образовывать гели с водой и рядом органических растворителей. Настоящее изобретение относится к соединениям с общей формулой (I) где R1 представляет собой водород, фенил, C1-6 алкил, которые дополнительно могут быть замещены R3,R3 представляет собой 5- или 6-членную ароматическую или гетероароматическую кольцевую систему, которая дополнительно может быть замещена бензильной или гидроксильной группами,R2 представляет собой OR4, NHR4,R4 представляет собой водород, C1-6 алкил или бензил,n - целое число от 1 до 12,либо соли упомянутых соединений. Органические гелеобразователи с общей формулой (I) обладают способностью к образованию гелей путем растворения соединения в растворителе и охлаждения полученного раствора до комнатной температуры. Данный процесс способствует образованию геля, что является видимым проявлением супрамолекулярной самосборки определенных органических молекул до образования наноразмерной структуры геля. Соединения с общей формулой (I), в особенности амидные производные, обладают способностью к образованию гелей при очень низких концентрациях. В настоящем изобретении термин "органический гелеобразователь" означает любое низкомолекулярное соединение (такое как соединения с общей формулой (I, способное к образованию геля на основе определенного растворителя. Соединение растворяется при нагревании, а гель образуется при охлаждении такого раствора. В настоящем описании "C1-C6 алкил" означает неразветвленные или разветвленные углеводородные цепи с количеством атомов углерода от 1 до 6. Примерами алкильной группы являются метил, этил, n-1 021031 пропил, изопропил, t-бутил, n-бутил и n-гексил. Соли соединений с общей формулой (I) включают в себя неорганические, аммиачные соли и соли замещенных аминов. Данное изобретение относится ко всем изомерам соединений, составляющих предмет настоящего изобретения, имеющим хиральный центр. Соединения с хиральным центром, составляющие предмет настоящего изобретения, могут использоваться в качестве энтантиомеров, рацемических либо энантиомерно обогащенных смесей. В настоящем описании термин "ароматическая группа" означает ароматические кольцевые системы, имеющие 5-10 атомов углерода, включенных в одно или два кольца. Примерами ароматической группы являются кольцевые системы бензола, нафталина, бифенила и т.д. Термин "гетероароматические" означает ароматические кольцевые системы из обозначенных выше,в которых один или более атомов углерода замещены атомами азота, кислорода или серы. Примерами гетероароматических кольцевых систем являются индол, пиридин, имидазол, индазол, бензимидазол,хинолин, изохинолин, бензтиазол, бензоксазол и т.д. В выбранных для исследования соединениях с общей формулой (I), взятых в отдельности или в любом сочетании, R2 представляет собой ОН или NHR4, n - целое число от 2 до 10. Выбранные соли соединений с общей формулой (I) представляют собой соли Na+ и K+. В предпочтительных соединениях с общей формулой (I) n имеет значение от 4 до 10, a R2 представляет собой NH2. Предпочтительные соли соединений общей формулы (I) представляют собой соли Na+. К особенно предпочтительным соединениям общей формулы (I) относятсяN-бутилоксамид-L-лейцин, метиловый эфир,N-бутилоксамид-L-лейцин,N-бутилоксамид-L-лейцин, натриевая соль,N-бутилоксамид-L-лейцинамид,N-гексилоксамид-L-лейцин, метиловый эфир,N-гексилоксамид-L-фенилаланин, метиловый эфир,N-гексилоксамид-L-лейцин,N-гексилоксамид-L-фенилаланин,N-гексилоксамид-L-лейцин, натриевая соль,N-гексилоксамид-L-фенилаланин, натриевая соль,N-гексилоксамид-L-лейцинамид,N-гексилоксамид-L-фенилаланинамид,N-додецилоксамид-L-лейцин, метиловый эфир,N-додецилоксамид-L-лейцин,N-додецилоксамид-L-лейцин, натриевая соль,N-додецилоксамид-L-лейцинамид. Получение предпочтительных соединений данного изобретения осуществляется по следующей схеме: Соединения общей формулы (I), где R2 означает OR4, могут представлять собой эфиры общей формулы (Ia) где R1 означает водород, фенил, C1-6 алкил, которые дополнительно могут быть замещены R3;R3 означает 5- или 6-членную ароматическую или гетероароматическую кольцевую систему, которая дополнительно может быть замещена бензильной или гидроксильной группами;n - целое число от 1 до 12. Соединения общей формулы (Ia) могут быть получены из соединений общей формулы (II) где R1 означает водород, фенил, C1-6 алкил, которые дополнительно могут быть замещены R3;R3 означает 5- или 6-членную ароматическую или гетероароматическую кольцевую систему, которая дополнительно может быть замещена бензильной или гидроксильной группами;R5 означает C1-6 алкил или бензил,путем реакции аминолиза с соединением общей формулы (V)CH3-(CH2)n-CH2-NH2 (V) где n - целое число от 1 до 12. Реакция осуществляется путем перемешивания раствора, состоящего из соединений общей формулы (II) и соединений общей формулы (V) в органическом растворителе при комнатной температуре. Соединения с общей формулой (II) могут быть получены из соединений общей формулы (IV) где R1 означает водород, фенил, C1-6 алкил, которые дополнительно могут быть замещены R3;R3 означает 5- или 6-членную ароматическую или гетероароматическую кольцевую систему, которая дополнительно может быть замещена бензильной или гидроксильной группами;R4 означает C1-6 алкил или бензил,а также из солей данных соединений (при этом соль может быть гидрохлоридом или тозилатом) путем ацилирования с использованием соединений с общей формулой (III) где R5 означает алкил или бензил. Реакция ацилирования может быть осуществлена в органических растворах путем капельного добавления раствора соединений общей формулы (III) в раствор соединений общей формулы (IV) и триэтиламина при температуре (-10)-0C. После этого полученную смесь нагревают до комнатной температуры и перемешивают в течение ночи. Соединения общей формулы (I), где R2 означает ОН, могут представлять собой соединения с общей формулой (Ib) где R1 означает водород, фенил, C1-6 алкил, которые дополнительно могут быть замещены R3;R3 означает 5- или 6-членную ароматическую или гетероароматическую кольцевую систему, которая дополнительно может быть замещена бензильной или гидроксильной группами;n - целое число от 1 до 12. Соединения общей формулы (Ib) могут быть получены из соответствующих эфиров общей формулы (Ia). Конверсия сложноэфирных групп в карбоновые кислоты может быть осуществлена любым известным способом, например путем гидролиза алкиловых эфиров раствором гидроксида лития либо путем гидрогенолиза бензиловых эфиров. В данной реакции раствор эфира гидрогенизируется над соответствующим катализатором (обычно палладий/углерод). Описание методов защиты и ее снятия можно найти, к примеру, в работе Теодора У. Грина и Питера Г.М. Уатса "Защитные группы в органическом синтезе" (Theodor W. Green, Peter G.M. Wuts, Protecting Groups in Organic Synthesis), опубликованнойJohn WileySons Inc. Соединения общей формулы (I), где R2 - это NHR6, могут быть представлены как соединения общей формулы (Ic) где R1 означает водород, фенил, C1-6 алкил, которые в дальнейшем могут быть замещены R3;R3 означает 5- или 6-членную ароматическую или гетероароматическую кольцевую систему, которая дополнительно может быть замещена бензильной или гидроксильной группами;n - целое число от 1 до 12. Соединения с общей формулой (Ic) можно получить из соответствующих эфиров общей формулы(Ia) путем реакции аминолиза с использованием соединений общей формулы (VI)R6-NH2 (VI) 6 где R означает водород, C1-6 алкил или бензил. Конверсия сложноэфирных групп в карбамоильную группу может быть осуществлена известными способами, например посредством проведения реакции с насыщенным NH3/MeOH либо раствором замещенных аминов. Соединения общей формулы (I) обладают способностью к образованию гелей при нагревании в подходящем растворителе с последующим охлаждением до комнатной температуры. В качестве альтернативы гель может быть получен путем растворения органического гелеобразователя в одном органическом растворителе с последующим смешиванием полученного раствора с другим растворителем. Таким образом, настоящее изобретение относится также к гелям, образованным соединениями общей формулы (I) или их солью, смешанной с растворителями. Изобретение также относится к способам получения таких гелей из соединений формулы (I) или их соли и растворителей, а также использованию данных гелей в различных целях. В качестве растворителей могут быть использованы промышленное топливо, такое как бензин, дизельное топливо и т.д. Кроме того, такие растворители, как Н 2 О, или органические растворители, такие как DMSO, DMF, EtOH, CH3CN, THF, CH2Cl2, ацетон, толуол, p-ксилол, тетралин, декалин или их смеси. Сведения, подтверждающие возможность осуществления изобретения Химический синтез соединений с общей формулой (I) Общая информация. Были приобретены реагенты производства Aldrich (Олдрич), Fluka (Флюка), Kemika (Кемика),Merck (Мерк) и Sigma (Сигма), которые были использованы без предварительной очистки. Все растворы были очищены и высушены стандартными методами. Наблюдение за ходом реакции производили при помощи тонкослойной хроматографии (ТСХ) на пластинах Merck Kieselgel HF254, результаты реакции визуализировали посредством УФ-лампы (254 нм) или паров I2. Полученные соединения подвергали хроматографической очистке посредством препаративной ТСХ с использованием силикагеля MerckHF254 и посредством колончатой хроматографии с использованием двуокиси кремния 0,063-0,2 мм(Merck). Выход реакции не был оптимизирован. Спектры ЯМР были записаны при помощи спектрометраBruker Avance с частотой 300/75 МГц, с использованием тетраметилсилана (ТМС) в качестве внутреннего стандарта. Химические сдвигиданы в частях на миллион (ppm), константы связи (J) - в Гц. Спиновые мультиплетности: s (синглет), d (дублет), t (триплет), q (квадруплет), р (пентет) и m (мультиплет). ИК-спектры показаны при использовании таблеток бромида калия на ИК-Фурье спектрометре ABBBomen MB 102, волновые числа (v) выражены в см-1. Оптическое вращение измеряли при помощи автоматического поляриметра Optical Activity AA-10 в кювете 1 дм при 569 нм; значения концентрации указаны в г/100 мл. 1. Общая методика получения N-алкил-N'-L-метиллейцил (фенилаланил) оксамидов (Ia)a) Получение метилового эфира N-(этоксиокеалил)-L-лейцина (фенилаланина) (II). В охлажденный (0C) раствор гидрохлорида аминокислоты IV (1 ммоль) и триэтиламина (2 ммоль) в сухом CH2Cl2 (10 мл) в течение 15 мин капельно добавляли раствор оксалилхлорида III в сухом CH2Cl2(5 мл). Реакционную смесь перемешивали в течение 30 мин при температуре 0C и в течение 20 ч при комнатной температуре. После этого добавили CH2Cl2 (10 мл) и смесь промывали последовательно 5%HCl, 5% NaHCO3 и водой. Органический слой высушивали над Na2SO4, растворитель удаляли под вакуумом. Полученный таким образом эфир II был использован без дополнительной очистки.b) В раствор метилового эфира N-(этоксиоксалил)-L-лейцина (фенилаланина) (II) в сухом CH2Cl2 добавили алкиламид V, после чего реакционную смесь перемешивали в течение 3 суток при комнатной температуре. Продукт реакции очищали путем кристаллизации (CH2Cl2 - петролейный эфир) или препаративной тонкослойной хроматографии (EtOAc - петролейный эфир, 100:25). Пример 1. Метиловый эфир N-бутилоксамид-L-лейцина (1) Молекулярный вес = 272,35. Молекулярная формула = C13H24N2O4. К раствору метилового эфира N-(этоксиоксалил)-L-лейцина (II) (0,270 г, 1,01 ммоль) в сухомCH2Cl2 (10 мл) добавили n-бутиламин (0,110 мл, 1,113 ммоль), после чего реакционную смесь перемешивали в течение 3 суток при комнатной температуре. Продукт реакции подвергали очистке путем кристаллизации (CH2Cl2 - петролейный эфир) или препаративной тонкослойной хроматографии (EtOAc - петролейный эфир, 200:50). Выход: 78,7%; []D = -13 (с 1, CH2Cl2); Молекулярный вес = 300,40. Молекулярная формула = C15H28N2O4. К раствору метилового эфира N-этоксиоксалил-L-лейцина (II) (1,066 г, 4,346 ммоль) в сухом CH2Cl2(40 мл) добавили n-гексиламин (0,64 мл, 4,968 ммоль), после чего реакционную смесь перемешивали в течение 3 суток при комнатной температуре. Продукт реакции подвергали очистке путем кристаллизации (CH2Cl2 - петролейный эфир) или препаративной тонкослойной хроматографии (EtOAc - петролейный эфир, 200:50). Выход: 70%; []D = -12 (с 1, CH2Cl2); 1 Н NMR (DMSO-d6):8,93 (1 Н, d, J=8,4, NHLeu), 8,76 (1 Н, t, J=5,8, NHhexyl), 4,36 (1 Н, ddd, J=3,5,J=8,4, J=10,6, CH, Leu), 3,63 (3H, s, OCH3), 3,16-3,08 (2H, m, CH2N), 1,86-1,77, 1,59-1,50, 1,49-1,41, 1,311,18 (1H, 2H, 2H, 2H и 4H, 4m, CH, Leu, CH2(, Leu);CH2, hexyl), 0,88, 0,84 (6H, 2d, J=5,9, CH3(, Leu, 0,86 (3H, t,J=6,9, CH3, hexyl),13 Молекулярный вес = 334,42. Молекулярная формула = C18H26N2O4. К раствору метилового эфира N-(этоксиоксалил)-L-фенилаланина (II) (4,900 г, 17,544 ммоль) в сухом CH2Cl2 (60 мл) добавили n-гексиламин (2,32 мл, 17,562 ммоль), после чего реакционную смесь перемешивали в течение 3 суток при комнатной температуре. Продукт реакции подвергали очистке путем препаративной тонкослойной хроматографии (EtOAc - петролейный эфир, 200:50). Выход: 75%; 1 Молекулярный вес = 384,56. Молекулярная формула = C21H40N2O4. К раствору метилового эфира N-(этоксиоксалил)-L-лейцина (II) (0,372 мл, 1,517 ммоль) в сухомCH2Cl2 (20 мл) добавили n-додециламин (0,35 мл, 1,522 ммоль), после чего реакционную смесь перемешивали в течение 3 суток при комнатной температуре. Продукт реакции подвергали очистке путем кристаллизации (CH2Cl2 - петролейный эфир) или препаративной тонкослойной хроматографии (EtOAc петролейный эфир, 200:50). Выход: 70,3%; []D = -9,5 (с 1, CH2Cl2);(CH2(, Leu), CH2Ndodecyl), 31,8; 29,51; 29,47; 29,45; 29,42; 29,17; 29,14; 29,10; 26,8; 22,5 (CH2, dodecyl), 24,8; 23,3; 21,5 (CH, Leu, CH3, , Leu), 14,4 (CH3, dodecyl); ИК: 3300, 1750, 1656, 1524. Общая методика получения N-алкил, N'-L-лейцилоксамидов (Ib). К раствору эфира Ia в МеОН и CH2Cl2 добавили 1N LiOH, после чего раствор перемешивали при комнатной температуре в течение ночи. Растворитель выпарили, остаток растворили в Н 2 О, после чего раствор подкислили 1N HCl. Продукт реакции экстрагировали EtOAc, органический слой промывали Н 2 О и сушили с Na2SO4. Для получения твердого продукта растворитель выпаривали под вакуумом. Пример 5. N-бутилоксамид-L-лейцин (2) Молекулярный вес = 258,32. Молекулярная формула = C12H22N2O4. К раствору метилового эфира N-бутилоксамид-L-лейцина (1) (0,247 г, 0,907 ммоль) в МеОН (3 мл) и CH2Cl2 (1 мл) добавили 1N LiOH (1,4 мл), после чего раствор перемешивали при комнатной температуре в течение ночи. Растворитель выпарили, остаток растворили в Н 2 О, после чего раствор подкислили 1NHCl. Продукт реакции экстрагировали EtOAc и органический слой промывали Н 2 О и высушивали сNa2SO4. Для получения твердого продукта растворитель выпаривали под вакуумом. Выход: 92,2%; []D = Молекулярный вес = 286,37. Молекулярная формула = C14H26N2O4. К раствору метилового эфира N-гексилоксамид-L-лейцина (5) (0,378 г, 1,258 ммоль) в МеОН (2,5 мл) и CH2Cl2 (1 мл) добавили 1N LiOH (1,9 мл), после чего раствор перемешивали при комнатной температуре в течение ночи. Растворитель выпарили, остаток растворили в Н 2 О, после чего раствор подкислили 1N HCl. Продукт реакции экстрагировали EtOAc и органический слой промывали Н 2 О и высушивали с Na2SO4. Для получения твердого продукта растворитель выпаривали под вакуумом. Выход: 99%; []D = Молекулярный вес = 320,39. Молекулярная формула = C17H24N2O4. К раствору метилового эфира N-гексилоксамид-L-фенилаланина (6) (0,043 г, 0,129 ммоль) в МеОН(1 мл) и CH2Cl2 (0,2 мл) добавили 1N LiOH (0,2 мл), после чего раствор перемешивали при комнатной температуре в течение ночи. Растворитель выпарили, остаток растворили в Н 2 О, после чего раствор подкислили 1N HCl. Продукт реакции экстрагировали EtOAc и органический слой промывали Н 2 О и высушивали с Na2SO4. Для получения твердого продукта растворитель выпаривали под вакуумом. Выход: 60,6%; 1 Молекулярный вес = 370,54. Молекулярная формула = C20H38N2O4. К раствору метилового эфира N-додецилоксамид-L-лейцина (13) (0,345 г, 0,097 ммоль) в МеОН (2,5 мл) и CH2Cl2 (0,7 мл) добавили 1N LiOH (1,4 мл), после чего раствор перемешивали при комнатной температуре в течение ночи. Растворитель выпарили, остаток растворили в Н 2 О, после чего раствор подкислили 1N HCl. Продукт реакции экстрагировали EtOAc и органический слой промывали Н 2 О и высушивали с Na2SO4. Для получения твердого продукта растворитель выпаривали под вакуумом. Выход: 99%;[]D= -9 (с 1, CH2Cl2); 1 Н NMR (DMSO-d6):12,79 (1 Н, s br, COOH), 8,77 (1 Н, t, J=6,0, NHdodecyl), 8,71 (1H, d, J=8,6, NHLeu),4,27 (1H, ddd, J=10,0, J=8,6, J=3,5, CH, Leu), 3,12 (2H, q, J=6,7, CH2N), 1,87-1,12 (23H, m, CH, Leu,CH2(, Leu), CH2, dodecyl), 0,90-0,82 (9H, m, CH3(, Leu) и СН 3, dodecyl),13 С NMR (DMSO-d6):173,6 (COOH), 160,6, 159,9 (CON), 50,9 (CH, Leu), 39,6, 39,3 (CH2(, Leu),CH2, dodecyl), 31,8; 29,51; 29,48; 29,46; 29,43; 29,18; 29,15; 29,12; 26,8; 22,6 (CH2, dodecyl), 24,9 (CH), 23,4; 21,5 (CH3(, Leu, 14,4 (CH3, dodecyl),ИК: 3313, 1745, 1656, 1519. Общая методика получения N-алкил,N'-L-лейциламидоксамидов (Ic) Раствор эфира (Ia) в CH2Cl2 и концентрированном NH3/МеОН выдерживали в течение 7 дней при температуре 4-8C. Осадок отфильтровывали, промывали МеОН и высушивали либо выпаривали под вакуумом. Пример 9. N-бутилоксамид-L-лейциламид (4) Молекулярный вес = 272,35. Молекулярная формула = C13H24N2O4. Раствор метилового эфира N-бутилоксамид-L-лейцина (1) (0,380 г, 1,395 ммоль) в CH2Cl2 (1 мл) и конц. NH3/MeOH (35 мл) выдерживали в течение 7 дней при температуре 4-8C. Осадок отфильтровывали, промывали МеОН. Выход: 89%; 1 Н NMR (DMSO-d6):8,78 (1 Н, t, J=6,0, NHbutyl), 8,36 (1 Н, d, J=9,0, NHLeu), 7,48, 7,11 (21H, 2s,CONH2), 4,28 (1H, dt, J=9,3, J=4,0, CH, Leu), 3,21-3,04 (2H, m, CH2N), 1,72-1,14 (7H, m, CH, CH2(, Leu),CH2, butyl), 0,96-0,71 (9H, m, CH3(, Leu) и CH3, butyl); 13 Молекулярный вес = 285,39. Молекулярная формула = C14H27N3O3. Раствор метилового эфира N-гексилоксамид-L-лейцина (5) (0,375 г, 1,248 ммоль) в CH2Cl2 (1 мл) и конц. NH3/MeOH (30 мл) выдерживали в течение 7 дней при температуре 4-8C. Осадок отфильтровывали, промывали МеОН. Выход: 86,2%; 1 Н NMR (DMSO-d6):8,78 (1 Н, t, J=6,0, NHhexyl), 8,37 (1 Н, d, J=9,0, NHLeu), 7,48, 7,11 (21H, 2s,CONH2), 4,28 (1H, dt, J=9,2, J=3,9, CH, Leu), 3,17-3,07 (2H, m, CH2N), 1,72-1,14 (11H, m, CH, CH2(, Leu),CH2, hexyl), 0,92-0,80 (9H, m, CH3(, Leu) и CH3, hexyl); 13 С NMR (DMSO-d6):173,6 (CONH2), 160,05, 159,99 (CON), 51,8 (CH, Leu), 41,4, 39,4 (CH2(, Leu),CH2, hexyl), 31,4; 29,1, 26,4; 22,5 (CH2, hexyl), 24,8 (CH, Leu), 23,5, 21,9 (CH3(, Leu, 14,3 (CH2, hexyl),ИК: 3432, 3385, 3287, 3208, 1685, 1652, 1515. Пример 11. N-гексилоксамид-L-фенилаланинамид (12) Молекулярный вес = 319,41. Молекулярная формула = C17H25N3O3. Раствор метилового эфира N-гексилоксамид-L-фенилаланина (6) (0,023 г, 0,0658 ммоль) в CH2Cl2(0,5 мл) и конц. NH3/MeOH (5 мл) выдерживали в течение 7 дней при температуре 4-8C. Осадок отфильтровывали, промывали МеОН. Выход: 80,9%; 1 Н NMR (DMSO-d6):8,67 (1 Н, t, J=5,9, NHhexyl), 8,37 (1H, d, J=8,7, NHPhe), 7,58, 7,25 (2H, 2s,CONH2), 7,28-7,13 (5H, m, CHarom), 4,47 (1H, dt, J=4,5, J=8,9, CH, Phe), 3,13-3,03 (4H, m, CH2N и Молекулярный вес = 369,55. Молекулярная формула = C20H39N3O3. Раствор метилового эфира N-додецилоксамид-L-лейцина (13) (0,375 г, 0,975 ммоль) в CH2Cl2 (1 мл) и конц. NH3/МеОН (25 мл) выдерживали в течение 7 дней при температуре 4-8C. Осадок отфильтровывали, промывали МеОН. Выход: 81,3%; 1 Н NMR (DMSO-d6):8,78 (1 Н, t, J=5,9, NHdodecyl), 8,36 (1 Н, d, J=9,1, NHLeu), 7,49, 7,11 (21H, 2s,CONH2), 4,28 (1H, dt, J=9,1, J=3,8, CH, Leu), 3,18-3,02 (2H, m, CH2N), 1,72-1,09 (23H, m, CH, CH2(, Leu),CH2, decyl), 0,91-0,81 (9H, m, CH3(, Leu) и CH3,dodecyl); 13(CH3(, Leu, 14,4 (CH2, dodecyl),ИК: 3389, 3291, 3198, 1686, 1653, 1511. Исследование гелеобразующих свойств органических гелеобразователей Было проведено испытание гелеобразующих свойств соединений, представляющих собой предмет данного изобретения, в результате чего были определены минимальные концентрации для образования геля (m.g.c). Результаты приведены в табл. 1 и 2. Методика проведения испытания. Эксперименты проводили посредством растворения определенного количества взвешенного органического гелеобразователя (10 мг) в измеренном объеме выбранного растворителя. В первом случае при использовании чистого растворителя для получения раствора пробу было необходимо нагреть. Образование геля происходило в результате охлаждения раствора до комнатной температуры. Растворитель многократно добавляли порциями до исчезновения геля. Во втором случае при использовании смесей растворителя пробу (10 мл) растворяли в первом растворителе, после чего добавляли измеренный объем (0,05-0,25 мл) второго растворителя. Гель образовывался в результате нагревания полученной смеси и ее последующего охлаждения. Второй растворитель многократно добавляли порциями до исчезновения геля. Для высокоэффективных гелеобразователей было определено значение минимальной концентрации для образования геля, равное приблизительное 2 мг. Для сравнения гелеобразующих свойств и химического строения соединений были испытаны гелеобразующие свойства соединений в составе некоторых органических растворителей различной полярности, воды и промышленного топлива. Таблица 1 Максимальный объем растворителя (в мкл), из которого может образовываться гель под воздействием определенного количества (10 мг) органических гелеобразователей (амидов и солей карбоновых кислот) Таблица 2 Максимальный объем растворителя (в мкл), из которого может образовываться гель под воздействием определенного количества (10 мг) органических гелеобразователей (эфиров и карбоновых кислот) ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение общей формулы (I) где R1 означает водород, фенил, C1-6 алкил, возможно замещенные группой R3;R3 означает бензил или 5- или 6-членную гетероароматическую кольцевую систему, содержащую в качестве гетероатома азот, и которая по выбору дополнительно может быть замещена бензилом или гидроксилом;n - целое число от 1 до 12,либо его соли. 2. Соединение по п.1, в которомn - целое число от 1 до 10,либо его соли. 3. Соединение общей формулы (I) по пп.1 и 2, в котором R2 представляет собой NH2, a n имеет значение от 2 до 10. 4. Соединение по п.2, в котором группа R2 представляет собой OR4. 5. Соединение по п.1 или 2, в котором группа R2 представляет собой ОН. 6. Соединение по п.1 или 2, в котором группа R2 представляет собой NHR4. 7. Соединение по любому из пп.1-6, в котором группа R1 представляет собой изобутильную группу. 8. Соединение по п.1, которое выбрано из следующих соединений:N-бутилоксамидо-L-лейцин, метиловый эфир,N-бутилоксамидо-L-лейцин,N-бутилоксамидо-L-лейцинамид,N-гексилоксамидо-L-лейцин, метиловый эфир,N-гексилоксамидо-L-фенилаланин, метиловый эфир,N-гексилоксамидо-L-лейцин,N-гексилоксамидо-L-фенилаланин,N-гексилоксамидо-L-лейцинамид,N-гексилоксамид-L-фенилаланинамид,N-додецилоксамидо-L-лейцин, метиловый эфир,N-додецилоксамидо-L-лейцин,N-додецилоксамидо-L-лейцинамид. 9. Способ получения соединения общей формулы (I) по п.1, включающий проведение реакции между соединениями общей формулы (II) и соединениями общей формулы (V)CH3-(CH2)n-CH2-NH2 (V) где значения n, R1 и R4 определены в п.1, а R5 представляет собой C1-6 алкил или бензил,для получения соединения общей формулы (Ia) 10. Способ по п.9, в котором проводят реакцию гидролиза или гидрогенолиза полученного соединения общей формулы (Ia) для получения соединений (Ib) 11. Способ по п.9, в котором проводят реакцию между полученными соединениями (Ia) и соединениями (VI)R6-NH2 (VI) для получения соединений (Ic) 12. Гель, содержащий в качестве гелеобразователя любое из соединений по п.1. 13. Гель по п.12, полученный растворением соединения по п.1 в растворителе. 14. Гель по п.13, отличающийся тем, что растворитель выбран из следующих веществ:a) коммерческое топливо, такое как бензин или дизельное топливо;b) органический растворитель, такой как ДМСО, ДМФА, этиловый спирт, CH3CN, ТГФ, CH2Cl2,ацетон, толуол, p-ксилол, тетралин, декалин; с) вода или смесь воды с органическим растворителем, таким как ДМСО или ДМФА. 15. Применение соединения по п.1 для получения гелей. 16. Применение по п.15 для образования геля из промышленного топлива.
МПК / Метки
МПК: A61K 8/04, A61Q 19/00, C07C 233/56, A61K 9/00
Метки: топлива, воды, промышленного, гелей, растворителей, органические, получения, амфифильные, углеводородного, основе, гелеобразователи, оксамидные, органических
Код ссылки
<a href="https://eas.patents.su/14-21031-amfifilnye-oksamidnye-organicheskie-geleobrazovateli-dlya-polucheniya-gelejj-na-osnove-organicheskih-rastvoritelejj-vody-i-uglevodorodnogo-promyshlennogo-topliva.html" rel="bookmark" title="База патентов Евразийского Союза">Амфифильные оксамидные органические гелеобразователи для получения гелей на основе органических растворителей, воды и углеводородного промышленного топлива</a>
Предыдущий патент: Мембранное фильтрационное устройство и способ очистки сточных вод
Следующий патент: Морской сейсмический источник
Случайный патент: Сборная панель для домостроения и способ изготовления такой панели












