Электрохимический датчик
Номер патента: 10172
Опубликовано: 30.06.2008
Авторы: Лоуренс Натан, Джоунз Тимоти Гэрет Джон, Вайлдгуз Грегори Джордж, Маллинз Оливер Клинтон, Комптон Ричард, Цзян Ли, Пандурангаппа Малингаппагари, Мередит Эндрю
Формула / Реферат
1. Электрохимический датчик, содержащий
по меньшей мере две различные редокс-системы, чувствительные к одним и тем же частицам, причем упомянутые по меньшей мере две различные редокс-системы установлены на рабочем электроде;
электрод сравнения, электронным образом связанный с рабочим электродом; и
противоэлектрод, электронным образом связанный с рабочим электродом и электродом сравнения.
2. Датчик по п.1, в котором частицы представляют собой протоны.
3. Датчик по п.1, в котором по меньшей мере две редокс-системы имеют максимальную или пиковую редокс-реакцию при различных напряжениях.
4. Датчик по п.1, в котором рабочий электрод содержит субстрат на основе углерода.
5. Датчик по п.4, в котором рабочий электрод содержит субстрат из углеродного порошка.
6. Датчик по п.4, в котором рабочий электрод содержит субстрат на основе алмаза.
7. Датчик по п.6, в котором рабочий электрод содержит субстрат на основе многостенных нанотрубок.
8. Датчик по п.1, содержащий детектор, выполненный с возможностью измерения редокс-потенциала указанных по меньшей мере двух редокс-систем в присутствии указанных частиц и для преобразования измерений в сигнал, соответствующий концентрации указанных частиц.
9. Электрохимический датчик для определения концентрации молекулярных частиц во флюиде, содержащий
по меньшей мере две различные редокс-системы, чувствительные к упомянутым молекулярным частицам, причем упомянутые по меньшей мере две различные редокс-системы связаны с рабочим электродом;
электрод сравнения, электронным образом связанный с рабочим электродом; и
противоэлектрод, электронным образом связанный с рабочим электродом и электродом сравнения;
источник напряжения и детектор электрического тока для выполнения измерений вольтамограмм и
анализатор для детектирования относительных сдвигов в указанных измерениях вольтамограмм.
11. Скважинный инструмент для измерения характерных параметров эффлюентов в стволе скважине, содержащий электрохимический датчик по п.1.
12. Скважинный инструмент для отбора проб из пластов для измерения характерных параметров эффлюентов в стволе скважины, содержащий электрохимический датчик по п.1.
13. Скважинный инструмент для измерения характерных параметров эффлюентов в стволе скважины, содержащий электрохимический датчик по п.1, укрепленный на постоянно установленной части ствола скважины.
Текст
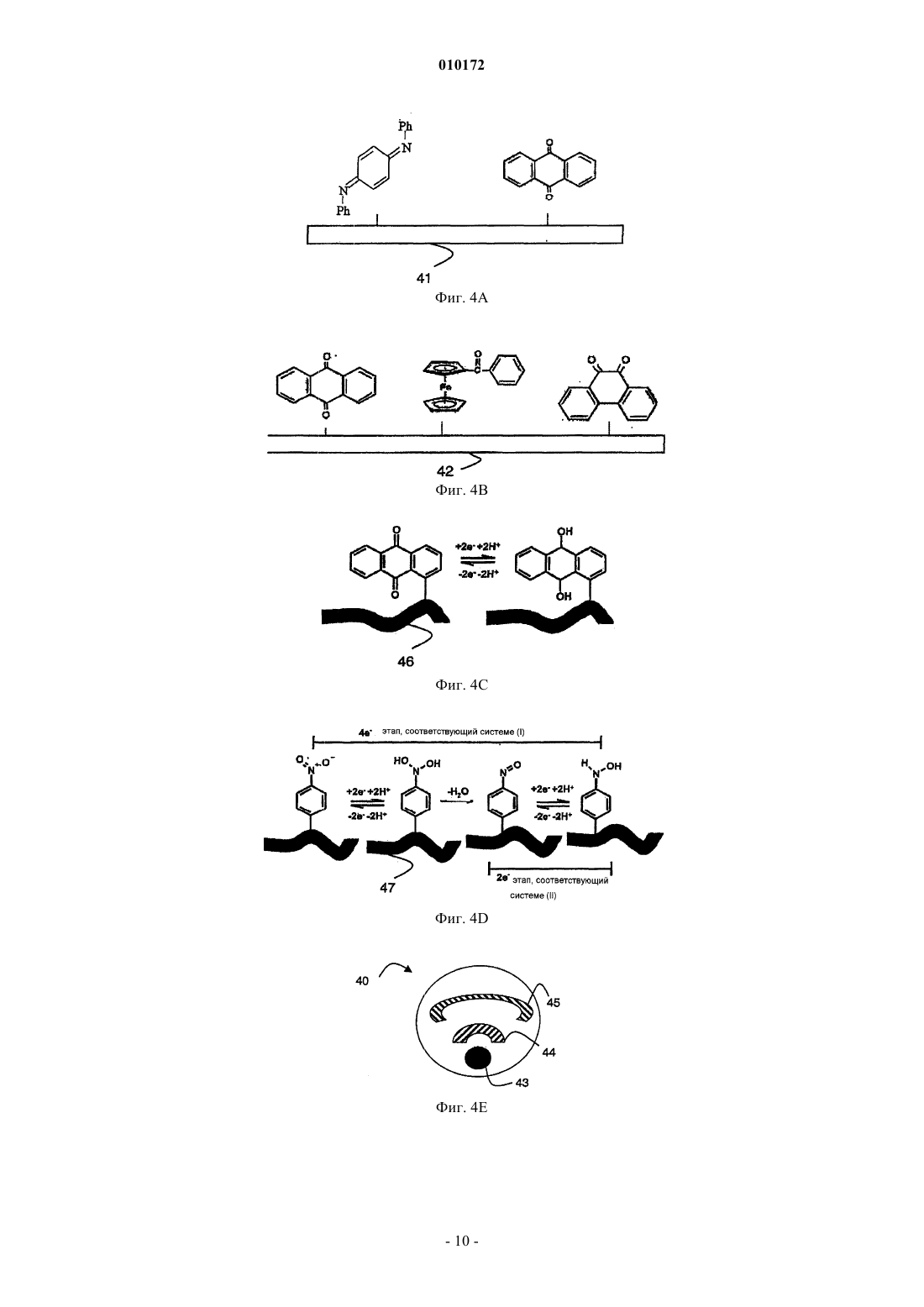
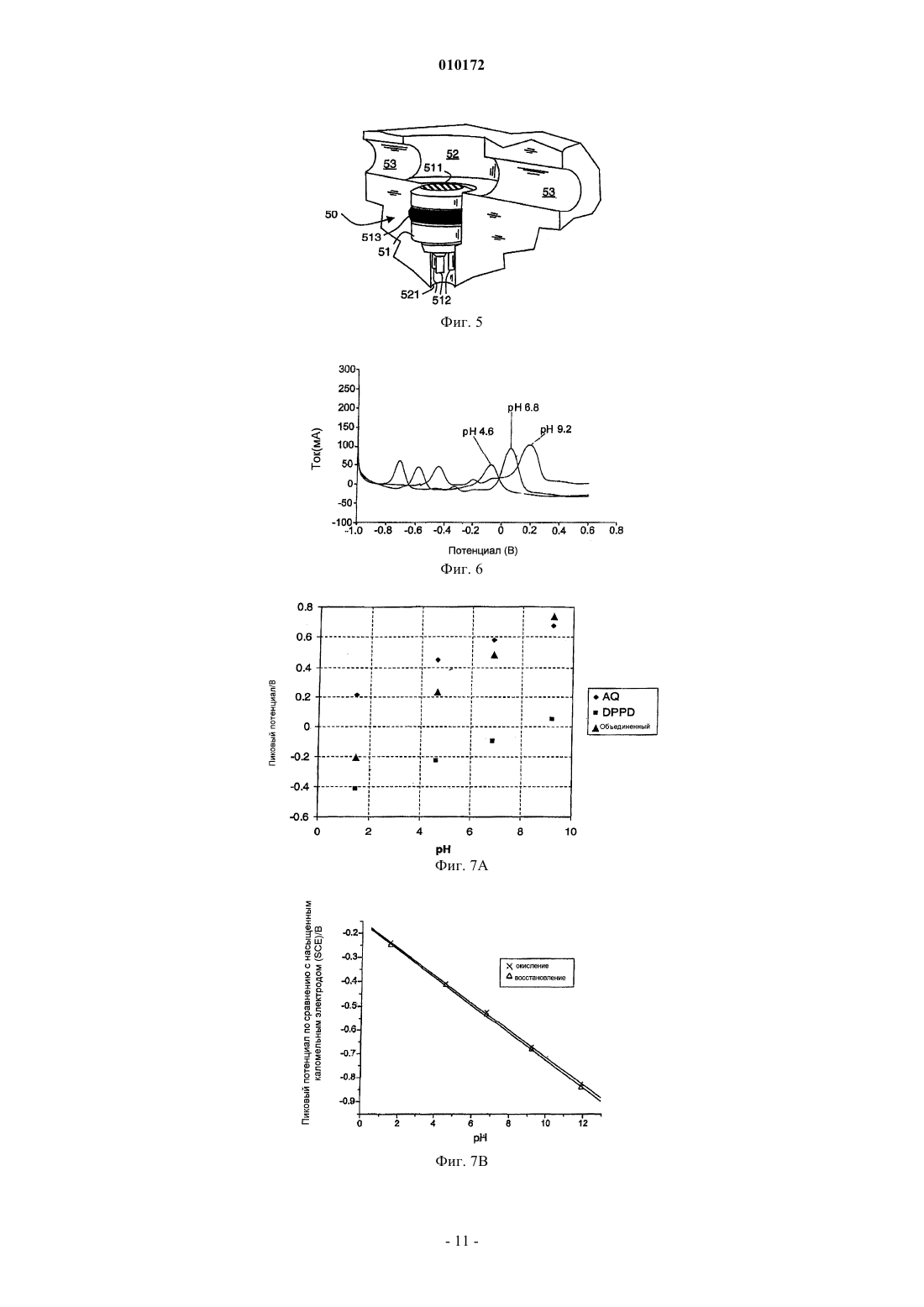
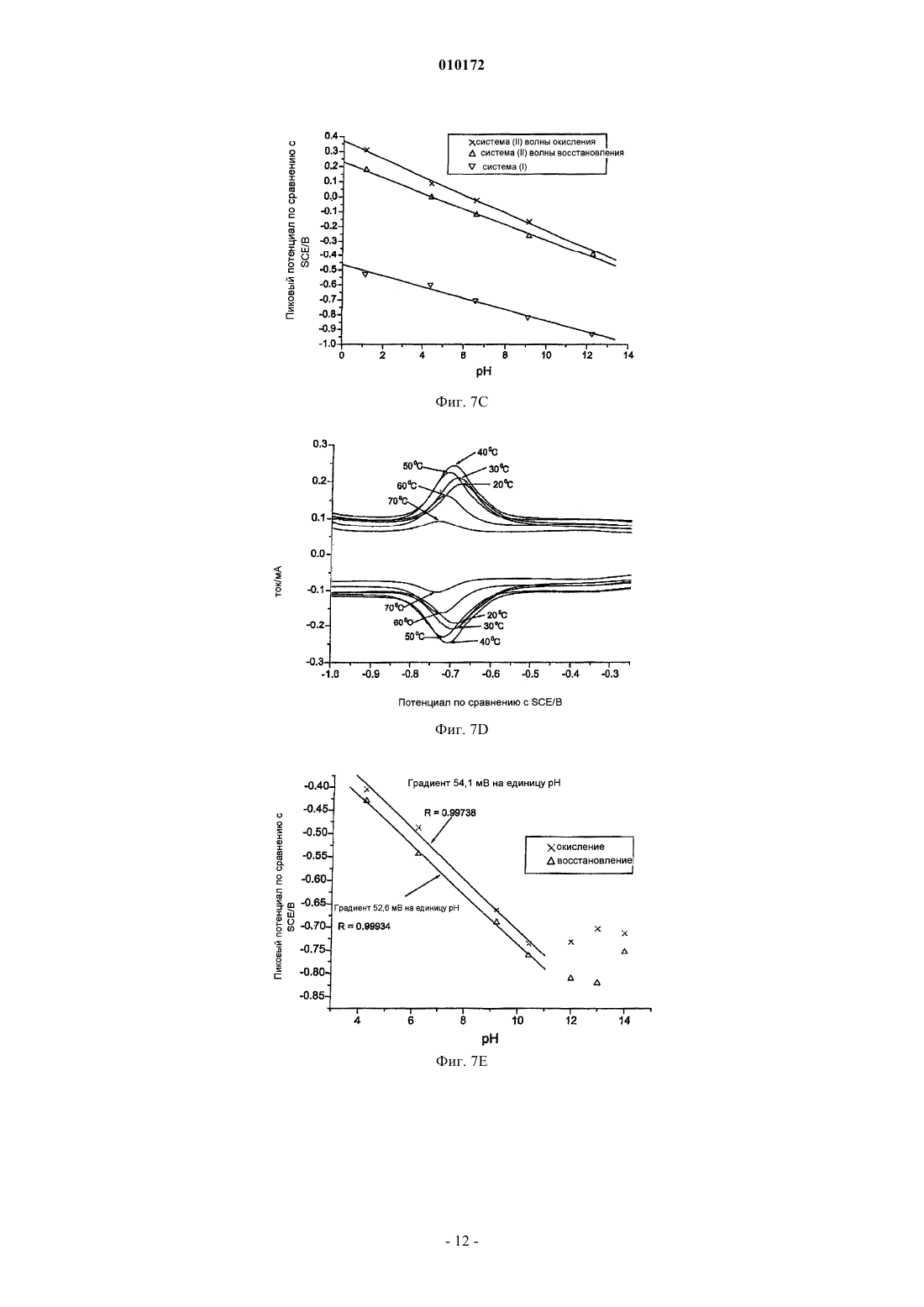
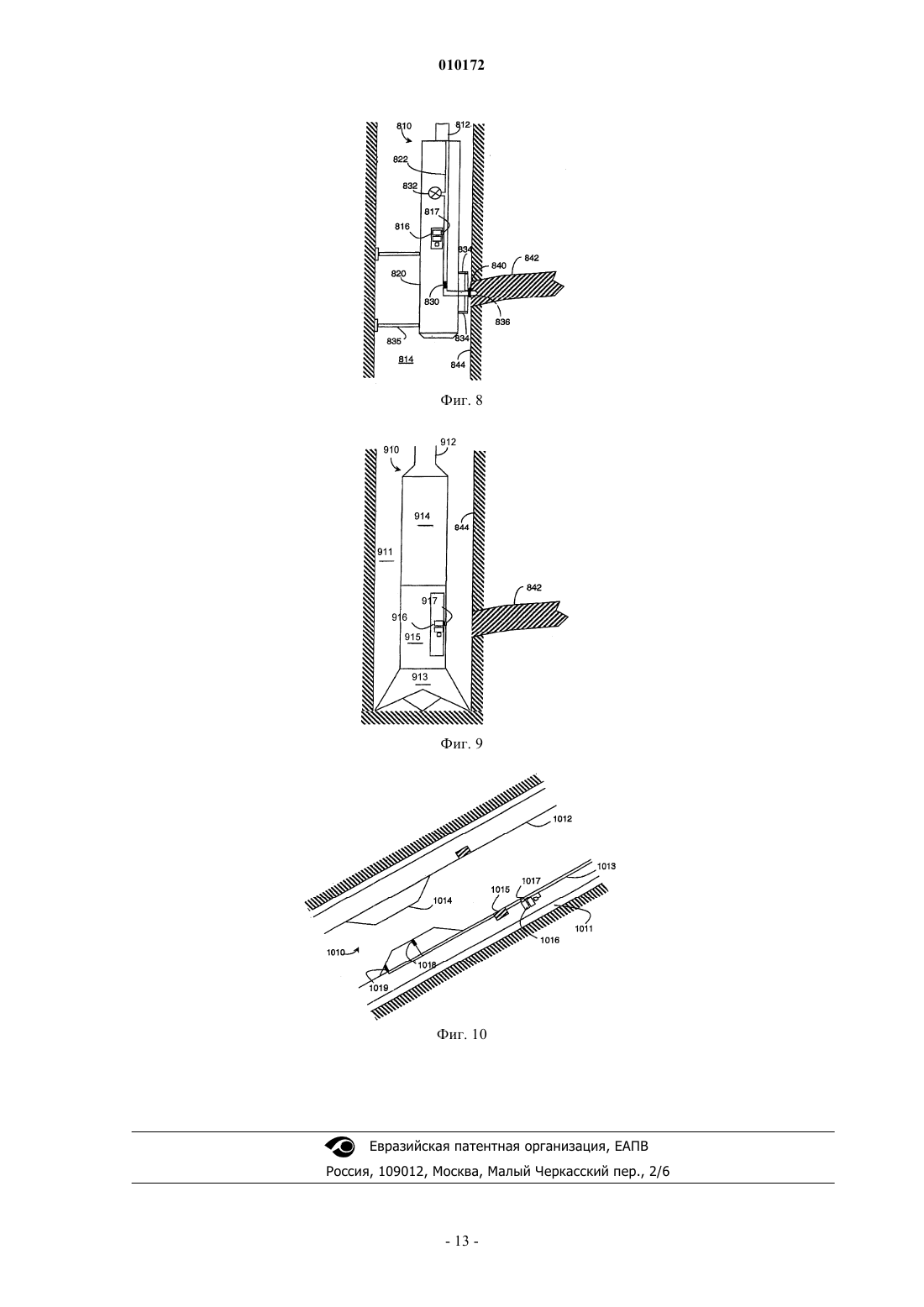
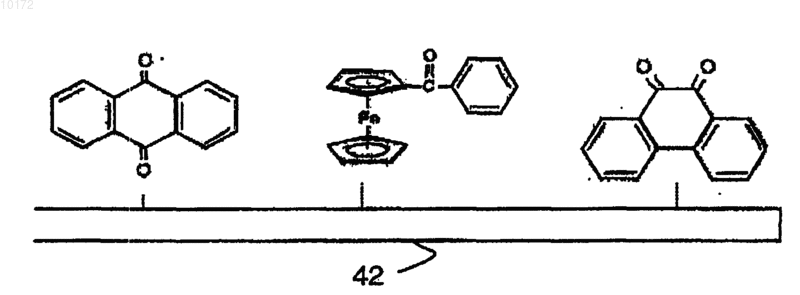
010172 Настоящее изобретение относится к химическому датчику для использования в скважине и к способам анализа флюидов, выделяющихся из подземных пластов. Более конкретно, изобретение имеет отношение к электрохимическому датчику для выполнения в скважине анализа рН и содержания ионов в эффлюентах, выделяющихся из подземного пласта. Уровень техники Репрезентативный анализ образцов скважинных флюидов представляет собой важный аспект определения качества и экономической ценности углеводородсодержащего пласта. В настоящее время анализ скважинных флюидов обычно выполняют способом кабельного каротажа, используя пластоиспытатель, такой как инструмент MDT производства Schlumberger OilfieldServices. Однако недавно было предложено проведение анализа скважинных флюидов либо при помощи датчиков, установленных в стволе скважины постоянно или квазистационарно, либо при помощи датчика, установленного на буровой колонне. Последний способ, при успешной реализации, обладает преимуществами при получении данных во время бурения, тогда как первый может быть использован как часть системы управления скважинами и добычей из них углеводородов. Для получения оценки состава скважинных флюидов, инструменты MDT используют оптический зонд для оценки количества углеводородов в образцах, отобранных из пласта. Другие датчики для определения различных компонентов пластовых флюидов используют измерение удельного сопротивления. В частности, знание химического состава пластовой (выделяемой из пластов) воды из скважины необходимо для снижения затрат и увеличения продуктивности на всех стадиях разведки и добычи нефти и газа. В частности, знание химического состава воды является важным для нескольких ключевых процессов добычи углеводородов, включающих в себя: прогноз и оценку минеральных отложений и коррозии; стратегию разделения нефть/вода и обратной закачки воды; понимание секционирования коллектора/фильтрационных интервалов; определение параметров прорыва воды; оценку обводненности Rw и оценки распределения H2S между нефтью и/или водой в скважине (если используется для измерений H2S). Некоторые химические частицы, растворенные в воде (такие как, например, Cl- и Na+) не меняют свою концентрацию при перемещении к поверхности либо как части потока через скважину, либо как образца, отобранного в скважине. Следовательно, информация об их количестве может быть получена из образцов, отобранных в скважине, и в некоторых случаях из образцов, отобранных из потока на поверхности. Однако характеристики химических частиц, таких как H+ (pH=-log[концентрация H+]), CO2 илиH2S могут значимо меняться по мере их перемещения к поверхности. Изменение происходит в основном вследствие разницы температуры и давления в скважине и на поверхности. В случае отбора образцов такое изменение также может происходить вследствие дегазации образца (нарушения герметичности),осаждения минералов в сосуде с образцом и (особенно в случае H2S) химической реакции с ячейкой для отбора образцов. Следует подчеркнуть, что рН, H2S или CO2 являются одними из наиболее критических параметров при оценке коррозии и отложений. Следовательно, очень важно иметь точное представление об их значениях в скважине. Концентрация протонов или ее логарифм, рН, может рассматриваться как наиболее важный критический параметр химического состава воды. Он определяет скорость многих важных химических реакций, а также растворимость химических веществ в воде, и (в расширительном смысле) в углеводородах. Следовательно, существует и будет существовать далее потребность в химических измерениях в скважинах. Однако до настоящего времени отсутствовали публикации относительно химических измерений, действительно выполняемых в нефтяной и газовой эксплуатационной скважине, несмотря на то,что в соответствующей литературе было предложено много различных способов и инструментов. Известны скважинные измерительные инструменты общего назначения как таковые для применения в области нефтепромыслового дела. Примеры таких инструментов раскрыты в патентах США 6023340; 5517024 и 5351532 или в международной заявке на патент WO 99/00575. Пример зонда для потенциометрических измерений резервуаров грунтовых вод описан в публикации Solodov, I.N., Velichkin,V.I., Zotov, A.V. et al. "Distribution and Geochemistry of Contaminated Subsurface Water in Fissured Volcanogenic Bed Rocks of the Lake Karachai Area, Chelyabinsk, Southern Urals" в Lawrence Berkeley LaboratoryReport 36780/UC-603(1994b), RAC-6, Ca, USA. Известный уровень техники в области потенциометрических измерений в условиях высоких температур и инструментов для этого описан, например, в опубликованной заявке на патент GB-2362469 А. Некоторые инструменты для химического анализа известны из химической лабораторной практики. Такие известные инструменты для анализа включают в себя, например, различные виды хроматографического, электрохимического и спектрального анализа. В частности, для измерений, как в лабораторных,так и в полевых условиях, состава воды (рН, Eh, H2S, CO2, Na+, Cl- и т.д.) для контроля качества грунтовых вод широко применялся потенциометрический способ. Патент США 5223117 раскрывает вольтаметрический микродатчик с двумя выводами, имеющий внутренний источник опорного напряжения,-1 010172 использующий молекулярную самосборку для формирования системы, в которой электрод сравнения и индикаторный электрод находятся на чувствительном электроде. Реперная молекула описывается как редокс-система, которая не является чувствительной к рН, тогда как молекула-индикатор образуется редокс-системой на основе гидрохинона, имеющего потенциал, который смещается при изменении рН. Слои как реперных молекул, так и молекул-индикаторов получают самосборкой на золотых (Au) микроэлектродах. В известном микродатчике значения рН получают из положения пика на вольтамограммах. Однако зачастую лабораторные системы не являются подходящими для применения в стволе скважины, поскольку редко удовлетворяют требованиям высокой прочности, стабильности, низких эксплуатационных расходов и низких энергетических затрат. Таким образом, задачей настоящего изобретения является предоставление устройства и способов для проведения электрохимических измерений в углеводородных скважинах во время бурения и добычи. Более конкретно, задачей настоящего изобретения является предоставление прочных датчиков для молекулярно-селективных электрохимических измерений, в частности, измерений рН. Сущность изобретения Настоящее изобретение обеспечивает выполнение своих задач путем предоставления электрохимического датчика, имеющего измерительный электрод по меньшей мере с двумя рецепторами, чувствительными к одним и тем же частицам. В предпочтительном варианте осуществления настоящего изобретения датчики представляют собой редокс-систему на основе, например, химии антрахинонов. Субстрат, на котором установлена редокс-система, предпочтительно выполнен на основе углерода в одной из его элементарных форм, такой как графит, углеродный порошок, алмаз. В одном из вариантов настоящего изобретения субстрат может представлять собой модифицированные нанотрубки, включая многостенные нанотрубки. Электрохимические технологии, использующие способ или датчик согласно настоящему изобретению, могут быть применены, например, как часть устройства для каротажа в эксплуатационных скважинах или опробователя пластов для необсаженных скважин (такого как модульный динамический пластоиспытатель, MDT). В последнем случае технология может обеспечивать в скважине проверку образцов воды в масштабе реального времени или измерение рН, что в свою очередь может быть использовано для прогнозирования образования минеральных отложений и оценки коррозии. Эти и другие особенности настоящего изобретения, предпочтительные варианты осуществления и их модификации, возможные приложения и преимущества будут оценены и поняты специалистами в данной области техники из нижеследующего подробного описания и чертежей. Краткое описание чертежей На фиг. 1 показана блок-схема основных элементов известного вольтаметрического датчика; фиг. 2 иллюстрирует блок-схему основных элементов известного электрохимического микродатчика и их работу; на фиг. 3 показана блок-схема известного скважинного зонда, использующего потенциометрические датчики; на фиг. 4 А - структура поверхности измерительного электрода согласно примеру настоящего изобретения; на фиг. 4 В - структура поверхности измерительного электрода с внутренним электродом сравнения согласно другому примеру настоящего изобретения; фиг. 4 С иллюстрирует редокс-реакцию измерительного электрода согласно другому примеру настоящего изобретения с использованием многостенной углеродной нанотрубки; фиг. 4D - редокс-реакцию измерительного электрода с внутренним электродом сравнения согласно другому примеру настоящего изобретения с использованием многостенной углеродной нанотрубки; на фиг. 4 Е показана геометрическая схема поверхности электрода по фиг. 4 В; фиг. 5 представляет собой вид в перспективе с частичным разрезом датчика согласно примеру настоящего изобретения в скважинном инструменте; на фиг. 6 показаны вольтамограммы, записанные с электрохимического датчика согласно настоящему изобретению, при трех различных значениях рН; на фиг. 7 А - сдвиг пикового потенциала для антрахинона, дифенил-п-фенилендиамина и комбинации этих двух редокс-систем; фиг. 7 В-С представляют собой графики пикового потенциала относительно рН для редокс-систем по фиг. 4 С и 4D, соответственно, в пределах рН от рН 1,0 до рН 12,0 при 293 K в различных условиях; на фиг. 8 показан пример датчика согласно настоящему изобретению, выполненного как часть кабельного устройства для опробования пластов в стволе скважины; на фиг. 9 - ствол скважины и нижняя часть бурильной колонны, включая забойный блок с датчиком согласно настоящему изобретению; и на фиг. 10 показан датчик, расположенный ниже расходомера Вентури по потоку, согласно настоящему изобретению.-2 010172 Осуществление изобретения Теория вольтаметрии и ее применение для измерений характеристик воды на поверхности при температуре окружающей среды являются хорошо разработанными. Способ основан на измерении электродвижущей силы (ЭДС) или потенциала E в потенциометрической ячейке, которая включает в себя измерительный электрод и электрод сравнения (полуэлементы). На фиг. 1 показаны обычные компоненты известной вольтаметрической ячейки 10. Измерительный электрод 11 погружен в раствор 13. Такой электрод состоит из внутреннего полуэлемента (например, Ag проволока, покрытая солью AgCl) в растворе с фиксированным рН (например, в некоторых рН электродах 0,1 M HCl), и ионоселективной мембраны 111 (такой как стеклянная мембрана, селективная к H+, в рН стеклянном электроде). Электрод 12 сравнения также содержит внутренний полуэлемент (обычно такой же AgCl; Ag), погруженный в концентрированный раствор KCl (например, 3M)/гель, насыщенныйAg+, который диффундирует (или течет) через опорную (жидкую) границу 121 раздела. Ион-селективный электрод 11 измеряет потенциал, который возникает вследствие разницы в активности или концентрации соответствующего иона (H+ в случае рН) во внутреннем растворе и в измеряемом растворе. Этот потенциал измеряют относительно опорного потенциала на электроде 12 сравнения,который является фиксированным вследствие постоянного состава стандартного раствора/геля. Электроды могут быть разделены (раздельные полуэлементы), или объединены в один ("комбинированный электрод"). Измеряемая ЭДС представляет собой суммарную функцию температуры и активности i-го иона,для которого измерительный электрод является селективным:E=E+(kТ)1og(ai),[1] где E представляет собой измеряемую электродвижущую силу (ЭДС) ячейки (все потенциалы выражены в вольтах), ai соответствует активности i-го иона и пропорционально его концентрации. Е представляет собой стандартный потенциал (при температуре T), соответствующий значению E в растворе с активностью i-го иона, равной единице. Термин в скобках представляет собой так называемый угловой коэффициент Нернста на графике E как функции log(ai) . Этот угловой коэффициент (или константа "k") вместе с константой ячейки (электрода) (Е) определяется экспериментально при помощи процедуры калибровки с использованием стандартных растворов с известными активностями i-го иона. Для качественных неповрежденных электродов такой угловой коэффициент должен быть очень близок к теоретическому угловому коэффициенту, равному (RT/Fz), где F представляет собой число Фарадея (23061 кал/М), R представляет собой газовую постоянную (1,9872 кал/М K), zi представляет собой заряд i-го иона. Уравнение Нернста [1] может быть переписано для датчиков рН, т.е. log a (H+) в виде: Е 0,5=K- (2,303 RTm/nF)pH,[2] где E0,5 представляет собой потенциал полуволны используемой редокс-системы, K представляет собой произвольную константу, R представляет собой константу идеального газа, m представляет собой количество протонов и n представляет собой количество электронов, перемещенных в редокс-реакции. На фиг. 2 показан микродатчик согласно патенту США 5223117. На фиг. 2 А схематично показан электрохимический датчик с противоэлектродом 21 и имеющий гораздо меньший относительный размер(с коэффициентом 1000) Au субстратом 22, который несет два типа молекулярных частиц М и R. ЧастицаR образует инертный электрод сравнения, а частица M представляет собой индикаторный электрод со специфическими рецепторами или специфической селективностью в отношении третьей частицы L. Схема линейной развертки вольтамограммы в верхней части фиг. 2 С показывает разницу в пиковых значениях тока для окисления в нормальных условиях. Когда третья частица L связывается с M (фиг. 2 В),эта разница увеличивается, что иллюстрируется сдвигом пиков в нижней части фиг. 2 С, таким образом,обеспечивая измерение концентрации L в растворе, окружающем датчик. В контексте настоящего изобретения важно отметить, что R специально выбирают таким образом, чтобы она была нечувствительной к частице L, например рН. На фиг. 3 схематично показаны элементы известного скважинного инструмента 30 для анализа, используемого Solodov et al. (см. раздел "Уровень техники"). Корпус инструмента 30 соединен с поверхностью посредством кабеля 31, по которому подается питание и сигналы. Компьютерная консоль 32 управляет инструментом, контролирует его работу и ведет запись результатов измерений. Инструмент 30 включает в себя сенсорную головку с несколькими селективными электрохимическими зондами 33, каждый из которых является селективным к различным молекулярным частицам. Также в корпусе инструмента размещены элементы 34 силового привода, которые приводят в действие головку, тестовая система 35 и приемопередатчики 36 для преобразования измерений в поток данных и для передачи указанного потока данных на поверхность. Электроды расположены в нижней части зонда и включают электроды для рН, Eh (или ORP (редокс-потенциала, Ca2+ (рСа), Na+ (pNa), S2- (pS), NH4+ (pNH4) и электрод сравнения (RE). H2S парциальное давление может быть вычислено из показаний рН и pS. Ниже подробно раскрыты аспекты и элементы настоящего изобретения. Настоящее изобретение предлагает новую молекулярную систему, в которой объединены редокссвойства двух молекул, что обеспечивает значительно более высокую точность и, в свою очередь, воз-3 010172 можность использования в скважине. В предпочтительном варианте осуществления для рН-чувствительного датчика антрахинон превращают в гомогенные производные на частицах углерода (AQC)AQC систему получают, используя 2 г углеродного порошка (со средним диаметром 1,5 мкм), смешанного с 10 см 3 раствора, содержащего 5 мМ соли прочный красный AL (антрахинон-1-диазоний хлорид), в которую добавлено 50 мМ фосфорноватистой кислоты (50%). Реакционную смесь выдерживают в течение 30 мин при 5 С, периодически помешивая, затем фильтруют отсосом воды. Избыток кислоты удаляют путем промывания дистиллированной водой, и в завершение порошок промывают ацетонитрилом для удаления из смеси не прореагировавшей соли диазония. Затем смесь сушат на воздухе, помещая в вытяжной шкаф на 12 ч, и, наконец, хранят в герметичном контейнере. Аналогично, фенантренхинон получают в качестве вторых молекулярных частиц, которые подвергаются редокс-реакции. В качестве альтернативы, N,N'-дифенил-п-фенилендиамин (DPPD), закрепленный на частицах углерода, подвергается редокс-процессу как показано ниже: Связывание DPPD с углеродом выполняют путем смешивания 4 г углеродного порошка с 25 мл 0,1M HCl + 0,1 M KCl и 20 мМ раствора DPPD в ацетоне. Реакционную смесь постоянно помешивают в течение 2 ч в мерном стакане и затем фильтруют, после чего промывают дистиллированной водой для удаления избытков кислоты и хлорида. Затем сушат, поместив в вытяжной шкаф на 12 ч, и хранят в герметичном контейнере. В статичной среде, в которой поверхность датчика не подвергается воздействию потока, существует возможность иммобилизовать нерастворимые в воде кристаллы DPPD непосредственно на поверхности электрода. Однако в окружающей среде скважины предпочтительно связать сенситивные молекулы с такой поверхностью при помощи химической связи. Модифицированный углеродный порошок иммобилизуют абразивным способом на базисную плоскость электрода из пиролитического графита (BPPG) до получения вольтаметрической характеристики,следуя процедуре, описанной у Scholz, F. and Meyer, В., "Voltammetry of Solid Microparticles ImmobilisedYork, 1998, 20, 1. Сначала электрод полируют бумагой для полировки стекла (Н 00/240) и затем бумагой на основе карбида кремния (Р 1000 С) для придания ему гладкости. Модифицированный углерод сначала смешивают и затем иммобилизуют на BPPG, осторожно натирая поверхность электрода фильтровальной бумагой, содержащей функционализированные частицы углерода. Полученная в результате модифицированная электродная поверхность схематично показана на фиг. 4 А, на которой показан электрод 41 со связанными DPPD и AQC. Дополнительные преимущества обеспечивает добавление внутреннего рН стандарта, включающего рН редокс-пару, для увеличения стабильности любого вольтаметрического показателя, в данном случае для того, чтобы устранить неопределенность, вызванную загрязнением внешнего электрода сравнения. В этой конфигурации датчик включает в себя два электрода сравнения. Подходящей реперной молекулой является, например, K5Mo(CN)8 или поливинилферроцен (PVF),каждая из которых имеет стабильный редокс-потенциал (K5Mo(CN)8 составляющий примерно 521 мВ) ,который значительно отличается от ожидаемого сдвига редокс-сигналов двух частиц-индикаторов во всей представляющей интерес области рН. Как показано в табл. 1 как потенциал окисления, так и потенциал восстановления K5Mo(CN)8 являются практически постоянными во всей представляющей интерес области рН. Реперные частицы на основе Mo могут удерживаться на твердом субстрате посредством ионных взаимодействий с сосуществующим катионным полимером, таким как поли(винилпиридин), который был закреплен в твердой фазе. Другие рН-независимые частицы, такие как ферроцианид, являются менее подходящими, поскольку редокс-пики размываются сигналами измерительной редокс-системы. На фиг. 4 В электрод 42 несет связанные молекулы AQC и PAQ вместе с FVF в качестве внутренней реперной молекулы. Большинство обычных форм проводящего углерода, используемых при производстве электродов,представляют собой стеклоуглерод, углеродные волокна, сажу, различные формы графита, углеродную пасту и углеродную смолу. Еще одна форма углерода, которая нашла широкое применение в области электрохимии с момента ее открытия в 1991, представляет собой углеродные нанотрубки (CNT). Структуру CNT приблизительно можно описать как свернутые листы графита, и она может быть сформирована в виде либо одно-, либо многостенных трубок. Одностенные углеродные нанотрубки (SWCNT) представляют собой одну полую графитовую трубку. С другой стороны, многостенные углеродные нанотрубки (MWCWT) состоят из нескольких концентрических трубок, вставленных одна в другую. Вышеупомянутые способы активации для связывания активных редокс-частиц с поверхностями графита или углерода могут быть расширены посредством химического восстановления солей арилдиазония фосфорноватистой кислотой для того, чтобы включить получение ковалентных производныхMWCNT при помощи хлорида антрахинон-1-диазония и тетрафторбората 4-нитробензолдиазония. Это приводит в результате к синтезу 1-антрахинонил-MWCNT (AQ-MWCNT) и 4-нитрофенил-MWCNTs(NB-MWCNT), как показано на фиг. 4 С и 4D, соответственно. Соответствующие субстраты 46 и 47 представляют собой многостенные углеродные нанотрубки. Процесс получения производных MWCNT включает следующие этапы: сначала 50 мг MWCNT перемешивают в 10 см 3 5 мМ раствора либо прочного красного AL (антрахинон-1-диазония хлорид), либо прочного красного GG (4-нитробензолдиазония тетрафторборат), в который добавляют 50 см 3 фосфорноватистой кислоты (Н 3 РО 2, 50% w/w в воде). Затем раствор выдерживают при 5 С в течение 30 мин,осторожно помешивая. Затем раствор фильтруют отсосом воды для удаления с поверхности MWCNT любых непрореагировавших частиц. Для удаления из смеси избытка кислоты дополнительно промывают деионизированной водой и наконец промывают ацетонитрилом для удаления непрореагировавшей соли диазония. Затем полученные производные MWCNT сушат на воздухе, поместив их в вытяжной шкаф на 12 ч, после чего их хранят в герметичном контейнере до момента использования. Необработанные многостенные нанотрубки можно приобрести у коммерческих производителей, например, у Nano-Lab Inc ofBrighton, MA, USA с чистотой 95%, диаметром 30+/-15 нм и длиной 5-20 мкм. Восстановление солей диазония с использованием фосфорноватистой кислоты, как показано, представляет собой универсальную технологию для получения производных порошка графита и MWCNT в больших количествах. Это имеет преимущество перед предыдущими способами, включающими в себя прямое электрохимическое восстановление солей диазония на поверхности электрода, поскольку способ химического активирования авторов изобретения предоставляет возможность для недорогого массового производства получения производных нанотрубок химическим способом для многочисленных приложений. Более того, получение производных MWCNT предоставляет возможность для минимизации габаритов датчиков до наноразмера. На фиг. 4 Е показана возможная геометрическая конфигурация или схема поверхности датчика 40,который подвергается воздействию жидкости в скважине. Поверхность включает в себя рабочий электрод 43, описанный со ссылкой на фиг. 4 А или 4 В, вместе с (внешним) электродом 44 сравнения и противоэлектродом 45. Схема микродатчика 50, включающая модифицированную поверхность, изготовленную согласно вышеупомянутой процедуре, показана на фиг. 5. Корпус 51 датчика закреплен на концевом участке отверстия 52. Корпус несет поверхность 511 электрода и контакты 512, которые обеспечивают контактные поверхности с источником напряжения и измерение посредством небольшого канала 521 на дне отверстия 52. Уплотнительное кольцо 513 защищает контактные поверхности и электронные схемы от скважинного флюида, который в рабочем состоянии проникает через канал 53 для образцов. Преимущество нового датчика заключается в том, что он включает в себя два измерительных или индикаторных электрода, или молекулы, которые измеряют два ЭДС или потенциала относительно одного и того же электрода сравнения, и являются чувствительными к одним и тем же частицам или молекулам окружающей среды. В результате увеличивается чувствительность к сдвигу в концентрации час-5 010172 тиц. Используя вышеупомянутые примеры AQC и DPPA, и рН (или концентрацию H+), уравнение Нернста, примененное к новому датчику, представляет собой сумму уравнений, описывающих отдельные измерительные электроды. Таким образом, комбинация потенциала полуволны E0,5(AQC) для антрахинона[4] дает потенциал полуволны E0,5 (S) для объединенной системы:E0,5(S) =Е 0,5(AQC) +E0,5(DPPD) = (K(AQC)+K(DPPD-2(2,303 RTm/nF)pH = K(S)-2(2,303 RTm/nF)pH, [5] где K(S) представляет собой сумму двух констант K(AQC) и K(DPPD). Поскольку сдвиг потенциала при изменении рН зависит от второго числителя, (теоретическая) чувствительность датчика удваивается. Использование дополнительной (третьей) редокс-системы, чувствительной к тем же самым частицам, в принципе мог бы дополнительно увеличить чувствительность. Однако поскольку способ детектирует сдвиги в расположении пиков вольтамограммы, требуются дополнительные меры для решения проблемы наложения пиков в такой трехмолекулярной системе. На фиг. 6 показаны результаты в некотором диапазоне рН растворов (рН 4,6, буфер 0,1 M уксусная кислота + 0,1 M ацетата натрия; рН 6,8, буфер 0,025 M динатрийфосфата + 0,025 M дигидрофосфата калия; рН 9,2, буфер 0,05 M динатрийтетраборат). На фигуре представлены соответствующие вольтамограммы квадратной волны, если стартовый потенциал был в достаточной степени отрицательным для того, чтобы и DPPD и AQ находились в своих восстановленных формах. На фиг. 7 А показана связь между редокс-потенциалом и рН как для DPPD , так и для AQ . График показывает линейную зависимость в области значений рН от 4 до 9 с соответствующим градиентом приблизительно 59 мВ/единиц рН (при 25 С), который согласуется с передачей n электронов, m протонов, где n и m вероятно являются равными двум. Путем объединения двух отдельных кривых способом, описанным уравнением [5], получают новую функциюс превосходной чувствительностью в отношении частиц, предназначенных для детектирования. Обнаружено, что для двух вышеописанных активированных частиц MWCNT пиковый потенциал с использованием циклической вольтаметрии (CV) является рН-зависимым. Такое поведение вольтамограммы согласуется с ранними исследованиями углеродного порошка ковалентно модифицированного группами 1-антрахинонила и может быть отнесено к двухэлектронному, двухпротонному восстановлению/окислению группы 1-антрахинонила в соответствующих частицах гидрохинона. При изучении NB-MWCNT можно наблюдать более сложный вольтаметрический паттерн. При первом сканировании с восстановлением наблюдается большой электрохимически необратимый пик(обозначенный как система I), точный пиковый потенциал которого зависит от изучаемого рН. Когда направление сканирования изменяется на обратное и сканирование ведется с окислением, наблюдается новый пик при потенциалах, более положительных, чем потенциалы, при которых наблюдался необратимый пик, который, как было обнаружено, при повторном проведении цикла ведет себя электрохимически обратимым способом, как соответствующая волна восстановления. Эта система обозначена как система II. Более того, обнаружено, что точный пиковый потенциал системы II изменяется вместе с изучаемым рН. Такое поведение согласуется с механизмом восстановления нитрогруппы в водной среде, как проиллюстрировано на примере нитробензола на фиг. 4D. Стоит отметить, что все последующие процедуры получения характеристик NB-MWCNT выполняют на системе II, которая соответствует обратимой паре арилнитрозо/арилгидроксиламин, после проведения нескольких начальных сканирований для образования этой редокс-пары. При изучении воздействия рН на AQ-MWCNT и NB-MWCNT в диапазоне рН от 1,0 до рН 12,0, используя CV и вольтаметрию с прямоугольной волной (SWV) при комнатной температуре, а также поведение AQ-MWCNT при повышенной температуре вплоть до 70C, был использован SWV, поскольку он обеспечивал острый, хорошо определяемый пик за одно сканирование. Поскольку окислению/восстановлению AQ-MWCNT или NB-MWCNT сопутствует потеря/приобретение протонов (см. фиг. 4 С и 4D, соответственно), пиковый потенциал зависит от локальной концентрации протонов, т.е.,рН, как описывается уравнением Нернста [6]: где m и n, количество перемещенных протонов и электронов, соответственно, оба вероятно равны двум в случае AQ-MWCNT, и паре арилнитрозо/арилгидроксиамин в случае NB-MWCNT. Вид [6] уравнения Нернста эквивалентен формуле уравнениям [1] и [2]. Обнаружено, что при комнатной температуре пиковые потенциалы как для AQ-MWCNT, так и дляNB-MWCNT, как предсказывалось, сдвигаются к более отрицательным потенциалам с увеличением рН. Было обнаружено, что соответствующий график пикового потенциала относительно рН является линейным на всей области изучаемого рН во всех случаях (см. фиг. 7 В и 7 С, соответственно), и было обнаружено, что сравнение градиента графиков пиковых потенциалов относительно рН близко к идеальному значению 58,1 мВ/единица рН за исключением необратимого пика (система I) для NB-MWCNT, который,-6 010172 как было обнаружено, сдвигается только при 37,6 мВ/единица рН. Ответ AQ-MWCNT на рН при повышенных температурах вплоть до 70C изучали при помощиSWV. Следует отметить, что рН используемых растворов может изменяться с температурой, и поэтому были использованы эти три конечных IUPAC буфера с известным рН для каждой изучаемой температуры. Они представляли собой буферы с рН 4,6, рН 6,8 и рН 9,2. При помощи уравнения Нернста было предсказано, что пиковые потенциалы должны сдвинуться в сторону более отрицательных значений при увеличении температуры из-за температурной зависимости формального потенциала (Еpeak). Однако фиг. 7D показывает, что при увеличении температуры пиковый потенциал сдвигается в сторону более отрицательных значений. Однако в отличие от поведения углеродного порошка, производные которого получены при помощи образования ковалентных связей группами антрохинонила (AQуглерод), где пиковые токи постоянно увеличивались с увеличением температуры после начального увеличения пикового тока вплоть до приблизительно 40C, пиковые токи AQ-MWCNT постепенно понижались с увеличением температуры. Такое поведение также ранее наблюдали для агломератов MWCNT при повышенных температурах. Температурная инвариантность полученных производных MWCNT не является до конца понятной, но имеет потенциальное преимущество для датчиков рН, которые требуются для использования в средах с повышенной температурой. На фиг. 7 Е показано влияние изменения рН при комнатной температуре для молекулярного антрахинона в жидкой фазе в зависимости от AQ-MWCNT, иммобилизованного на BPPG электроде. 1 мМ растворы антрахинона приготовили для каждого рН и изучали, используя циклическую вольтаметрию при оголенном BPPG электроде. Изменение пикового потенциала в зависимости от рН для обоих случаев во всей области рН от 1,0 до 14,0 изучали в дополнительных экспериментах, которые проводили при рН 10,5, рН 13,0 и рН 14,0. График пикового потенциала в зависимости от рН как для 1 мМ антрахинона в растворе, так и для иммобилизованных AQ-MWCNT показывает, что в случае AQ-MWCNT наблюдался линейный ответ на всей области изучаемого рН. Однако для антрахинона в жидкой фазе график не является линейным выше приблизительно рН 10,5 (фиг. 7E). Это можно объяснить pKa для удаления первого протона, pKai, восстановленной формы антрахинона (см. фиг. 4C) в растворе, равном примерно pKai=10. pKa для удаленного второго протона равен примерноpKa2=12. При более высоких рН, чем рН 10 восстановленные формы антрахинона могут быть депротонированы, вызывая изменение пикового потенциала в зависимости от рН. Отсутствие такого отклонения от линейности наблюдается для AQ-MWCNT. Из этого можно сделать вывод, что полученные производные на поверхности MWCNT могут изменять pKa группы антрахинонила. Это ясно демонстрирует, что полученные производные на MWCNT усиливают преимущество аналитической чувствительности рН,поскольку окно рН для применения расширено подходящим образом для полученных производных AQMWCNT по сравнению со свободным антрахиноном в растворе. Анализ пикового потенциала как функции рН при каждой температуре показывает хорошее согласие между экспериментальными и теоретически предсказанными значениями, таким образом, показывая,что данный механизм может быть использован в качестве простого, недорого рН зонда, который работает в широких температурных пределах. Новый зонд может быть размещен внутри различных инструментов и устройств для использования в стволе скважины, как описано в приведенных ниже примерах. На фиг. 8-11 показан датчик в различных возможных приложениях для использования в скважине. На фиг. 8 показано устройство 810 для опробования пластов, удерживаемое кабелем 812 в стволе 814 скважины. Устройство 810 представляет собой хорошо известный модульный динамический пластоиспытатель (MDT, Mark of Schlumberger), описанный в патенте США 3859851 и патенте США 3780575, правообладателями которых являются авторы настоящего изобретения совместно с Urbanosky,и патенте США 4994671 правообладателями которых являются авторы настоящего изобретения совместно с Safinya et al., причем упомянутый известный пластоиспытатель модифицирован путем введения электрохимического датчика 816 для анализа, подробно описанного выше (фиг. 8). Модульный динамический пластоиспытатель содержит корпус 820 длина которого составляет приблизительно 30 м, и который содержит основной трубопровод или трубку 822. Инструмент 816 для анализа соединен с трубопроводом 822 через отверстие 817. В дополнение к новой системе датчиков 816 пластоиспытатель содержит оптический анализатор 830 флюида в нижней части трубопровода 822. Поток подается через трубопровод 822 при помощи насоса 832, расположенного в верхней части трубопровода 822. Рычаги 834 с гидроприводом и противорычаги 835 прикреплены снаружи корпуса 820 и несут головку 836 зонда для отбора проб флюида. Основание головки 836 зонда изолировано от ствола 814 скважины уплотнительным кольцом 840 или другими уплотнительными устройствами, например пакерами. Перед завершением скважины модульный динамический пластоиспытатель опускают в скважину на кабеле 812. После достижения целевой глубины, т.е. слоя 842 пласта, для которого необходимо произвести анализ, рычаги 834 с гидроприводом удлиняются таким образом, чтобы привести головку 836 зонда для отбора проб в соприкосновение с пластом. Уплотнительное кольцо 840 в основании 836 зонда для отбора проб формирует уплотнение между боковой стороной ствола скважины 844 и пластом 842, в который введен зонд 836, и предотвращает захват зондом 836 для отбора проб флюида непосредственно из ствола скважины 814.-7 010172 После введения зонда 836 для отбора проб в пласт 842, вниз по кабелю 812 подают электрический сигнал с поверхности для того, чтобы запустить насос 832 и системы 816 и 830 датчиков, и начать отбор образцов флюида из пласта 842. Электрохимический детектор 816 выполнен с возможностью измерения рН и содержания ионов в эффлюенте пласта. Сосуд (не показан) внутри инструмента MDT изначально может быть заполнен калибровочным раствором для выполнения калибровки датчиков на месте (в скважине). Модуль MDT также может содержать резервуар с большим объемом калибровочного раствора и/или раствора для очистки, который может периодически прокачиваться через объем датчика с целью очистки и повторной калибровки. Электрохимические зонды в скважинном инструменте типа MDT могут быть использованы для абсолютных измерений параметров в скважине, которые значимо отличаются от параметров, измеренных в образцах на поверхности (таких как рН, Eh, растворенные H2S, CO2). Такая корректировка значений, полученных на поверхности, важна для подтверждения корректности модели химии воды. Дополнительные возможные способы применения нового датчика и системы разделения лежит в области скважинных измерений в процессе бурения (MWD). Принцип измерений MWD известен и раскрыт в большом количестве литературных источников, включая, например, патент США 5445228,озаглавленный "Способ и устройство для отбора образцов пласта во время бурения углеводородной скважины". На фиг. 9 показан ствол 911 скважины и нижняя часть бурильной колонны 912, включая забойный блок 910 (BHA). BHA несет на своей концевой части головку 913 бура. Он включает в себя дополнительные утяжеленные бурильные трубы, которые используются для установки дополнительного оборудования, такого как переводник 914 для устройств телеметрии и переводник 915 для датчиков. Переводник для устройств телеметрии обеспечивает телеметрическую связь с поверхностью, например, при помощи гидроимпульсной скважинной телеметрии. Переводник для датчиков включает в себя новый электрохимический блок 916 для анализа, описанный выше. Блок 916 для анализа собирает флюиды из ствола скважины через небольшое углубление 917, защищенное от обломков породы и других частиц металлической сеткой. Во время операции бурения ствола скважины жидкость проникает в углубление 917 и затем анализируется блоком 916 датчиков. Результаты передаются из блока сбора данных в блок 914 телеметрии,преобразуются в телеметрические сигналы и передаются на поверхность. Третий способ применения показан на фиг. 10. На фигуре показан расходомер Вентури 1010, хорошо известный в промышленности и описанный, например, в патенте США 5736650. Укрепленный на эксплуатационной насосно-компрессорной или обсадной колонне 1012, расходомер с проводным соединением 1013 с поверхностью устанавливают внутри скважины 1011, следуя известным процедурам, как раскрыто, например, в патенте США 5829520. Расходомер состоит, по существу, из перетяжки или шейки 1014 и двух отводов 1018, 1019 давления, расположенных обычным способом на входе и в месте максимального сужения, соответственно. Обычно расходомер Вентури объединен с плотномером 1015, расположенным выше или ниже по потоку. Новый электрохимический модуль 1016 для анализа предпочтительно расположен ниже расходомера Вентури по потоку для использования преимущества от эффекта перемешивания, которое расходомер Вентури оказывает на поток. Углубление 1017, защищенное металлической сеткой, обеспечивает впускное отверстие для блока. Во время добычи скважинный флюид втекает в углубление 1017 и затем анализируется модулем 1016. Результаты передаются из модуля сбора данных на поверхность по кабелю 1013. Были описаны различные варианты осуществления и приложения настоящего изобретения. Описания вариантов предназначены для иллюстрации настоящего изобретения. Специалистам в данной области техники должно быть очевидно, что могут быть выполнены модификации описанного изобретения без отступления от объема формулы изобретения, приведенной ниже. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Электрохимический датчик, содержащий по меньшей мере две различные редокс-системы, чувствительные к одним и тем же частицам, причем упомянутые по меньшей мере две различные редокс-системы установлены на рабочем электроде; электрод сравнения, электронным образом связанный с рабочим электродом; и противоэлектрод, электронным образом связанный с рабочим электродом и электродом сравнения. 2. Датчик по п.1, в котором частицы представляют собой протоны. 3. Датчик по п.1, в котором по меньшей мере две редокс-системы имеют максимальную или пиковую редокс-реакцию при различных напряжениях. 4. Датчик по п.1, в котором рабочий электрод содержит субстрат на основе углерода. 5. Датчик по п.4, в котором рабочий электрод содержит субстрат из углеродного порошка. 6. Датчик по п.4, в котором рабочий электрод содержит субстрат на основе алмаза. 7. Датчик по п.6, в котором рабочий электрод содержит субстрат на основе многостенных нанотру-8 010172 бок. 8. Датчик по п.1, содержащий детектор, выполненный с возможностью измерения редокспотенциала указанных по меньшей мере двух редокс-систем в присутствии указанных частиц и для преобразования измерений в сигнал, соответствующий концентрации указанных частиц. 9. Электрохимический датчик для определения концентрации молекулярных частиц во флюиде, содержащий по меньшей мере две различные редокс-системы, чувствительные к упомянутым молекулярным частицам, причем упомянутые по меньшей мере две различные редокс-системы связаны с рабочим электродом; электрод сравнения, электронным образом связанный с рабочим электродом; и противоэлектрод, электронным образом связанный с рабочим электродом и электродом сравнения; источник напряжения и детектор электрического тока для выполнения измерений вольтамограмм и анализатор для детектирования относительных сдвигов в указанных измерениях вольтамограмм. 11. Скважинный инструмент для измерения характерных параметров эффлюентов в стволе скважине, содержащий электрохимический датчик по п.1. 12. Скважинный инструмент для отбора проб из пластов для измерения характерных параметров эффлюентов в стволе скважины, содержащий электрохимический датчик по п.1. 13. Скважинный инструмент для измерения характерных параметров эффлюентов в стволе скважины, содержащий электрохимический датчик по п.1, укрепленный на постоянно установленной части ствола скважины.
МПК / Метки
МПК: G01N 33/28, G01N 27/30, G01N 27/416, G01N 27/333
Метки: датчик, электрохимический
Код ссылки
<a href="https://eas.patents.su/14-10172-elektrohimicheskijj-datchik.html" rel="bookmark" title="База патентов Евразийского Союза">Электрохимический датчик</a>
Предыдущий патент: Способ получения полупроводниковых плёнок из четырёх и более компонентных сплавов элементов групп ib – iiia – via
Следующий патент: Установки и способы для переработки cos по реакции клауса
Случайный патент: Протеинкиназа candida albicans, обладающая активностью фосфорилирования циклинзависимых протеинкиназ, и способы ее применения