Способ выделения секоизоларицирезинола и дигидрокверцетина из древесины
Номер патента: 16246
Опубликовано: 30.03.2012
Авторы: Меньшов Владимир Михайлович, Цветков Юрий Евгеньевич, Нифантьев Николай Эдуардович, Цветков Дмитрий Евгеньевич, Яшунский Дмитрий Владимирович
Формула / Реферат
1. Способ выделения секоизоларицирезинола и дигидрокверцетина из древесины, в котором измельченную древесину сучковой зоны лиственницы (Larix) или пихты (Abies) экстрагируют нерасслаивающейся смесью органического растворителя с водой, при содержании растворителя 50-75%, с получением экстракта, содержащего секоизоларицирезинол и дигидрокверцетин, обрабатывают экстракт для удаления растворителя с получением конечной смеси, содержащей секоизоларицирезинол и дигидрокверцетин.
2. Способ по п.1, отличающийся тем, что в качестве сучковой зоны древесины используют ²белые сучки².
3. Способ по п.1, отличающийся тем, что в качестве органического растворителя используют ацетон.
4. Способ по п.1, отличающийся тем, что в качестве органического растворителя используют изопропиловый спирт.
5. Способ по п.1, отличающийся тем, что в качестве органического растворителя используют этиловый спирт.
6. Способ по любому из пп.1, 3-5, отличающийся тем, что содержание органического растворителя в смеси с водой составляет от 60 до 70%.
7. Способ выделения секоизоларицирезинола и дигидрокверцетина из древесины, в котором измельченную древесину сучковой зоны лиственницы (Larix) или пихты (Abies) экстрагируют нерасслаивающейся смесью органического растворителя с водой, при содержании растворителя 50-75%, с получением экстракта, содержащего секоизоларицирезинол и дигидрокверцетин, обрабатывают экстракт для удаления растворителя с получением смеси, содержащей секоизоларицирезинол и дигидрокверцетин, которую подвергают избирательной экстракции и кристаллизации с выделением секоизоларицирезинола и дигидрокверцетина.
8. Способ по п.7, отличающийся тем, что в качестве сучковой зоны древесины используют ²белые сучки².
9. Способ по п.7, отличающийся тем, что в качестве органического растворителя используют ацетон.
10. Способ по п.7, отличающийся тем, что в качестве органического растворителя используют изопропиловый спирт.
11. Способ по п.7, отличающийся тем, что в качестве органического растворителя используют этиловый спирт.
12. Способ по любому из пп.7, 9-11, отличающийся тем, что содержание органического растворителя в смеси с водой составляет от 60 до 70%.
13. Способ выделения секоизоларицирезинола и дигидрокверцетина из древесины, в котором измельченную древесину сучковой зоны лиственницы (Larix) или пихты (Abies) экстрагируют нерасслаивающейся смесью органического растворителя с водой, при содержании растворителя 50-75%, с получением экстракта, содержащего секоизоларицирезинол и дигидрокверцетин, затем экстракт обрабатывают для удаления неполярных компонентов, удаляют надосадочную жидкость, а полученный остаток хроматографируют на слое силикагеля с последующим удалением элюата, получая сухую смесь секоизоларицирезинола и дигидрокверцетина.
14. Способ по п.13, отличающийся тем, что в качестве сучковой зоны древесины используют ²белые сучки².
15. Способ по п.13, отличающийся тем, что в качестве органического растворителя используют ацетон.
16. Способ по п.13, отличающийся тем, что в качестве органического растворителя используют изопропиловый спирт.
17. Способ по п.13, отличающийся тем, что в качестве органического растворителя используют этиловый спирт.
18. Способ по любому из пп.13, 15-17, отличающийся тем, что содержание органического растворителя в смеси с водой составляет от 60 до 70%.
19. Применение секоизоларицирезинола и дигидрокверцетина, полученных экстракцией измельченной древесины сучковой зоны лиственницы (Larix) или пихты (Abies) нерасслаивающейся смесью органического растворителя с водой, при содержании растворителя 50-75%, с получением экстракта, содержащего секоизоларицирезинол и дигидрокверцетин, обработкой экстракта для удаления растворителя с получением конечной смеси, содержащей секоизоларицирезинол и дигидрокверцетин, в качестве компонентов биологически активных добавок и химико-фармацевтических изделий.
20. Применение секоизоларицирезинола и дигидрокверцетина, полученных экстракцией измельченной древесины сучковой зоны лиственницы (Larix) или пихты (Abies) нерасслаивающейся смесью органического растворителя с водой, при содержании растворителя 50-75%, с получением экстракта, содержащего секоизоларицирезинол и дигидрокверцетин, обработкой экстракта для удаления растворителя с получением смеси, содержащей секоизоларицирезинол и дигидрокверцетин, которую подвергают избирательной экстракции и кристаллизации с выделением секоизоларицирезинола и дигидрокверцетина, в качестве компонентов биологически активных добавок и химико-фармацевтических изделий.
21. Применение секоизоларицирезинола и дигидрокверцетина, полученных экстракцией измельченной древесины сучковой зоны лиственницы (Larix) или пихты (Abies) нерасслаивающейся смесью органического растворителя с водой, при содержании растворителя 50-75%, с получением экстракта, содержащего секоизоларицирезинол и дигидрокверцетин, затем обработкой экстракта для удаления неполярных компонентов, удалением надосадочной жидкости, хроматографированием полученного остатка на слое силикагеля с последующим удалением элюата, получением сухой смеси секоизоларицирезинола и дигидрокверцетина, в качестве компонентов биологически активных добавок и химико-фармацевтических изделий.
Текст
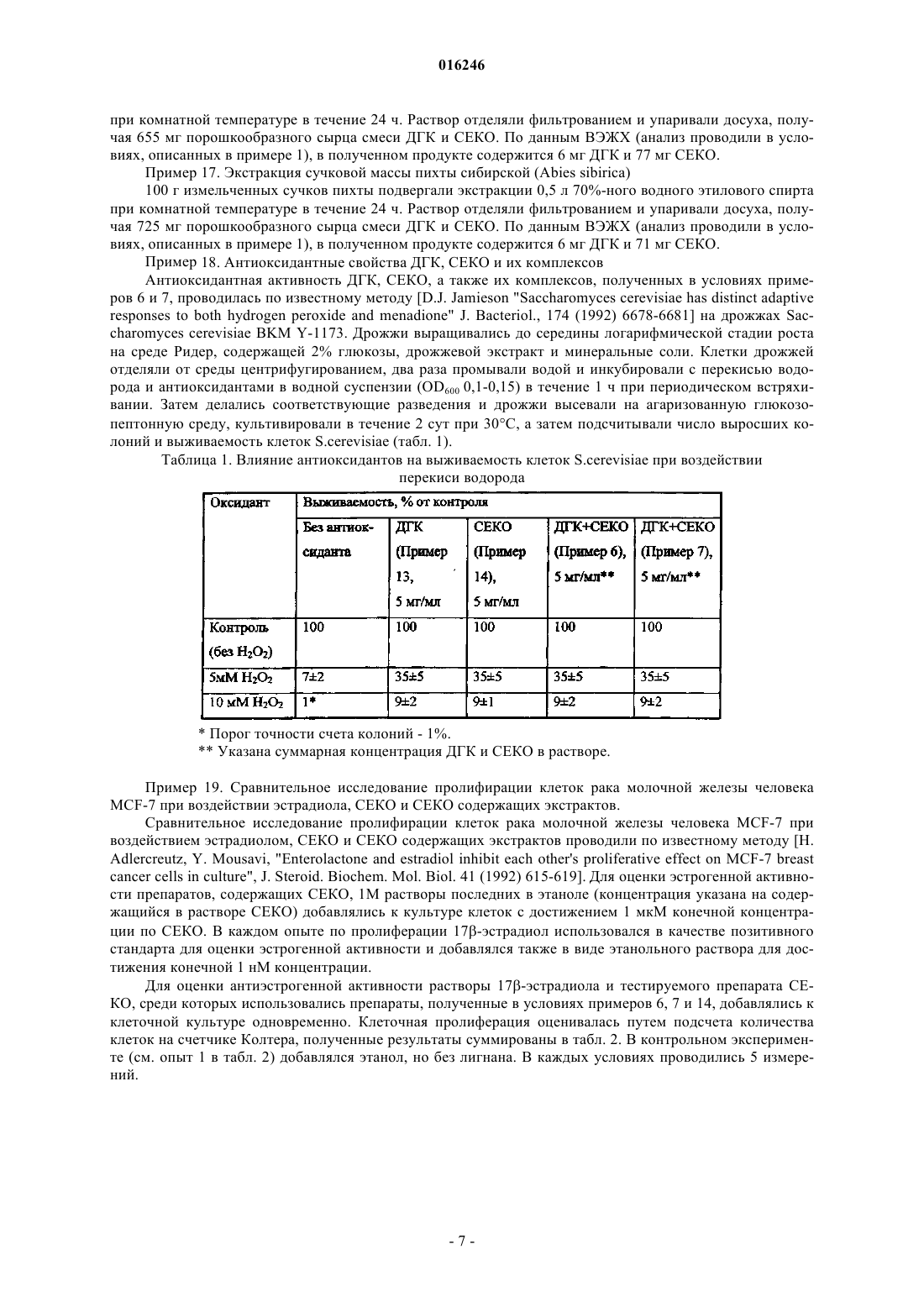
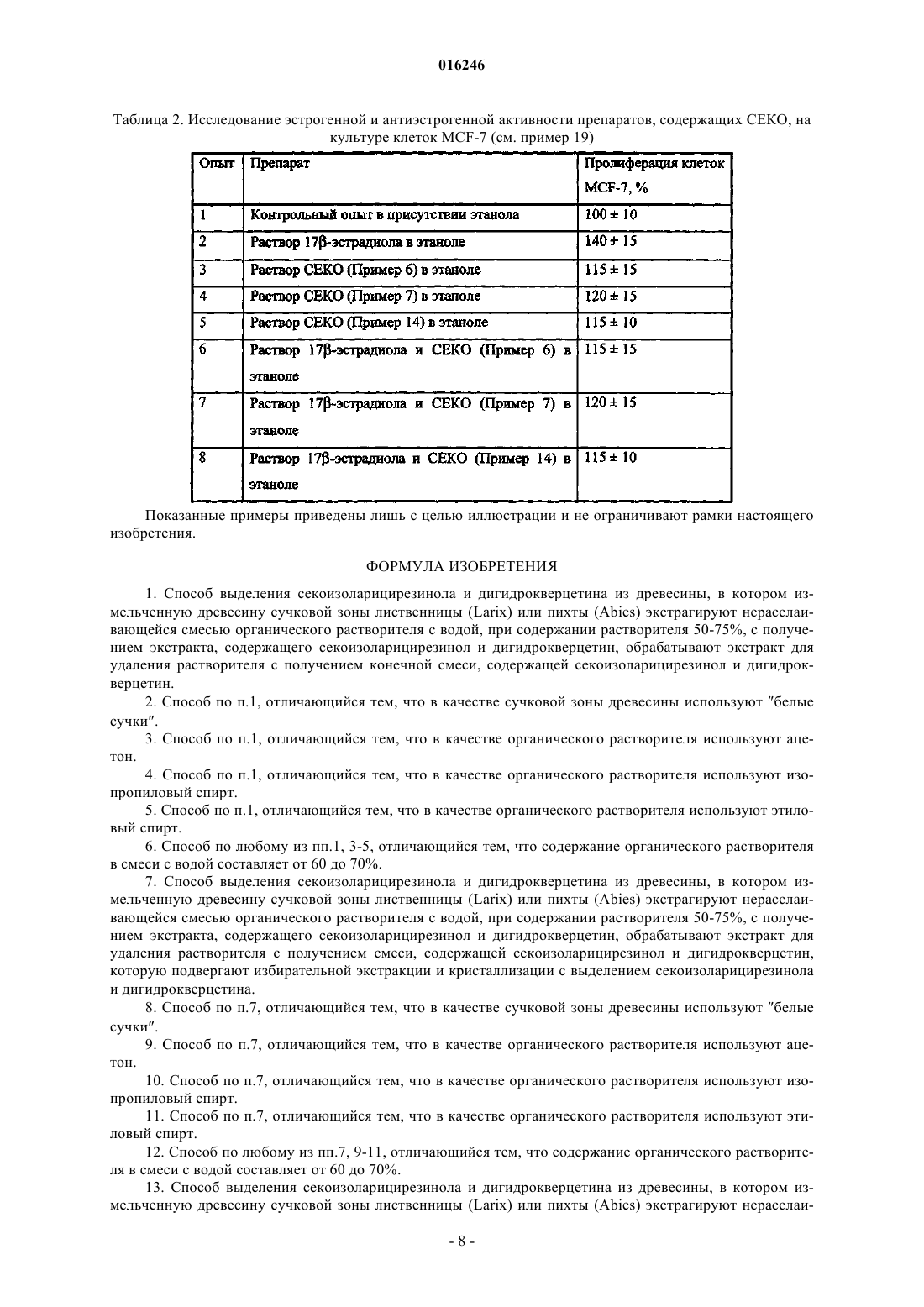
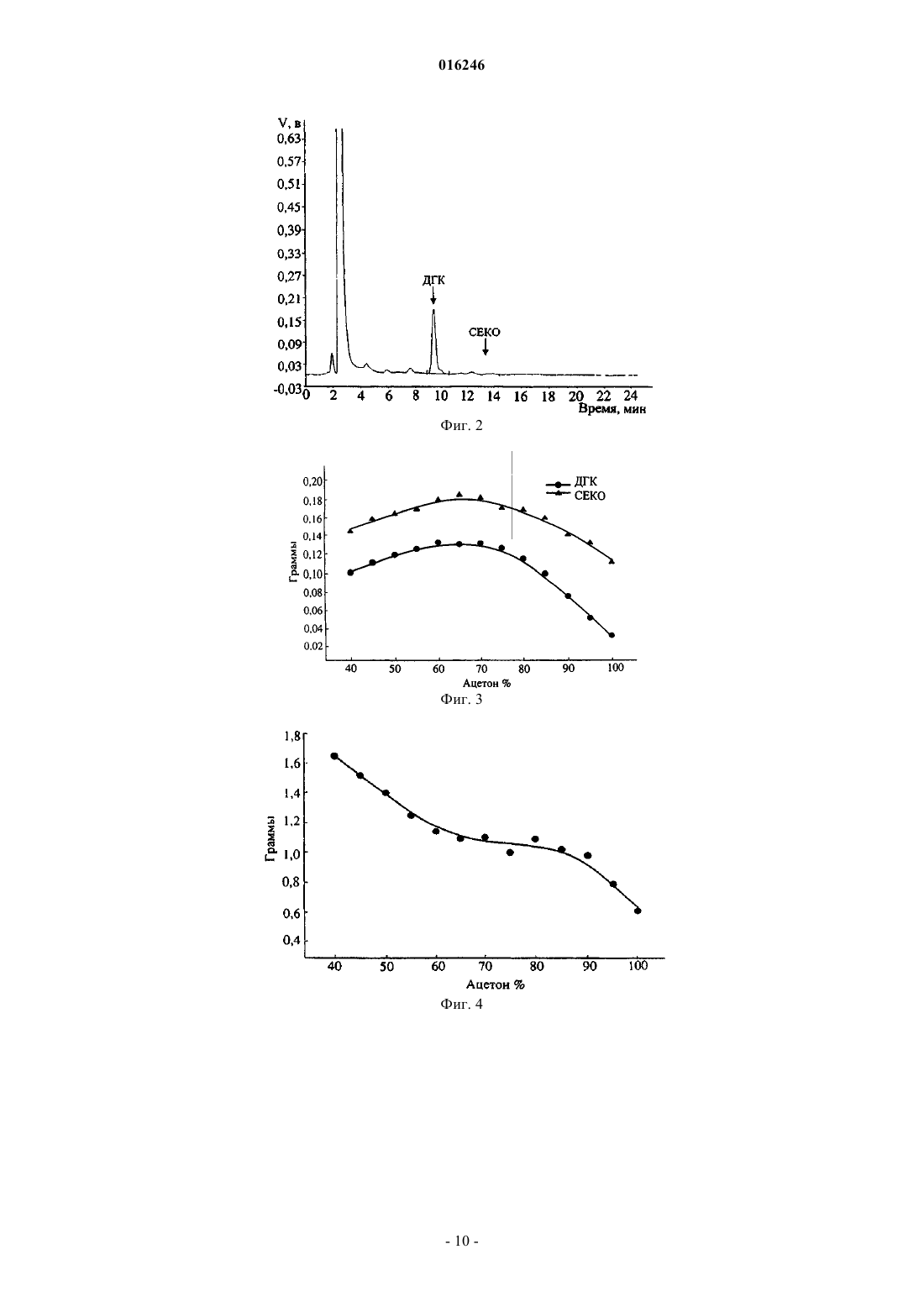
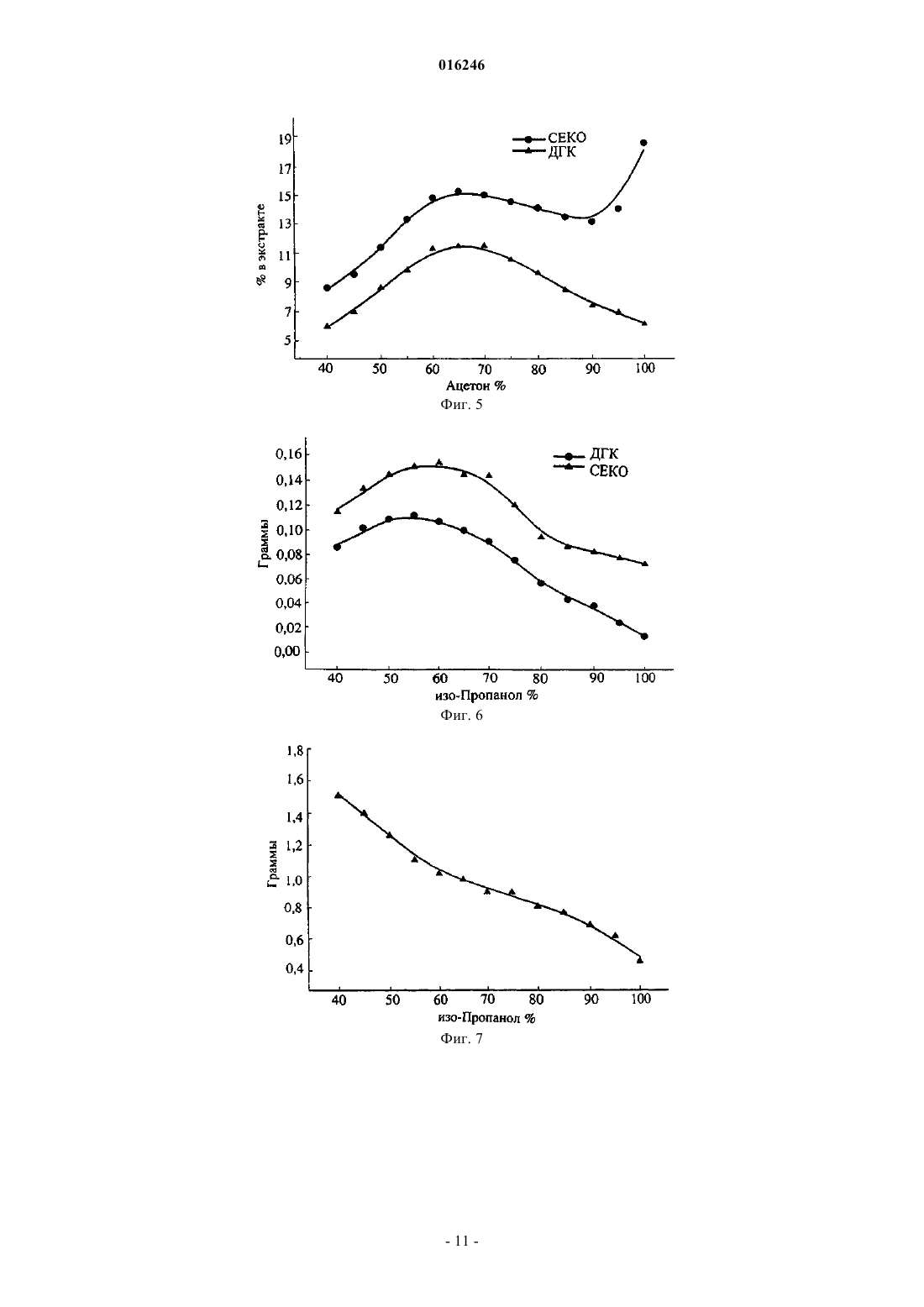
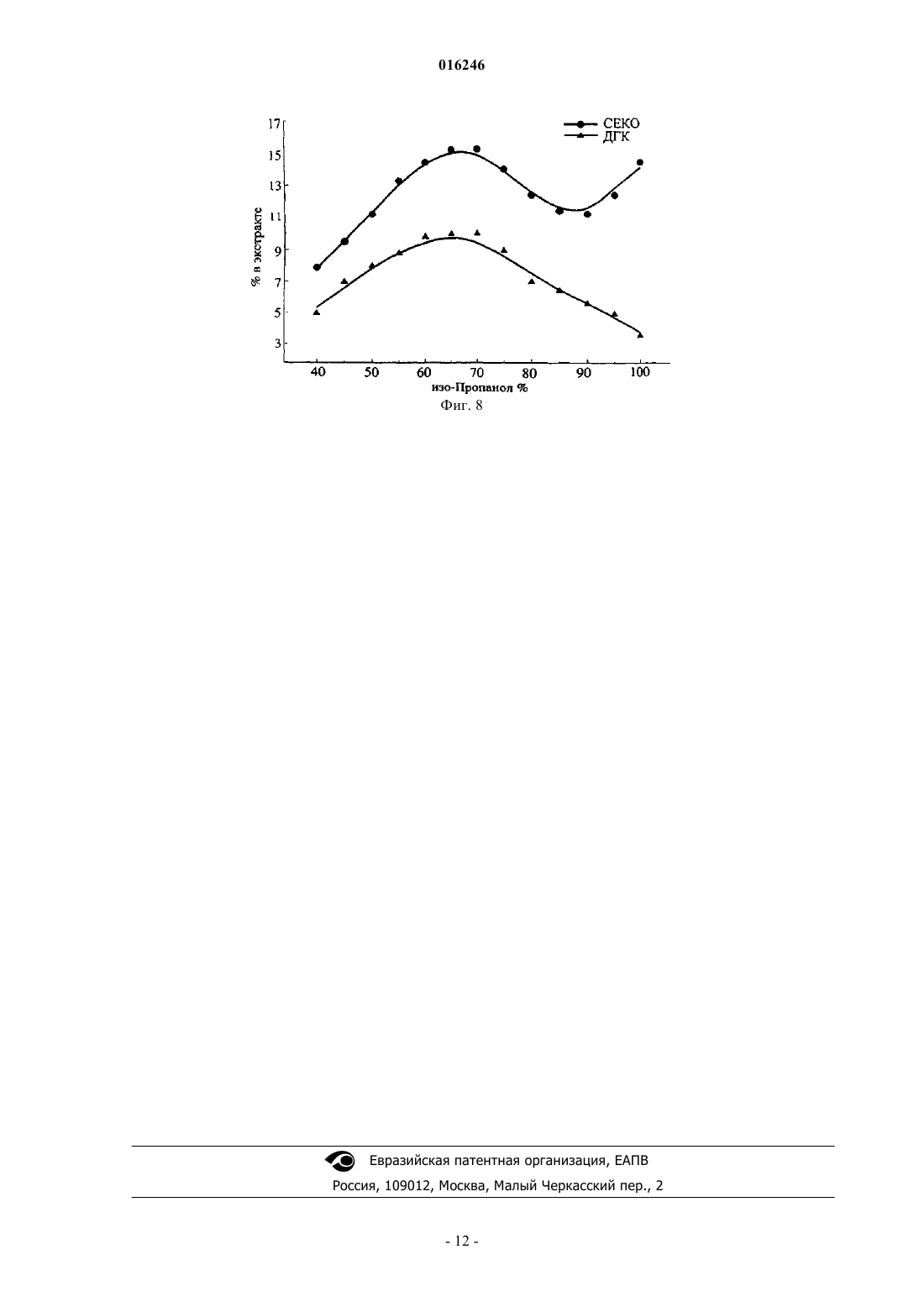
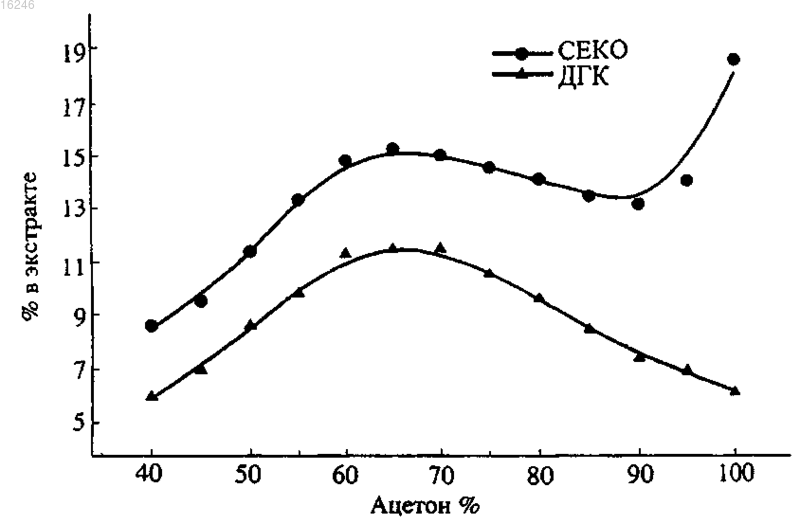
СПОСОБ ВЫДЕЛЕНИЯ СЕКОИЗОЛАРИЦИРЕЗИНОЛА И ДИГИДРОКВЕРЦЕТИНА ИЗ ДРЕВЕСИНЫ Предложен способ выделения секоизоларицирезинола и дигидрокверцетина из древесины. В предложенном способе измельченную древесину сучковой зоны экстрагируют нерасслаивающейся смесью органического растворителя с водой при содержании растворителя 50-75%, с получением экстракта, содержащего секоизоларицирезинол и дигидрокверцетин, обрабатывают экстракт для удаления растворителя с получением конечной смеси, содержащей секоизоларицирезинол и дигидрокверцетин. В другом варианте выполнения измельченную древесину сучковой зоны экстрагируют нерасслаивающейся смесью органического растворителя с водой, при содержании растворителя 50-75%, с получением экстракта, содержащего секоизоларицирезинол и дигидрокверцетин, обрабатывают экстракт для удаления растворителя с получением смеси,содержащей секоизоларицирезинол и дигидрокверцетин, которую подвергают избирательной экстракции и кристаллизации с выделением секоизоларицирезинола и дигидрокверцетина. В еще одном варианте выполнения измельченную древесину сучковой зоны экстрагируют нерасслаивающейся смесью органического растворителя с водой, при содержании растворителя 50-75%, с получением экстракта, содержащего секоизоларицирезинол и дигидрокверцетин,затем экстракт обрабатывают для удаления неполярных компонентов, удаляют надосадочную жидкость, а полученный остаток хроматографируют на слое силикагеля с последующим удалением элюата, получая сухую смесь секоизоларицирезинола и дигидрокверцетина. Предлагается также применение секоизоларицирезинола и дигидрокверцетина в качестве компонентов биологически активных добавок и химико-фармацевтических изделий. Нифантьев Николай Эдуардович,Яшунский Дмитрий Владимирович,Меньшов Владимир Михайлович,Цветков Юрий Евгеньевич, Цветков Дмитрий Евгеньевич (RU) Стояченко И.Л. (RU)(71)(73) Заявитель и патентовладелец: НИФАНТЬЕВ НИКОЛАЙ ЭДУАРДОВИЧ (RU) 016246 Область техники Настоящее изобретение относится к области высокотехнологичной лесохимической переработки древесины. В изобретении предложен способ выделения из древесины деревьев ценных физиологически активных соединений, включая обогащенные лигнанами и флавоноидами экстракты (лигнан-флавоноидные комплексы), а также разделенных лигнанов и флавоноидов, предназначенных для последующего использования при получении биологически активных добавок и химико-фармацевтических изделий. Уровень техники Лигнаны и флавоноиды относятся к классу фенольных соединений, содержащихся в различных частях растений, например в древесине хвойных пород деревьев. Содержащие производные лигнанов и флавоноидов химические экстракты и изготавливаемые на их основе препараты находят широкое применение в медицине и косметике, пищевой промышленности, в качестве агрохимических препаратов при производстве растениеводческой продукции, а также в других областях. Одним из представляющих интерес соединений, относящихся к лигнанам, является секоизоларицирезинол (СЕКО). В качестве представителя класса флавоноидов в способе по данному изобретению получают дигидрокверцетин (ДГК), для обозначения которого в литературе часто используют синоним таксифолин. ДГК достаточно широко изучался в исследовательских лабораториях для выяснения областей его практического использования. В России ДГК наиболее широко применяется в составе целого ряда биологически активных препаратов (например, препараты Капилар, Флукол и др.) и некоторых продуктов питания, что связано с высокими антиоксидантным, гепатопротекторным, иммуностимулирующим,противомикробным и другими практически полезными свойствами этого соединения. Так, на основе ДГК, выделяемого из опилок лиственницы сибирской и даурской, создан регулятор роста и развития сельскохозяйственных культур, коммерциализация которого проводится под коммерческим обозначением Лариксин (патент РФ 2229213; патент РФ 2256328). СЕКО также представляет собой весьма перспективный препарат для практического использования, особенно для производства лекарственных и биологически активных препаратов, а также функциональных продуктов питания, благодаря антиоксидантным, противовоспалительным, фитоэстрагенным,противомикробным и другим полезным свойствам этого соединения. Так, известна фармацевтическая композиция (WO 03/020254) на основе СЕКО (выделен из растения Stereospermum personatum), а также функциональные продукты питания (WO 02/080702), гепатопротекторные, противораковые препараты(US 2006/0035964) и другие препараты, включающие СЕКО. Известно, что сучковые зоны и ветки хвойных пород деревьев содержат значительные количества фенольных соединений [В. Holmbom, C. Eckerman, P. Eklund, J. Hemming, L. Nisula, M. Reunanen, R.Reviews 2: 331-340, 2003). Авторами настоящего изобретения, однако, было экспериментально установлено, что предпочтительным сырьем для выделения представляющих интерес соединений в промышленном производстве являются только так называемые белые сучки, то есть сучки, несущие живые ветки(см. пример 1 ниже). Получение фенольных соединений из сучковых зон древесины известно [см. патентную публикацию US 2004/0199032 от 7.10.2004]. В указанной публикации раскрыт способ выделения фенольных соединений из содержащей сучковые зоны древесины, в котором выполняют экстракцию измельченной древесины сучковой зоны полярным растворителем с последующим выделением веществ из экстракта. К недостаткам описанного способа можно отнести следующие технические ограничения. Предложенные условия разработаны для выделения одного целевого продукта, представителя класса лигнанов 7-гидроксиматаирезинола (HMR). Однако древесина хвойных деревьев содержит обычно не один компонент, относящийся к фенольным соединениям, причем такие компоненты относятся не только к классу лигнанов. Кроме них в древесине содержатся и представители класса флавоноидов, также как и производные лигнанов, имеющие большую практическую ценность. Экономическая целесообразность переработки указанного типа древесного сырья требует разработки способов одновременного извлечения соединений разных классов, например лигнанов и флавоноидов, для их дальнейшего использования. Однако оказалось, что указанный известный способ [US 2004/0199032 от 7.10.2004] является малоэффективным для одновременного выделения лигнанов в смеси с флавоноидами, которые имеют отличный от лигнанов профиль растворимости в органических растворителях. Другим недостатком известного способа является необходимость подготовки древесины для экстракции, включающей стадии промывки алканом для удаления летучих компонентов, а также последующую сушку, в том числе для удаления содер-1 016246 жащейся в древесине воды, присутствие которой видимо снижает экстрагирующую способность растворителя. Применяемый в указанном способе полярный растворитель определен обобщенно, посредством указания на константу диэлектрической проницаемости (которая должна быть больше 3 при 25C). Указанным величинам диэлектрической проницаемости, например, отвечают такие технологически важные растворители, как диэтиловый эфир, хлороформ и хлористый метилен (их диэлектрические проницаемости 4.34, 4.70 и 8.9, соответственно), в которых ДГК очень мало растворим, что не позволяет использовать указанные растворители для экстракции ДГК. В известном способе (US 2004/0199032 от 7.10.2004) также отмечено, что в качестве полярного растворителя можно применять смесь ацетон:вода, однако выбранное соотношение (95:5 об.%) компонентов смеси не позволяет получить представляющий интерес ДГК с достаточным выходом (см. пример 2 ниже). Задачей настоящего изобретения является разработка способа выделения фенольных соединений из древесины, лишенного указанных недостатков. Использование предложенного метода открывает широкие перспективы для производства широкого спектра биологически активных добавок, химикофармацевтических изделий и других продуктов. Поставленная задача решается настоящим изобретением. В способе по изобретению измельченную древесину сучковой зоны экстрагируют нерасслаивающейся смесью органического растворителя с водой, при содержании органического растворителя 50-75%, с получением экстракта, содержащего СЕКО и ДГК, обрабатывают экстракт для удаления растворителя с получением конечной смеси, содержащей СЕКО и ДГК. Промывка измельченной древесины сучковой зоны алканом, как в известном способе [US 2004/0199032 от 7.10.2004], или током CO2 (в т.ч. в условиях сверхкритической флюидной экстракции) позволяет только извлечь из древесной массы простейшие низкомолекулярные большей частью малополярные органические соединения, что не влияет на эффективность экстракции смеси ДГК и СЕКО в экспериментальных условиях настоящего изобретения. В другом варианте выполнения изобретения полученную смесь, содержащую СЕКО и ДГК, дополнительно подвергают избирательной экстракции и кристаллизации с выделением очищенных целевых соединений. В другом варианте выполнения изобретения экстракт, содержащий секоизоларицирезинол и дигидрокверцетин, дополнительно обрабатывают для удаления неполярных компонентов, удаляют надосадочную жидкость, а полученный остаток хроматографируют на слое силикагеля с последующим удалением элюата, получая сухую смесь секоизоларицирезинола и дигидрокверцетина. При этом в способах по данному изобретению в качестве древесины можно использовать древесину хвойных пород деревьев, предпочтительно лиственницы (Larix), в частности лиственницы сибирской(Larix sibirica) и даурской (Larix dahurica) и пихты (Abies), в частности пихты сибирской (Abies sibirica), а в качестве сучковой зоны древесины используют белые сучки. Как следует из данных, приведенных в примерах 2 и 3, наибольшая эффективность извлечения СЕКО и ДГК достигается при использовании смесей органического растворителя и воды, а в чистом органическом растворителе она ниже. Также, растворимость ниже и в чистой воде (не показано на фиг. 3-8), в которой целевые соединения имеют весьма ограниченную растворимость (растворение в воде требует нагревания). Поэтому важнейшим свойством используемого органического растворителя по данному изобретению является его способность смешиваться с водой в диапазоне указанных соотношений, давая гомогенную смесь с требуемой растворяющей активностью. Анализ растворителей по данному изобретению показывает, что их полярность характеризуется величиной константы диэлектрической проницаемости от 10 до 40 при 25-30C. В качестве органического растворителя могут использовать ацетон, при этом его содержание в смеси с водой составляет от 50 до 75%, предпочтительно от 60 до 70%. В другом варианте выполнения в качестве органического растворителя могут использовать изопропиловый спирт, при этом его содержание в смеси с водой составляет от 50 до 75%, предпочтительно от 60 до 70%. В других вариантах выполнения в качестве органического растворителя могут использовать и другие растворители, например этиловый спирт, удовлетворяющие указанным выше характеристикам, при этом содержание растворителя в смеси с водой составляет от 50 до 75%, предпочтительно от 60 до 70%. Ключевым преимуществом настоящего изобретения является обеспечение эффективного одновременного извлечения из древесной массы как соединения ряда лигнанов, так и флавоноидного соединения, представляющих практический интерес для использования их в виде смеси или после разделения. Преимуществом перед известным способом является также и простота выделения целевых соединений по настоящему изобретению, не требующая специальной отсушки экстрагируемой древесины (в известном способе применяют лиофильную сушку), измельчения замороженной древесной массы и промывания алканом перед экстракцией водно-органической смесью. Выходы ДГК в условиях данного изобретения соответствуют лучшим известным способам получе-2 016246 ния данного соединения из природных объектов (например, по способам, описанным в следующих источниках: Нифантьев Э.Е., Коротеев М.П., Казиев Г.З., Уминский А.А. Способ выделения дигидрокверцетина //Патент РФ 2180566, 2001 г.; Нифантьев Э.Е., Коротеев М.П., Казиев Г.З., Волков Г.А., Гатаулин Р.Ш. Способ комплексной переработки древесины лиственницы //Патент РФ 2233858, 2003 г.). Выход СЕКО в условиях данного изобретения существенно превышает таковой при экстракции из других известных природных источников, например из растений Stereospermum personatum - 0,03% (WO 03/020254), Carissa edulis - 0,0004% [Phytochemistry, 22 (1983) 749], Uniperus chinensis - 0,00245% [Phytochemistry, 31 (1992)3659]. Ниже приведены примеры, не ограничивающие рамки изобретения, снабженные сопроводительными чертежами, на которых: на фиг. 1 показана хроматограмма экстракта из опилок белых сучков лиственницы; на фиг. 2 - хроматограмма экстракта из опилок черных сучков; на фиг. 3 - результаты экстракции сучковой массы (белые сучки) лиственницы ацетоном и водноацетоновыми смесями, показаны весовые количества ДГК и СЕКО в экстрактах; на фиг. 4 - результаты экстракции сучковой массы (белые сучки) лиственницы ацетоном и водноацетоновыми смесями, показан общий вес экстрактов после упаривания растворителя; на фиг. 5 - результаты экстракции сучковой массы (белые сучки) лиственницы ацетоном и водноацетоновыми смесями, показано содержание ДГК и СЕКО в упаренных ацетоновом и водно-ацетоновых экстрактах; на фиг. 6 - результаты экстракции сучковой массы (белые сучки) лиственницы изопропанолом и водно-изопропанольными смесями, показаны весовые количества ДГК и СЕКО в экстрактах; на фиг. 7 - результаты экстракции сучковой массы (белые сучки) лиственницы изопропанолом и водно-изопропанольными смесями, показан общий вес экстрактов после упаривания растворителя; на фиг. 8 - результаты экстракции сучковой массы (белые сучки) лиственницы изопропанолом и водно-изопропанольными смесями, показано содержание ДГК и СЕКО в упаренных изопропаноловом и водно-изопропаноловых экстрактах. Обогащенные лигнанами и флавоноидами экстракты (лигнан-флавоноидные комплексы), как и лигнаны и флавоноиды после разделения, имеют широкое применение для получения биологическиактивных добавок и химико-фармацевтических изделий разных типов. При этом соответствующая биологическая активность лигнан-флавоноидных комплексов определяется содержанием в них лигнанного и флавоноидного компонентов, что демонстрируют приведенные ниже примеры, не ограничивающие рамки изобретения. Так, антиоксидантные свойства лигнан-флавоноидных комплексов определяются суммарным содержанием в них лигнанного (СЕКО) и флавоноидного (ДГК) компонентов. Табл. 1 демонстрирует антиоксидантные свойства ДГК, СЕКО, а также их комплексов, экстрагируемых из сучковой массы лиственницы согласно данному изобретению (описание эксперимента дано в примере 18). Из табл. 1 видно, что эквимолекулярные количества ДГК и СЕКО проявляют одинаковую антиоксидантную активность, как и лигнан-флавоноидные комплексы, содержащие то же суммарное количество в них лигнанного (СЕКО) и флавоноидного (ДГК) компонентов. Это позволяет использование лигнан-флавоноидных комплексов наряду с их разделнными лигнанным (СЕКО) и флавоноидным (ДГК) компонентами при производстве антиоксидантных химико-фармацевтических изделий и биологически-активных добавок, связанных с лечением и профилактикой сердечно-сосудистых заболеваний и инфекционных поражений, корректировкой липидного обмена, укреплением иммунного статуса и других. Важнейшая сфера применения образующихся по данному изобретению лигнан-флавоноидных комплексов и выделенного лигнанного компонента (СБКО) является использование при получении химикофармацевтических изделий и биологически-активных добавок, предназначенных для профилактики и лечения эстраген опосредованных процессов. При этом известно, что СЕКО, как и ДГК, обладают низкой эстрагенной активностью, однако под действием ферментативной системы микрофлоры СЕКО претерпевает превращение в энтеролактон (ENL), обладающий эстрагенной активностью. Это и определяет применение содержащим СЕКО продуктам, как биологического предшественника ENL, а также может использоваться для получения химико-фармацевтических изделий и биологически активных добавок,предназначенных для профилактики и лечения эстраген опосредованных процессов, связанных с онкологическими заболеваниями, развитием гиперплазии, нарушениями здоровья женщин, в том числе вызванных менопаузой. В качестве примера, не ограничивающего рамки настоящего изобретения, в табл. 2 показана эстрагенная активность СЕКО, а также комплексов СЕКО и ДГК, экстрагируемых из сучковой массы лиственницы согласно данному изобретению (описание эксперимента дано в примере 19). При использовании препаратов, содержащих одинаковое количество СЕКО, наблюдается одинаковый пролиферативный эффект (эксперимент с клетками MCF-8), а также и способность конкурентно ингибировать аналогичный эффект природного гормона - эстрадиола.-3 016246 Пример 1. Хроматографический анализ компонентов экстрактов массы белых сучков и черных сучков и хроматографический анализ компонентов экстрактов. Экстракцию образцов измельченной массы (для корректного сопоставления экспериментальных данных в этом и последующих примерах приведены результаты экстракции частиц толщиной до 1 мм,проходящие через сито с размером каналов диаметром 3 мм) белых и черных сучков лиственницы сибирской (Larix sibirica, далее лиственницы), несущих живые и мертвые ветки, проводили 70%-водным ацетоном при комнатной температуре в течение 24 ч (соотношение образец - растворитель 1:10). Аликвоты растворов (10 мкл) анализировали посредством ВЭЖХ [Э.Е. Нифантьев, М.П. Коротеев, Г.З. Казиев, В.К. Бельский, А.И.Сташ, А.А. Грачев, В.М. Меньшов, Ю.Е. Цветков, Н.Э. Нифантьев, "К вопросу об идентификации флавоноида дигидрокверцетина.", ЖОХ, 16 (2006) 161-163] на колонке Ultrasphere ODS(5 мкм, 4,6 мм 25 см; Beckman) в системе ацетонитрил (20%) - вода, содержащей 1 мл/л трифторуксусной кислоты при скорости потока 0,8 мл/мин с использованием УФ-детектора (254 нм). Количественная характеристика содержания ДГК и СЕКО в экстрактах проводилась по калибровочным кривым, полученным при хроматографическом анализе аналитически чистых образцов ДГК и СЕКО. Анализ хроматограмм экстрактов (фиг. 1, 2) свидетельствует о содержании ДГК и СЕКО в белых сучках в количестве 1,2 и 1,7% от общего веса, соответственно, а в черных сучках присутствуют только следы СЕКО, а содержание ДГК составляет лишь около 0,5% от общего веса. Эти данные указывают на то, что масса белых сучков является предпочтительным сырьем для выделения ДГК и СЕКО. Пример 2. Экстракция сучковой массы лиственницы ацетоном и водно-ацетоновыми смесями и хроматографический анализ компонентов экстрактов. Стандартные порции (10 г) измельченной массы белых сучков лиственницы подвергали экстракции в 100 мл ацетона или водно-ацетоновых смесях разного состава при комнатной температуре в течение 24 ч. Экстракты отделяли фильтрованием через стеклянный фильтр ( 3) и упаривали досуха. Навеску сухого остатка (25 мг) растворяли в 10 мл ацетонитрила и анализировали посредством ВЭЖХ, как описано выше в примере 1 для определения содержания ДГК и СЕКО в исходном образце сучковой массы с использованием хроматографических характеристик заведомо чистых образцов ДГК и СЕКО. Результаты экспериментов суммированы на фиг. 3-5, на которых показаны весовые количества ДГК и СЕКО в экстрактах (фиг. 3), общий вес экстрактов после упаривания растворителя (фиг. 4), а также содержание ДГК и СЕКО в упаренных ацетоновом и водно-ацетоновых экстрактах (фиг. 5). Анализ хроматограмм свидетельствует о том, что при экстракции смесями при содержании ацетона в интервале от 50 до 75%, в особенности от 60 до 70% достигается наиболее эффективное экстрагирование ДГК и СЕКО. При увеличении содержания ацетона в экстрагенте свыше 75% либо при снижении ниже 50% содержание ДГК и СЕКО в экстракте снижается. Кроме этого при экстрагировании смесями с содержанием воды свыше 50% наблюдается увеличение общей массы экстракта за счет извлечения из сучковой массы нецелевых компонентов, в особенности хорошо растворимых в водных средах производных углеводов и других соединений, что в дальнейшем усложняет очистку ДГК и СЕКО. Пример 3. Экстракция сучковой массы лиственницы изопропиловым спиртом и водно-изопропанольными смесями и хроматографический анализ компонентов экстрактов. Экстракцию стандартных порций (10 г) измельченной массы белых сучков лиственницы проводили в 100 мл изопропилового спирта или водно-изопропанольными смесями разного состава при комнатной температуре в течение 24 ч. Экстракты сначала обрабатывали, а затем анализировали с помощью ВЭЖХ, как описано в примере 2. Результаты экспериментов суммированы на фиг. 6-8, на которых показаны весовые количества ДГК и СЕКО в экстрактах (фиг. 6), общий вес экстрактов после упаривания растворителя (фиг. 7), а также содержание ДГК и СЕКО в упаренных изопропанольном и водно-изопропанольных экстрактах (фиг. 8). Анализ хроматограмм и данных по общему весу экстрактов свидетельствует о том, что при экстракции смесями при содержании изопропанола в интервале от 50 до 75%, в особенности от 60 до 70%, достигается наиболее эффективное экстрагирование ДГК и СЕКО. При увеличении содержания изопропанола в экстрагенте свыше 75%, либо при снижении ниже 50%, содержание ДГК и СЕКО в экстракте снижается. Кроме этого, при экстрагировании смесями с содержанием воды свыше 50% наблюдается увеличение общей массы экстракта за счет извлечения из сучковой массы нецелевых компонентов, в особенности производных углеводов, что в дальнейшем усложняет очистку ДГК и СЕКО. Пример 4. Исследование кавитационной дезинтеграции сучковой массы в воде с последующей экстракцией органическими растворителями 300 г измельченных сучков лиственницы подвергали кавитационной обработке в 10 л воды при 95C по способу, описанному в патенте РФ 2180566, опубликованном 20.03.2002, и патенте РФ 2233858, опубликованном 10.08.2004. Образующуюся смесь охлаждали до комнатной температуры, нерастворимые компоненты отделяли фильтрованием или центрифугированием (2 ч при 2000 об/мин). По-4 016246 пытки проэкстрагировать фильтрат, представляющий собой устойчивую эмульсию, с помощью несмешивающихся с водой растворителей различной полярности (алканы, ароматические соединения, эфиры,хлорированные растворители) не привели к успеху, так как не достигалось образование слоев органической и водной фаз, даже при добавке в смеси растворов NaCl и алифатических спиртов, что обычно способствует разделению слоев при экстракции водных растворов. Таким образом, способ выделения ДГК и СЕКО из сучковой массы, включающий на первом этапе кавитационную дезинтеграцию в воде, на практике не является эффективным. Пример 5. Экстракция сучковой массы лиственницы 70%-ным водным ацетоном 1 кг измельченных сучков лиственницы подвергали экстракции 5 л 70%-ного водного ацетона при комнатной температуре в течение 24 ч. Раствор отделяли фильтрованием и упаривали досуха, получая 87 г порошкообразного сырца смеси ДГК и СЕКО. По данным ВЭЖХ (анализ проводился в условиях, описанных в примере 1), в полученном продукте содержится 9,8 г ДГК и 14,3 г СЕКО. Пример 6. Экстракция сучковой массы лиственницы Экстракцию измельченных сучков лиственницы проводили 70%-ным водным ацетоном, как описано в примере 5. К образцу полученного продукта весом 5 г прибавляли 50 мл воды и кипятили 1 ч при перемешивании, горячий раствор отделяли от маслообразного остатка, упаривали досуха и получали 1,8 г обогащенного ДГК и СЕКО продукта-сырца, содержащего 23% ДГК (414 мг) и 32% СЕКО (576 мг) (по данным ВЭЖХ в условиях, описанных в примере 1). Пример 7. Экстракция сучковой массы лиственницы 70%-ным водным изопропанолом 1 кг измельченных сучков лиственницы подвергали экстракции 5 л 70%-ного водного изопропанола при комнатной температуре в течение 24 ч. Раствор отделяли фильтрованием и упаривали досуха, получая 83 г порошкообразного продукта-сырца, содержащего 7,4 г ДГК и 12,2 г СЕКО (по данным ВЭЖХ в условиях, описанных в примере 1). Пример 8. Экстракция сучковой массы лиственницы 70%-ным водным этанолом. 0,1 кг измельченных сучков лиственницы подвергали экстракции 720 мл 70%-ного водного этилового спирта при комнатной температуре в течение 24 ч. Раствор отделяли фильтрованием и упаривали досуха, получая 7,12 г порошкообразного продукта-сырца, содержащего 655 мг ДГК и 810 мг СЕКО (по данным ВЭЖХ в условиях, описанных в примере 1). Пример 9. Получение смеси СЕКО и ДГК в соотношении примерно 1:1 чистотой, равной 75% и более. Экстракцию измельченных сучков лиственницы проводили 70%-ным водным ацетоном, как описано в примере 5. К образцу полученного продукта весом 5 г прибавляли смесь этилацетат-петролейный эфир (1:2, 10 мл) и перемешивали при 50C, температуру доводили до комнатной и надосадочную жидкость отделяли декантацией (или фильтрованием через бумажный или стеклянный фильтр). Полученный остаток хроматографировали на слое силикагеля, элюируя смесь ДГК и СЕКО метилтретбутиловым эфиром (100 мл). Элюат упаривали досуха, получая 1,45 г порошка, представляющего по данным ВЭЖХ (в условиях, описанных в примере 1) смесь ДГК и СЕКО в соотношении примерно 1:1 чистотой, равной 75% или более. Аналогично проводили и выделения смесей СЕКО и ДГК указанной чистоты при обработке органических экстрактов сучковой массы другими водно-органическими смесями по данному изобретению, например, образующимися из продуктов, полученных в примерах 2, 7, 8 и 15-17. При этом соотношения СЕКО и ДГК в выделяемом продукте определяется их содержанием в исходном сырье. Пример 10. Получение смеси СЕКО и ДГК в соотношении примерно 1:1 чистотой, равной 75% и более. Экстракцию измельченных сучков лиственницы проводили 70%-ным водным ацетоном, как описано в примере 5. Образец полученного продукта весом 5 г перемешивали 10-120 мин при нагревании не выше 50C с 10-30 мл смеси углеводородного растворителя и более полярного растворителя, взятых в таком соотношении, что при проведении тонкослойной хроматографии на стандартных пластинках с силикагелем величины хроматографической подвижности (Rf) СЕКО и ДГК находятся в интервале 00,05. После окончания перемешивания температуру смеси доводили до комнатной, и надосадочную жидкость отделяли декантацией (или фильтрованием через бумажный или стеклянный фильтр). Полученный остаток хроматографировали на слое силикагеля, элюируя смесь ДГК и СЕКО метилтретбутиловым эфиром (100 мл). Элюат упаривали досуха, получая 1,45 г порошка, представляющего по данным ВЭЖХ (в условиях, описанных в примере 1) смесь ДГК и СЕКО в соотношении примерно 1:1 чистотой, равной 75% или более. В качестве углеводородного растворителя могут использовать технологически доступные алифатические или ароматические соединения, например индивидуальные алканы, петролейный эфир, толуол и другие. В качестве полярного растворителя могут использовать органические соединения, характеризующиеся величиной константы диэлектрической проницаемости от 4 до 25 при 25-30C. Например,можно использовать смесь этилацетата и петролейного эфира в соотношении 1:2. Аналогично проводили и выделения смесей СЕКО и ДГК указанной чистоты при обработке органических экстрактов сучковой массы другими водно-органическими смесями по данному изобретению,-5 016246 например, образующимися из продуктов, полученных в примерах 2, 7, 8 и 15-17. При этом соотношения СЕКО и ДГК в выделяемом продукте определяется их содержанием в исходном сырье. Пример 11. Получение смеси СЕКО и ДГК в соотношении примерно 1:1 чистотой, равной 75% и более. Экстракцию измельченных сучков лиственницы проводили 70%-ным водным ацетоном, как описано в примере 5. Образец полученного продукта весом 5 г перемешивали 10-60 мин при нагревании не выше 50C с 10-30 мл смеси углеводородного растворителя и более полярного растворителя с величиной константы диэлектрической проницаемости от 4 до 25 при 25-30C. В качестве углеводородного растворителя могут использовать технологически доступные алифатические или ароматические соединения,например индивидуальные алканы, петролейный эфир, толуол и другие. Количества взятого полярного компонента зависит от величины его диэлектрической проницаемости. Так, при диэлектрической проницаемости от 20 до 25 берется 10 об.%, при диэлектрической проницаемости от 15 до 20 берется 20 об.%,при диэлектрической проницаемости от 10 до 15 берется 30 об.%, а при диэлектрической проницаемости от 4 до 10 берется 40 об.%. Например, в соответствии с указанными характеристиками растворителей можно использовать смесь этилацетата и петролейного эфира в соотношении 1:2. После окончания перемешивания температуру смеси доводили до комнатной и надосадочную жидкость отделяли декантацией (или фильтрованием через бумажный или стеклянный фильтр). Полученный остаток хроматографировали на слое силикагеля, элюируя смесь ДГК и СЕКО метилтретбутиловым эфиром (100 мл). Элюат упаривали досуха, получая 1,45 г порошка, представляющего по данным ВЭЖХ (в условиях, описанных в примере 1) смесь ДГК и СЕКО в соотношении примерно 1:1 чистотой, равной или более 75%. Аналогично проводили и выделения смесей СЕКО и ДГК указанной чистоты при обработке органических экстрактов сучковой массы другими водно-органическими смесями по данному изобретению,например, образующимися из продуктов, полученных в примерах 2, 7, 8 и 15-17. При этом соотношение СЕКО и ДГК в выделяемом продукте определяется их содержанием в исходном сырье. Пример 12. Получение образцов СЕКО и ДГК чистотой, равной 75% и более Экстракцию измельченных сучков лиственницы проводили 70%-ным водным ацетоном, как описано в примере 5. К образцу полученного продукта весом 5 г прибавляли 50 мл воды и кипятили 1 ч при перемешивании, горячий раствор отделяли от маслообразного остатка, температуру раствора доводили до комнатной и экстрагировали хлороформом (830 мл). Органическую фазу отделяли, сушили и упаривали досуха, получая 670 мг сырца СЕКО с чистотой, равной 75% или более (определено ВЭЖХ в условиях, описанных в примере 1). Оставшуюся после экстракции водную фазу экстрагировали этилацетатом(330 мл), экстракты объединяли, высушивали и упаривали досуха, получая 481 мг сырца ДГК с чистотой, равной 75% или более (определено ВЭЖХ в условиях, описанных в примере 1). Аналогично проводили и выделения смесей СЕКО и ДГК указанной чистоты при обработке органических экстрактов сучковой массы другими водно-органическими смесями по данному изобретению, например, образующимися из продуктов Примеров 2, 7, 8 и 15-17. При этом соотношения СЕКО и ДГК в выделяемом продукте определяется их содержанием в исходном сырье. Пример 13. Получение ДГК чистотой 95-97% и более. ДГК чистотой 95-97% и более получали перекристаллизацией сырца (пример 12). Например, образец ДГК (0,48 г), полученный в условиях примера 12, растворяли в 5 мл деаэрированной воды при 7080C, охлаждали образующийся раствор до 4C и выдерживали смесь до окончания кристаллизации. Выпавшие кристаллы отфильтровали и высушили в вакууме, получив 0.31 г ДГК указанной чистоты, контролируемой по данным ВЭЖХ в условиях, описанных в примере 1. Данные спектра 13C ЯМР (, м.д.;DMSO-d6; Bruker WM-250, 62,9 MHz): 71,6 (C3), 83,1 (C2), 95,0 (C8), 96,0 (C6), 100,5 (C10), 115,2 (C5'),115,4 (C2'), 119,5 (C1'), 145,0 (C4'), 145,8 (C3'), 162,6 (C9), 163,4 (C5), 166,8 (C7), 197,9 (C4). Пример 14. Получение СЕКО чистотой 95-97% и более. СЕКО чистотой 95-97% и более получали перекристаллизацией сырца (пример 12). Например, образец СЕКО (660 мг), полученный в условиях примера 12, растворяли в 7 мл диэтилового эфира при 30C, раствор охлаждали до 4C и выдерживали смесь до окончания кристаллизации. Выпавшие кристаллы отфильтровали и высушили в вакууме, получив 405 мг СЕКО указанной чистоты, контролируемой по данным ВЭЖХ в условиях, описанных в примере 1. Данные спектра 13C ЯМР (, м.д.; DMSO-d6;Bruker WM-250, 62,9 MHz): 34,0 (C3,3'), 42,5 (C2,2'), 55,5 (OMe), 60,3 (C1,1'), 113,0 (C6,6'), 115,0 (C9,9'),121,1 (C5,5'), 132,2 (C4,4'), 144,3 (C7,7'), 147,2 (C8,8'). Пример 15. Экстракция сучковой массы пихты сибирской (Abies sibirica). 100 г измельченных сучков пихты подвергали экстракции 0.5 л 70%-ного водного ацетона при комнатной температуре в течение 24 ч. Раствор отделяли фильтрованием и упаривали досуха, получая 733 мг порошкообразного сырца смеси ДГК и СЕКО. По данным ВЭЖХ (анализ проводили в условиях, описанных в примере 1), в полученном продукте содержится 7 мг ДГК и 91 мг СЕКО. Пример 16. Экстракция сучковой массы пихты сибирской (Abies sibirica) 100 г измельченных сучков пихты подвергали экстракции 0.5 л 70%-ного водного изопропанола-6 016246 при комнатной температуре в течение 24 ч. Раствор отделяли фильтрованием и упаривали досуха, получая 655 мг порошкообразного сырца смеси ДГК и СЕКО. По данным ВЭЖХ (анализ проводили в условиях, описанных в примере 1), в полученном продукте содержится 6 мг ДГК и 77 мг СЕКО. Пример 17. Экстракция сучковой массы пихты сибирской (Abies sibirica) 100 г измельченных сучков пихты подвергали экстракции 0,5 л 70%-ного водного этилового спирта при комнатной температуре в течение 24 ч. Раствор отделяли фильтрованием и упаривали досуха, получая 725 мг порошкообразного сырца смеси ДГК и СЕКО. По данным ВЭЖХ (анализ проводили в условиях, описанных в примере 1), в полученном продукте содержится 6 мг ДГК и 71 мг СЕКО. Пример 18. Антиоксидантные свойства ДГК, СЕКО и их комплексов Антиоксидантная активность ДГК, СЕКО, а также их комплексов, полученных в условиях примеров 6 и 7, проводилась по известному методу [D.J. Jamieson "Saccharomyces cerevisiae has distinct adaptiveresponses to both hydrogen peroxide and menadione" J. Bacteriol., 174 (1992) 6678-6681] на дрожжах Saccharomyces cerevisiae BKM Y-1173. Дрожжи выращивались до середины логарифмической стадии роста на среде Ридер, содержащей 2% глюкозы, дрожжевой экстракт и минеральные соли. Клетки дрожжей отделяли от среды центрифугированием, два раза промывали водой и инкубировали с перекисью водорода и антиоксидантами в водной суспензии (OD600 0,1-0,15) в течение 1 ч при периодическом встряхивании. Затем делались соответствующие разведения и дрожжи высевали на агаризованную глюкозопептонную среду, культивировали в течение 2 сут при 30C, а затем подсчитывали число выросших колоний и выживаемость клеток S.cerevisiae (табл. 1). Таблица 1. Влияние антиоксидантов на выживаемость клеток S.cerevisiae при воздействии перекиси водорода Порог точности счета колоний - 1%.Указана суммарная концентрация ДГК и СЕКО в растворе. Пример 19. Сравнительное исследование пролифирации клеток рака молочной железы человекаMCF-7 при воздействии эстрадиола, СЕКО и СЕКО содержащих экстрактов. Сравнительное исследование пролифирации клеток рака молочной железы человека MCF-7 при воздействием эстрадиолом, СЕКО и СЕКО содержащих экстрактов проводили по известному методу [H.cancer cells in culture", J. Steroid. Biochem. Mol. Biol. 41 (1992) 615-619]. Для оценки эстрогенной активности препаратов, содержащих СЕКО, 1 М растворы последних в этаноле (концентрация указана на содержащийся в растворе СЕКО) добавлялись к культуре клеток с достижением 1 мкМ конечной концентрации по СЕКО. В каждом опыте по пролиферации 17-эстрадиол использовался в качестве позитивного стандарта для оценки эстрогенной активности и добавлялся также в виде этанольного раствора для достижения конечной 1 нМ концентрации. Для оценки антиэстрогенной активности растворы 17-эстрадиола и тестируемого препарата СЕКО, среди которых использовались препараты, полученные в условиях примеров 6, 7 и 14, добавлялись к клеточной культуре одновременно. Клеточная пролиферация оценивалась путем подсчета количества клеток на счетчике Колтера, полученные результаты суммированы в табл. 2. В контрольном эксперименте (см. опыт 1 в табл. 2) добавлялся этанол, но без лигнана. В каждых условиях проводились 5 измерений.-7 016246 Таблица 2. Исследование эстрогенной и антиэстрогенной активности препаратов, содержащих СЕКО, на культуре клеток MCF-7 (см. пример 19) Показанные примеры приведены лишь с целью иллюстрации и не ограничивают рамки настоящего изобретения. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ выделения секоизоларицирезинола и дигидрокверцетина из древесины, в котором измельченную древесину сучковой зоны лиственницы (Larix) или пихты (Abies) экстрагируют нерасслаивающейся смесью органического растворителя с водой, при содержании растворителя 50-75%, с получением экстракта, содержащего секоизоларицирезинол и дигидрокверцетин, обрабатывают экстракт для удаления растворителя с получением конечной смеси, содержащей секоизоларицирезинол и дигидрокверцетин. 2. Способ по п.1, отличающийся тем, что в качестве сучковой зоны древесины используют белые сучки. 3. Способ по п.1, отличающийся тем, что в качестве органического растворителя используют ацетон. 4. Способ по п.1, отличающийся тем, что в качестве органического растворителя используют изопропиловый спирт. 5. Способ по п.1, отличающийся тем, что в качестве органического растворителя используют этиловый спирт. 6. Способ по любому из пп.1, 3-5, отличающийся тем, что содержание органического растворителя в смеси с водой составляет от 60 до 70%. 7. Способ выделения секоизоларицирезинола и дигидрокверцетина из древесины, в котором измельченную древесину сучковой зоны лиственницы (Larix) или пихты (Abies) экстрагируют нерасслаивающейся смесью органического растворителя с водой, при содержании растворителя 50-75%, с получением экстракта, содержащего секоизоларицирезинол и дигидрокверцетин, обрабатывают экстракт для удаления растворителя с получением смеси, содержащей секоизоларицирезинол и дигидрокверцетин,которую подвергают избирательной экстракции и кристаллизации с выделением секоизоларицирезинола и дигидрокверцетина. 8. Способ по п.7, отличающийся тем, что в качестве сучковой зоны древесины используют белые сучки. 9. Способ по п.7, отличающийся тем, что в качестве органического растворителя используют ацетон. 10. Способ по п.7, отличающийся тем, что в качестве органического растворителя используют изопропиловый спирт. 11. Способ по п.7, отличающийся тем, что в качестве органического растворителя используют этиловый спирт. 12. Способ по любому из пп.7, 9-11, отличающийся тем, что содержание органического растворителя в смеси с водой составляет от 60 до 70%. 13. Способ выделения секоизоларицирезинола и дигидрокверцетина из древесины, в котором измельченную древесину сучковой зоны лиственницы (Larix) или пихты (Abies) экстрагируют нерасслаи-8 016246 вающейся смесью органического растворителя с водой, при содержании растворителя 50-75%, с получением экстракта, содержащего секоизоларицирезинол и дигидрокверцетин, затем экстракт обрабатывают для удаления неполярных компонентов, удаляют надосадочную жидкость, а полученный остаток хроматографируют на слое силикагеля с последующим удалением элюата, получая сухую смесь секоизоларицирезинола и дигидрокверцетина. 14. Способ по п.13, отличающийся тем, что в качестве сучковой зоны древесины используют белые сучки. 15. Способ по п.13, отличающийся тем, что в качестве органического растворителя используют ацетон. 16. Способ по п.13, отличающийся тем, что в качестве органического растворителя используют изопропиловый спирт. 17. Способ по п.13, отличающийся тем, что в качестве органического растворителя используют этиловый спирт. 18. Способ по любому из пп.13, 15-17, отличающийся тем, что содержание органического растворителя в смеси с водой составляет от 60 до 70%. 19. Применение секоизоларицирезинола и дигидрокверцетина, полученных экстракцией измельченной древесины сучковой зоны лиственницы (Larix) или пихты (Abies) нерасслаивающейся смесью органического растворителя с водой, при содержании растворителя 50-75%, с получением экстракта,содержащего секоизоларицирезинол и дигидрокверцетин, обработкой экстракта для удаления растворителя с получением конечной смеси, содержащей секоизоларицирезинол и дигидрокверцетин, в качестве компонентов биологически активных добавок и химико-фармацевтических изделий. 20. Применение секоизоларицирезинола и дигидрокверцетина, полученных экстракцией измельченной древесины сучковой зоны лиственницы (Larix) или пихты (Abies) нерасслаивающейся смесью органического растворителя с водой, при содержании растворителя 50-75%, с получением экстракта,содержащего секоизоларицирезинол и дигидрокверцетин, обработкой экстракта для удаления растворителя с получением смеси, содержащей секоизоларицирезинол и дигидрокверцетин, которую подвергают избирательной экстракции и кристаллизации с выделением секоизоларицирезинола и дигидрокверцетина, в качестве компонентов биологически активных добавок и химико-фармацевтических изделий. 21. Применение секоизоларицирезинола и дигидрокверцетина, полученных экстракцией измельченной древесины сучковой зоны лиственницы (Larix) или пихты (Abies) нерасслаивающейся смесью органического растворителя с водой, при содержании растворителя 50-75%, с получением экстракта,содержащего секоизоларицирезинол и дигидрокверцетин, затем обработкой экстракта для удаления неполярных компонентов, удалением надосадочной жидкости, хроматографированием полученного остатка на слое силикагеля с последующим удалением элюата, получением сухой смеси секоизоларицирезинола и дигидрокверцетина, в качестве компонентов биологически активных добавок и химикофармацевтических изделий.
МПК / Метки
МПК: A61K 36/15, B01D 11/02, A61K 31/352, A61K 31/085
Метки: способ, древесины, выделения, секоизоларицирезинола, дигидрокверцетина
Код ссылки
<a href="https://eas.patents.su/13-16246-sposob-vydeleniya-sekoizolaricirezinola-i-digidrokvercetina-iz-drevesiny.html" rel="bookmark" title="База патентов Евразийского Союза">Способ выделения секоизоларицирезинола и дигидрокверцетина из древесины</a>
Предыдущий патент: Производные замещенных пиридинов
Следующий патент: Топическая композиция для уменьшения темных кругов, отечности и отвисания кожи в области глаз человека и способ ее применения
Случайный патент: Вещество, обладающее нейромодуляторной активностью