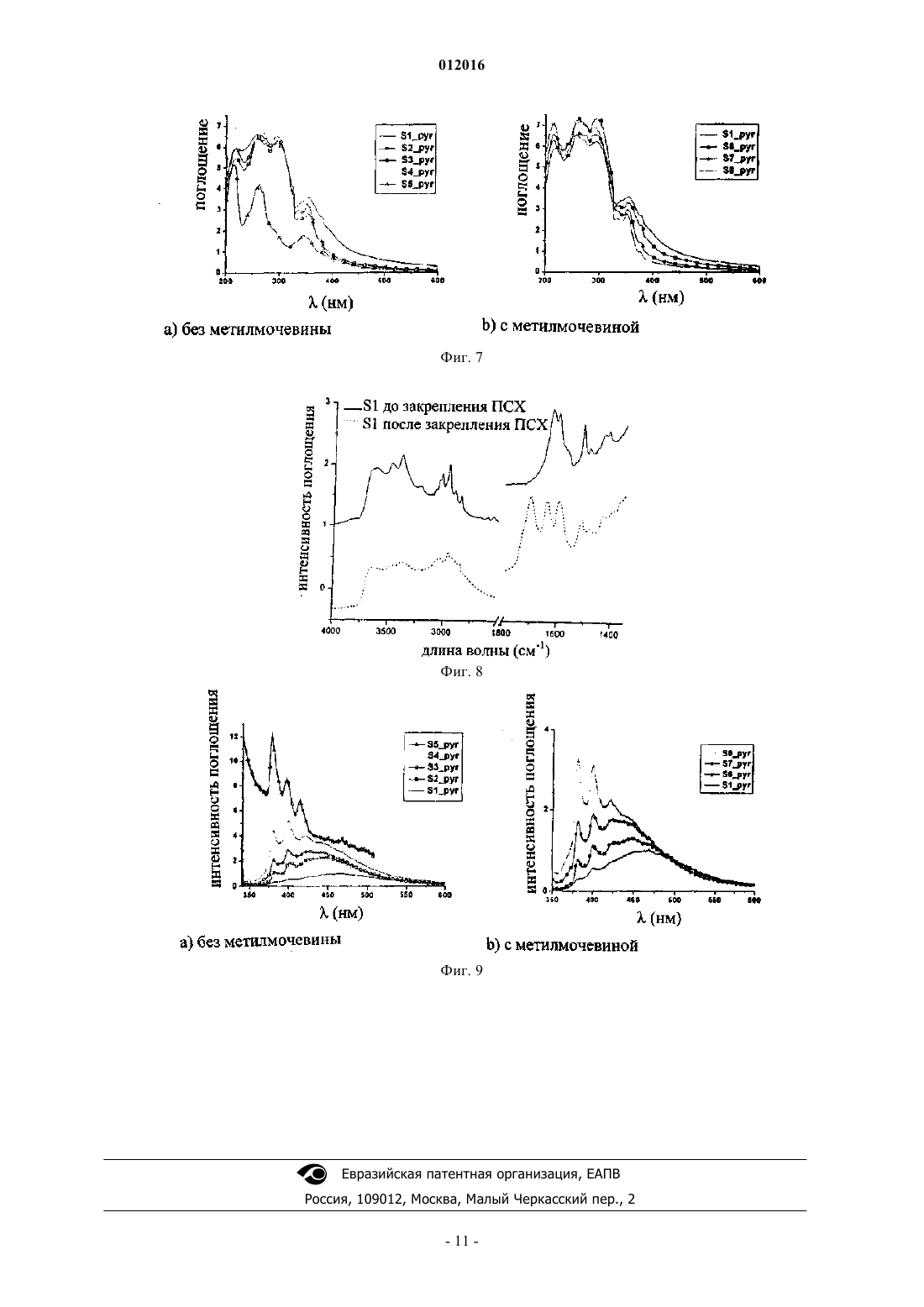
Способ распределения функциональных молекул по поверхности носителя и носитель, получаемый в результате этого способа
Номер патента: 12016
Опубликовано: 30.06.2009
Авторы: Сироль Сабина, Фажула Франсуа, Бане Филипп, Лернер Дан, Разави Аббас, Брюнель Даниель
Формула / Реферат
1. Способ распределения закрепленных функциональных органических цепей, в котором прививают на поверхность носителя, изготовленного из неорганического пористого материала,
1) силан общей формулы RnR'3-n-Si-L-X, где R является алкильной группой с числом атомов углерода от 1 до 2, причем R одинаковы или различны, a R' представляет собой галоген или алкоксигруппу с числом атомов углерода от 1 до 12, причем R' одинаковы или различны, n является целым числом от 0 до 2, L представляет собой жесткий или гибкий "линкер", а X является функциональной группой, обеспечивающей ковалентное связывание при реакциях присоединения или замещения;
2) вспомогательный агент, выбираемый для сильной сольватации функциональной группы прививаемой функциональной цепи, чтобы предотвратить агрегацию функциональных групп и занять пространство между функциональными группами X;
а затем отмывают привитый носитель полярным растворителем для удаления вспомогательного агента;
возможно, отверждают и пассивируют привитый носитель.
2. Способ по п.1, в котором L представляет собой жесткий "линкер", выбираемый из арила, моно- и бифенила, нафталина, простого полиарилового эфира или эфира дифенола.
3. Способ по п.2, в котором в качестве жесткого "линкера" используется фенильная группа.
4. Способ по п.1, в котором L представляет собой гибкий "линкер", выбираемый из алкилов, имеющих от 1 до 12 атомов углерода.
5. Способ по пп.1-4, в котором функциональную группу X выбирают из галогена, гидроксильной, карбоксильной, аминогруппы, изоцианата, тиола или глицидила.
6. Способ по п.5, в котором вспомогательный агент выбирают в зависимости от функциональной группы X следующим образом:
производное мочевины, амид или карбамат, если X - амин;
диол или аминокислота, если X - галоген;
производное мочевины, амид или ксантат, если X - тиол;
производное мочевины, амид или аминокислота, если X - нитрил;
производное мочевины или амид, если X - изоцианат.
7. Способ по п.6, в котором функциональная группа X - галоген, а вспомогательный агент - диол или аминокислота, или X - амин, а вспомогательный агент - производное мочевины, амид или карбамат.
8. Способ по п.7, в котором вспомогательный агент - производное мочевины, а функциональная группа - амин.
9. Способ по любому из предшествующих пунктов, в котором соотношение силана и вспомогательного агента составляет от 1:20 до 1:1.
10. Носитель из неорганического пористого материала, привитый закрепленными функциональными органическими цепями, распределенными по его поверхности, получаемый способом по любому из пп.1-9.
Текст
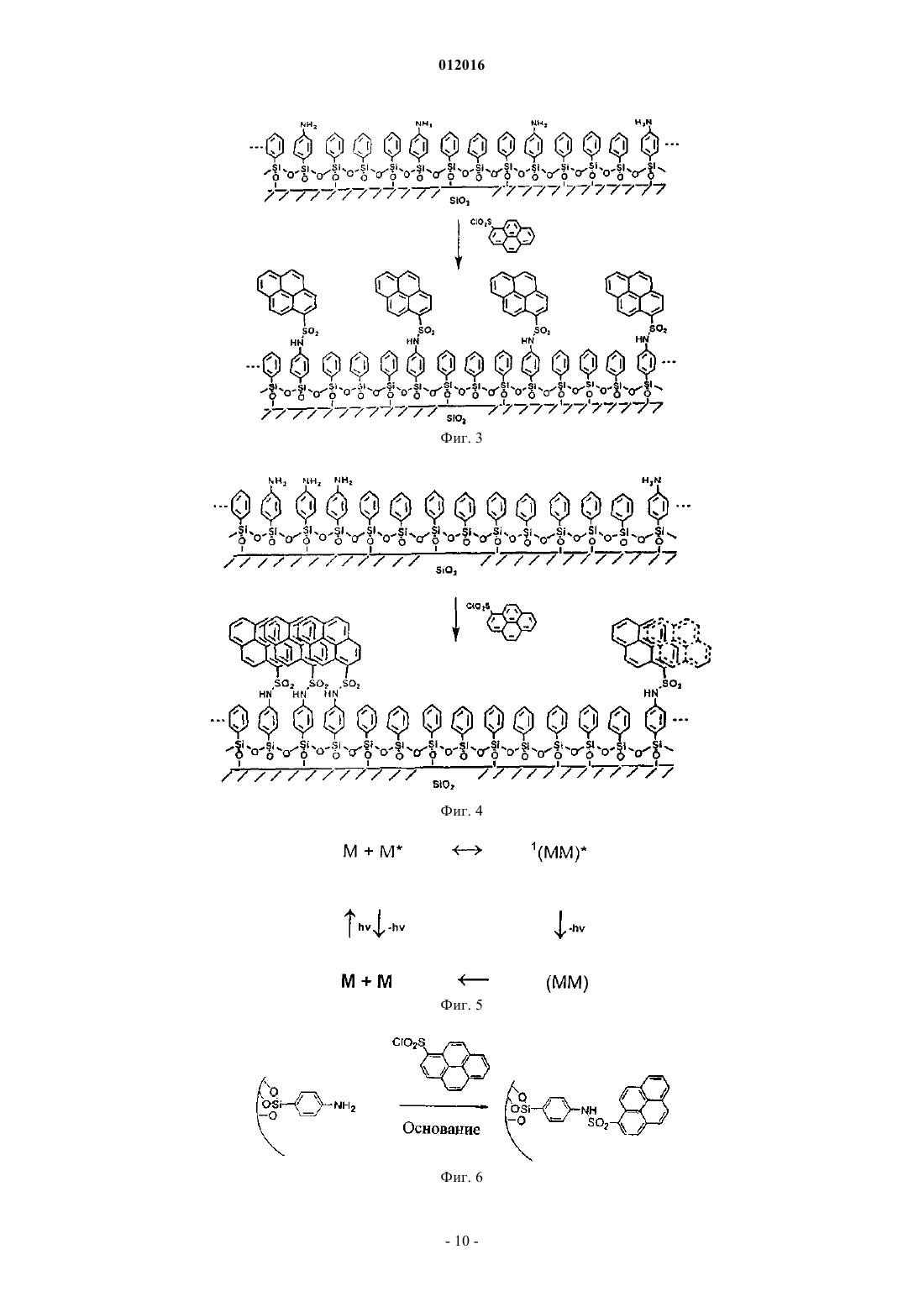
012016 Данное изобретение относится к области регулируемого пространственного распределения функциональных групп по неорганической поверхности в ходе однореакторного синтеза. Присоединение органических молекулярных структур к неорганическим поверхностям обеспечивает уникальную возможность управлять свойствами поверхности. Для внедрения органических групп и молекул на поверхность неорганических материалов использовались различные способы. Гибридные органические-неорганические материалы получали путем прямой прививки или осаждения на неорганическую поверхность (оксиды металлов, такие как, например, диоксид кремния, диоксид титана, оксид алюминия, диоксид циркония и т.п., или металлы, такие как, например, кремний, золото, платина) органических молекул, содержащих способные к присоединению функциональные группы, такие как, например, алкокси- или галогеносиланы, производные фосфоновых или фосфиновых кислот, сульфонаты, карбоксилаты, олефины, тиолы или дисульфиды, как описано, например, в статьях W.A. Aue and C.R. Hastings,J. Chromatog., 42 (1969) 319, K.G. Allum, R.D. Hancok, I.V. Howell, S. McKenzie, R.C. Pitkethly and P.J. Robinson,J. Organometal. Chem., 87 (1975) 203, O. Leal, D.L. Anderson, R.G. Bowman, F. Basolo and R.L. Burwell, Jr.,J. Am. Chem. Soc., 97 (1975) 5125, J.F. Fritz and J.N. King, Anal. Chem., 48 (1976) 570, P. Tundo and P. Venturello,J. Am. Chem. Soc., 101 (1979) 6606, H. Engelhardt and P. Orth, J. Liq. Chromatog., 10 (1987) 1999, A. Cauvel,G. Renard, and D. Brunei, J. Org. Chem., 1997. 62: p. 749, H.D. Abruna, T.L. Meyer and R.W. Murray, Inorg.Chem., 18 (1979) 3233, H.D. Abruna, T.L. Meyer and R.W. Murray, Inorg. Chem., 20 (1981 ) 1481, P. Sutra,F. Fajula, D. Brunei, P. Lentz, G. Daelen and J.B. Nagy, Colloid and Surfaces, 158 (1999) 21, D. Brunei,A. Cauvel, F. Di Renzo, F. Fajula, B. Fubini, B. Onida and E. Garrone, New J. Chem., 24 (2000) 807-813,M. Etienne, J. Bessiere and A. Walcarius, Sens. Actuators B, 76 (2001) 531. Более новый способ получения диоксида кремния с гибридной функциональностью, включающий однореакторный золь-гель синтез с использованием органических триалкоксисиланов, которые конденсируются совместно с тетраалкоксисиланами или силикатами, используемыми в качестве источника диоксида кремния, описан, например, в статьях K.J. Shea, D.A. Loy and D.W. Webster, Chem. Mater., 1 (1989) 574, D.J. Macquarrie, Chem. Commun., (1996) 1775, S.L. Burkitt, S.D. Sims and S. Mann, Chem. Commun.(1996) 1367, R.J.P. Corriu, J.J.E. Moreau, P. Thepot, M. Wong Chi Man, Chem. Mater., 4 (1992), M.H. Lim,C.F. Blanford and A. Stein, Chem. Mater., 10 (1998) 467. Сборные однослойные структуры, содержащие функциональные группы на неорганической поверхности, находят широкое научное и практическое применение в различных областях, таких как, например, адсорбция, ионообмен, катализ, зондирование, нелинейная оптика и распознавание биомолекул. Управление распределением, в основном, дисперсией функциональных групп очень важно для повышения производительности этих материалов в большинстве указанных областей применения. Однако в литературе имеется только несколько примеров обсуждения изоляции активных центров и регулирования расстояния между привитыми функциональными группами. В первом подходе две аминные группы прививали на фиксированном расстоянии друг от друга путем их связывания с разделяющим агентом,несущим карбонильную группу, способным образовывать иминные связи, который после прививки следует удалять при помощи специфической реакции. Этот способ описан, например, в статьях G. Wulff,В. Heide, G. Helmeier, in J. Amer. Chem. Soc., 1986, 108, 1089 или G. Wulff, B. Heide, G. Helmeier, in React.Polym., 1987, 6, 299. Эту стратегию заимствовали из предыдущих работ по молекулярному импринтингу на матрице из сшитого пористого полимера, инициированных, в основном, K.J. Shea et al. (K.J. Shea andAm. Chem. Soc., 1980, 102, 3149; K.J. Shea and T.K. Dougherty, J. Am. Chem. Soc., 1986, 108, 1091), и этот подход стимулировал других исследователей для создания более приспособляемых активных центров внутри впечатанной полимерной хиральной полости, как описано в работе J.J. Becker and M.R. Gagne,Асе Chem. Res., 2004, 37, 798-804. Аналогичные методологии были адаптированы Tahmassebi и Sasaki (D.С. Tahmassebi, Т. Sasaki, J.Org. Chem., 1994, 59, 679) и Hwang et al. (K.-O. Hwang, Y. Yakura, F.S. Ohuchi, T. Sasaki, Mater. Sci. Eng.,С 1995, 3, 137), a также Liu et al. (J. Liu, Y. Shin, L.-Q. Wang, Z. Nie, J.W.D. Samuels,. H. Chang, G. Fryxell,and G.J. Exarhos, in J. Phys. Chem. A 2000, 104, 8328) и Shin et al. (Y. Shin, J. Liu, L.-Q. Wang, Z. Nie,G. Fryxell, W.D. Samuels and G.J. Exarhos, Ang. Chem. Int. Ed. 2000, 39, 2702). Они прикрепляли две или три молекулы аминопропилсилана, используя различные типы темплатов с двумя или тремя ответвлениями, которые были связаны с защищаемой частью поверхности иминными связями во время нанесения на нее однослойного покрытия из длинноцепочечных органических силанов. Эти темплатные молекулы впоследствии удаляли гидролизом в кислой среде, чтобы оставить в монослойном покрытии впечатанные прямоугольные или треугольные микрополости. Следует отметить, что эта процедура позволяла получить не отдельные свободные точки, а свободные участки поверхности. Кроме того, не удавалось получить однородное распределение темплатов по поверхности из-за возможной агрегации этих молекул,приводящей к негативному влиянию на размер и форму полостей.Katz и Davis использовали похожий подход с прививкой изолированных аминогрупп путем прямого синтеза диоксида кремния с импринтингом с помощью методики золь-гель синтеза in situ (A. Katz andM.E. Davis, Nature, 000, 403, 286). В этой работе аминные функциональные группы защищали присоединением карбаматной группы, несущей отпечаток, которая кроме изоляции центра создавала при ее уда-1 012016 лении организованные в пространстве пустые участки. Следует отметить, что формирование конечного геля с прикрепленными и распределенными аминными центрами требовало также последующего удаления впечатанной молекулы и контроля распределения центров, который осуществляли при помощи тестмолекул с одной или двумя активными группами, образующими связь. Позднее Jones и др. исследовали изоляцию привитой аминной функциональной группы с помощью методики молекулярного структурирования с использованием большой молекулы тритилимина (трифенилметилимина), индивидуально закрепленной на поверхности диоксида кремния (М.W. McKittrick and С.W. Jones, Chem. Mater. 2003, 15, 1132-1139; M.W. McKittrick and С.W. Jones, J. Am. Chem. Soc., 2004,126, 3052-3053). Изоляцию аминного центра после блокирования силанола и гидролиза иминновой защитной связи контролировали путем реакции веществ, содержащих аминные функциональные группы, с терефталилхлоридом, которая приводила к образованию соединений с моно- или диамидными группами,и анализа непрореагировавших монохлоридов кислот, как описано выше. Другую стратегию использовали Bonneviot и др. для создания гидрофильных центров на частично силилированном диоксиде кремния, полученном с использованием мицелл в качестве темплата (L. Bonneviot,A. Badiei, N. Crowther, US-A-2004/0035791). Поскольку диоксид кремния типа МСМ-41 обычно изготавливают путем совместной сборки силикатов с длинноцепочечным катионом алкилтриметиламмония в качестве темплатного агента, авторы воспользовались преимуществом присутствия положительно заряженного поверхностно-активного вещества (ПАВ) в качестве противоиона для силикатов в получаемом мезопористом диоксиде кремния, чтобы привить имеющиеся в окружающей среде силаны с создающим основание триметилсилилирующим агентом. После удаления ПАВ частично триметилированная поверхность материала содержала силановые группы, полученные из силикатов после замещения ПАВ, которые были равномерно распределены по минеральной поверхности. Эти материалы с силанольными группами, окруженными гидрофобной средой, были доступны для дальнейшей модификации поверхности, например дополнительной функционализации путем создания каталитических центров. Такая стратегия включает многостадийную процедуру и может использоваться только для диоксида кремния, полученного с использованием мицелл в качестве темплата. Эти методы сложны и требуют длительной и трудоемкой обработки. В данном изобретении предлагают альтернативный подход к разработке гибридных материалов на основе прикрепляемых к минеральному каркасу органических цепей, имеющих функциональные цепи -LX с одним активным центром, распределенные между нефункциональными цепями -L. Он основан на разбавлении функционального прикрепляемого агента-предшественника нефункциональными агентами в соотношении более 1:4 с целью получения равномерного распределения функциональных групп. Предпочтительно, чтобы разделяющий агент имел такую же органическую цепь L, что и функциональный агент. Взаимодействия функциональных групп между собой и взаимодействия между функциональными группами и носителем, такие как, например, водородные связи для аминов, могут создавать в ходе прививки некоторую упаковку функциональных цепей. Несмотря на разбавление, близость функциональных групп может привести к образованию скоплений прикрепленных функциональных цепей. Это наносит вред истинному молекулярному распределению функциональных групп, что показано на фиг. 1.Moreau и др. (J.J.E. Moreau, Luc Vellutini, Michel Wong Chi Man, and Catherine Bied, Chem. Eur. J. 2003, 9, 1594-1599) разработали способ синтеза организованных трехмерных гибридных структур путем гомогенной реакции гидролиза-конденсации соответствующих силилированных органических молекул. Способ учитывает возможную самоассоциацию классов соединений в ходе надмолекулярной сборки,которая в состоянии направить пространственную организацию функциональных органических молекул в протяженную структуру, похожую на нановолокно, используя множественные водородные связи. Это описано, например, в работах J. van Esch и др. (J. van Esch, S. de Feyter, R.M. Kellogg, F. de Schryver and(J.M. Lehn, Angew. Chem. Inter. Ed., 1990, 29, 1304-1319). Благодаря группам бис-мочевины, которые несут в себе эти предшественники, молекулы собираются в надмолекулярную ассоциацию за счет множества водородных связей, как описано в работе J.J.E. Moreau и др. (J.J.E. Moreau, B.P. Pichon, M. Wong ChiMan, С. Bied, H. Pritzkow, J.-L. Bantignies, P. Dieudonne and Jean-Louis Sauvajol, Angew. Chem. Int. Ed. 2004, 43, 203-206). Интересно, что хиральные силилированные дикарбамидциклогексильные производные приводят к образованию гибридных материалов со спиральной морфологией, имеющих противоположную хиральность по сравнению с конфигурацией органической субструктуры. Этот эффект описан в работе J.J.E. Moreau и др. (J.J.E. Moreau, L. Velluti, M. Wong Chi Man and С. Bied, J. Am. Chem. Soc., 2001,123, 1509-1510). Цель данного изобретения состоит в том, чтобы использовать способ ассоциации для построения структуры в ходе двойной функционализации неорганических структур. Также целью данного изобретения является разработка однореакторного способа распределения функциональных групп по поверхности носителя. Другая цель данного изобретения состоит в том, чтобы улучшить распределение функциональных-2 012016 групп по поверхности носителя. Еще одной целью данного изобретения является регулирование распределения функциональных групп по поверхности носителя. Таким образом, данное изобретение представляет способ пространственного разделения закрепленных функциональных органических цепей за счет их разбавления закрепленными нефункциональными органическими цепями в присутствии растворимых молекулярных производных, способных к самосборке и взаимодействию с функциональными органосиланами. Разделение осуществляют, занимая пространство сольватирующимся агентом, который выступает в роли заполнителя пространства. Нефункциональные группы предпочтительно имеют ту же природу, что и функциональные группы, чтобы эффективно предупреждать агрегацию, и занимают пространство между активными группами. Список чертежей На фиг. 1 представлены функционализованные гибридные материалы: а) упакованные функциональные группы X, полученные в результате недостаточного разбавления закрепленных функциональных цепей XL; b) распределенные функциональные цепи XL. На фиг. 2 представлено распределение закрепленных функциональных цепей XL, полученное в результате разбавления нефункциональными цепями L со вспомогательным агентом АА'В. На фиг. 3 представлено распределение р-аминофенилсилана, закрепленного на поверхности диоксида кремния с фенилсиланом, что показывает отсутствие взаимодействия с пиреном. На фиг. 4 представлено распределение р-аминофенилсилана, закрепленного на поверхности диоксида кремния с фенилсиланом без эффекта распределения, что показывает образование эксимера пирена. На фиг. 5 показаны энергетические уровни эксимера MM. На фиг. 6 представлена реакция закрепления пиренсульфонилхлорида на парааминофенилсилане. На фиг. 7 представлены спектры поглощения образцов S1-S4 и S6-S8 после закрепления пиренсульфонилхлорида. На фиг. 8 представлены ИК-спектры образца S1 до и после закрепления пиренсульфонилхлорида. На фиг. 9 представлены спектры флуоресценции образцов S1-S4 и S6-S8 после закрепления пиренсульфонилхлорида. В предпочтительном варианте реализации данного изобретения предлагают способ функционализации неорганического носителя, включающий стадии: а) предоставления неорганического носителя, изготовленного из пористого материала; б) прививки функциональных групп на поверхность носителя: 1) силана общей формулы RnR'3-n-Si-L-X, где R является алкильной группой с числом атомов углерода от 1 до 4, предпочтительно с числом атомов углерода 1 или 2, причем R одинаковы или различны,R' представляет собой галоген или алкоксигруппу с числом атомов углерода от 1 до 12, причем R' одинаковы или различны, n является целым числом от 0 до 2, L представляет собой жесткий или гибкий "линкер" или звено, а X является функциональной группой, обеспечивающей ковалентное связывание в реакциях присоединения или замещения; 2) вспомогательного агента, выбираемого для сильной сольватации функциональной группы прививаемой функциональной цепи, чтобы предотвратить агрегацию функциональных групп и занять пространство между функциональными группами X; в) отмывки привитого носителя после стадии б) полярным растворителем для удаления вспомогательного агента; г) возможного отверждения и пассивации привитого носителя. Вспомогательный агент обычно выбирают из производных мочевины, бис-мочевины, тиомочевины,триэтаноламина, 2,6-аминопиридина, амидов, аминоспиртов, аминокислот, циануровой кислоты, производных барбитуровой кислоты, моно-, ди- или триглицеридов или их комбинации. Предпочтительно его выбирают в зависимости от функциональной группы, как показано в табл. 1. Таблица 1-3 012016 Предпочтительно функциональная группа X представляет собой галоген, а вспомогательным агентом является диол или аминокислота, или X представляет собой амин, а вспомогательным агентом является производное мочевины, амид или карбамат. Наиболее предпочтительным сочетанием является амин в качестве функциональной группы X и производное мочевины в качестве вспомогательного агента. Вспомогательный агент, выступающий в качестве разделяющего агента, предпочтительно совместим с силаном по морфологии, и/или размеру, и/или природе, и/или возможности закрепления на носителе, но не имеет функциональной группы X. Количество разделяющего агента, используемого в данном изобретении, по меньшей мере, равно количеству привитых цепей. Верхний предел зависит от степени его растворимости. Отношение силана к разделяющему агенту предпочтительно составляет от 1:20 до 1:1, более предпочтительно от 1:10 до 1:8. Функционализованный материал можно отверждать и пассивировать. Способ по данному изобретению основан на образовании надмолекулярных сборок путем ассоциации функциональных фрагментов органического происхождения и самособирающихся вспомогательных молекул. Это предотвращает агрегацию функционального органического предшественника в ходе формирования границы раздела органического и неорганического веществ. Вспомогательные молекулы способны к самосборке и к специфическому взаимодействию с функциональными группами X, как показано на фиг. 2. Предпочтительно вспомогательные молекулы выбирают из производных мочевины, бисмочевины, тиомочевины, триэтаноламина, 2,6-амидопиридина, амидов, аминоспиртов, аминокислот,циануровой кислоты, производных барбитуровой кислоты, моно-, ди- или триглицеридов или их сочетаний. Наиболее предпочтительными вспомогательными агентами являются производные мочевины. Они обеспечивают дополнительное преимущество, поскольку их можно использовать повторно и удалять простой промывкой. Способ можно использовать для двойной функционализации либо с помощью однореакторного золь-гель синтеза, либо с помощью прививки на минеральную поверхность в одном реакторе. В более предпочтительном варианте реализации данного изобретения поверхность диоксида кремния функционализируют смесью, включающей аминоалкил- или аминоарилсилан, а также алкилсилан или фенилсилан, в соответствии с золь-гелевой поверхностной полимеризацией, описанной, например, Т. Martin и др. (Т. Martin, A. Galameau, D. Bruneli, V. Izard, V. Hulea, A.C. Blanc, S. Abramson, F. Di Renzo and F. Fajula,in Stud. Surf. Sci. Catal., 135 (2001) 29-O-02) или S. Abramson и др. (S. Abramson, M. Lasperas, A. Galameau,D. Desplantier-Giscard and D. Brunei in Chem. Comm. (2000), 1773-1774). Эту функционализацию осуществляют в присутствии производных мочевины в качестве вспомогательных молекул. Формирование двойной функциональности на неорганической поверхности с помощью функциональных соединений с одним активным центром выполняется за одну стадию. Вспомогательные молекулы мочевины впоследствии удаляют на стадии отмывки полярным растворителем, которую обычно выполняют после стадии прививки. Предпочтительно неорганический носитель изготавливают из пористых частиц неорганического оксида, которые обладают по меньшей мере одной из следующих характеристик: они имеют поры с диаметром в диапазоне от 3,5 до 30 нм; они имеют пористость в диапазоне от 0,4 до 4 см 3/г; они имеют удельную площадь поверхности в диапазоне от 100 до 1500 м 2/г и они имеют средний диаметр в диапазоне от 0,1 до 500 мкм. Носитель может быть разных видов. В зависимости от природы носителя, степени его гидратации или гидроксилирования, а также способности удерживать воду может потребоваться его дегидратация в более или менее высокой степени в зависимости от желаемого содержания радикалов -ОН на поверхности. Специалисты могут с помощью стандартных тестов определить обработку дегидратацией, а также возможно дегидроксилированием, которую следует применить к носителю в зависимости от желаемого содержания радикалов -ОН на поверхности. Более предпочтительно изготавливать исходный носитель из диоксида кремния. Обычно диоксид кремния можно нагревать до 100-1000 С и предпочтительно до 140-800 С в атмосфере инертного газа,например в азоте или аргоне, при атмосферном давлении или в вакууме около 1 Па (10-5 бар), в течение по меньшей мере 60 мин. Для такой тепловой обработки диоксид кремния можно смешивать, например,с NH4Cl для ускорения дегидратации. Для силана на стадии б) (1), если "линкер" L является гибким звеном, его можно выбрать из алкилов, имеющих от 1 до 12 атомов углерода, простых эфиров или тиоэфиров. Если "линкер" является жестким звеном, его можно выбирать из арила, моно- и бифенила, нафталина, простого полиарилового эфира или эфира дифенола. Предпочтительно, чтобы "линкер" являлся жестким звеном, и более предпочтительно, чтобы это была фенильная группа. Жесткий линкер будет удерживать активные центры в отдалении от поверхности носителя, ограничивая таким образом их нежелательные взаимодействия. Функциональная группа X делает возможным ковалентное связывание путем реакций присоединения или замещения. Ее можно выбирать из галогена, гидроксильной, карбоксильной, аминогруппы, изоцианата, тиола или глицидила. Предпочтительно, чтобы это был галоген или аминогруппа. Предпочтительно, чтобы разделяющий агент имел ту же реакционную группу, что и силан, по от-4 012016 ношению к Si в носителе. Разделяющий агент удерживает функциональные группы X в отдалении друг от друга, что позволяет создать одиночные центры, как показано на фиг. 3. Это можно сравнить с результатами, полученными при такой же функционализации без вспомогательных производных молекул, показанными на фиг. 4. Распределение аминогрупп, закрепленных на поверхности диоксида кремния, можно исследовать путем изучения флуоресценции молекул пирена, закрепленных ковалентными связями на аминных группах. Для определения эффективности распределения можно производить обнаружение эксимеров, поскольку спектр излучения мономера или эксимера позволяет определить, как расположены молекулярные образования - вблизи друг с другом или нет, эти молекулярные образования могут быть свободными или присоединенными к большим молекулам или твердому телу. Эксимер означает пару молекул, предпочтительно идентичных, образованных при диффузии в среде, в которой одна из молекул М находится в возбужденном состоянии, а другая, М - в основном состоянии. Взаимодействие, происходящее между М и М, поглощает часть энергии возбуждения М, оставшаяся энергия распределяется между парой ММ. Пара ММ существует в течение нескольких наносекунд, после чего испускает фотоны, возвращаясь в основное состояние отталкивания, как показано на фиг. 5, где приведены энергетические уровни пары ММ. Поскольку комплекс разрушен и конечное состояние является состоянием отталкивания, геометрия излучения не фиксирована. Таким образом, спектр излучения эксимера не структурирован и имеет смещение в красную сторону. Привитые функциональные группы реагируют с такими молекулами, как пирен, которые могут образовывать эксимеры, находясь достаточно близко друг от друга, что позволяет оценить распределение функциональных групп. Реакция прививки протекает при температуре от 60 до 120 С в инертной атмосфере. Стадию отмывки осуществляют при комнатной температуре полярным растворителем, который удаляет вспомогательный разделяющий агент. Полярный растворитель можно выбирать из спирта, воды или их смеси. Стадия отверждения, если ее проводят, протекает при температуре, выбираемой между 110 и 200 С,в зависимости от функциональных групп. Стадия пассивации, если ее выполняют, устраняет остаточный силанол. Ее осуществляют с силилирующим агентом, например хлортриметилсиланом, гексаметилдисилазаном, триметилсилилимидазолом, N,О-бис(триметилсилил)трифторацетамидом или другим пассивирующим агентом, который является инертным по отношению к функциональной группе X привитого силана. В данном изобретении также раскрывают привитые неорганические носители, в которых привитые функциональные группы эффективно распределены по поверхности носителя. Функционализованные носители по данному изобретению можно использовать для изготовления новых каталитических компонентов с одним активным центром за счет реакции металлизации. Эти каталитические компоненты на носителе при активации подходящим активирующим агентом можно использовать в качестве каталитических систем для олигомеризации и полимеризации. Примеры Исходным материалом для носителя является диоксид кремния, поставляемый компанией GraceDavisson под наименованием G5H. Он имеет удельную площадь поверхности 515 м 2/г, объем пор 1,85 см 3/г,диаметр пор 14,3 нм и индекс CBET (Брунауэр-Эммет-Теллер), равный 103. Общая методика прививки путем нанесения покрытия была адаптирована из предыдущей работыMartin и др. ("Towards total hydrophobisation of MCM-41 silica surface" ("К вопросу полной гидрофобизации поверхности диоксида кремния MCM-41") by Т. Martin, A. Galameau, D. Brunei, V. Izard, V. Hulea,А.С. Blanc, S. Abramson, F. Di Renzo and F. Fajula. in Stud. Surf. Sci. Catal., 2001, 135, 29-O-02). Были получены несколько образцов привитого диоксида кремния. Пример 1. Получение привитого носителя S1. Для S1 в качестве агента для прививки использовали парааминофенилтриметоксисилан (n-NH2-PhSi). 3 г носителя из диоксида кремния (3 г) предварительно активировали нагреванием до 180 С в вакууме (133 Па (1 торр в течение 18 ч. Затем его охлаждали до комнатной температуры в атмосфере аргона и добавляли 90 мл сухого толуола вместе с 2,66 г (12,48 ммоль) парааминофенилтриметоксисилана (nNH2-Ph-Si) в качестве агента для прививки (5 молекул на нм 2). Суспензию перемешивали в атмосфере аргона при комнатной температуре в течение 1 ч. Затем в реакционную смесь добавляли 224 мл воды (1,5 экв. на добавленный силан), 118 мг паратолуолсульфоновой кислоты (0,05 экв. на добавленный силан), 23 мг фторида аммония (0,05 экв. на добавленный силан) и перемешивали смесь в течение 1 ч при комнатной температуре, затем нагревали ее до 60 С в течение 6 ч, а затем до 120 С в течение 1 ч. В ходе последней стадии производили азеотропную перегонку при помощи аппарата Дина-Старка. Функционализованный диоксид кремния отделяли фильтрацией и последовательно промывали дважды 200 мл толуола, дважды 200 мл метанола, дважды 200 мл смеси метанола и воды с объемным отношением 1:1, 1 раз 200 мл метанола и дважды 200 мл диэтилового эфира. В конце выделенные образцы подвергали экстракции в аппарате Сокслета смесью дихлорметана и диэтилового эфира с объемным отношением 1:1.-5 012016 После прививки путем нанесения покрытия привитый носитель отверждали нагреванием в атмосфере влажного азота при температуре 130 С в течение ночи. Структура пор сохранялась. Пассивацию производили следующим образом. Материалы, содержащие закрепленные цепи с аминогруппами, откачивали при температуре 130 С в течение 8 ч, затем после охлаждения до комнатной температуры суспендировали в сухом толуоле. Добавляли 2,8 мл (14 ммоль/г) триметилсилилимидазола,после чего реакционную смесь перемешивали при температуре 60 С в течение ночи. Твердую фазу отделяли фильтрацией и последовательно промывали дважды 200 мл толуола, дважды 200 мл метанола, дважды 200 мл дихлорметана и дважды 200 мл диэтилового эфира. В конце выделенные образцы подвергали экстракции в аппарате Сокслета смесью дихлорметана и диэтилового эфира с объемным отношением 1:1. Пример 2. Получение привитого носителя S2. Для получения S2 использовали тот же агент для прививки n-NH2-Ph-Si, разбавляя его фенилтриметоксисиланом (n-Ph-Si) в отношении n-Ph-Si/n-NH2-Ph-Si, равном 2. Порядок действий был аналогичным примененному для получения привитого носителя S1, за исключением того, что использовали смесь 0,9 г (4,2 ммоль) n-NH2-Ph-Si и 1,68 мг (1,85 мл, 8,48 ммоль) nPh-Si. Пример 3. Получение привитого носителя S3. Для получения S3 использовали тот же агент для прививки n-NH2-Ph-Si, разбавляя его фенилтриметоксисиланом (n-Ph-Si) в отношении n-Ph-Si/n-NH2-Ph-Si, равном 4. Порядок действий был аналогичным примененному для получения привитого носителя S1, за исключением того, что использовали смесь 0,53 г (2,5 ммоль) n-NH2-Ph-Si и 1,97 мг (1,86 мл, 9,96 ммоль) nPh-Si. Пример 4. Получение привитого носителя S4. Для получения S4 использовали тот же агент для прививки n-NH2-Ph-Si, разбавляя его фенилтриметоксисиланом (n-Ph-Si) в отношении n-Ph-Si/n-NH2-Ph-Si, равном 9. Порядок действий был аналогичным примененному для получения привитого носителя S1, за исключением того, что использовали смесь 0,266 г (1,25 ммоль) n-NH2-Ph-Si и 2,23 мг (2,1 мл, 11,25 ммоль) nPh-Si. Пример 5. Получение привитого носителя S5. Для получения S5 использовали тот же агент для прививки n-NH2-Ph-Si, разбавляя его фенилтриметоксисиланом (n-Ph-Si) в отношении n-Ph-Si/n-NH2-Ph-Si, равном 19. Порядок действий был аналогичным примененному для получения привитого носителя S1, за исключением того, что использовали смесь 0,13 г (0,6 ммоль) n-NH2-Ph-Si и 2,34 г (2,21 мл, 11,83 ммоль) nPh-Si. Примеры 6-8. Получение привитого носителя S6-S8 в соответствии с данным изобретением. Методика, использованная для приготовления образцов S6, S7 и S8, была аналогична методике приготовления, соответственно, образцов S2, S3 и S4, за исключением того, что в реакционную силановую смесь в растворе 60 мл сухого толуола добавляли раствор 0,9 г метилмочевины в 6 мл метанола. 0,9 г (12,2 ммоль) метилмочевины (5 молекул на нм 2) в качестве вспомогательного агента растворяли в 6 мл сухого метанола, после чего добавляли в раствор в 60 мл сухого толуола смеси соответствующих образцам S2, S3 и S4 количеств парааминофенилтриметоксисилана и фенилтриметоксисилана для приготовления образцов S6, S7 и S8 соответственно. После гомогенизации каждый из трех растворов добавляли к отдельному образцу носителя из диоксида кремния (3g), прошедшему активацию путем нагревания до 180 С в вакууме (133 Па (1 торр в течение 18 ч, и затем охлажденному до комнатной температуры в атмосфере аргона. После контакта в течение 1 ч в реакционную смесь добавляли 224 мл (1,5 экв. на добавленный силан) воды, 118 мг (0,05 экв. на добавленный силан) паратолуолсульфоновой кислоты и 23 мг (0,05 экв. на добавленный силан) фторида аммония, реакционную смесь перемешивали в течение 1 ч при комнатной температуре, затем в течение 6 ч при 60 С, а затем в течение 1 ч при 120 С. В ходе последней стадии производили азеотропную перегонку при помощи аппарата Дина-Старка. Функционализованный диоксид кремния отделяли фильтрацией и последовательно промывали дважды 200 мл толуола, дважды 200 мл метанола, дважды 200 мл смеси метанола и воды с объемным отношением 1:1, 1 раз 200 мл метанола и дважды 200 мл диэтилового эфира. В конце выделенные образцы подвергали экстракции в аппарате Сокслета смесью дихлорметана и диэтилового эфира с объемным отношением 1:1. После прививки нанесением покрытия привитый носитель отверждали нагреванием в атмосфере влажного азота при температуре 130 С в течение ночи. Структура пор сохранялась. Стадию пассивации проводили аналогично способу, использованному для получения образцов S1S5. Характеристики привитых носителей приведены в табл. 2. Затем определяли распределение функциональных групп по поверхности носителя путем взаимодействия этих функциональных групп с пиреном. Сначала синтезировали пиренсульфонилхлорид (PSC). Раствор 0,41 г (1,45 ммоль) пиренсульфокислоты в 16 мл тионилхлорида нагревали при температуре 80 С до окончания выделения SO2 и HCl. Затем избыток тионилхлорида перегоняли при пониженном давлении и остаток растворяли в 20 мл диметилформамида. Затем пиренсульфонилхлорид прикрепляли к диоксиду кремния, привитому аминогидрокарбилсиланом, как показано на фиг. 6. Вещество, содержащее закрепленные цепи с аминогруппами, откачивали при 130 С в течение 18 ч, затем после охлаждения до комнатной температуры из него готовили суспензию в диметилформамиде. Таким образом получали раствор пиренсульфонилхлорида в диметилформамиде с концентрацией 0,72 моль/л и триэтиламина в соотношении 2 экв. пиренсульфонилхлорида на 1 экв. привитого аминосилана и 2 экв. основания на 1 экв. привитого аминосилана. Реакционную смесь перемешивали при температуре окружающей среды в течение 18 ч. Твердую фазу отделяли фильтрацией и последовательно промывали дважды 200 мл диметилформамида, дважды 200 мл метанола, дважды 200 мл дихлорметана и дважды 200 мл диэтилового эфира. Характеристики образцов после реакции с пиренсульфонилхлоридом приведены в табл. 3. Таблица 3 Спектры поглощения гибридного материала в диапазоне УФ-видимый свет измеряли прибором, основанным на диффузном отражении, Perkin-Elmer Lambda 14, оборудованным интегрирующей сферойLabsphere, North Sutton, USA. Диоксид кремния помещали в выемку глубиной 0,05 мм, сделанную в кварцевой пластинке, которую затем накрывали стандартной кварцевой пластиной (ячейка QS-100,Hellma). Контрольная ячейка была заполнена BaSO4. Спектры получали с помощью преобразования Кубелки-Мунка (KM).KM=(1-отражающая способность)2/2 отражающая способность После прикрепления пирена возникающую новую зону поглощения от 320 до 420 нм и более связывали с присутствием пирена, как показано на фиг. 7. Такое дополнительное поглощение соответствует поглощению агрегатов пирена. Абсорбция возрастала с повышением содержания привитых функциональных групп, тем самым показывая, что количество закрепленного пирена пропорционально плотности привитых функциональных групп. Кроме того, все ИК-спектры после прикрепления пирена показали, что полосы v(N-H) при 3480-3390 см-1 и o(N-H) при 1625 см-1 были менее интенсивными, чем аналогичные полосы исходного материала, тем самым, показывая, что аминные группы прореагировали, и,значит, реакция прикрепления прошла успешно. Это видно из фиг. 8. Это наблюдение было подтверждено элементным и термогравиметрическим анализом материала перед и после прививки. Изотермы адсорбции и десорбции азота при 77 K перед и после прививки были аналогичны, что указывает на сохранение пористой структуры материала. Химические реакции не повлияли на структуру материала. Были также получены спектры флуоресценции. Их получали на спектрофлуориметре, построенном на основе двух монохроматоров Jobin Yvon М 25, каждый из которых имел решетку с 1200 линий/мм (поворотное устройство Черни, 1/4 м). Каждый монохроматор имел плавно настраиваемые щели. Регистрацию производили с помощью фотоумножителя R928 (Hamatsu). Для записи спектров полоса пропускания была зафиксирована на 8 нм. Измерения производили под прямым углом или фронтально, с ячейкой, расположенной под углом 60 к падающему лучу. Образцы помещали между двумя кварцевыми пластинами, как описано для метода диффузного отражения;-7 012016 или в виде тонких пленок, полученных путем орошения секции прозрачной для флуоресценции пленки (Scoth 3M), растянутой на жесткой рамке. Эти спектры для всех 7 образцов приведены на фиг. 9. Кроме полос флуоресценции мономера при 376 и 390 нм, для образцов с S1 по S3 и с S6 по S7, полученных без метилмочевины и с ней, был обнаружен широкий пик с центром около 460 нм. Этот пик соответствует флуоресценции эксимера. Это предполагает, что смешивание двух органосиланов может значительно разбавить парааминофенилсилан, сохраняя число привитых групп постоянным, а также, что доля привитых функциональных групп не была распределена, о чем свидетельствует присутствие эксимера. Такое отсутствие распределения можно приписать взаимодействию между аминными группами части парааминофенилсилана, которое способствует их упаковке. Соотношение мономер (M)/эксимер (E) в зависимости от разбавления показано в табл. 4. Таблица 4 Развертка спектральной области является приближенной из-за того, что не была сделана поправка на зависимость чувствительности детектора от длины волны. Добавление метилмочевины в качестве вспомогательного агента в соответствии с данным изобретением приводит к увеличению соотношения мономер/эксимер по сравнению с образцами без добавления метилмочевины. Это видно из спектров флуоресценции всех образцов. С другой стороны, образец S5, соответствующий очень высокому разбавлению, не давал эксимерного излучения, а излучение мономера присутствовало только при 376 и 390 нм. Следует отметить, что этот очень сильно разбавленный и распределенный закрепленный пирен давал полосу при 376 нм со значительно более высокой интенсивностью, чем при 390 нм. Действительно, флуоресценция мономера имела тонкую структуру в виде набора тонких полос, ассоциируемых с колебательными модами молекулы. Колебательная полоса III, находящаяся в диапазоне 390-400 нм, известна тем, что она имеет постоянную интенсивность, тогда как полоса I, расположенная в диапазоне 372-384 нм, значительно изменяет интенсивность в зависимости от полярности среды, в которой находится пирен (например, 0,48 в ацетонитриле, 0,88 в бензоле и 1,65 в гексане - K. Kalyanasundaram and J.K. Thomas, J. Am. Chem. Soc., 99(1977) 2039-2044). При увеличении разбавления в присутствии или в отсутствие метилмочевины в качестве распределяющего агента флуоресценция мономера при 372-384 нм возрастает по сравнению с флуоресценцией при 390-400 нм. Таким образом, спектральный анализ показывает, что использование мочевины улучшает размещение прививаемых функциональных групп в среде, которая немного менее полярна, при содержании функциональных групп в среде менее чем 33%. Поэтому результаты флуоресцентного анализа подтверждают улучшенное разделение при разбавлении в присутствии метилмочевины. Таким образом, добавление метилмочевины очень эффективно для разделения прививаемых функциональных групп на поверхности носителя. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ распределения закрепленных функциональных органических цепей, в котором прививают на поверхность носителя, изготовленного из неорганического пористого материала,1) силан общей формулы RnR'3-n-Si-L-X, где R является алкильной группой с числом атомов углерода от 1 до 2, причем R одинаковы или различны, a R' представляет собой галоген или алкоксигруппу с числом атомов углерода от 1 до 12, причем R' одинаковы или различны, n является целым числом от 0 до 2, L представляет собой жесткий или гибкий "линкер", а X является функциональной группой, обеспечивающей ковалентное связывание при реакциях присоединения или замещения; 2) вспомогательный агент, выбираемый для сильной сольватации функциональной группы прививаемой функциональной цепи, чтобы предотвратить агрегацию функциональных групп и занять пространство между функциональными группами X; а затем отмывают привитый носитель полярным растворителем для удаления вспомогательного агента;-8 012016 возможно, отверждают и пассивируют привитый носитель. 2. Способ по п.1, в котором L представляет собой жесткий "линкер", выбираемый из арила, моно- и бифенила, нафталина, простого полиарилового эфира или эфира дифенола. 3. Способ по п.2, в котором в качестве жесткого "линкера" используется фенильная группа. 4. Способ по п.1, в котором L представляет собой гибкий "линкер", выбираемый из алкилов, имеющих от 1 до 12 атомов углерода. 5. Способ по пп.1-4, в котором функциональную группу X выбирают из галогена, гидроксильной,карбоксильной, аминогруппы, изоцианата, тиола или глицидила. 6. Способ по п.5, в котором вспомогательный агент выбирают в зависимости от функциональной группы X следующим образом: производное мочевины, амид или карбамат, если X - амин; диол или аминокислота, если X - галоген; производное мочевины, амид или ксантат, если X - тиол; производное мочевины, амид или аминокислота, если X - нитрил; производное мочевины или амид, если X - изоцианат. 7. Способ по п.6, в котором функциональная группа X - галоген, а вспомогательный агент - диол или аминокислота, или X - амин, а вспомогательный агент - производное мочевины, амид или карбамат. 8. Способ по п.7, в котором вспомогательный агент - производное мочевины, а функциональная группа - амин. 9. Способ по любому из предшествующих пунктов, в котором соотношение силана и вспомогательного агента составляет от 1:20 до 1:1. 10. Носитель из неорганического пористого материала, привитый закрепленными функциональными органическими цепями, распределенными по его поверхности, получаемый способом по любому из пп.1-9.
МПК / Метки
МПК: B05D 1/18
Метки: носителя, этого, распределения, результате, способ, функциональных, носитель, молекул, получаемый, способа, поверхности
Код ссылки
<a href="https://eas.patents.su/12-12016-sposob-raspredeleniya-funkcionalnyh-molekul-po-poverhnosti-nositelya-i-nositel-poluchaemyjj-v-rezultate-etogo-sposoba.html" rel="bookmark" title="База патентов Евразийского Союза">Способ распределения функциональных молекул по поверхности носителя и носитель, получаемый в результате этого способа</a>
Предыдущий патент: Способ каталитического дегидрирования легких алканов
Следующий патент: Способ полимеризации олефинов в присутствии катализатора полимеризации олефинов
Случайный патент: Фунгицидные композиции