Способ определения функционального состояния печени живого организма путем количественного измерения метаболизации субстратов
Формула / Реферат
1. Способ определения функционального состояния печени живого организма, включая человека, включающий следующие этапы: внутривенное введение по меньшей мере одного меченого 13С субстрата в концентрации от 0,1 до 10 мг/кг веса тела, причем концентрация субстрата выбирается таким образом, чтобы динамика метаболизации в линейной области была далека от насыщения, непрерывное определение содержания минимум одного меченого 13С продукта метаболизации в выдыхаемом воздухе в определенный интервал времени в течение 25 мин, начиная с внутривенного введения.
2. Способ по п.1, отличающийся тем, что минимум одним меченым 13С продуктом метаболизации в выдыхаемом воздухе является 13CO2.
3. Способ по одному из предыдущих пунктов, отличающийся тем, что в качестве меченого 13С субстрата применяется субстрат, из которого путем реакции дезалкилирования алкоксильной группы, в частности метоксильной группы, высвобождается 13CO2.
4. Способ по одному из предыдущих пунктов, отличающийся тем, что в качестве субстрата применяется меченый 13С метацетин, фенацетин, аминопирин, кофеин, эритромицин и/или этоксикумарин.
5. Способ по одному из предыдущих пунктов, отличающийся тем, что определяется абсолютное содержание меченого 13С продукта метаболизации, в частности абсолютное содержание 13CO2, в выдыхаемом воздухе.
6. Способ по одному из предыдущих пунктов, отличающийся тем, что выдыхаемый воздух полностью или частично через дыхательную маску и соединительную трубку непрерывно подается в измерительный прибор.
7. Способ по одному из предыдущих пунктов, отличающийся тем, что он комбинируется с другими аналитическими методами, в частности с компьютерно-томографической волюметрией или магнитно-резонансной томографией.
Текст
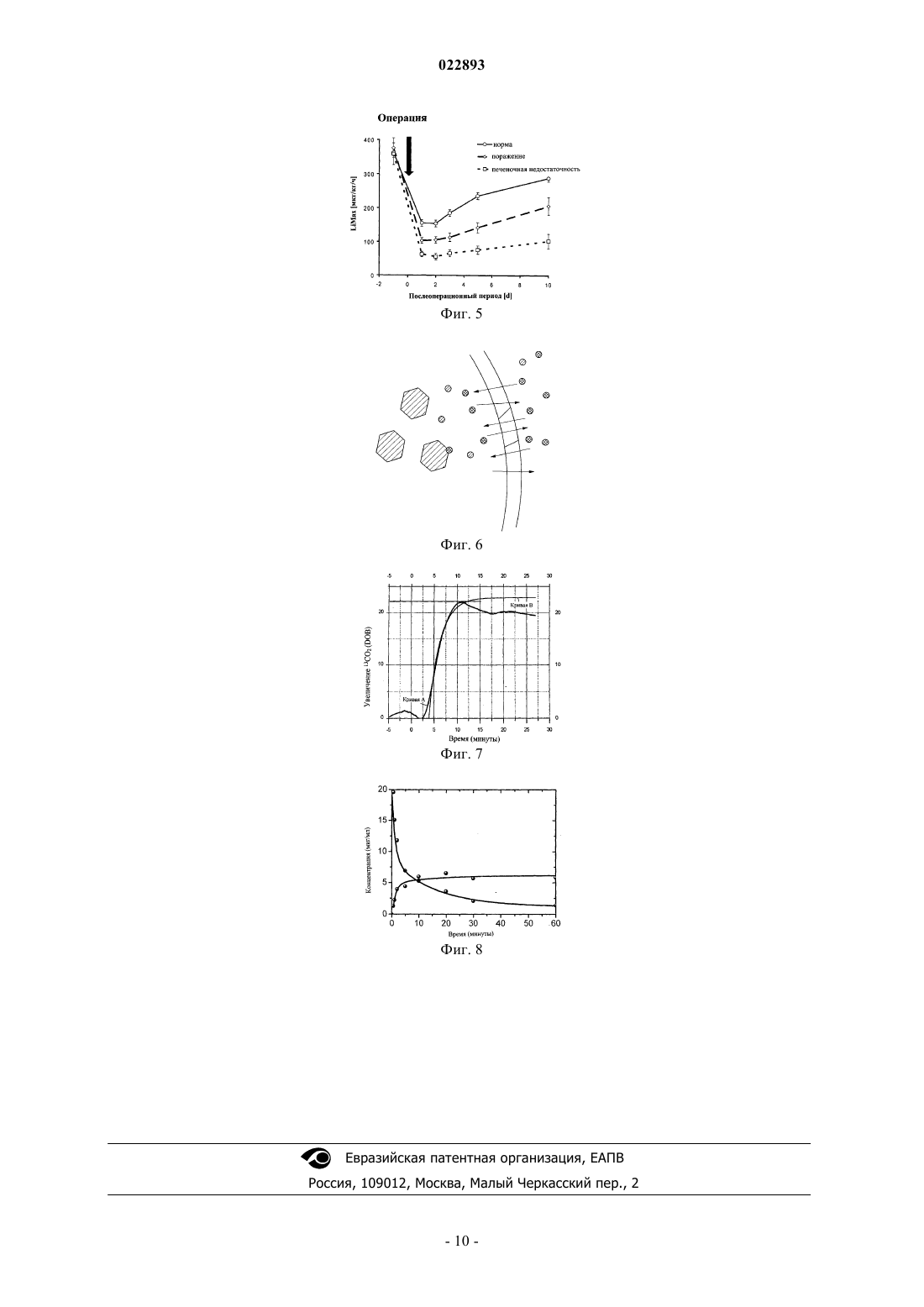
СПОСОБ ОПРЕДЕЛЕНИЯ ФУНКЦИОНАЛЬНОГО СОСТОЯНИЯ ПЕЧЕНИ ЖИВОГО ОРГАНИЗМА ПУТМ КОЛИЧЕСТВЕННОГО ИЗМЕРЕНИЯ МЕТАБОЛИЗАЦИИ СУБСТРАТОВRU-C1-2240789 М.-X. КУПАЛЬ,13 С-метацетиновый дыхательный тест в оценке функции печени при хронических вирусных гепатитах, Здоровье Украины, 2006, ноябрь,22 [найдено 15.01.2012] Найдено из Интернет URL: http://health-ua.com/ Представленное изобретение относится к способу определения функционального состояния печени живого организма, в частности человека, включающему в себя введение минимум одного меченого 13 С субстрата, который преобразуется печенью с высвобождением минимум одного меченого 13 С продукта метаболизации, и определение содержания минимум одного меченого 13 С продукта метаболизации в выдыхаемом воздухе за определенный интервал времени при помощи минимум одного измерительного прибора с минимум одним блоком обработки результатов. Данный метод позволяет описать измеренное первоначальное увеличение содержания минимум одного меченого 13 С продукта метаболизации в выдыхаемом воздухе посредством дифференциального уравнения первого порядка, и из решения дифференциального уравнения первого порядка определить значение Amax(DOBmax) и постоянную времени tau увеличения содержания меченого 13 С продукта метаболизации. Изобретение относится к способу определения функционального состояния печени живого существа в соответствии с ограничительной частью п.1 формулы изобретения. Печень является жизненно-важным органом для функциональной способности живого существа, в частности человека, поскольку в печени происходит ферментативное расщепление многих субстанций,например медикаментов. При этом расщепление субстанций катализируется преимущественно семейством цитохромов, в частности, в форме оксигеназ Р 450. К тому же с давних пор известно, что различные цитохромы метаболизируют различные субстанции. Известно также, что путем измерения концентрации метаболизированных субстанций может быть определено функциональное состояние печени. Так, в статье Мацумото и др. (Digestive Diseases Science, 1987, т. 32, c. 344-348) описывается пероральное введение 13 С-метацетина здоровым и имеющим поражения печени пациентам, причем 13 Сметацетин преобразуется в печени с высвобождением 13 СО 2. Определение содержания 13 СО 2 в выдыхаемом воздухе позволяет сделать вывод о степени поражения печени. Браден и др. (Aliment Pharmacol. Thier., 2005, т. 21, с. 179-185) описывает измерение соотношения 13 СО 2/12 СО 2 в выдыхаемом воздухе индивидов, которым предварительно также был перорально введен 13 С-метацетин. При этом преимущественно производятся непрерывные замеры в течение 60 мин для определения максимальной активности ферментов. Однако такого подхода недостаточно для применения в клинической практике, поскольку, в частности, на основе перорального введения 13 С-метацетина, можно сделать вывод лишь о том, функционирует ли печень вообще или, возможно, функционирует еще более или менее хорошо. Однако из этого врач не может сделать вывод о непосредственной стратегии лечения. Кроме того, применяемые до настоящего времени способы диагностики печени не являются индивидуально-специфическими, а позволяют лишь получить статистические данные о пациентах в целом. Это означает, что при помощи упомянутых измерений могут быть сделаны выводы о том, повышена ли вероятность негативного заключения при определенном результате измерения или нет. Также из индивидуального измерения невозможно сделать непосредственное заключение о функциональном состоянии печени. Поэтому желательно разрабатывать простые тесты, которые позволяют делать прогностические выводы относительно функциональных резервов ткани клеток печени. Обычные лабораторные данные не являются достаточно точными для надежной оценки комплексных биологических процессов в печени, а также ее изменений при заболевании. Способ анализа, дающий возможность количественного определения функционального состояния печени, описан в патенте WO 2007/000145 А 2. Способ базируется на введении метаболизирующегося в печени субстрата и определении максимальной скорости превращения субстрата, что позволяет сделать вывод о функциональной способности печени пациента. Способ, который позволяет сделать индивидуальное заключение о количественных показателях метаболизации отдельного органа, в частности печени, может в различных вариантах исполнения иметь следующие свойства: 1. Динамика метаболизации субстрата в печени пациента исследуется в режиме реального времени и с высоким разрешением. При этом может быть предусмотрено, чтобы инициирование метаболизации по сравнению с нарастанием метаболизации происходило быстро, то есть желательно, чтобы 70% инициации метаболизации происходило минимум в 2 раза быстрее. 2. Метаболизация измеряется непосредственно, то есть либо продукт метаболизации непосредственно доступен для измерения или же может быть измерена другая величина, находящаяся в жесткой пропорциональной зависимости от продукта метаболизации. Это означает, например, при исследовании газовой дыхательной смеси, что предпочтительно измеряется каждое дыхание, но по крайней мере два дыхания в минуту. Таким образом, не прибегают к временному хранению пробы газовой дыхательной смеси и частичному отбору пробы из газовой дыхательной смеси, учитывая возможность возникновения погрешностей способа. 3. Под влиянием физиологических факторов измеренная величина меняется не более чем на 20%, то есть чем меньше влияние физиологических факторов, как, например, распределения субстрата по телу током крови, тем точнее количественное определение продукта метаболизации. 4. Процесс метаболизации введенного субстрата однозначен и происходит исключительно или более чем на 90% в клетках печени и больше нигде в теле. 5. Эффективность реакции в процессе метаболизации не варьируется от человека к человеку, потому что это шло бы вразрез с индивидуальным количественным определением. Таким образом, процессы метаболизации, имеющие сильные генетические вариации, исключены. Если генетическая вариация процесса метаболизации вообще имеет место, то, по крайней мере, должна быть известна сила вариации генетически неизмененного процесса метаболизации. 6. Благоприятнее всего, если процесс метаболизации происходит посредством энзимов печени либо коэнзимов печени, которые равномерно проявляются во всех клетках печени. Если в особых отделах печени происходит скопление энзимов или коэнзимов печени, то может быть сделано максимум одно взвешенное для этих отделов заключение о функциональном состоянии печени. Другие реакции метабо-1 022893 лизации также не могут настолько сильно угнетать энзимы или коэнзимы печени, чтобы это приводило к изменению процесса метаболизации более чем на 30%, а тем самым и к более чем 30% изменению динамики метаболизации. Известные до сего времени способы не позволяют выполнить перечисленные пункты. Поэтому в основе представленного изобретения лежит задача представить способ, позволяющий давать индивидуальное заключение о количественных показателях метаболизаци печени. Эта задача решается представленным способом определения функционального состояния печени живого существа, в частности функционального состояния печени человека, в соответствии с п.1 формулы изобретения. При этом соответствующий изобретению способ включает в себя этапы введения минимум одного меченого 13 С субстрата, преобразуется печенью с высвобождением минимум одного меченого 13 С продукта метаболизации, в частности 13CO2, и этап определения содержания минимум одного образованного меченого 13 С продукта метаболизации, в частности 13 СО 2, в выдыхаемом воздухе через определенный интервал времени при помощи измерительного прибора с минимум одним блоком обработки результатов. При этом количество образованного меченого 13 С продукта метаболизации, в частности 13 СО 2, в выдыхаемом воздухе, предпочтительно пропорционально количеству минимум одного введенного субстрата. Соответствующий изобретению метод характеризуется тем, что, основываясь на полученных данных,становится возможным описать измеренное начальное увеличение содержания минимум одного меченого 13 С продукта метаболизации, в частности содержания 13 СО 2, в выдыхаемом воздухе при помощи дифференциального уравнения первого порядка. Из решения этого дифференциального уравнения первого порядка определяются далее максимальное значение Amax (называемое также DOBmax, причем DOB означает "delta over baseline"), а также постоянная времени tau увеличения содержания меченого 13 С продукта метаболизации, в частности содержания 13 СО 2. При этом максимальное значение Amax или DOBmax соответствует максимуму динамики метаболизации, а постоянная времени tau соответствует постоянной времени роста динамики метаболизации. Изобретение позволяет приспособить ("подогнать") кривую к фактически измеренным значениям изменения во времени содержания 13 С, причем кривая представляет собой решение дифференциального уравнения первого порядка и показывает минимум два значения, а именно максимальное значение Amax и постоянную времени т (tau). При решении дифференциального уравнения идет речь, в частности, об экспоненциальной функции, которая приблизительно описывает первоначальное увеличение содержания меченого 13 С продукта метаболизации в выдыхаемом воздухе. Ее значения Amax und tau представляют собой характерные величины, характеризующие первоначальные параметры увеличения. Таким образом,представленное изобретение позволяет путем определения двух параметров измеренного первоначального увеличения провести анализ картин заболевания печени с особо четким разделением и высоким разрешением. В частности, анализ также и параметра tau наряду с максимальным значение Amax позволяет провести анализ с таким четким разделением. Тем самым, данное изобретение предоставляет врачу более совершенные исходные данные для постановки диагноза. Метаболизируемый субстрат транспортируется в клетки печени. Дифференциальное уравнение, посредством которого происходит транспортировка субстанции в клетки печени, может быть описано следующим уравнением причем X обозначает концентрацию метаболизируемого субстрата, а С - коэффициент диффузии. Предполагается, что коэффициент диффузии С в первом приближении является пространственнонезависимым. Поскольку при анализе динамики метаболизации не может быть произведено разрешение с пространственной привязкой или происходит усреднение по всем местам, пространственная зависимость уменьшается до видимого коэффициента диффузии Cave и получается следующее уравнение Существенно, что этап метаболизации на энзиме происходит быстрее диффузионной динамики, то есть, по крайней мере, в два раза быстрее. Так, метаболизация, например, посредством цитохрома CYPP450 1 А 2, происходит в среднем за субмиллисекунды. Ввиду метаболизации субстрата субстрат воспринимается печенью, в результате чего снижается концентрация субстрата X, и до полного расщепления субстанции сохраняется градиент концентрации между содержимым клетки и наружной стороной клетки. Факторы на более длинной шкале времени заданы функцией f(X,Y,Z,). Эти факторы влияния должны в начале динамики метаболизации составлять менее 20% от динамики метаболизации, с тем что-2 022893 бы дифференциальное уравнение (ДУ) могло быть описано ДУ первого порядка согласно следующему уравнению Решение этого ДУ соответствует уравнению причем Cave представляет постоянную времени tau превращения, а X - концентрацию введенного субстрата. Момент t=0 получается из приспособления динамики или инициирования метаболизации. Если обнаруживается меченый 13 С продукт метаболизации, например 13CO2, то увеличение концентрации продукта метаболизации А пропорционально уменьшению введенного субстрата X. В результате этого из экспоненциально нисходящего движения субстрата получается экспоненциально восходящее движение продукта метаболизации согласно причем Amax является максимальной амплитудой настроенной функции, а тем самым и соответствует максимальной концентрации или количеству продукта метаболизации, a tau является постоянной времени превращения. Итак, имеется экспоненциальная кривая, описывающая увеличение. Таким образом, в предпочтительном варианте осуществления изобретения решение дифференциального уравнения первого порядка соответствует уравнению причем y(t) соответствует динамике метаболизации минимум одного субстрата, t - времени измерения, t0- началу метаболизации, tau - постоянной времени превращения и Amax - максимальной амплитуде настроенной функции либо максимальной концентрации продукта метаболизации, и А 0 - начальной концентрации продукта метаболизации. Соответственно, из приведенного выше уравнения можно определить Amax и постоянную времени tau. Вышеназванная экспоненциальная функция предпочтительно настраивается на замеры первоначального увеличения содержания минимум одного меченого 13 С продукта метаболизации в выдыхаемом воздухе. Затем из настройки выводятся максимальное значение Amax и постоянная времени tau. При этом для определения количественных показателей функционального состояния печени живого существа важно, что значение Amax пропорционально числу участвующих в метаболизации клеток печени и что постоянная времени tau дает информацию о доступности метаболизируемого вещества для энизмов или коэнзимов печени. В одном из вариантов осуществления представленного изобретения увеличение меченого 13 С продукта метаболизации, в частности увеличение СО 2, в выдыхаемом воздухе до уровня 70% от максимального значения меченого 13 С продукта метаболизации, в частности увеличения 13CO2, предпочтительно до максимального значения меченого 13 С продукта метаболизации, в частности увеличения 13CO2, описывается дифференциальным уравнение первого порядка. В особенно предпочтительном варианте осуществления изобретения теперь можно исходя из значения Amax или DOBmax при помощи следующего уравнения определить максимальную степень превращения минимум одного субстрата в печени причем RPDB соответствует значению 0,011237 (стандарт Pee Dee Belemnite соотношения 13CO2/12CO2), P норме выработки CO2, M - молярной массе введенной субстанции и BW - массе тела индивида. При применении соответствующего изобретению способа определения функционального состояния печени следует учитывать, что при большой постоянной времени tau непосредственно считываемый максимум процесса метаболизации или динамики метаболизации может отличаться от определяемого из дифференциального уравнения первого порядка максимума Amax либо DOBmax. Это обусловлено тем, что при медленном повышении скорости метаболизации усиливается влияние других факторов, как, например, распределения субстрата по телу. По этой причине желательно быстро вызвать инициирование метаболизации, как это, например, может происходить путем внутривенного введения метаболизируемого субстрата. Внутривенное введение субстрата гарантирует быструю доставку субстрата в печень и связанное с этим быстрое инициирование метаболизации субстрата. Внутривенное введение также позволяет обеспечить достаточно высокий градиент субстрата между клетками печени и кровью, что дает возможность наладить динамику метаболизациии и достичь максимальной скорости превращения субстрата. Кроме того, предпочтительно, чтобы метаболизируемый субстрат имел структурные элементы, соответствующие показанным на фиг. 1 структурам. В частности, в качестве меченого 13 С субстрата следует применять соединение, которое позволяет высвобождать 13CO2 путем реакции дезалкилирования ал-3 022893 коксильной группы R1, в частности метоксильной группы. В общем и целом применяемые субстраты могут быть большими или малыми молекулами, которые имеют шестичленное кольцо либо из атомов углерода, либо из изотопов углерода, а также алкоксильную группу, причем алкоксильная группа сначала гидроксилируется посредством имеющихся в печени цитохромов Р 450, причем затем отщепляется 13CO2. Примерами подходящих субстратов являются, в частности, 13 С-метацетин, фенанцетин, этоксикумарин, кофеин, эритромицин и/или аминопирин. При этом возможно также, чтобы атом углерода замещался другим атомом, например азотом или серой. Возможно также, чтобы применяемые субстраты базировались на соединениях с пятичленным кольцом, которые замещены по крайней мере одной алкоксильной группой R1. Разумеется, здесь также один или два атома углерода пятичленного кольца могут замещаться другими атомами, например азотом или серой. Разумеется, возможно также, чтобы применяемые субстраты имели различные заместители. Так, показанные на фиг. 1 остатки R2, R3, R4, R5 и R6 могут быть выбраны из группы, содержащей галогены, алкильные группы, карбоксильные группы,эфирные группы или силановые группы. Разумеется, этот перечень возможных заместителей не исчерпывающий и может расширяться, включая привычные для специалиста заместители. Меченый 13 С субстрат предпочтительным образом вводится в концентрации от 0,1 до 1 0 мг на кг массы тела. При этом концентрация метаболизируемого субстрата должна быть подобрана таким образом, чтобы динамика метаболизации в линейной области была далека от насыщения. При превышении концентрацией субстрата определенного значения становится невозможным описать при помощи дифференциального уравнения первого порядка увеличение содержания меченого 13 С продукта метаболизации, в частности увеличение 13 СО 2 в выдыхаемом воздухе. Так, в случае применения 13 С-метацетина в качестве метаболизируемого субстрата вводимое количество не должно превышать 10 мг на кг массы тела. В рамках представленного способа определяется предпочтительно абсолютное содержание меченого 13 С продукта метаболизации, в частности содержание 13 СО 2 в выдыхаемом воздухе. При этом измерение содержания меченого 13 С продукта метаболизации, в частности содержание 13 СО 2 в выдыхаемом воздухе, должно происходить как в режиме реального времени, так и непрерывно. Непрерывное определение концентрации меченого 13 С продукта метаболизации, в частности концентрации 13 СО 2 в выдыхаемом воздухе, в измерительном приборе приводит к определению большего числа точек ввода данных,следствием чего является более высокое разрешение и степень точности образованного полученными точками ввода данных графика измерений. Надежное определение максимального значения Amax илиDOBmax и постоянной времени tau должно базироваться минимум на пяти точках замера, предпочтительно минимум на семи точках замера. В особенно предпочтительном варианте осуществления изобретения представленный способ комбинируется с другими аналитическими методами, в частности с компьютерно-томографической (КТ) волюметрией. Это позволяет составить обширное заключение о состоянии здоровья пациента и целенаправленном планировании операции, например в случае появления новообразований. В другом варианте осуществления изобретения представленный способ комбинируется с другими аналитическими методами, в частности с магнитно-резонансной томографией (МРТ). При этом метаболизируемый меченый 13 С субстрат локализуется в печени при помощи снимков МРТ. Динамика метаболизации определяется при помощи представленного метода и может быть сопоставлена с разрешенной по времени МРТ. Комбинация этих двух методов позволяет исследовать отдельные энзимы в особенности в печени с разрешением в пространстве и по времени. В общем и целом разрешение по времени МРТ слишком медленное для отслеживания динамики метаболизации. Если же синхронизировать данные полученных снимков с динамикой метаболизации представленного способа, то можно получить лучшее отображение метаболизации, например, путем оценки данных МРТ в различные моменты времени. Дополнительно в одном из вариантов метаболизируемые меченые 13 С субстраты могут быть подобраны так, чтобы они метаболизировались энзимами или коэнзимами, которые распределены в печени неоднородно, а сконцентрированы в определенных участках. Таким образом могут быть определены показатели метаболизации отдельных участков печени. Для определения динамики метаболизации и пространственного отражения этого процесса для однородно распределенного в печени энзима или коэнзима необходимо обеспечить, чтобы субстрат очень быстро и эффективно попадал в клетки печени и там без помех определялся посредством МРТ, в то время как при помощи представленного метода одновременно измеряется динамика метаболизации. Примером выполнения этого является меченый 13 С метацетин, который посредством агента растворения пропиленгликоля в водном растворе может быть растворен в достаточно высокой концентрации. Концентрация пропиленгликоля составляет от 10 до 100 мг/мл, благодаря чему может быть получен раствор метацетина концентрацией от 0,2 до 0,6%. Такая особая комбинация меченого 13 С субстрата (метацетина) и агента растворения пропиленгликоля в водном растворе позволяет почти без фона произвести измерение МРТ меченого 13 С метацетина. Естественное соотношение изотопов 13 С может оказать сильное негативное воздействие на измерения МРТ. Создающему сильные помехи фоновому сигналу могут способствовать все атомы углеводорода метацетина, агента растворения и остальных органических субстанций в клетках печени. Благодаря специ-4 022893 альному подбору маркировки 13 С на связанной через эфирную группу метильной группе в метацетине(то есть метоксильной группе) изотопический сдвиг меченого 13 С углерода в метацетине отличается от сигналов МРТ атомов углеводорода агента растворения и аминокислот и, таким образом, от большинства других органических субстанций в клетках печени. Другие места маркировки 13 С не проявляют этого преимущества и тем самым препятствуют эффективным измерениям МРТ. Контраст снимков МРТ может быть усилен благодаря умелому подбору импульсов путем использования эффектов соединения (например, NOE, DEPT и т.п.). В частности, при очень плохом функциональном состоянии печени комбинация двух способов дает заметные синергические эффекты. Дополнительно комбинация обеспечивает возможность пространственного разрешения микроциркуляции печени. Определенные при помощи представленного способа значения Amax и tau могут найти множество различных применений. Особое значение имеют при этом следующие виды и области применения: определение функционального состояния печени, наблюдение за формированием печени после операции,планирование операций, в частности, на пораженной печени, определение функции трансплантированной печени, заключение по поводу сепсиса, в частности у пациентов отделения реанимации, определение поражения печени лекарственными средствами при регистрации лекарственных средств, наблюдение за длительными поражениями печени, определение поражений печени генетически модифицированными продуктами питания, в области техники безопасности в химической промышленности, в производственной медицине, при профилактическом обследовании по поводу рака печени, наблюдении за заболеваниями печени, определении дозировки лекарственных средств, обнаружении поражений печени у животных, в медицине окружающей среды и при обычном исследовании функции печени. Далее представленное изобретение будет детально рассмотрено на основе следующих примеров осуществления со ссылкой на фигуры, при этом детальное рассмотрение не ограничивает пределы правовой охраны изобретения. Фигуры показывают следующее: фиг. 1 - схематичное изображение субстанций, пригодных для осуществления способа; фиг. 2 - схематичное изображение осуществления соответствующего изобретению способа измерения; фиг. 3 - графическое изображение кинетики роста на основе измеренных значений DOB за время измерения; фиг. 4 а - графическое изображение кинетики роста при нормальном функциональном состоянии печени; фиг. 4b - графическое изображение кинетики роста при циррозе печени; фиг. 4 с - графическое изображение кинетики роста при тяжелых поражениях печени; фиг. 4d - графическое изображение кинетики роста при печеночной недостаточности; фиг. 5 - графическое изображение максимальной степени превращения LiMAx в течение времени при нормальном функциональном состоянии печени, ограниченной функции печени и печеночной недостаточности; фиг. 6 - схематичное изображение транспортировки введенной субстанции в печень; фиг. 7 - графическое изображение кинетики роста для определения данных максимального значения А и постоянной времени tau; фиг. 8 - графическое изображение уменьшения концентрации метаболизируемого субстрата и увеличения концентрации продукта метаболизации в крови. В предпочтительном варианте осуществления представленного способа происходит определение функционального состояния печени человека по схеме, как показано на фиг. 2. В ходе этого измерения метаболизация инициируется путем внутривенного введения метаболизируемого субстрата, в частности 13 С-метацетина 1 в соединении с изотоническим раствором поваренной соли 1 а. Путем внутривенного введения субстрата обеспечивается необходимое для анализа быстрое введение субстрата и быстрое инициирование метаболизации субстрата. При этом инициирование метаболизации субстрата, вызванное ферментативным преобразованием субстрата в печени, опережает ритм дыхания. Перенос введенного субстрата в печень и происходящее там преобразование или разложение субстрата схематично изображено на фиг. 6. Введенный субстрат (кружки, заштрихованные перекрестными штрихами), как, например, С-метацетин, при помощи специального модуля переноса транспортируется в клетки печени, там преобразуется посредством соответствующих энзимов (шестиугольники, заштрихованные одинарными линиями), в частности оксигеназов Р 450, например, путем дезалкилирования с определенной константой скорости реакции, и дезалкилированный продукт (кружки, заштрихованные одинарными линиями), например парацетамол, при помощи особого модуля переноса, а также меченый 13 С продукт метаболизации (кружки, заштрихованные одинарными линиями), например 13CO2, при помощи специального модуля переноса транспортируются из клеток печени в кровь. Наряду с активизацией субстрата под воздействием энзимов, в частности оксигеназов Р 450, возможно также высвобождение или активизация субстрата при помощи засвечивания или других быстрых процессов. Высвобожденный продукт метаболизации, например 13CO2, через кровь переносится в легкие и оттуда выдыхается. Выдыхаемый воздух предпочтительно через дыхательную маску и соединительную трубку непрерывно направляется в измерительный прибор 2 и обрабатывается при помощи компьютера 3 (Stockmann et al., Annais of Surgery, 2009, 250: 119-125). Измерительный прибор, который может быть использован для представленного метода, описан в т.ч. в патенте WO 2007/107366 А 1. Применение специфического измерительного прибора позволяет наблюдать за метаболизацией субстрата в каждом дыхании в режиме реального времени. Это поясняется на фиг. 3. Диаграмма фиг. 3 показывает повышение концентрации 13CO2 в форме величины DOB в выдыхаемом воздухе, причем повышение соответствует дифференциальному уравнению первого порядка. При этом 1 DOB обозначает изменение соотношения 13CO2 к 12CO2 на одну тысячную выше естественного соотношения. Из этого повышения, как уже было описано, могут быть выведены как Amax или DOBmax, так и постоянная времениtau. После увеличения 13CO2 до максимума происходит уменьшение концентрации 13CO2, что связано с дальнейшими динамическими процессами в теле, способствующими уменьшению сигнала измерительного устройства. Описанная динамика метаболизации позволяет прямо и непосредственно следить за метаболизацией введенного субстрата имеющимися в печени энзимами. Так, предпочтительно вводимый субстрат метацетин деметилируется энзимом CYP1A2. Анализ кинетики роста введенного метацетина, соответствующей дифференциальному уравнению первого порядка, и выведенные на этой основе параметры Amax и tau теперь позволяют непосредственно определять функциональное состояние печени. При этом максимальное значение Amax позволяет сделать вывод о количестве здоровых клеток печени и об имеющемся в распоряжении для обмена веществ объеме печени, в то время как прирост в форме постоянной времениtau позволяет сделать выводы о скорости поступления субстрата в клетки печени. В частности, постоянная времени tau позволяет определить, в состоянии ли печень вообще воспринимать субстраты. Фиг. 7 показывает на примере определение значимых параметров на основе графика, изображающего увеличение 13CO2 в воздухе дыхания после приема меченого 13 С метацетина, сравн. с разъяснениями к фиг. 3. Основываясь на полученных точках ввода данных (кривая А) с измеренным максимальным значением А, составляющим 22,01 DOB, производится согласование (настройка) с подобным описанному выше решением дифференциального уравнения первого порядка (кривая В). Из решения дифференциального уравнения согласно происходит определение амплитуды Amax согласованной функции с 22,09 DOB и постоянной времени tau для преобразования, составляющей 2,42 мин. При этом небольшая постоянная времени, равная 2,42 мин,указывает на хорошую проницаемость печени, в то время как медленный подъем кривой, базирующейся на замеренных значениях, указывает на постоянные времени в диапазоне выше 5 мин и тем самым на уплотнение ткани печени и связанную с этим пониженную проницаемость печени. Наряду или дополнительно к определению содержания меченого 13 С продукта метаболизации, как,например 13 СО 2, в выдыхаемом воздухе для оценки функционального состояния печени можно также отследить уменьшение концентрации дезалкилированного продукта в крови и вывести из соответствующей кинетики роста постоянную времени tau. Этот вариант способа показан на фиг. 8. Изменения концентрации введенного меченого 13 С субстрата, например 13 С-метацетина, и образованного в печени продукта дезалкилирования, например парацетамола, отслеживаются при помощи подходящего аналитического метода, например высокопроизводительной жидкостной хроматографии. Концентрация 13 С-метацетина снижается по причине метаболизации (экспоненциально убывающая кривая начинается при исходной концентрации 20 мкг/мл 13 Сметацетина), в то время как концентрация парацетамола, в свою очередь, возрастает (нижняя кривая на фиг. 8). Первоначальные изменения концентрации здесь также могут быть описаны при помощи дифференциального уравнения первого порядка. При помощи описанного решения дифференциального уравнения первого порядка могут быть выведены соответствующие постоянные времени, причем постоянная времени т 1 первоначального быстрого увеличения концентрации парацетамола составляет 1,3 мин, в то время как постоянная времени т 2 последующего замедленного увеличения концентрации, обусловленного дальнейшим распределением в крови, составляет 16 мин. Представленный способ определения функционального состояния печени может быть использован для решения множества задач. Так, способ позволяет дать оценку общего состояния здоровья пациента, в частности оценку функционального состояния печени пациента. На фиг. 4a-d увеличение метаболизации представлено как функция времени. При этом для различных картин болезни получаются различные кинетики роста с разными максимальными значениями А и разными постоянными времени т. Как было описано, значение А позволяет определить максимальную степень превращения LiMAx, которая прямо пропорциональна функциональному состоянию печени. Фиг. 4 а показывает нормальное функциональное состояние печени с максимальной степенью превращения LiMAx, составляющей 504 мкг/ч/кг, в то время как на фиг. 4b-4d раскрываются различные картины болезни. При циррозе печени метаболизация введенного субстрата ограничена, так что максимальная степень превращения LiMAx всего лишь достигает 307 мкг/ч/кг. При других поражениях печени вплоть до печеночной недостаточности максимальная степень превращения введенного субстрата уменьшается соответственно до 144 мкг/ч/кг (фиг. 4 с) либо 55 мкг/ч/кг (фиг. 4d). Представленный способ позволяет также прогнозировать либо отслеживать формирование печени или контролировать состояние печени после операции, как, например после резекции печени. Так, при помощи представленного метода можно уже через несколько минут после операции на печени или даже во время операции проверить, способна ли печень функционировать и в каком объеме. На фиг. 5 представлены показатели функционального состояния печени после операции на печени. Так, существенно различаются максимальные степени превращения LiMAx у обычной здоровой печени,ослабленной печени и сильно пораженной печени. Восстановление печени после операции, как правило,занимает несколько дней. Если максимальная степень превращения LiMAx, а вместе с тем и показатели функционального состояния печени после операции очень низкие, то можно прогнозировать, что печень пациента не поправится и он с высокой долей вероятности умрет. Однако представленный способ позволяет быстро распознать такие критические случаи, так что соответствующим пациентам может быть в качестве альтернативы, например, произведена пересадка печени и благодаря этому они будут спасены. Представленный способ позволяет также еще до начала операции прогнозировать ее исход и значит соответствующим образом планировать операцию. Так, например, в сочетании с компьютернотомографической волюметрией перед операцией на печени можно определить не только пораженную ткань, например опухолевую ткань, но и всю подлежащую удалению ткань. Это необходимо, поскольку при лечении опухоли нужно удалять как можно больше ткани вокруг нее, чтобы свести к минимуму риск рассеивания опухоли. Однако если удалить слишком большой объем печени, пациент может умереть. Величина удаляемого объема печени зависит от функционального состояния остающегося объема печени. Поэтому благодаря точному определению функционального состояния имеющегося объема печени операция может быть запланирована очень точно, так что пациент имеет оптимальные шансы на выживание и выздоровление. Это можно проиллюстрировать следующим примером. Если объем опухоли составляет, например,153 мл, то целесообразно удалить в целом около 599 мл объема печени. Таким образом, при общем объеме печени в 1450 мл остаточный объем составил бы 698 мл, что гарантировало бы выживание пациента. Максимальная степень превращения LiMAx введенного 13 С-метацетина составляет перед операцией 307 мкг/ч/кг. Желаемый остаточный объем в 698 мл соответствовал бы максимальной степени превращенияLiMAx в 165 мкг/ч/кг. Поэтому уже во время операции при помощи представленного метода можно непрерывно определять степень превращения, обеспечивая достижение необходимого для выживания остаточного объема в 698 мл. В данном случае остаточный объем печени после операции составляет 625 мл и имеет максимальную степень превращения в 169 мкг/ч/кг. Благодаря непосредственному сопоставлению здорового объема печени со значением LiMAx резецируемый объем печени для достижения целевого значения LiMAx может быть определен при помощи простого тройного правила. Представленный способ позволяет также определить функциональную способность или послеоперационную функциональную неспособность (PNS) пересаженной печени. После пересадки печени примерно в 5% случаев пересаженная печень не функционирует, например, по причине недостаточного кровоснабжения. До настоящего времени это удавалось распознать лишь спустя несколько дней. При помощи же представленного метода возможно уже через несколько минут распознать, что печень перестала функционировать, поскольку постоянная времени т дает информацию о доступности введенного субстрата для печени. Соответственно пациент может незамедлительно получить лечение и может быть,например, проведена новая трансплантация. При помощи представленного способа возможно также измерение успеха операции после пересадки печени и планирование дальнейших этапов лечения. Так, после пересадки печени при помощи представленного метода измерения могут быть прямо и непосредственно определены показатели функционального состояния печени и оптимизировано дальнейшее лечение пациента с учетом индивидуальных особенностей. Кроме того, представленный способ позволяет оценить угрозу сепсиса для пациентов отделения реанимации. Известно, что в реаниматологии существует очень высокая угроза смерти от сепсиса. Теперь же представленный способ измерения позволяет непосредственно при поступлении в отделение и во время лечения определять, имеются ли поражения печени или клетки печени функционируют нормально. Определение поражения печени имеет значение, в частности, при регистрации медикаментов и лекарственных средств. Поэтому одной из важнейших областей применения представленного способа является его использование для контроля поражений печени, вызванных медикаментами и лекарственными средствами в период регистрации лекарственных средств. В ходе регистрации лекарственного средства должна быть проведена токсикологическая экспертиза, подтверждающая, что регистрируемые лекарственные средства не поражают печень. Обычно надежная оценка рисков делается на основании ряда различных опытов на животных. Тем не менее, у людей нередко проявляются неожиданные побочные явле-7 022893 ния, которые с трудом обнаруживаются в ходе опытов на животных. При помощи же представленного способа может быть точно и в количественном выражении определено токсическое воздействие не человека и животное. На основе представленного способа, который позволяет достоверно определять количественные показатели функционального состояния печени, становится возможным быстрее и точнее проводить исследования дозировки лекарственных средств. При помощи данного способа могут отслеживаться также длительные поражения, связанные с перестройкой печени под влиянием лекарственных средств, например контрацептивов. При регулярном приеме лекарственных средств, например контрацептивов, могут произойти изменения в печени, которые вначале влияют на доступность клеток печени, а позднее приводят к снижению функциональной способности печени. Эти изменения в печени могут быть обнаружены при помощи времени нарастания т, посредством которого может быть определена скорость поступления субстанций в клетки печени, и максимального значения А, которое позволяет сделать вывод о количестве здоровых клеток печени. Поэтому регулярные тесты при помощи представленного способа измерения дают возможность обнаружить такие изменения в печени. Основываясь на полученных данных, врач может во избежание дальнейших изменений в печени изменить предписание о введении лекарства. Влияние генетически модифицированных веществ и продуктов питания на живые существа, в частности на людей, в настоящее время обнаруживается с большим трудом. Это обусловлено, в частности,тем, что концентрации вредных биологических веществ нередко находятся ниже предела или на пределе обнаружения или же их вредность до сих пор вообще не была известна. Представленное изобретение позволяет однозначно подтвердить, что генетически модифицированные продукты питания причиняют вред печени. Также при помощи представленного способа можно контролировать и идентифицировать влияние химикатов в химической или фармацевтической промышленности. Это позволяет надежно следить за здоровьем людей на рабочем месте. Дальнейшие области применения представленного способа относятся к сфере производственной медицины для оценки риска заболеваний, предупреждения рака печени, при наблюдении за болезнями печени, например гепатитом, при подтверждении поражений печени у животных, например, вызванных крестовником Якова у лошадей, отравлениях и в медицине окружающей среды для поиска вредных для печени субстанций в почве, пище и/или питьевой воде. Особенно предпочтительной областью применения представленного способа является определение дозы медикаментов. Поскольку печень метаболизирует многие из введенных лекарственных средств, при хорошем функциональном состоянии печени соответственно метаболизируется большая часть лекарственных средств, в то время как при не очень хорошем функциональном состоянии печени метаболизируется меньшая доля лекарственных средств. Но для пациента это означает, что в зависимости от функционального состояния печени дозировка лекарственного средства в теле оказывается различной и соответственно может оказывать различное действие. Поэтому оптимальное действие лекарственного средства должно быть согласовано с функциональным состоянием печени. В качестве примера здесь следует отметить введение такролимуса, иммуносупрессивного препарата против реакции отторжения при трансплантации органов. Точное определение дозы такролимуса имеет большое значение, поскольку слишком большая доза такролимуса является токсичной, а слишком маленькая доза недейственной. При точном знании функционального состояния печени становится возможным точно определить дозу и оптимизировать действие лекарственного средства. Представленный способ, учитывая его простоту и быстроту действия, может также применяться домашним врачом с целью проверки печени, чтобы выявить функциональное состояние печени как части состояния здоровья. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ определения функционального состояния печени живого организма, включая человека,включающий следующие этапы: внутривенное введение по меньшей мере одного меченого 13 С субстрата в концентрации от 0,1 до 10 мг/кг веса тела, причм концентрация субстрата выбирается таким образом,чтобы динамика метаболизации в линейной области была далека от насыщения, непрерывное определение содержания минимум одного меченого 13 С продукта метаболизации в выдыхаемом воздухе в определенный интервал времени в течение 25 мин, начиная с внутривенного введения. 2. Способ по п.1, отличающийся тем, что минимум одним меченым 13 С продуктом метаболизации в выдыхаемом воздухе является 13CO2. 3. Способ по одному из предыдущих пунктов, отличающийся тем, что в качестве меченого 13 С субстрата применяется субстрат, из которого путем реакции дезалкилирования алкоксильной группы, в частности метоксильной группы, высвобождается 13CO2. 4. Способ по одному из предыдущих пунктов, отличающийся тем, что в качестве субстрата применяется меченый 13 С метацетин, фенацетин, аминопирин, кофеин, эритромицин и/или этоксикумарин. 5. Способ по одному из предыдущих пунктов, отличающийся тем, что определяется абсолютное со-8 022893 держание меченого 13 С продукта метаболизации, в частности абсолютное содержание 13CO2, в выдыхаемом воздухе. 6. Способ по одному из предыдущих пунктов, отличающийся тем, что выдыхаемый воздух полностью или частично через дыхательную маску и соединительную трубку непрерывно подается в измерительный прибор. 7. Способ по одному из предыдущих пунктов, отличающийся тем, что он комбинируется с другими аналитическими методами, в частности с компьютерно-томографической волюметрией или магнитнорезонансной томографией.
МПК / Метки
МПК: A61B 5/083, A61K 49/00
Метки: количественного, живого, организма, путем, состояния, способ, метаболизации, функционального, определения, субстратов, печени, измерения
Код ссылки
<a href="https://eas.patents.su/11-22893-sposob-opredeleniya-funkcionalnogo-sostoyaniya-pecheni-zhivogo-organizma-putem-kolichestvennogo-izmereniya-metabolizacii-substratov.html" rel="bookmark" title="База патентов Евразийского Союза">Способ определения функционального состояния печени живого организма путем количественного измерения метаболизации субстратов</a>
Предыдущий патент: Устройство для введения внутриматочного средства контрацепции
Следующий патент: Способ и устройство для производства лопающихся леденцов
Случайный патент: Спортивный снаряд -тренажер