Комплекс гадолиния с полиаминокислотами и его применение для формирования изображений при диагностике
Номер патента: 378
Опубликовано: 24.06.1999
Авторы: Руссо Оливье, Симоно Кристиан, Шаэфер Мишель, Мейер Доминик
Формула / Реферат
1. Комплекс гадолиния с полиаминокислотами общей формулы:

в которой R означает группу формулы:
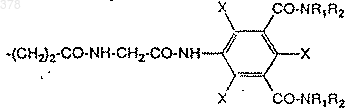
в которой Х означает Вr или I,
R1 означает атом водорода, группу (С1-С3)алкил или моно- или полигидрокси-(С2-С8) алкил, и
R2 означает моно- или полигидрокси-(С2-С8) алкил или же
R1 обозначает Н, а R2 означает группу формулы А:
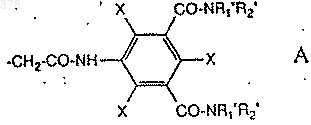
где X имеет указанные выше значения, a R'1 и R'2 имеют любое из значений, указанных для R1 и R2, за исключением значения А, при этом группа -CO-NR1R2 или -CO-NR'1R'2 содержит, по крайней мере, 2 гидроксильные группы, а М обозначает Н или катион минерального или органического основания.
2. Комплекс формулы I по п.1, в которой группа -CO-NR1R2 или -CO-NR'1R'2 содержит, по меньшей мере, 6 гидроксильных групп.
3. Комплекс формулы I по любому из п.1-2, в которой М означает органический или минеральный катион, выбранный из Na+ и из катионов производных лизина, аргинина, N-метилглюкамина или диэтаноламина.
4. Комплекс формулы I по любому из пп.1-3, в которой R1 и R2 означает СН2-(СНОН)4-CH2OH и Х означает Вr.
5. Комплекс формулы I по любому из пп.1-4, в которой R1 означает Н, R2 означает A, a R'1 и R'2 означают СН2-(СНОН)4-СН2OН и Х означает Вr.
6. Композиция на основе контрастного агента, отличающаяся тем, что в качестве указанного агента она содержит комплекс по любому из пп.1-5 в виде соли с фармацевтически приемлемым основанием и фармацевтический носитель.
Текст
1 Настоящее изобретение относится к комплексным соединениям металла с полиаминокислотами и к композициям на основе контрастного агента, которые можно применять для формирования изображений при диагностике. Такие соединения представляют собой производные с разветвленной цепью гадотериновой кислоты, которая выпускается в продажу в виде соли меглюмина под товарным знакомDotarem в качестве контрастного вещества при формировании изображений с помощью магнитного резонанса. Гадотерат меглюмина является стабильным комплексным соединением,его спино-решеточная релаксация при 37 С и при 20 МГц составляет приблизительно 3,5 мМ-1 с-1, т.е. величину того же порядка, что и у других выпускаемых в продажу контрастных веществ. Комплексные соединения гадолиния согласно изобретению имеют величину релаксации R1, превышающую 20 мM-1c-1. Это позволяет вводить субъекту диагностический состав,в котором молярная концентрация комплексного Gd3+ и, следовательно, концентрация самого соединения согласно изобретению в 6 раз и даже в 10 раз меньше, чем концентрации, которые применяются в настоящее время в клиниках при достижении сигнала той же интенсивности. Поскольку осмолярность растворов комплексов согласно изобретению при одной и той же релаксационной способности значительно меньше осмолярности растворов Dotarem'a и даже осмолярности растворов неионных соединений, таких как гадодиамид, то можно использовать растворы, в которых массовое содержание активного начала будет выше, чем в растворах, которые применяются ныне как наилучшие,с достижением изображений прекрасного качества без появления побочных нежелательных эффектов. Кроме металлического тяжелого иона Gd3+ эти комплексы содержат атомы брома или иода и являются непрозрачными для рентгеновских лучей; они также достаточно растворимы, в частности, из-за присутствия гидрофильных групп вокруг ароматических колец, в связи с чем они могут быть использованы в традиционной рентгенологии или дихроматографии. Соединения согласно изобретению имеют следующую формулу: где X имеет указанные выше значения, a R'1 иR'2 независимо друг от друга имеют любое из значений, указанных для R1 и R2, за исключением значения А, при этом -CO-NR1R2 или-CO-NR'1R'2 содержат, по крайней мере, 2 гидроксильные группы, а М обозначает Н или минеральный или органический катион. Среди фармацевтически приемлемых катионов можно назвать Na+ или производные лизина, аргинина,N-метилглюкамина или диэтаноламина. Алкильные группы могут быть линейными или разветвленными. Предпочтительными являются соединения,в которых группы -CO-NR1R2 или -CO-NR'1R'2 имеют, по крайней мере, 6 гидроксильных групп, в частности означают группу -CON(CH2(CHOH)4CH2-ОН)2. Соединения формулы I могут быть получены путем взаимодействия амина формулы II: в которой X, R1, R2 имеют указанные выше значения, с комплексом гадолиния формулы III,соответствующей описанной формуле I, в которой R = -(CH2)2 СООН, в присутствии агента сочетания, в частности одного из тех агентов,которые используются при синтезе пептидов,такого как карбодиимид, например, в водном растворе. Амины формулы II, в которых R2 отличен от А, могут быть получены путем взаимодействия аминоспирта HNR1R2 с дихлоридом дикислоты формулы IV: в которой функция NH2 защищена в виде фталимида, с последующим гидразинолизом. Аминоспирты HNR1R2 являются известными продуктами и могут быть получены методами, аналогичными тем, которые описаны в литературе. Можно, в частности, назвать выпускаемые в продажу аминоспирты, в которых:ii) R1 = Н и R2 = СН 2-СНОН-СН 2 ОН или СН 2-(СНОН)2-СН 2 ОН;iv) а также глюкозамин,и те спирты, которые описаны в заявках на европейский патент ЕР-А-558 395, ЕР-А-25 083 и ЕР-А-33 426. Амины формулы II, в которых R2 означаетA, a R1 означает Н, получают простым взаимодействием амина формулы H2NA с дихлоридом дикислоты формулы IV, предварительно Nзащищенным. Следует отметить, что аминH2NA, который соответствует амину формулыII, в которой R2 отличен от А, может быть получен в соответствии с описанным выше способом. Другим объектом изобретения является композиция с контрастным агентом, предназначенная для формирования изображений в диагностике с помощью магнитного резонанса, которая содержит соединение формулы I в фармацевтически приемлемом носителе в необходимом для исследования количестве. Их фармацевтические формы зависят от пути введения. Предпочтительно, фармацевтической формой указанных композиций являются водные растворы физиологически приемлемых солей комплекса формулы I. Кроме того, композиции согласно изобретению могут содержать стабилизаторы, различные добавки, предназначенные для создания изотонического раствора или для установления фиксированного значения рН, а также любой другой тип добавок, широко используемых в данной области. Концентрация композиции зависит от пути и от зоны введения. Обычно концентрация составляет 0,01-0,5 М и, предпочтительно, от 0,05 до 0,1 М. Одноразовая доза зависит от структуры комплексного соединения и от вида исследования, обычно она составляет от 0,005 до 0,1 ммол/кг. Ниже описаны примеры получения комплекса формулы III в водном растворе, амина формулы II, в котором R1 = R2 = CH2(СН 000378 4 ОН)4 СН 2OН, и амина, в котором R1 = H и R2 = A,в котором R'1 = R'2 = СН 2(СНОН)4 СН 2OН. Получение комплекса формулы III Стадия а) Медленно вливают 167 г диметил-2 бромглютарата в суспензию, состоящую из 30 г 1,4,7,10-тетраазациклододекана и 97 г карбоната калия в 875 мл ацетонитрила; затем смесь перемешивают в инертной атмосфере при 60 С в течение 48 ч, во время которых добавляют 83 г диметил-2-бромглютарата. После этого фильтруют реакционную среду при комнатной температуре и раствор концентрируют досуха. Остаточное масло очищают с помощью хроматографии на диоксиде кремния, элюируя смесью дихлорметан - метанол с градиентом (от 100/0 до 80/20), и получают 43 г сложного октаэфира в виде масла. Стадия b) Полученное масло, растворенное в 72 мл метанола, вводят в водный раствор NaOH (68 гNaOH; 340 мл воды) и смесь выдерживают при перемешивании при 70 С в течение 48 ч. Метанол удаляют при уменьшенном давлении, а водную фазу экстрагируют с помощью метиленхлорида и затем вводят в нее около 800 мл катионообменной смолы Амберлит, поставляемой фирмой Rohm и Haas под названием IRC 50 (слабая кислота). После контактирования в течение 1 ч смолу удаляют и вводят в раствор 680 мл анионообменной смолы Амберлит под названием IRA 458 (сильное основание). После 12 ч смолу отделяют и вводят в колонку; целевой продукт выделяют путем элюирования с помощью 4 л 3 Н водного раствора уксусной кислоты, затем 4 л 6 Н раствора. После удаления растворителя под уменьшенным давлением получают 31 г белых кристаллов. ЯМР 13 С (200 МГц; ДМСО-d6: Т=30 С); 24; 31; 48; 62; 172; 174. Стадия с) 29,4 г октакислоты, полученной на предыдущей стадии, суспендируют в 530 мл воды с 15,8 г GdCl3, 6 Н 2 О при перемешивании; 1 Н водный раствор NaOH медленно вводят до стабилизации значения рН среды на уровне, равном 6,5. Среду затем фильтруют через фильтр Millipore с ячейкой, равной 0,45 мкм, и фильтрат концентрируют досуха. После осушения получают 49,3 г соли натрия комплекса гадолиния формулы III в виде твердого вещества бежевого цвета, содержащего NaCl, который образуется во время комплексообразования. Этот продукт может быть очищен путем осаждения в водном этаноле и обработки для удаления избытка Gd3+, не вошедшего в комплекс, с помощью хелатирующей смолы, такой,которая поставляется фирмой Biorad Laboratories под товарным знаком CHELEX. Релаксация: R1 (37C; 20 МГц) =5,9 мМ-1 с-1; 5 Хроматография: ВЭЖХ на колонке Hibar(50/50 - об/об). Время удержания: 2 мин. Получение амина формулы II, в которой(Соединение IIа). Стадия а) При перемешивании постепенно вводят 179 г хлорида N-фталоилглицина в раствор, охлажденный до 0 С, состоящий из 119 г дихлорида 5-амино-2,4,6-трииодизофталевой кислоты в 500 мл диметилацетамида. Смесь перемешивают несколько часов при 0 С, затем после выдержки в течение ночи при комнатной температуре медленно вводят в 10 л воды. Образующийся осадок отделяют и растворяют в 3 л этилацетата. Этот раствор промывают водным раствором бикарбоната натрия, затем водой,сушат и концентрируют. Получают 125 г дихлорида 2,4,6-трииод-5 фталимидоацетамидоизофталевой кислоты. Стадия b) Выдерживают 5 ч при 80 С раствор 104 г дихлорида полученной выше кислоты, 208 г дисорбитиламина и 50 мл триэтиламина в 1000 мл диметилацетамида. Образовавшийся осадок отделяют и удаляют растворитель путем отгонки при пониженном давлении; остаток растворяют в воде с рН 3 и вводят в контакт с 750 мл катионообменной смолы Амберлит, которая продается фирмой Rohm и Нааs под названиемIRN 77 (сильная кислота). После перемешивания в течение 2 ч отделяют смолу и вводят в водный раствор (700 мл) очищенного диамида 17 мл гидразингидрата. После перемешивания в течение 5 ч при 80 С среду подкисляют при комнатной температуре, добавляя 26 мл 10 Н раствора соляной кислоты. Отделяют образовавшийся осадок и пропускают раствор через колонку с 500 мл слабой анионообменной смолы (Амберлит IRA 67), затем 80 мл слабой катионообменной смолы (Амберлит IRC 50); обрабатывают полученный раствор с помощью 4 л смолы Амберлит (сильная кислота), на которой удерживается целевой продукт. Его элюируют водным раствором NH4 ОH. Выход полученного амина II в виде твердого вещества бежевого цвета составляет 70%. Хроматография ВЭЖХ: колонка LiChrospher 100 RP 18,5 мкм (Merck) высота =25 см,диаметр = 4 мм; Элюант: СН 3 СN/РIС В 8 0,05 М (Waters) 5/95, расход: 1 мл/мин. Время удержания изомеров: приблизительно 8 мин.PIC B8: смесь октановой сульфокислоты/метанола/ацетата кальция/воды. 6 Получение амина формулы II, в которой(Соединение IIb) Работают аналогично способу, указанному выше для получения целевого продукта. Молекулярный пик его масс-спектра, определяемый посредством электрораспыления, является корректным. При высокоэффективной жидкостной хроматографии время удержания изомеров составляет приблизительно 8 мин при тех же условиях, которые описаны выше. Исходную 5-амино-2,4,6-трибромизофталевую кислоту получают с выходом 85% путем обработки с помощью 100 мл брома раствора 87 г 5-аминоизофталевой кислоты в 1300 мл воды и 380 мл концентрированной соляной кислоты. ТСХ: SiO2 Merck: С 6 Н 6/СН 3 СОС 2 Н 5/НСО 2 Н (60/25/11) Rf=0,8; Дихлорид соответствующей кислоты получают классическим методом, воздействуя с помощью SOCl2 на соответствующую двухосновную кислоту, с выходом 88%. ТСХ: SiO2 Merck:CH2Cl2 Rf=0,9. При высокоэффективной жидкостной хроматографии фталимидов (дихлорид кислоты и диамид) время удерживания соответственно составляет 11 мин и от 15 до 30 мин на колонкеLiChrospher 100 RP 18,5 мкм (Merck) длина 250 мм; диаметр 4 мм, при скорости 1 мл/мин,элюируя, в первом случае, смесью 60/40 ацетонитрила и 0,01 М водного раствора КН 2 РO4 и, во втором случае, той же самой смесью при соотношении компонентов 7/97 (об/об). Получение амина формулы II с R1 = H,R2 = A, R'1 =R'2 = CH2 (CHOH)4 СН 2 ОН, X = 1(Соединение IIc) Перемешивают в течение 24 ч при 70 С раствор в 400 мл диметилацетамина 59 г дихлорида 2,4,6-трииод-5-фталимидоацетамидоизофталевой кислоты, 200 г амина IIа, полученного вышеописанным методом, и 29,5 мл трибутиламина. После этого удаляют растворитель при пониженном давлении и очищают остаток посредством хроматографии на 4 кг адсорбента XAD 1600 (Rohm и Haas), элюируя смесью СН 3 ОН/Н 2 О. Обрабатывают водный раствор, который содержит целевой фталимид (теоретически 80%), так же, как в предыдущем случае, с помощью гидразингидрата, для того чтобы получить целевой амин II с выходом, равным 85%. Гель-хроматография: Superdex 30 в колонке 16 мм/60 см (Pharmacia). Элюант: буфер 0,1 М(Waters) длина = 25 см, диаметр = 4,6 мм. Элюант: СН 3 СN/КН 2 РO4 0,01M (15/85) (без СН 3 СN в течение 5 мин). Скорость: 1 мл/мин. Время удержания изомеров: приблизительно 18 мин. Получение амина формулы II, где R1=H,R2=A, R'1=R'2= СН 2 (СНОН)4 СН 2OН и Х=Вr (Соединение IId) Стадия а) При 70 С вводят 17,3 г дихлорида 5 фталимидоацетамидо-2,4,6-трибромизофталевой кислоты в 185 мл диметилацетамида, 11,3 мл триэтиламина и 66,6 г соединения IIb. После перемешивания в течение 24 ч выливают реакционную среду при комнатной температуре в 2 л метиленхлорида и отделяют образовавшийся осадок. Его очищают путем хроматографии в виде водного раствора на 3 л полистирольной смолы типа XAD 1600, производимой фирмойRohm и Нааs. Выход составляет 90%. Стадия b) Выдерживают при 80 С в течение 5 ч раствор 37,5 г соединения, полученного выше, в 130 мл воды и 2 мл 35%-го водного раствора гидразина. После охлаждения среду доводят до рН 1, добавляя 10 Н водный раствор НСl, затем осуществляют хроматографию последовательно на 100 мл катионной (IRN 77) и анионной (IRA 67) смолах Амберлит, а затем на 500 мл катионообменной кислой полистирольной смолы типа IMAC HP222, которую поставляет фирмаRohm и Нааs, и элюируют целевой продукт с помощью 3 М водного раствора NH4OH, затем выделяют осаждением в этаноле после концентрирования. Хроматография ВЭЖХ: колонка LiChrospher 100 RP 18, 5,25 мкм, длина 25 см, диаметр 4 мм; (Merck), элюант: водный раствор НСl (рН 3,4)/СН 3 СN 97/3; скорость 1 мл/мин; время удержания: 4,5-8 мин. Масс-спектр (электрораспыление): в соответствии с нормой. Получение амина формулы II, в которой(Соединение IIе). Стадия а) Растворяют 25 г дихлорида 5-фталимидоацетамидо-2,4,6-трииодизофталевой кислоты в 170 мл диметилацетамида при комнатной температуре с 13 г 4(N-метил)аминобутан-1,2,3 триола и 22,8 мл трибутиламина. Реакционную среду выдерживают в течение 8 ч при перемешивании при комнатной температуре, затем концентрируют при пониженном давлении. Очищают остаток путем хроматографии в виде водного раствора на катионной смоле Н+ Амберлит IRN 77. Выход более 95%. Стадия b) 8 Вводят 75 г полученного выше продукта при 80 С в 50 мл воды, содержащей 1,43 мл 35% водного раствора гидразина и выдерживают смесь при этой температуре в течение 5 ч,затем доводят до рН=1, добавляя 10 Н водный раствор НСl. Отделяют осадок, а водную фазу хроматографируют на 100 мл катионной смолы Н+ Амберлит IRC 50, затем на 20 мл анионной смолы ОН+ Амберлит IRA 67. После концентрирования получают целевой продукт с выходом, равным 80%. ТСХ: на кремневой пластине Merck 60 F; элюант: этилацетат/изопропанол/15 Н водный аммиачный раствор (35/35/40). Rf = 0,7. Пример 1. Соединение формулы I, в которой М = Na и Выдерживают в течение 48 ч при комнатной температуре при перемешивании 1 г комплекса гадолиния формулы III, 5 г соединенияIIа и 6,8 г хлоргидрата 1-(3 диметиламинопропил)-3-этил-карбодиимида в 13 мл воды; рН реакционной среды поддерживают при 7, добавляя несколько раз 1 Н водный раствор НС 1. Реакционную среду, к которой добавляют 50 мл воды, подвергают ультрафильтрации с помощью кассеты minisette типа nova, которую поставляет фирма Filtron (США) и которая содержит одну мембрану из полиэфирсульфона с порогом разрыва 5 кДa. Получают 2 г сырого продукта в виде соли натрия, который может быть очищен с помощью эксклюзивной хроматографии со стерическим эффектом на колонке геля Superdex, которую поставляют фирма Pharmacia, элюируя водой. Хроматография ВЭЖХ: колонка Hibar Licrosorb Diol 5 мкм, длина = 25 см, диаметр = 4 мм (Merck). Элюант: KH2PO4 0,01 М/СН 3 СN (45/55). Скорость: 1 мл/мин. Время удержания: 6 мин. Пример 2. Соединение формулы I, в которой М = Na и Постепенно вводят 50 г 1-(3-диметиламинопропил)-3-этил-карбодиимида в раствор 7,4 г комплекса гадолиния формулы III и 37 г амина IIb в 100 мл воды и выдерживают среду при рН 7, добавляя 1 Н НСl. После перемешивания в течение 48 ч при комнатной температуре 9 подвергают среду ультрафильтрации, так же,как в примере 1, но с мембраной, имеющей порог разрыва 3 кДa, затем вводят в контакт с 500 мл анионной ионообменной смолы АмберлитIRA 458 (сильное основание). После удаления смолы и испарения воды,получают 14 г целевого продукта в виде твердого вещества бежевого цвета. Сырой продукт может быть выделен из реакционной среды путем осаждения этиловым спиртом. Хроматография: ВЭЖХ колонка Hibar Licrosorb Diol 5 мкм, длина = 25 см, диаметр = 4 мм. Элюант: КН 2 РO4 0,01 М/СН 3 СN (45/55 об/об). Скорость: 1 мл/мин. Время удержания: 5 мин. Пример 3. Соединение формулы I, в которой М = Na и Растворяют 0,3 г комплекса гадолиния формулы III и 3,5 г соединения IIc в 10 мл воды и прикапывают раствор 1 Н НСl до рН 6,5, затем добавляют 1,1 г хлоргидрата 1-(3-диметиламинопропил)-3-этилкарбодиимида. После перемешивания в течение 24 ч при комнатной температуре добавляют 80 мл воды и очищают, как указано выше, посредством ультрафильтрации с помощью мембраны с порогом разрыва 8 кДa с получением 1,5 г соли натрия целевого комплекса в виде белого порошка. В случае необходимости, можно также осуществить реакцию при температуре около 40 С в присутствии каталитического количества соли натрия(N-гидроксисукцинимидил)-3 сульфоновой кислоты. Продукт может быть очищен посредством осаждения в изопропаноле. Эксклюзивная хроматография со стерическим эффектом: 4 колонки, поставляемые фирмой Shodex (JP) под названием ОН Pak SBHQ диаметром 8 мм и длиной 30 см, установлены последовательно и заполнены полигидроксиметакрилатным гелем; пределы эксклюзии относительно пуллулана: 106 кДа (SB-804); 105 кДа (SB-803); 104 кДа (SB-802-5); 104 кДа (SB802-5). Элюант водный раствор Растворяют 1,8 г соли натрия комплекса формулы III и 21,8 г амина (соединение IId) в 45 мл воды. После подкисления с помощью 1 Н водного раствора НСl до рН 6 доводят среду до 40 С перед введением 2,2 г хлоргидрата 1-(3 диметиламинопропил)-3-этил-карбодиимида и 0,165 г натриевой соли (N-гидроксисукцинимидил)-3-сульфоновой кислоты. После перемешивания в течение 2 ч смесь выливают в 600 мл этанола и растворяют образовавшийся осадок в 270 мл воды. Подвергают раствор ультрафильтрованию,как указано выше, с помощью мембраны, порог разрыва которой равен 1 кДа. После испарения воды получают 15 г целевого продукта в виде белого порошка. Эксклюзивная хроматография со стерическим эффектом: условия, аналогичные условиям примера 3. Время удержания 33,7 мин. Пример 5. Соединение формулы I, в которой М = Na. Работая аналогично примеру 1, но исходя из комплекса формулы III (соль натрия) и из амина IIе, получают целевой продукт. ВЭЖХ: условия осуществления примера 2. Время удержания 3 мин. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Комплекс гадолиния с полиаминокислотами общей формулы:R1 обозначает Н, а R2 означает группу формулы А: где X имеет указанные выше значения, a R'1 иR'2 имеют любое из значений, указанных для R1 и R2, за исключением значения А, при этом группа -CO-NR1R2 или -CO-NR'1R'2 содержит,по крайней мере, 2 гидроксильные группы, а М обозначает Н или катион минерального или органического основания. 12 2. Комплекс формулы I по п.1, в которой группа -CO-NR1R2 или -CO-NR'1R'2 содержит,по меньшей мере, 6 гидроксильных групп. 3. Комплекс формулы I по любому из пп.12, в которой М означает органический или минеральный катион, выбранный из Na+ и из катионов производных лизина, аргинина, Nметилглюкамина или диэтаноламина. 4. Комплекс формулы I по любому из пп.13, в которой R1 и R2 означает СН 2-(СНОН)4CH2OH и Х означает Вr. 5. Комплекс формулы I по любому из пп.14, в которой R1 означает Н, R2 означает A, a R'1 иR'2 означают СН 2-(СНОН)4-СН 2OН и Х означает Вr. 6. Композиция на основе контрастного агента, отличающаяся тем, что в качестве указанного агента она содержит комплекс по любому из пп.1-5 в виде соли с фармацевтически приемлемым основанием и фармацевтический носитель.
МПК / Метки
МПК: A61K 49/00
Метки: комплекс, диагностике, применение, полиаминокислотами, гадолиния, изображений, формирования
Код ссылки
<a href="https://eas.patents.su/7-378-kompleks-gadoliniya-s-poliaminokislotami-i-ego-primenenie-dlya-formirovaniya-izobrazhenijj-pri-diagnostike.html" rel="bookmark" title="База патентов Евразийского Союза">Комплекс гадолиния с полиаминокислотами и его применение для формирования изображений при диагностике</a>
Предыдущий патент: Способы получения бензо [b] тиофенов
Следующий патент: Способ приготовления материала на основе минеральной ваты
Случайный патент: Модуль перемещения координатного устройства и способ управления тяговым усилием его электропривода










