Способ очистки сточных вод от ионов тяжелых металлов
Формула / Реферат
1. Способ очистки сточных вод от ионов тяжелых металлов с использованием соли двухвалентного железа, отличающийся тем, что применяется железосодержащая суспензия, в которой массовое (г/л) отношение компонентов составляет: m(FeSO4Ч 7H2O):m(NaOH):m(NaNO3)=9,8:2,8:1, а соотношение их концентраций (моль/л) равно C(FeSO4Ч 7H2O):C(NaOH):C(NaNO3)=0,75:1,5:0,25, имеющая pH 8-10, дозирование которой в очищаемые воды производится в соответствии с соотношением S m(Men+):m(Feобщ.)=1:3, но не более 1 г/л Feобщ. при механическом перемешивании или барботаже воздухом и доведении pH очищаемой воды до 9-12,0 единиц раствором гидроксида натрия.
2. Способ по п.1, отличающийся тем, что источником железа является технический сульфат железа (II), представляющий отходы металлургической промышленности.
3. Способ по п.1, отличающийся тем, что железосодержащая суспензия выдерживается для формирования высокой химической активности к ферритообразованию и способности к адсорбции ионов тяжелых металлов не менее 20 мин до ее введения в очищаемую воду.
4. Способ по п.1, отличающийся тем, что в случае присутствия в очищаемых водах ионов хрома (VI) количество сформированной железосодержащей суспензии должно быть достаточным для восстановления их до ионов хрома (III).
5. Способ п.4, по которому на 1 мг Cr+6 используется 16 мг FeSO4Ч 7H2O.
Текст
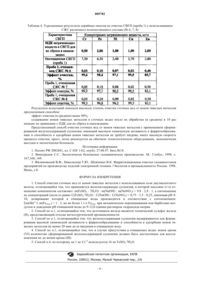
005782 Изобретение относится к охране водных объектов окружающей среды от загрязнений высокотоксичными ионами тяжелых металлов и предназначено для использования на предприятиях черной и цветной металлургии, а также в машиностроительной, электротехнической, металлообрабатывающей промышленностях и других отраслях, осуществляющих процессы очистки сточных вод от ионов тяжелых металлов. Известные реагентные методы предусматривают в основном осаждение ионов тяжелых металлов в форме гидроксидов. Осаждение гидроксидов металлов Ме(ОН)n протекает в диапазоне рН, величина которого для каждого металла различна. К тому же, ряд металлов (Al, Zn, Cd, Pb, Сr) образуют амфотерные гидроксиды, что не позволяет количественно выделить их из растворов. Кроме того, разбавление обработанных растворов приводит к гидролизу соединений этих металлов,что также препятствует их осаждению. Получаемые осадки гидроксидов металлов имеют большой объем и трудно обезвоживаются. Наиболее близким по сущности является способ удаления ионов тяжелых металлов из концентрированных растворов и сточных вод, включающий их обработку избытком соли двухвалентного железа,подщелачивание до рН 9-10 единиц и введение катализатора процесса ферритизации персульфатов, или перманганатов, или перхлоридов щелочных металлов [1]. Известный способ требует нагрева образовавшейся суспензии до 60-90 С, выдерживание при этой температуре до полного окончания процесса ферритизации, после чего суспензия охлаждается и разделяется путем фильтрования на жидкую и твердую фазу. Недостатками данного способа являются- длительность технологического процесса очистки;- сложность и трудоемкость процесса, что не позволяет применять его в производственных условиях. Задача предполагаемого изобретения заключается в применении сформированной железосодержащей суспензии (СЖС) с высокой химической активностью к ферритообразованию и способностью к адсорбции ионов тяжелых металлов, что позволит: проводить очистку сточных вод без нагрева, увеличить скорость процесса очистки, упростить технологический процесс и снизить его стоимость. Поставленная задача решается тем, что для очистки сточных вод от ионов тяжелых металлов применяется сформированная железосодержащая суспензия, в которой массовое (г/л) отношение компонентов составляет: m(FeSO47H2O) : m(NaOH) : m(NaNO3) = 9,8 : 2,8 : 1, а оптимальное соотношение концентраций (моль/л) компонентов равно C(FeSO47H2O) : C(NaOH) : C(NaNO3) = 0,75 : 1,5 : 0,25 и имеющая рН 8-10 единиц. Источником железа является технический сульфат железа (II), представляющий отходы металлургической промышленности (РУП Белорусский металлургический завод, г. Жлобин). Нитрат натрия активирует процесс ферритизации и повышает эффективность ферритов к адсорбции ионов тяжелых металлов. Массовое отношение компонентов и выбор оптимального соотношения их концентраций определены теоретически и экспериментально с учетом стехиометрии реакций, протекающих при ферритообразовании, которые можно представить в общем виде [2, с. 167]: 6FeSO4 + 12NaOH + O2 = 2Fe3O4 + 6 Н 2 О + 6Na2SO4;Me(OH)n + nFe(OH)3 Me(FeO2)n + nH2O, а также с учетом растворимости сульфата железа (II). Нитрат натрия способствует окислению определенного количества ионов Fe2+ в Fe3+ (1:2), активируя процесс ферритизации: 2FeSO4 + NaNO3 + H2SO4 = Fe2(SO4)3 + NaNO2 + H2O. Определены различные варианты состава для получения сформированной железосодержащей суспензии и рассмотрены их физические свойства. Исследованию подвергалась суспензия, имеющая различный количественный состав компонентов, представленная в табл. 1. Наиболее приемлемыми вариантами суспензии для ее дозирования в сточные воды являются 6, 7 и 8, т.к. имеют хорошую текучесть, со временем не густеют и не расслаиваются.-1 005782 Таблица 1. Количественный состав компонентов и физические свойства СЖС Приготовление суспензии (вариант 6) проводилось по следующей методике. В мерную колбу емкостью 1 л, наливалось 700 см 3 водопроводной воды (t=18-20C) и при постоянном перемешивании растворялось 409 г технического сульфата железа (II) с массовой долей (FeSO47 Н 2 О), равной 51%. Затем в полученный раствор при постоянном перемешивании засыпалось 60 г технического гидроксида натрия. Получалась однородная, вязкая суспензия грязно-зеленого цвета, имеющая кислую реакцию среды(рН=6,0). В полученную суспензию при постоянном перемешивании вносилось 21,3 г нитрата натрия. После тщательного перемешивания рН суспензии доводился до 9 единиц раствором гидроксида натрия с= 40% и доливалась водопроводная вода до объема, равного 1 л. Для формирования высокой химической активности к ферритообразованию и способности к адсорбции ионов тяжелых металлов железосодержащая суспензия должна быть выдержана не менее 20 мин до ее введения в очищаемую воду [2, с.168]. Сформированная железосодержащая суспензия дозируется в очищаемую воду с учетом массового соотношения суммы ионов тяжелых металлов в них (m (Ме+n); мг/л) и дозируемого железа общегоm(Feoбщ.); мг/л ) соответственно 1 : 3. Масса железа общего при дозировке в очищаемую воду не должна превышать 1 г/л. В этом случае обеспечивается ферромагнитный характер формируемых осадков [2, с.168]. Количество дозируемой сформированной железосодержащей суспензии должно быть увеличено,если в сточных водах имеются ионы хрома (VI) - Сr+6, в связи с тем, что их необходимо восстановить до Сr+3 (на 1 мг Сr+6 надо взять 16 мг FeSO4 7H2O):Cr+6 + 3Fe2+Сr+3 +3Fe3+. Объемы (V) доз СЖС (6) для очистки сточной воды, имеющей различный количественный состав ионов тяжелых металлов (ИТМ), представлены в табл. 2 и 3. Таблица 2. Объемы дозируемой СЖС (6) в зависимости от суммарной массы ИТМ в очищаемой воде-2 005782 Таблица 3. Объемы дозируемой СЖС (6) в зависимости от содержания хрома (VI) в очищаемой воде Дозируется сформированная железосодержащая суспензия в очищаемую воду при постоянном механическом перемешивании или барботаже воздухом и добавляется определенный объем (в зависимости от исходной величины рН очищаемой воды) раствора гидроксида натрия (с массовой долей 10-40%) до рН 9-12,0. Выход магнитной фазы увеличивается с ростом количества введенного щелочного реагента. Появление в осадке магнитной фазы происходит при рН = 10,5-12,0. Подщелачивание обрабатываемого раствора сопровождается изменением его окраски от темно-зеленой до черной и образованием хлопьевидных структур, которые при дальнейшем перемешивании приобретают мелкодисперсную форму. Момент образования в растворе дисперсной черной взвеси следует считать моментом окончания перемешивания[3, с.8]. Процесс очистки сточных вод от ионов тяжелых металлов с применением сформированной железосодержащей суспензии проводится без нагревания. Быстро образующийся осадок ферритов тяжелых металлов в течение 10-15 мин хорошо уплотняется в процессе отстаивания. Причиной быстрого отстаивания является плотный характер образующихся частиц, содержащих в своей структуре небольшое количество межкристаллизационной воды [3, с.8]. Ферриты хорошо сорбируют ионы хрома, кадмия, свинца, меди, никеля, кобальта, ртути, марганца и бериллия, они имеют емкость по тяжелым металлам в 1000-10000 раз большую, чем магнетит [2, с. 169]. Осадки ферритов тяжелых металлов, получаемые при обработке сточных вод предложенным способом, можно подвергать экологически безопасному долговременному складированию в земных недрах,не прибегая к строительству громоздких и дорогостоящих спецполигонов, т.к. ферриты устойчивы к воздействию избытка разбавленных растворов сильных минеральных кислот и кислых природных вод, что обусловлено особым строением их кристаллической решетки [1]. Степень очистки сточных вод предлагаемым способом контролировалась унифицированными методами анализа (Унифицированные методы анализа вод./ Под ред. проф. Ю.Ю. Лурье/.М.: Химия, 1973,с. 263, 270, 282, 304, 308) лабораторией химического анализа отдела охраны окружающей среды, аккредитованной на право проведения испытаний в Системе аккредитации лабораторий Республики Беларусь. Усредненные результаты серийных опытов по очистке сточной воды гальванического производства(СВГП) (проба 1) с использованием сформированной железосодержащей суспензии различного количественного состава ( 6, 7, 8) представлены в табл. 4.-3 005782 Таблица 4. Усредненные результаты серийных опытов по очистке СВГП (проба 1) с использованием СЖС различного количественного состава ( 6, 7, 8) Результаты испытаний показали высокую степень очистки сточных вод от ионов тяжелых металлов предлагаемым способом: эффект очистки (в среднем) выше 90%; содержание ионов тяжелых металлов в сточных водах после их обработки (в среднем) в 10 раз меньше по сравнению с ПДК для их сброса в канализацию. Представленный способ очистки сточных вод от ионов тяжелых металлов с применением сформированной железосодержащей суспензии, имеющей высокую химическую активность к ферритообразованию и способность к адсорбции ионов тяжелых металлов не требует нагрева, имеет высокую скорость процесса очистки, прост, легко реализуется на обычном технологическом оборудовании, экономически выгоден и экологически безопасен. Источники информации 1. Патент РФ 2082681, кл. С 02F 1/62, опубл. 27.06.97. Бюл.18. 2. Виноградов С.С. Экологически безопасное гальваническое производство. М.: Глобус, 1998, с. 167,168, 169. 3. Филиновский В.Ф., Никольская Т.Ю., Шевченко В.К. Ферритизационная очистка гальваностоков предприятий по производству изделий электронной техники //Экология и промышленность России. 1998. Июнь, с.8. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ очистки сточных вод от ионов тяжелых металлов с использованием соли двухвалентного железа, отличающийся тем, что применяется железосодержащая суспензия, в которой массовое (г/л) отношение компонентов составляет: m(FeSO47 Н 2 О) : m(NaOH) : m(NaNO3) = 9,8 : 2,8 : 1, а соотношение их концентраций (моль/л) равно C(FeSO47H2O) : C(NaOH) : C(NaNO3) = 0,75 : 1,5 : 0,25, имеющая рН 810, дозирование которой в очищаемые воды производится в соответствии с соотношением:m(Men+): m(Feобщ.) = 1 : 3, но не более 1 г/л Feобщ. при механическом перемешивании или барботаже воздухом и доведении рН очищаемой воды до 9-12,0 единиц раствором гидроксида натрия. 2. Способ по п.1, отличающийся тем, что источником железа является технический сульфат железа(II), представляющий отходы металлургической промышленности. 3. Способ по п.1, отличающийся тем, что железосодержащая суспензия выдерживается для формирования высокой химической активности к ферритообразованию и способности к адсорбции ионов тяжелых металлов не менее 20 мин до ее введения в очищаемую воду. 4. Способ по п.1, отличающийся тем, что в случае присутствия в очищаемых водах ионов хрома(VI) количество сформированной железосодержащей суспензии должно быть достаточным для восстановления их до ионов хрома (III). 5. Способ п.4, по которому на 1 мг Сr+6 используется 16 мг FeSO47 Н 2 О. Евразийская патентная организация, ЕАПВ Россия, 109012, Москва, Малый Черкасский пер., 2/6
МПК / Метки
МПК: C02F 1/62
Метки: тяжелых, сточных, ионов, вод, очистки, металлов, способ
Код ссылки
<a href="https://eas.patents.su/5-5782-sposob-ochistki-stochnyh-vod-ot-ionov-tyazhelyh-metallov.html" rel="bookmark" title="База патентов Евразийского Союза">Способ очистки сточных вод от ионов тяжелых металлов</a>
Предыдущий патент: Осажденные частицы диоксида кремния для кошачьего туалета
Следующий патент: Способ получения углеводородов
Случайный патент: Производные 5,6-дигидро-2h-[1,4]оксазин-3-иламина в качестве ингибиторов бета-секретазы (bace)